基于辅因子化学本质及功能的分类与讨论
王志鹏邓 耿(清华大学化学系,北京00084;Department of Chemistry,TexasA&M University,Texas 77840,USA)
基于辅因子化学本质及功能的分类与讨论
王志鹏1,2邓 耿1,*
(1清华大学化学系,北京100084;2Department of Chemistry,TexasA&M University,Texas 77840,USA)
摘要:辅因子是蛋白质或酶结构的重要组成部分,在许多酶的功能中发挥重要乃至关键作用。在科研和教学中,现有的辅因子概念及其分类系统不够清晰准确。本文从化学本质和功能上将辅因子分为催化型、载体型和底物型3类,并以若干典型的辅因子为例讨论辅因子的特异性及再生性等问题。
关键词:辅因子;辅酶;辅基;分类
1 引言
绝大多数酶都是蛋白质。在蛋白酶的化学结构中,除了氨基酸组成的多肽链外,还有很多非蛋白结构,包括金属离子、有机小分子、金属有机/无机配合物等,人们将其统称为辅因子(cofactor)。这些非蛋白结构与无活性的蛋白酶前体(即原酶,apoenzyme)结合构成全酶(holoenzyme),共同完成酶的正常生理功能[1]。相关的酶促反应在生物体系中广泛存在,尤其在合成与代谢有机分子的生物机制中发挥关键作用。值得注意的是,除了辅因子之外,全酶中的非蛋白结构还可能是反应底物、参与调节的信号分子、氨基酸侧链的表达后修饰或是其他衍生化结构,但只有辅因子能直接参与酶催化反应。
辅因子概念最早在20世纪前期被提出,统称除蛋白骨架外的所有非蛋白结构,因此在许多早期文献中,变构调节的作用位点也被归入辅因子结合位点中[2]。随着对酶及蛋白结构研究的深入,人们逐渐认识到辅因子应当是参与酶促反应的必需组分,因此将辅因子的概念进一步严格化。1997年,国际纯粹与应用化学联合会给出了辅因子的推荐定义[3],将其表述为“保持酶活性所必需的有机分子或离子”,并指出,“辅因子结合没有功能活性的原酶,组成有活性的合酶”。2010年,Fischer等[4]进一步提出,辅因子不仅在功能上为活性酶分子所必需,在结构上也应结合到酶催化反应的活性中心。因此,从功能上看,辅因子的作用是“全或无”,而修饰基团的作用是“多或少”。即没有辅因子,酶无法发挥其作用;而没有修饰基团,只是酶或者相应蛋白的活性高低不同。从结构上看,辅因子直接参与催化反应区域(无论其作为催化剂还是底物),而其他非蛋白结构是局部修饰蛋白、以改变空间结构等方式间接改变酶促反应的催化区域。因此,某些为了稳定蛋白结构而存在的金属离子或者在变构作用中修饰上的磷酸基团等,都不能被视为辅因子。
辅因子的分类也经历了一个发展历程。传统观点认为,辅因子可以根据其与对应蛋白质结合的紧密程度分为辅酶和辅基。其中,结合紧密、不可通过透析除去者为辅基(prosthetic group);而结合松散、可以通过透析或超滤除去者为辅酶(coenzyme)[5]。考虑到辅酶常常是一些金属有机配合物或者有机小分子,也有人认为辅因子是特指无机离子或者配合物,辅酶是指有机金属化合物,辅基则是指与酶紧密结合甚至以共价键结合的辅酶[6]。在很多场合,人们甚至直接用“辅酶”一词泛指非底物的非蛋白质结构。由于非蛋白化合物的结构多样性,以上几种分类方法都过于简单,除了区分辅因子与蛋白结合的牢固程度外[5,7],并不能反映辅因子作用的化学本质。随着生物化学和生物有机化学的发展,现在科学界已经可以对大部分辅因子的化学本质与作用机理进行深入描述,从这一角度对辅因子的功能及其分类进行讨论,将更符合其内在逻辑和学科发展趋势[8]。例如,欧洲生物信息学中心建立了辅因子数据库[9],并在此基础上对辅因子的结构和功能分类进行了系统研究。本文基于辅因子功能角度,提出了有益教学和研究参考的辅因子分类方法。
2 辅因子的功能及其分类概述
辅因子的结构和功能极高的多样性与其参与酶促反应的化学本质有着密切关系。一般而言,酶的催化作用只能针对一种或者一类结构非常类似的底物进行;而为了催化一类反应常常需要特定的辅因子参与。但辅因子并不一定是特异性的,因为不同的酶可以使用同一种辅因子,例如乙醇脱氢酶使用烟酰胺腺嘌呤二核苷酸(NAD+)为辅酶,而乙醛脱氢酶同样也使用NAD+为辅酶。事实上,辅因子不仅可以以同样的催化机理催化不同类型的反应,还可以以不同的催化机理催化不同的反应,甚至还可以作为不同化合物的合成原料参与酶促反应。根据辅因子自身化学结构与其在酶催化循环中的作用,我们认为辅因子可以从功能上分为3类,如图1所示。
第一类辅因子作为反应的催化剂核心,位于酶的活性中心,是酶催化机理实现的必要条件,是催化反应所必需的部分,因此相当于催化剂本身,我们称之为催化型辅因子(catalysis-type cofactor)。这类辅因子实质上是弥补了氨基酸结构的局限性,在反应(催化循环)后恢复原始状态。常见的含有金属辅基以及一些参与催化过程的辅酶属于此类。为保证催化中心的稳定性,第一类辅因子通常都与蛋白酶的蛋白骨架通过共价键直接相连。
第二类辅因子常常作为某些被广泛使用为电子、原子或原子团的载体,反应(催化循环)后不能直接恢复原始状态,但可以通过原反应的逆反应或其他类似简单反应实现恢复,因此相当于一个特定基团的载体,我们称之为载体型辅因子(carrier-type cofactor)。这类辅因子的另一个重要特征是一般不与酶进行共价键连接,酶的每一个催化循环中使用一个分子并将其转化为其对应产物。该对应产物可以作为其他逆过程酶的辅因子参与并转化回原来的辅因子。
第三类辅因子作为某些特定生物活性小分子合成的原料,在反应后被消耗,不能直接通过一步逆反应恢复,需要进行复杂的代谢过程而实现重新合成,因此相当于酶促反应的底物,我们称之为底物型辅因子(substrate-type cofactor)。需要说明的是,同一种辅因子可能同时属于上述3类辅因子的一种或者多种,这是辅因子的多功能性决定的。表1中,我们总结了常见的辅因子及其主要功能和分类。
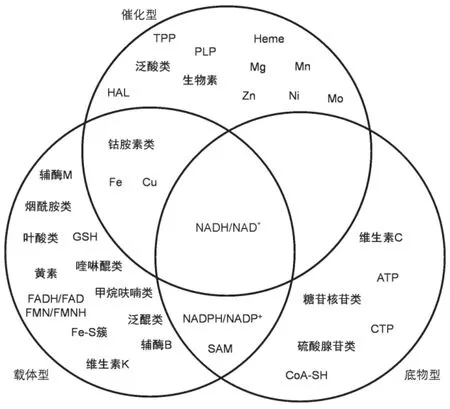
图1 常见的辅因子分类
3 催化型辅因子——磷酸吡哆醛类[23]
磷酸吡哆醛(PLP)即维生素B6,是一类非常重要且广泛存在的辅酶(图2a)。其关键反应位点是吡啶-4-醛基,可以与酶活性位点的氨基以亚胺形式相连,在催化过程中与底物的氨基反应形成底物亚胺(图2b),而吡啶共轭体系的作用是稳定底物-PLP亚胺的α-碳负离子形式。因此,PLP的主要催化方式是通过与底物氨基形成亚胺,进一步活化α-H以稳定α-碳负离子,其可以催化的反应多种多样。PLP最直接的功能是氨基酸消旋酶(racemase)的主要辅酶,通过夺取氨基酸的α-H,使得氨基酸经过负离子中间体而消旋化(图2c)。PLP也是大多数脱羧酶的辅酶,可稳定氨基酸的脱羧反应中间体α-碳负离子(图2d)。此外,通过与氨基酸α-H的交换,底物-PLP亚胺可以水解产生吡哆胺而催化生物转氨反应(图2e)。PLP的例子说明,同一种反应机理可以被用到不同酶的不同催化过程中。
4 载体型辅因子——辅酶NAD类[24]
辅酶NAD类包括烟酰胺腺嘌呤二核苷酸(NAD+)及烟酰胺腺嘌呤二核苷酸磷酸(NADP+)(图3a),它们具有糖基化烟酰胺(维生素B3)的结构。其中,吡啶环电子中心是其主要的催化位点(图3b)。在被H-还原后,氧化型的NAD+将转化为还原型的NADH。从其作用机理上看,NAD+参与可逆的氧化还原反应是其最典型的反应。例如NAD+作为乙醇脱氢酶(alcohol dehydrogenase)的辅酶,其作用机理如图3c所示。其反应产物NADH是另外一些还原酶的辅酶,例如提供H-还原碳-碳双键等等,在维生素E以及萜类化合物的合成中都有涉及。
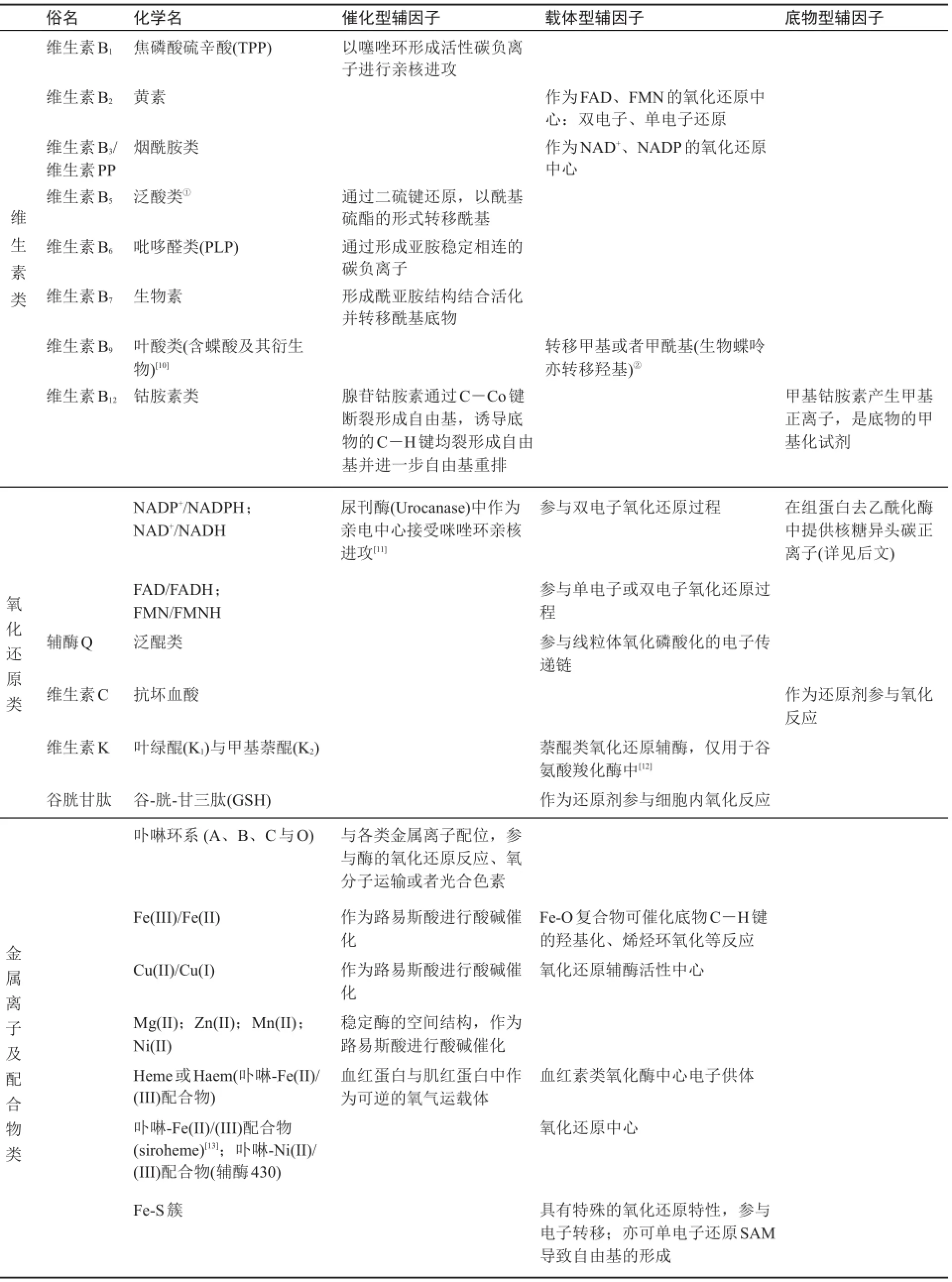
表1 常见的辅因子及其功能分类[2,4]
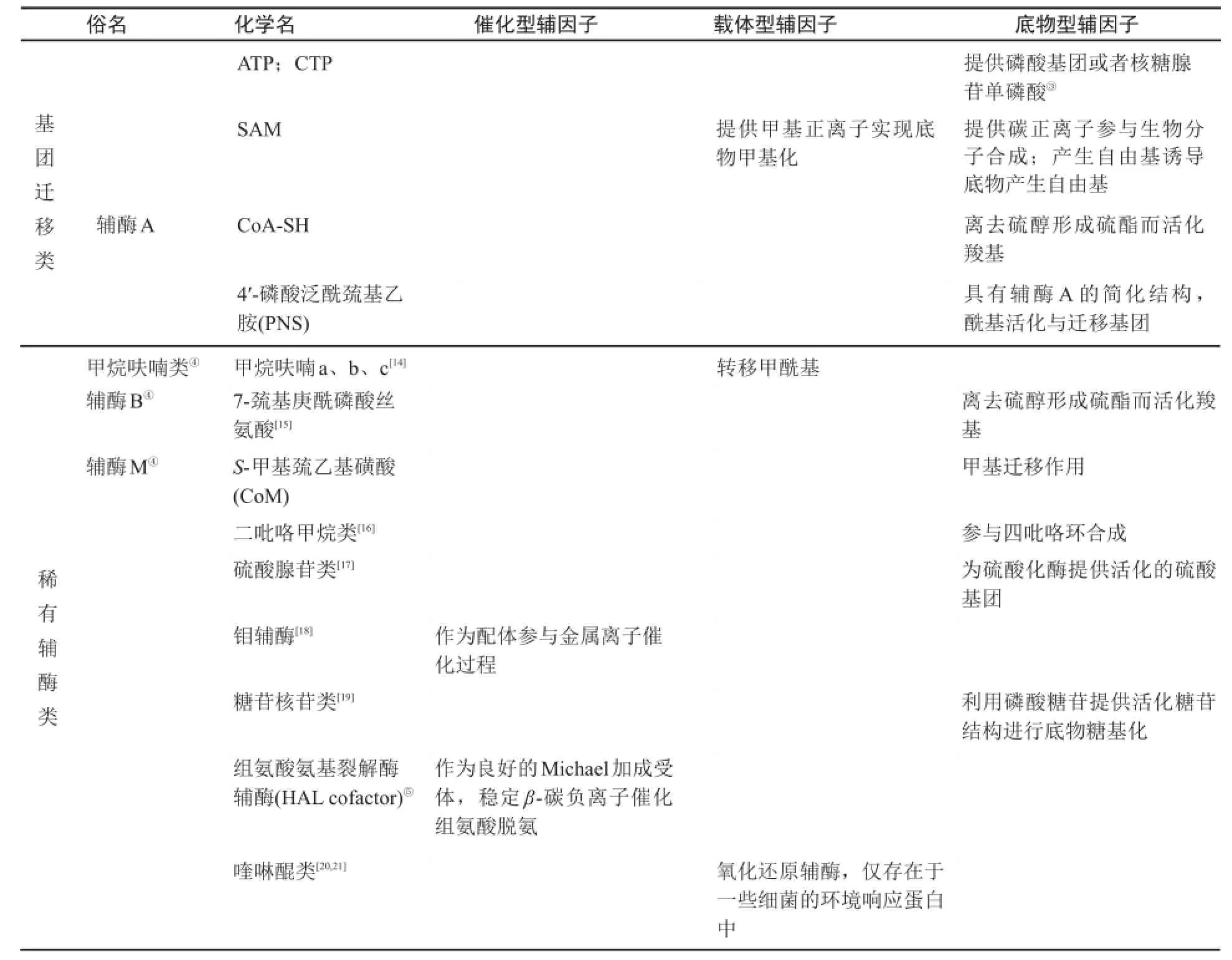
表1 常见的辅因子及其功能分类[2,4](续)
NAD+参与的第二类反应是“掩蔽的氧化还原反应”(masked redox reaction)。在这类反应中,酶通过NAD+参与的氧化-还原两步反应,实现对产物的立体控制或区域选择。例如UDP-葡萄糖-4-差向异构酶(UDP-glucose-4-epimerase)催化UDP-葡萄糖的4位羟基异构化反应时,就利用NAD+将醇氧化为酮得到前手性中心,再通过控制还原过程实现异构化(图4a)。与之类似,3-脱氢奎尼酸合成酶(3-dehydroquinate synthase)催化机理的关键步骤是脱除磷酸基团得到烯醇负离子,但是正常情况下,用碱脱除α-H相对比较困难。如果选择利用其相邻碳原子上的羟基,则可以通过将羟基氧化为羰基以增强其α-H的酸性而更容易被脱除,而后续步骤保持不变(图4b)。
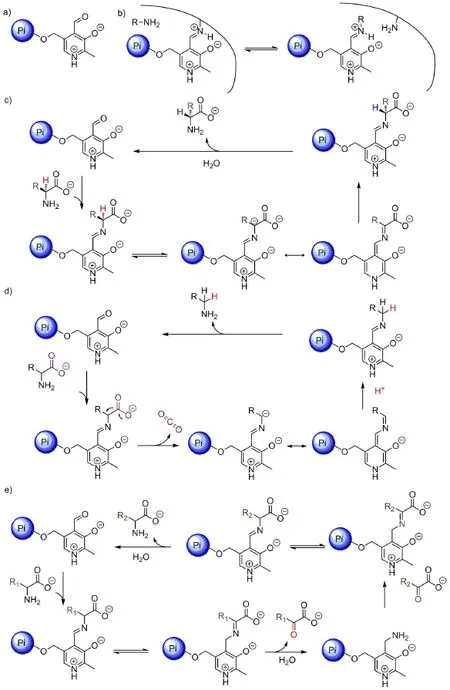
图2 PLP通过与氨基酸的氨基结合形成亚胺而实现催化的3类反应
NAD+参与的第三类反应与其可以形成稳定的碳正离子有关。当NAD+中的糖环采取半缩醛式构象时,2-位上的环外O―C共价键可以发生异裂得到碳正离子,并通过与环内氧原子共轭形成氧鎓离子以稳定自身。在组蛋白去乙酰化酶(HDAC)[25]中,NAD+解离得到的碳正离子进攻乙酰基的氧原子,经过多步转化最终实现脱乙酰化(图4c)。此外,如表1中提到在组氨酸降解代谢中,NAD+在尿刊酶(urocanase)催化下作为亲电中心接受咪唑环亲核进攻,最终导致稳定的咪唑环系被羟基化而破坏[26](图4d)。由此可见,NAD+实际上催化的反应多种多样,参与氧化酶的催化过程和间接的氧化催化都体现了载体型辅因子的特点;同时,它还保留了糖环衍生物的特点。

图3 NAD+的结构与基本氧化催化机理
5 底物型辅因子——SAM类[27]
SAM的结构如图5a所示,中心锍离子的S―C键可以异裂而转移碳正离子,主要作为很多重要生物活性分子合成的甲基化试剂,或在自由基-SAM酶体系中作为自由基引发剂。SAM可以参与多类生物合成反应,如图5所示。第一类反应是最直接的,通过转移碳正离子实现甲基化(图5a)。第二类反应是利用甲硫氨酸产生的γ-碳正离子进行的反应。例如利用羧基进攻该γ-碳正离子得到α-氨基丁内酰胺,而α-氨基丁内酰胺是进一步合成细菌群体效应信号分子(quorum sensor)的一种原料(图5b)。再如在α-氨基环丙基羧酸(ACC)的生物合成中,SAM在ACC合成酶的催化下转化为ACC(图5c)。利用甲硫氨酸γ-碳正离子还可以合成一些重要的寡聚物或者高聚物。例如,SAM可以由氨基进攻γ-碳正离子形成寡聚氨基酸,而后者是合成重要的铁螯合剂(siderophore)类化合物的原料(图5d)。此外,SAM也可以首先在SAM脱羧酶催化下脱羧,然后再发生氨基进攻γ-碳正离子聚合形成多胺类化合物(图5e)。SAM的第三类反应发生在核糖环系,例如在氟乙酸的生物合成过程中,第一步是氟离子进攻核糖-5-碳正离子而解离甲硫氨酸,含氟的糖环经过多步重排反应最终形成氟乙酸(图5f)。
6 结论
本文对辅因子、辅酶、辅基等概念进行总结,基于辅因子的化学本质将其分为催化型辅因子、载体型辅因子和底物型辅因子3类;对已知的大多数辅因子都进行了归类总结,并进一步结合若干实例探讨了辅酶催化机理与催化反应多样性等问题。随着新的非蛋白结构的不断发现,以及人们对现有辅因子的深入研究[28],相信本文的分类系统能够对教学及实际应用提供帮助。
感谢康奈尔大学博士生王淼参与讨论和提出的建议。

图4 以NAD+为辅酶的一些酶促过程
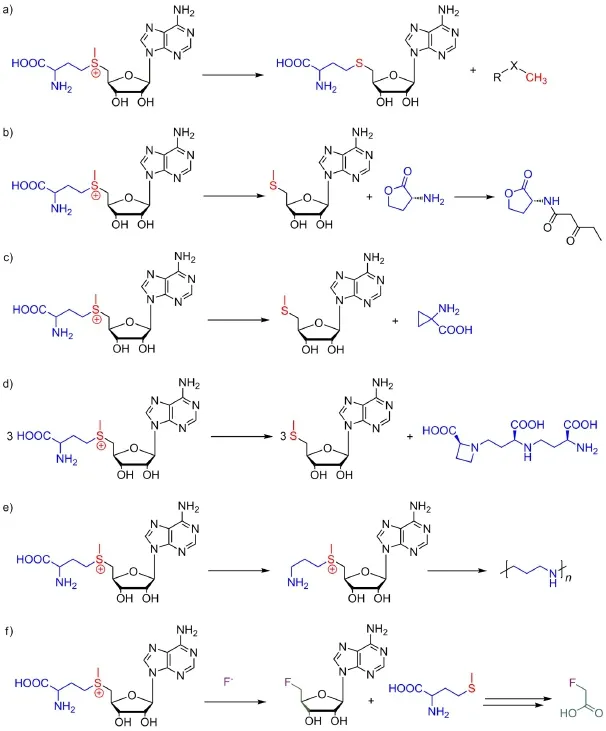
图5 SAM作为反应底物参与的几类典型反应
参考文献
[1]郑穗平,郭 勇,潘 力.酶学.第2版.北京:科学出版社,2009.
[2]Larsson,A.;Reichard,P.J.Bio.Chem.1966,241,2533.
[3] McNaught,A.D.;Wilkinson,A.IUPAC Compendium of Chemical Terminology,2nd ed.;Blackwell Scientific Publications:Oxford,1997.
[4]Fischer,J.D.;Holliday,G.L.;Rahman,S.A.;Thornton,J.M.J.Mol.Biol.2010,403,803.
[5]王镜岩,朱圣庚,徐长达.生物化学(上册).北京:科学出版社,2002.
[6]Nelson,D.Lehninger Principles of Biochemistry;W.H.Freeman and Company:New York,2008.
[7]邹国林,朱汝璠.酶学.武汉:武汉大学出版社,1997.
[8]Kulkarni,N.S.;Deshpande,M.S.General Enzymology;Himalaya Pub.House:Mumbai,India,2007.
[9]Fischer,J.D.;Holliday,G.L.;Thornton,J.M.Bioinformatics 2010,26,2496.
[10]Benkovic,S.J.Annu.Rev.Biochem.1980,49,227.
[11]Rétey,J.Arch.Biochem.Biophys.1994,314,1.
[12]Stenflo,J.;Suttie,J.W.Annu.Rev.Biochem.1977,46,157.
[13] Murphy,M.J.;Siegel,L.M.;Tove,S.R.;Kamin,H.Proc.Natl.Acad.Sci.U.S.A.1974,71,612.
[14]Vorholt,J.A.;Thauer,R.K.Eur.J.Biochem.1997,248,919.
[15]Noll,K.M.;Rinehart,K.L.;Tanner,R.S.;Wolfe,R.S.Proc.Natl.Acad.Sci.U.S.A.1986,83,4238.
[16]Jordan,P.M.;Warren,M.J.FEBS Lett.1987,225,87.
[17]Negishi,M.;Pedersen,L.G.;Petrotchenko,E.;Shevtsov,S.;Gorokhov,A.;Kakuta,Y.;Pedersen,L.C.Arch.Biochem.Biophys.2001,390,149.
[18]Mendel,R.R.;Hänsch,R.J.Exp.Bot.2002,53,1689.
[19] Ginsburg,V.Progress in Clinical and Biological Research 1977,23,595.
[20]Salisbury,S.A.;Forrest,H.S.;Cruse,W.B.T.;Kennard,O.Nature 1979,280,843.
[21]Johannis,A.D.Eur.J.Biochem.1991,200,271.
[22] Schomburg,D.;Salzmann,M.Enzyme Handbook 1;Springer:New York,1990;pp 991.
[23]Toney,M.D.Wiley Encyclopedia of Chemical Biology;John Wiley&Sons,Inc.:New York,2008.
[24] Belenky,P.;Bogan,K.L.;Brenner,C.Trends Biochem.Sci.2007,32,12.
[25]Chang,J.H.;Kim,H.C.;Hwang,K.Y.;Lee,J.W.;Jackson,S.P.;Bell,S.D.;Cho,Y.J.Bio.Chem.2002,277,34489.
[26]Rétey,J.Arch.Biochem.Biophys.1994,314,1.
[27]Mato,J.M.;Lu,S.C.Hepatology 2007,45,1306.
[28]Bogerd,H.P.;Fridell,R.A.;Madore,S.;Cullen,B.R.Cell 1995,82,485.
中图分类号:O6;G64
doi:10.3866/PKU.DXHX20160439www.dxhx.pku.edu.cn
*通讯作者,Email:dengg13@mails.tsinghua.edu.cn
Discussion and Classification of Cofactors Based on Their Chemical Essences and Functions
WANGA.Zhipeng1,2DENG Geng1,*
(1Department of Chemistry,Tsinghua University,Beijing 100086,P.R.China;
2Department of Chemistry,Texas A&M University,Texas 77840,USA)
Abstract:Cofactors are vital parts of proteins and enzymes,which play remarkably significant roles in the functional realization of enzyme catalyzing processes.However,in current study system of cofactors,the definition and classification are not clear enough.In this article,we suggest to divide the various cofactors into three major groups:catalysis-type cofactors,carrier-type cofactors,and substrate-type cofactors according to their chemical essences and catalytic mechanisms,followed by the discussion of several typical cofactor examples to demonstrate the specificity and regeneration of cofactors.
Key Words:Cofactor;Coenzyme;Prosthetic group;Classification

