反相高效液相色谱法测定硫唑嘌呤代谢产物6-巯基嘌呤血浆药物浓度
朱妍妍,柏智能,唐丽琴
(1.安徽中医药大学,安徽 合肥 230031;2.安徽省立医院,安徽 合肥 230001)
反相高效液相色谱法测定硫唑嘌呤代谢产物6-巯基嘌呤血浆药物浓度
朱妍妍1,2,柏智能1,2,唐丽琴2
(1.安徽中医药大学,安徽 合肥230031;2.安徽省立医院,安徽 合肥230001)
摘要:目的建立反相高效液相色谱法(RP-HPLC)检测人血浆中硫唑嘌呤(AZA)代谢产物6-巯基嘌呤(6-MP)的浓度,为临床进行血药浓度监测提供基础。方法采用Hypersil ODS2色谱柱(250 nm×4.6 nm,5 μm),流动相为乙腈-0.3%冰乙酸化(3∶97),流速为0.8 mL·min-1,检测波长323 nm,血浆样品经15%高氯酸去蛋白后加氢氧钠(NaOH)调节pH后20 μL进样分析。结果6-MP血浆样品在0.02~2.00 mg·L-1范围内线性关系良好,最低检测下限(LLOQ)为0.02 mg·L-1;LLOQ、高浓度(1.5 mg·L-1)、中浓度(1 mg·L-1)和低浓度(0.05 mg·L-1)提取回收率分别为85.71%、92.93%、103.53%和96.02%,质控四个浓度的日内与日间精密度均<15.0%,符合中国药典生物样本分析相关规定。结论该实验成功建立一种简单、快速、高灵敏度的6-MP血浆浓度测定方法,符合AZA血药浓度监测和药代动力学研究的相关规定。
关键词:硫唑嘌呤;色谱法,反相;血药浓度
硫唑嘌呤(azathioprine,AZA)是临床上最常用的免疫抑制剂之一[1],主要用来治疗系统红斑狼疮、白血病、类风湿关节炎和炎症性肠病(IBD)等多种自身免疫性疾病及预防器官组织移植后排异反应[2]。AZA本身是一种无活性的前体药物,在体内几乎全部代谢为6-巯基嘌呤(6-MP)[3]。AZA口服生物利用度低,个体差异性大,具有剂量依赖性[4],低剂量给药治疗效果差,高剂量给药患者出现各种严重不良反应[5],据有关报道显示,口服AZA后大约20%~30% 患者出现不良反应,常见的有造血系统损害、 肝脏损害、感染、胰腺炎、胃肠道反应、肿瘤等[6]。因此,为了提高临床疗效和减少不良反应的发生,临床服用AZA的患者需监测6-MP的浓度。本研究成功建立了反相高效液相色潽法(RP-HPLC)测定人血浆中硫唑嘌呤代谢物6-MP浓度,该方法取血样量少,对患者损伤小,操作简单、快速,有较高的灵敏度和准确度,适合临床上用于进行药物浓度监测及相关药动学研究。
1仪器与试药
1.1仪器和设备Waters高效液相色谱(包括2487紫外检测器,515四元泵,TC-100柱温箱,HS色谱工作站V400+);JK-DY500型医用数控超声清洗器(合肥金尼克机械制造有限公司);BT25S电子天平(北京赛多利斯科学仪器有限公司);XW-80A微型漩涡混合仪(上海沪西分析仪器厂);TGL-16G离心机(上海安亭科学仪器厂)。
1.2药品与试剂6-MP对照品(色谱纯,Solarbio,20150225),乙腈(色谱纯,天津市福晨化学仪器厂,批号2014/10/22);冰乙酸(分析纯,无锡展望化工试剂有限公司,2014/08/20);氢氧化钠(分析纯,安徽医药站化玻部)等。
2实验方法与结果
2.1色谱条件色谱柱为Hypersil ODS2(250 nm×4.6 nm,5 μm),流动相为乙腈-0.3%冰乙酸(3∶97),流速为0.8 mL·min-1,检测波长323 nm,柱温为30 ℃。
2.26-MP标准贮备液的配制取6-MP对照品10 mg,精密称定,至10 mL棕色容量瓶,移取800 μL0.05 μmol·L-1NaOH溶液溶解后,纯化水定容至10 mL,即得1.00 g·L-1的6-MP贮备液。
2.3加药血浆样品预处理全血3 500 r·min-1离心10 min,取血浆样品200 μL加入45 μL 15%高氯酸沉淀剂去除蛋白质,涡旋振荡1 min,15 000转离心10 min,精密移取180 μL上清液,加入12 μL 4 mol· L-1NaOH溶液调pH, 20 μL进样检测。
2.4方法学考察
2.4.1专属性在“2.1”项色谱条件下,按“2.3”项下操作,检测空白血浆、标准品溶液和加药血浆样品,6-MP与血浆中内源性组分分离度高且峰形较好,分离度>1.5,空白血浆无杂质峰干扰。6-MP的相对保留时间为7.040 min,色谱图见图1。
2.4.2标准工作曲线及线性范围取180 μL空白血浆加入20 μL对照品溶液,配制成一系列浓度0.02、0.05、0.10、0.25、0.50、1.00、2.00 mg·L-1的质控样品,按“2.3”项下操作,20 μL进样检测。以6-MP血浆浓度为自变量,峰高为因变量,用加权最小二乘法进行回归分析,求得6-MP的直线回归方程即标准曲线为Y= 4 319.3X-13.486(n=7,r=0.999 9),结果表明6-MP在0.02~2.00 mg·L-1范围内线性关系良好,LLOQ为0.02 mg·L-1。
2.4.3方法准确度和精密度按“2.4.2”项下操作,配制LLOQ、低、中、高4个浓度的质控(QC)样品各制备5份,按照“2.3”项下处理样品,1 d测定1批,连续测定5 d,并同时制备标准曲线。以标准曲线计算QC样品浓度,对QC样品的测定结果进行统计分析,计算本方法的准确度(方法回收率)和精密度,结果见表1。

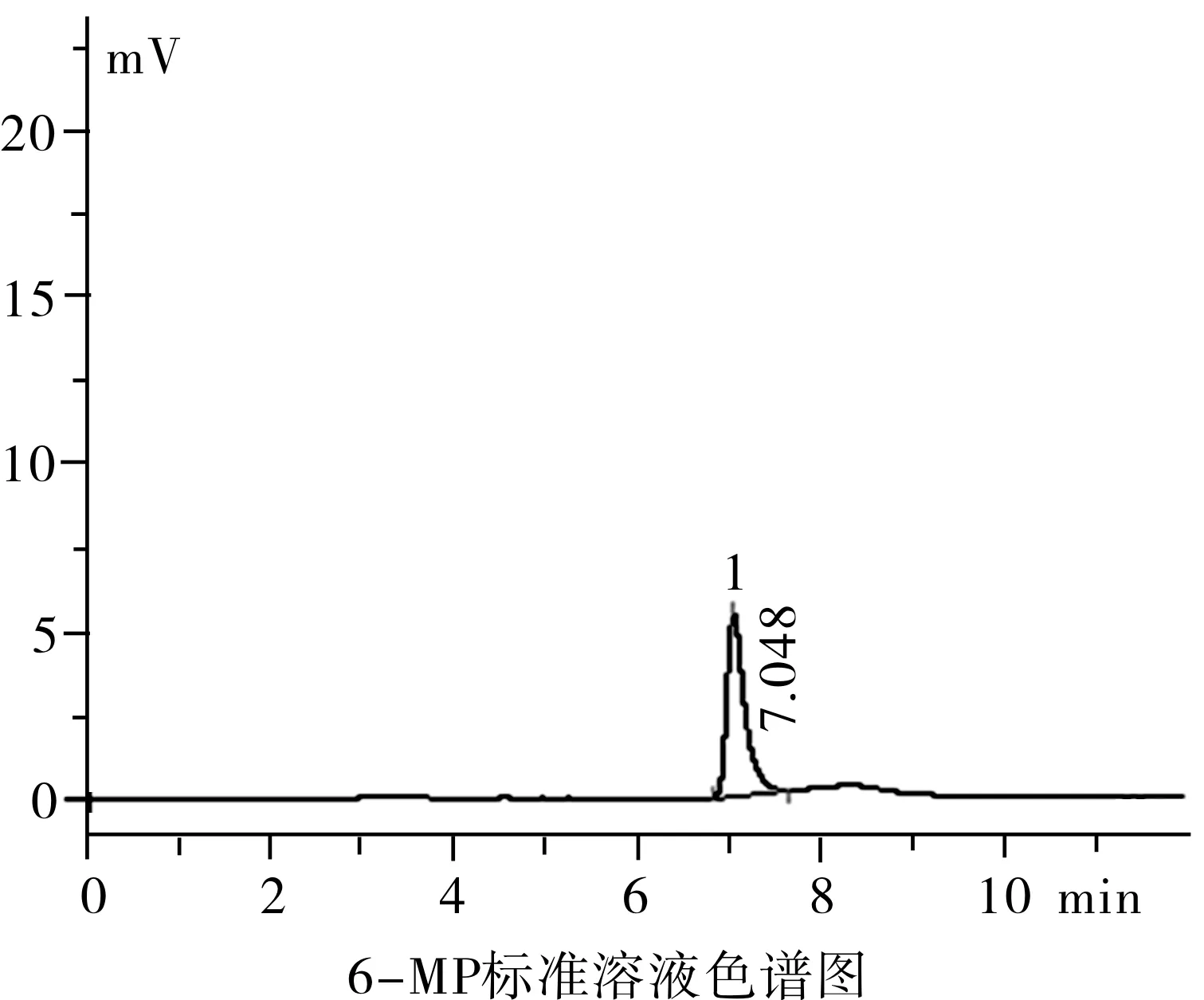

注:1为6-MP。
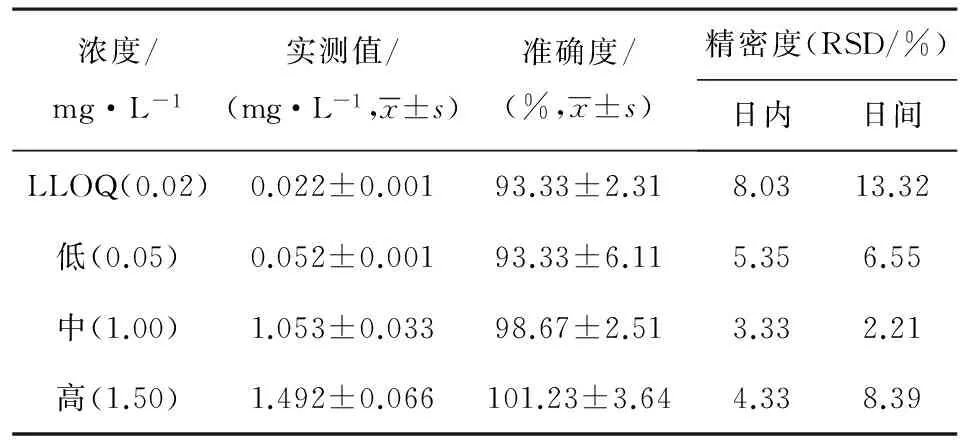
图1 6-MP血浆色谱图
2.4.4提取回收率按“2.4.2”项下操作,配制LLOQ、低、中、高4个浓度的质控样品各制备5份,按“2.3”项下同法操作,20 μL进样分析,将实际所测峰高带入当日用流动相配制的标准曲线,得相应浓度,计算其RSD,将计算所得浓度与理论浓度相比,即得提取回收率,结果见表2。

表2 6-MP的提取回收率(n=5)
2.4.5稳定性考察(1)反复冻融稳定性:按照“2.4.2”项下操作,配制LLOQ、低、中和高4个浓度的质控样品各制备5份,反复冻融3次后,按“2.3”项下方法操作,20 μL进样检测,RSD分别为9.05%、4.28%、3.08%和2.84%,均小于15%,符合中国药典生物样本分析相关规定。(2)样品预处理后室温放置稳定性:按照“2.4.2”项下操作,配制LLOQ、低、中和高4个浓度的质控样品各制备5份,按“2.3”项下方法操作,于不同时间进样检测分析,室温放置24 h内,RSD分别为10.57%、1.85%、8.28%和8.73%,均小于15%,表明样品预处理后室温放置稳定性符合中国药典生物样本分析相关规定。
3讨论
3.1色谱条件的确定查阅相关文献[7],多采用甲醇-水(5∶90)为流动相。但在实验中发现,乙腈-冰醋酸为流动相的色谱图比甲醇-水(5∶90)更好,且流动相乙腈和冰乙酸的配比对6-MP出峰时间及峰形均有较大影响,乙腈的比例能显著影响6-MP的出峰时间,冰乙酸的比例显著影响峰形。经过反复实验,最终确定以乙腈-0.3%冰乙酸(3∶97)为流动相,实验结果更加准确。在此色谱条件条件下,6-MP与血浆中内源性物质分离完全,且峰形更好,保留时间合适,检测效率较高,更适于临床血药浓度监测。
3.2血样处理方法血浆样品的处理方法会严重影响的测定结果,液-液萃取法步骤较复杂,而直接沉淀法则简单易行,临床上使用较多,但该方法仍存在一定的弊端,如有的蛋白沉淀剂并不能使蛋白沉淀完全,常易导致色谱柱堵塞,提取回收率过低等。本研究经反复验证,采用15% 高氯酸作为沉淀剂,沉淀较为完全,分离效果较好,方法提取回收率高,且该法操作简单,只需沉淀离心即可,更适用于临床进行血药浓度监测[8-9]。
4结论
本课题成功筛选出灵敏度高、选择性好、专属性强、分析快速等优点的人血浆中6-MP的HPLC测定方法,快速简捷、采血量少,其准确度和精密度良好,符合生物样本分析要求,符合临床药物浓度监测和人体药代动力学研究需要。
参考文献
[1]谢偲,岳丽杰,丁慧,等.6-巯基嘌呤致急性淋巴细胞白血病患儿不良反应及其与TPMT基因多态性的关系[J].中国当代儿科杂志,2014,16(5):499-503.
[2]Cangemi G,Barabino A,Barco S,et al.A validated HPLC method for the monitoring of thiopurine metabolites in whole blood in paediatric patients with inflammatory bowel disease[J].International Journal of Immunopathology and Pharmacology,2012,25(2):435-444.
[3]夏泉,黄燕,汪燕燕,等.巯嘌呤甲基转移酶基因多态性联合硫鸟嘌呤核苷酸血药浓度监测在硫唑嘌呤治疗炎症性肠病治疗中的临床应用[J].中国临床药理学与治疗学,2014,19 (3):302-308.
[4]沈如飞,曾繁典,师少军.硫唑嘌呤的药理作用和临床应用研究进展[J].中国药师,2013(9):1409-1412.
[5]Nielsen SN,Frandsen TL,Nersting J,et al.Pharmacokinetics of 6-Thioguanine and 6-Mercaptopurine Combination Maintenance Therapy of Childhood ALL:Hypothesis and Case Report[J].Journal of Pediatric Hematology/oncology,2015,37(3):206-209.
[6]马晓菡.硫唑嘌呤治疗激素依赖溃疡性结肠炎的疗效及安全性评价[J].国际消化病杂志,2014,34(2):114-117.
[7]黄燕,夏泉,汪燕燕,等.HPLC 法测定炎症性肠病患者红细胞中硫鸟嘌呤核苷酸浓度[J].中国药房,2013,24 (26):2436-2438.
[8]朱霞,王雪丁,晁康,等.高效液相色谱法测定人红细胞6-硫鸟嘌呤核苷酸和6-甲基巯基嘌呤核苷酸的浓度[J].中国临床药理学杂志,2016,32(3):257-260.
[9] 杨言言.HPLC法测定兰索拉唑肠溶片的血药浓度[J].安徽医药,2012,16(2):180-181.
Determination of 6-mercaptopurine in human plasma by RP-HPLC
ZHU Yan-yan1,2,BAI Zhi-neng1,2,TANG Li-qin2
(1.AnhuiUniversityofChineseMedcine,Hefei,Anhui230031,China;2.DepartmentofPharmacy,AnhuiProvincialHospital,Hefei,Anhui230001,China)
Abstract:ObjectiveTo establish a reversed phase high-performance liquid chromatography(RP-HPLC)method to determine 6-mercaptopurine (6-MP) in human plasma,thereby providing the foundation for clinical blood concentration monitoring.MethodsUsing Hypersil ODS2 column (250 nm ×4.6 nm,5 μm),the mobile phase was acetonitrile -0.3% glacial acetic acid (3∶97),the flow rate was 0.8 mL · min-1,the detection wavelength was set at 323 nm,and plasma samples were extracted by 20 μL 15% perchloric acid.ResultsA linearity was observed within the rangefrom 0.02 mg ·L-1to 2.00 mg ·L-1,the lowest detection limit was 0.02 mg ·L-1,the average method recovery rate of four concentrations were 85.71%,92.93%,103.53% and 96.02%,respectively,and the intra-day and inter-day precision are<15% and in line with the Chinese Pharmacopoeia biological sample analysis regulations.ConclusionsThe experiment successfully established a simple,fast,and low cost 6-MP plasma concentration measuring method with high sensitivity and good stability.Particularly,the method needs less blood.It is also in line with the relevant provisions of the AZA blood drug concentration monitoring and pharmacokinetics study.
Key words:Azathioprine;Chromatography,reverse-phase;Plasma concentration
通信作者:唐丽琴,女,教授,主任药师,硕士生导师,研究方向:临床药学和药理学,E-mail:tulcyl@vip.sina.com
doi:10.3969/j.issn.1009-6469.2016.06.015
(收稿日期:2016-04-06,修回日期:2016-05-06)

