查尔酮类化合物的合成及在有机合成中的应用
赵 莹,马 跃,张建平,赵永光
(河北科技师范学院化学工程学院,河北 秦皇岛,066600)
查尔酮类化合物的合成及在有机合成中的应用
赵 莹,马 跃,张建平,赵永光
(河北科技师范学院化学工程学院,河北 秦皇岛,066600)
对近年来查尔酮类化合物的催化合成方法进行了综述,以期为开发合成查尔酮类化合物相关反应的新型催化剂和新工艺提供指导,并介绍了查尔酮类化合物在有机合成中的应用。
查尔酮;催化剂;合成
查尔酮属于黄酮类化合物,是一类具有多种生物活性的化学物质,其化学结构为1,3-二苯基丙烯酮,以其为母体的化合物主要存在于甘草、红花等多种植物中。目前研究发现,此类化合物具有抗肿瘤、抗寄生虫、抗HIV、抗菌、抗炎、抗血小板凝集、抗溃疡等多种药理作用[1~6]。查尔酮类化合物及其衍生物含有许多反应活性中心,是一类重要的有机合成中间体,应用前景十分广泛[7~10]。
合成查尔酮的常见方法是以苯甲醛和苯乙酮为反应物,利用酸、碱、金属氧化物等催化剂进行羟醛缩合反应。笔者总结近年来查尔酮类化合物的催化合成方法,力求为开发合成查尔酮类化合物相关反应的新型催化剂和新工艺提供指导。此外,介绍了查尔酮类化合物在有机合成中的应用。
1 查尔酮类化合物的合成
1.1 碱催化合成查尔酮
1.1.1 传统碱催化合成查尔酮 文献上报道最多的是用强碱KOH或NaOH催化羟醛缩合反应,尽管强碱催化该反应副产物较多,但由于反应条件温和,操作简便,原料易得,该方法在查尔酮的合成中仍有重要应用。
Kolher等[11]在NaOH/EtOH体系中,用苯乙酮和苯甲醛及其衍生物进行缩合反应制得了查尔酮化合物,产率为25%~35%(图1)。
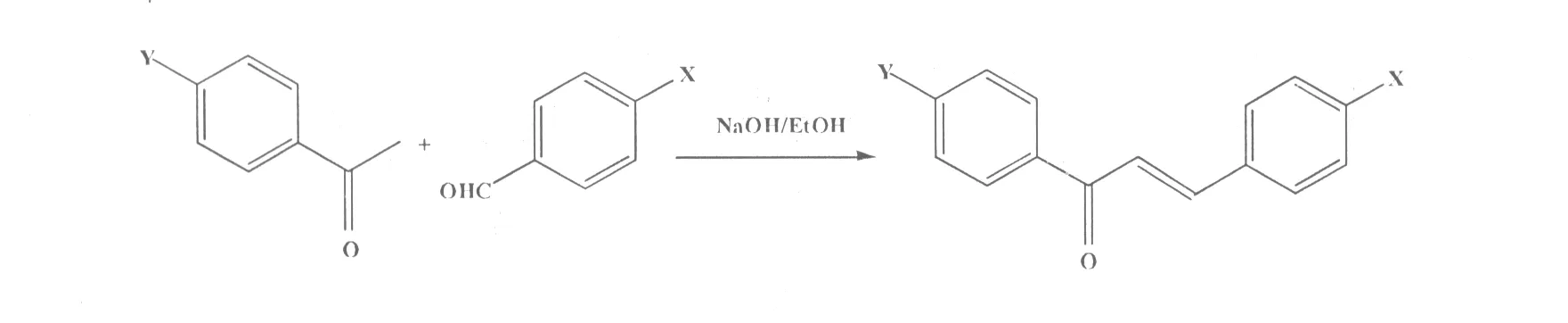
图1 NaOH催化合成查尔酮
厉恩振等[12]通过3步反应全合成具有高效抗肿瘤活性的毛叶假鹰爪素C化合物及其衍生物。查尔酮的合成是φ(EtOH)=0.95的溶液中用KOH催化剂,冰浴中30 min内逐滴加入苯甲醛,而后室温下回流24 h,产率可达78%(图2)。
党珊等[13]报道了以未保护羟基的取代邻羟基查尔酮和取代苯甲醛为原料,在稀 NaOH/EtOH溶液中,室温反应,合成了23种 2′-羟基查尔酮(图3),收率48%~90%。此方法条件温和,步骤简捷,为类似化合物的合成提供了依据。

图2 KOH催化合成查尔酮

图3 邻羟基查尔酮的合成
冯丽等[14]以含乙酰基或甲酰基的二茂铁基化合物与相应的芳香醛或酮为原料,EtOH为溶剂,KOH催化合成查尔酮化合物,产物进一步以Suzuki反应与芳基化合物偶联,合成了结构更为复杂的目标化合物(图4)。
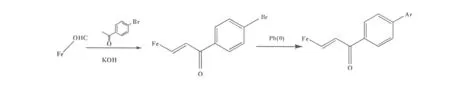
图4 二茂铁基查尔酮的合成
程格等[15]用固态反应的方法合成查尔酮(图5)。此方法将苯乙酮、苯甲醛和NaOH放在一起研磨,操作简便,反应时间短,消耗能量少,优点较多。但这种方法的缺陷是苯环上不能有羟基。

图5 研磨法NaOH催化合成查尔酮
1.1.2 强碱弱酸盐催化合成查尔酮 王存德[16]使用球磨技术促进取代苯甲醛和苯乙酮的固相羟醛缩合(图6),反应时间明显缩短,收率可达到90%~98%。

图6 无溶剂条件下查尔酮的合成
钟琦等[17]在K2CO3/THF/CH3CN体系中,发生偶联反应,制备出了一系列的查尔酮化合物(图7),收率为64%~85%。

图7 偶联反应合成查尔酮
Sebti等[18]在LiNO3/CH3CN体系中,利用芳香醛和芳香酮为原料,得到查尔酮化合物,产率为32%~98%(图8)。
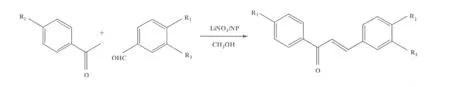
图8 LiNO3催化合成查尔酮
Sebti等[19]以芳香醛和芳香酮为原料,以质子性CH3OH为溶剂,用NaNO2或LiNO3,室温下反应16~48 h,制得相应的反式查尔酮,收率为70%~98%(图9)。

图9 NaNO2催化合成查尔酮
吴峰等[20]以苯乙酮的衍生物和苯甲醛衍生物为初始原料,在CH3OH及N,N-二甲基甲酰胺的混合溶剂的体系中,利用微波进行间歇式加热合成了8种查尔酮衍生物(图10)。

图10 微波法合成查尔酮
1.1.3 有机弱碱催化合成查尔酮 Khupse等[21]以有机弱碱哌啶作催化剂的条件下,通过缩合反应合成了查尔酮化合物,产率为80%(图11)。

图11 有机弱碱哌啶催化合成查尔酮
1.1.4 固体超强碱催化合成查尔酮 传统的碱催化方法往往副反应比较多,催化剂不能回收利用,随着绿色化学方法概念的普及,许多新型碱催化剂也逐渐被应用,它们大多具有收率高、操作简便、环境污染小等优点。
Na/NaOH/γ-Al2O3型固体超强碱是一种新型的固体碱,已成功应用于烯烃的双键转移反应、含杂原子不饱和化合物双键转移反应、共轭双烯的加氢加胺反应、烷基苯的侧链烷基化反应、酯化及酯交换反应等。李修刚等[22]以苯乙酮和苯甲醛为原料,Na/NaOH/γ-Al2O3型固体超强碱为催化剂,反应3 h合成查尔酮(图12),收率可达97%。该反应具有条件温和、催化效率高和后处理简单等优点。
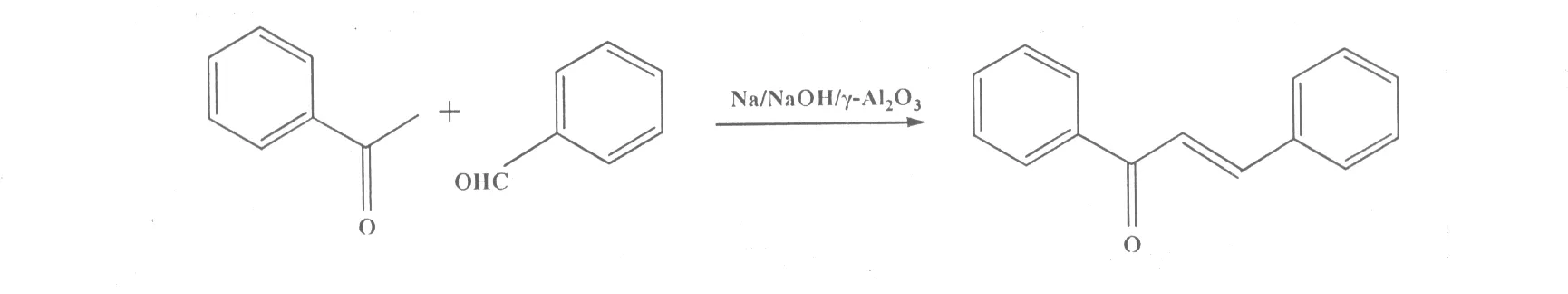
图12 固体超强碱Na/NaOH/γ-Al2O3催化合成查尔酮
KF-Al2O3催化剂由于其催化活性高,价格低廉,且易于保存被广泛应用于各类有机合成反应。以下是化学工作者使用该催化剂采取不同手段合成的查尔酮。
陆文兴等[23]在KF-Al2O3的催化下以芳香醛和芳香酮为原料,制得了查尔酮化合物,收率为55%~99%。
王书香等[24]在无溶剂条件下,室温下研磨苯乙酮、芳香醛与KF-Al2O3,放置一定时间,得到94%~98%的查尔酮化合物(图13)。该法反应条件温和,操作简便,催化剂KF-Al2O3可回收并重复利用。
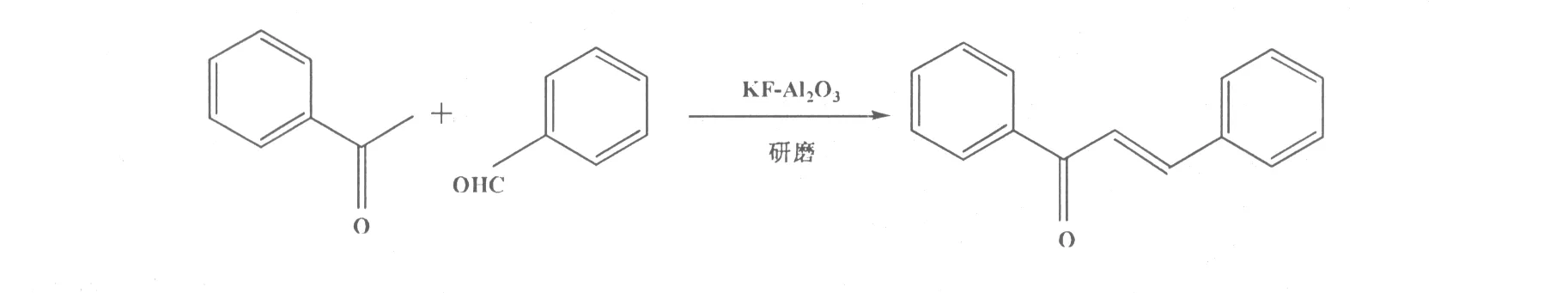
图13 KF-Al2O3催化研磨法合成查尔酮
黄丹等[25]以苯乙酮和取代苯甲醛为原料,KF-Al2O3催化下,采用超声波技术合成查尔酮类化合物(图14),研究了超声辐射功率、辐射时间对产物产率的影响,得出了最佳合成反应条件。超声功率为250 W,反应30 min,查尔酮的产率达95%以上。该方法操作简单、条件温和、反应速度快、产率高。

图14 超声辅助条件下KF-Al2O3催化合成查尔酮
曾碧涛等[26]以苯乙酮和取代苯甲醛为原料,利用微波辐射促进无溶剂羟醛缩合反应合成了8个查尔酮衍生物(图15),产率90%~98%。

图15 微波辅助条件下KF-Al2O3催化合成查尔酮
1.2 酸催化合成查尔酮
碱催化剂在查尔酮的合成中具有广泛而重要的应用,然而对于芳环上含有羟基的芳香醛,由于阴离子的离域作用(图16),导致缩合反应在碱性条件下难以进行。而以HCl,BF3,B2O3,对甲苯磺酸等传统酸作此类反应的催化剂则比较常用,其中最为常用的是EtOH饱和的HCl溶液,但是只有10%~40%的产率制约了传统酸的使用[27]。

图16 碱催化剂对羟基芳香醛的离域作用
Petrov等[28]以SOCl2/EtOH为催化剂,合成了16种查尔酮化合物(图17),产率较高,该方法不受芳香醛的芳环上羟基的影响。
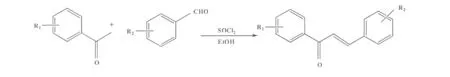
图17 SOCl2催化合成查尔酮
杨立等[28]采用F-C酰基化反应,以α,β-不饱和酰氯为初始母环,在Lewis酸AlCl3催化下,制得相应的查尔酮(图18),收率为20%。但是,由于酰基化试剂不易制备,再加上F-C酰基化反应进行的难易程度不一致,副反应较多,因此导致用该反应制备查尔酮时的产率不令人满意。

图18 AlCl3催化合成查尔酮
徐琼等[29]以竹炭磺酸为催化剂,120 ℃无溶剂条件下,回流24 h,高产率地合成了查尔酮类化合物(图19)。催化剂经反复利用其催化活性不降低。
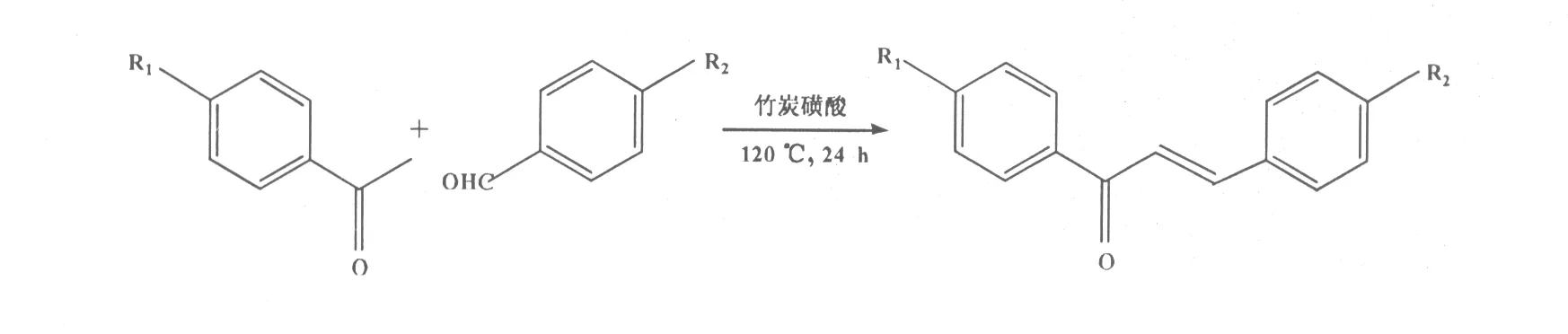
图19 竹炭磺酸催化合成查尔酮
关丽萍等[30]用2,4-二羟基苯乙酮或4-羟基苯乙酮为原料与多种醛发生反应,乙二醇为反应溶剂,硼酸为酸催化剂,合成了多个羟基查尔酮(图20)。此方法合成虽然收率不高,但是该法可以很简便的合成羟基查尔酮类衍生物。

图20 H3BO3催化合成查尔酮
Iranpoor等[31]用无水RuCl3作催化剂,无溶剂条件下,用油浴加热,在密封的玻璃管里进行羟醛缩合反应,合成了查尔酮及其衍生物(图21),收率90%~94%。该法采取无溶剂合成,减少了对环境的危害。
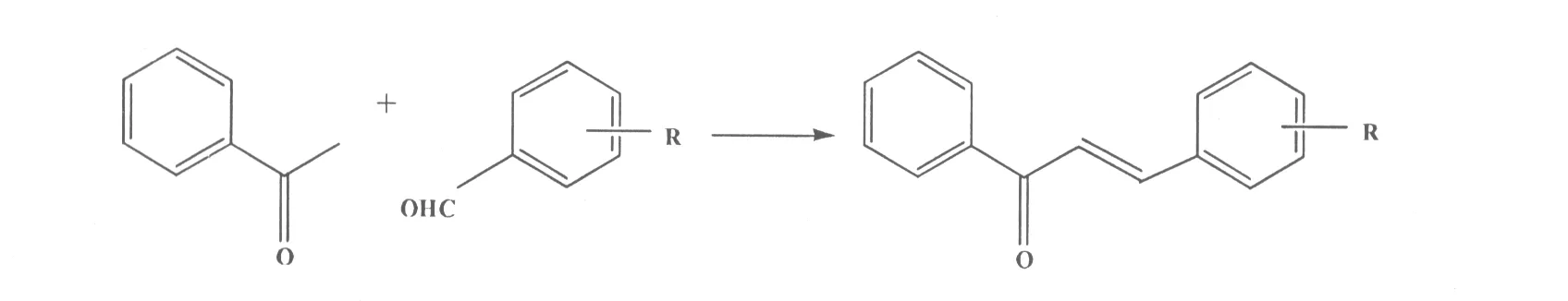
图21 RuCl3催化合成查尔酮
吴春等[32]以肉桂酰氯为初始原料,利用芳基锡引入C环,在NiCl2(PPh3)作催化剂的条件下,发生交叉偶联反应,得到13种不同的查尔酮类化合物(图22),收率为53%~92%。

图22 NiCl2(PPh3)催化合成查尔酮
1.3 相转移催化剂催化合成查尔酮
徐洲等[33]在四丁基溴化铵(TBAB)存在下,水介质中微波促进合成了羟基查尔酮及其衍生物(图23)。TBAB起到胶束的作用,且微波加热时需采取间歇加热方式,防止连续加热使水冲出体系。

图23 TBAB催化合成查尔酮
段宏昌等[34]报道了以苯甲醛衍生物和苯乙酮为原料,弱碱碳酸钾为催化剂,十六烷基三甲基溴化铵为相转移催化剂,水为溶剂,回流6 h,合成查尔酮化合物,产率高达90%。该方法具有反应条件温和、化学选择性强、不用惰性气体保护、产物易分离、合成方法简单等优点。
蒋新宇等[35]报道了以聚乙二醇 (PEG) 为相转移催化剂进行了苯甲醛与苯乙酮的克莱森-施密特缩合反应,合成查尔酮,产率80%。
刘汉文等[36]用聚乙二醇PEG-400作为相转移催化剂,在碱性的无水EtOH体系中,苯乙酮与苯甲醛室温下反应3.5 h,合成查尔酮(图24),产率可达98.1%。

图24 PEG-400催化合成查尔酮
1.4 离子液体催化合成查尔酮
离子液体完全由离子组成,具有特殊的理化性质,熔点低、不挥发、液程范围宽等优点。与传统的酸性催化剂相比,以离子液体催化羟醛缩合反应的方法具有产物便于分离,反应后的离子液体在真空条件下加热处理后可反复利用,且由于反应中不使用有毒的有机溶剂,不会对环境造成污染,是一种绿色环保的合成方法。该法的缺点是离子液体往往价格较高,黏度大,在均相体系存在离子液体催化剂与产物难以分离的问题。
Lalita等[37]研究发现,Zn-Al水滑石能较好的催化羟醛缩合反应,而以Zn-Al水滑石做支持剂负载离子液体后,二者的交互作用能改变酸碱位点,负载离子液体兼具离子液体和载体材料的特性,有利于降低成本,扩大界面积,提高催化性能。
吴浩等[38]以离子液体1,3-二丁基-2-甲基四氟硼酸咪唑盐为反应溶剂,采用水滑石作催化剂实现绿色无污染的查尔酮合成(图25)。此反应体系易于产物分离,反应时间短,反应产率高,溶剂和催化剂水滑石可以循环使用,几乎无环境污染产物产生,是一种环境友好并且有实际应用价值的查尔酮合成新方法。

图25 水滑石催化合成查尔酮
王壮坤[39]报道了以4-氯-1-丁醇,N-甲基吡唑和苯甲酸钠为原料,用微波法制得碱性离子液体,以苯甲醛和苯乙酮为原料,AIL为催化剂,经微波促进缩合反应合成查尔酮化合物(图26)。

图26 AIL催化合成查尔酮
胡晓允等[40]在无溶剂条件下,将碱性离子液体——乙醇胺乙酸盐用于催化苯乙酮与醛的Claisen-Schmidt 缩合反应制备了查尔酮。
1.5 金属及金属氧化物催化合成查尔酮
Zhu等[41]以Pb/C作催化剂,在三甲基氯硅烷存在下,DMF为溶剂,高效合成了查尔酮化合物(图27),该方法具有反应条件温和,产率高,操作简便等特点。
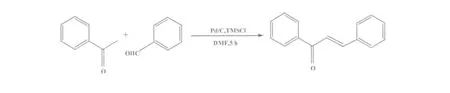
图27 Pb/C催化合成查尔酮
Engman等[42]发现有机碲氧化物BMPTO能够很好地催化芳香醛和芳香酮的羟醛缩合反应(图28),收率87%~97%。但由于BMPTO制备较困难,并且价格昂贵,因此限制了该反应的使用。
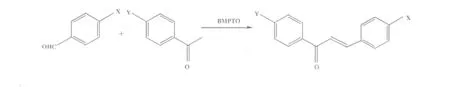
图28 BMPTO催化合成查尔酮
此外,Knatam等[43]在无溶剂条件下,以ZnO作支持剂,分别以MgO,BaO,K2O,Na2O作催化剂,140 ℃反应3 h,催化合成了查尔酮化合物,其中MgO具有更高的催化性能,而进一步以MgO附着在不同的支持剂上,显示ZnO作支持剂具有更好的催化活性。
1.6 其他方法合成查尔酮
赵志刚等[44]利用芳基锂引入C环,与原料肉桂酸及其酯发生亲核取代反应,制得了相应的查尔酮类化合物(图29)。
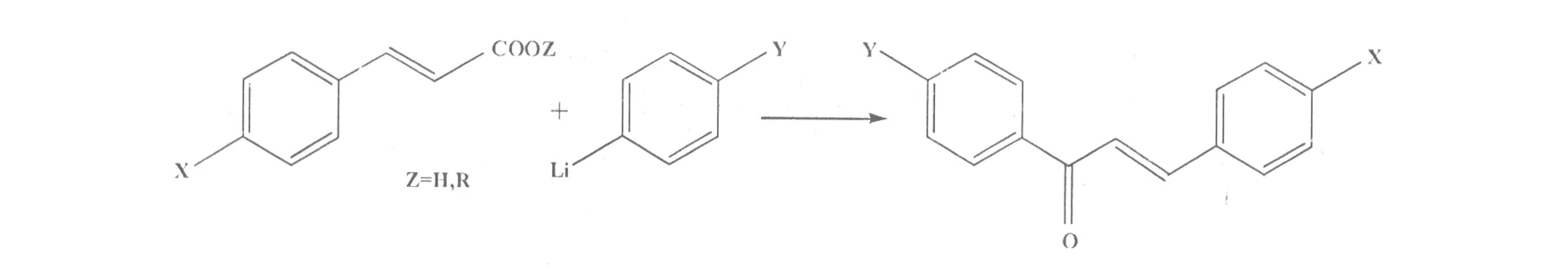
图29 以肉桂酸及其酯为原料的查尔酮合成
侯玲等[45]利用氯化亚砜、过氧化苯甲酰、N-溴代丁二酰亚胺、乙酸钠等试剂,使苯乙酮发生自身缩合反应来制备查尔酮衍生物,产率约为72%。
姜文清等[46]在NKC-9酸性树脂催化下,芳醛与苯乙酮缩合合成了5种查尔酮,收率81%~92%。该方法产率高,易于分离,且NKC-9酸性树脂可重复利用。
2 查尔酮在有机合成中的应用
2.1 合成吡啶类化合物
吡啶类化合物是一类重要的具有生物药理活性的物质,并且该化合物的光学性质在液晶、光敏化剂等方面也有着广泛的应用。因此,对其研究以及应用也是近年来的科研热点。2001年,Cave等[47]就报道了一种较为有效的合成吡啶类化合物的方法,该方法在碱性条件下,通过将芳香醛和芳香酮研磨合成查尔酮,再向体系中加入另外一种芳香酮继续研磨,发生迈克尔加成反应生成1,5-二酮类化合物,在少量的醋酸溶剂中,1,5-二酮和醋酸铵被高产率的氧化形成吡啶环。
2.2 合成黄酮类化合物
查尔酮类化合物是合成黄酮类化合物的前体,湖南大学的张红[48]从简单的芳香醛和间苯二酚出发,经醛酮缩合得到甲氧基甲醚保护的关键中间体系列查尔酮,查尔酮经水解反应得到系列羟基查尔酮,而后发生亲核取代得到系列异戊烯基取代的查尔酮类衍生物。最后,查尔酮用不同的关环方法合成黄烷酮、黄酮醇类化合物。
2.3 合成二氢查尔酮
在大多数植物的果实内大部分都含有各种类型的二氢查尔酮衍生物,报道称此类化合物多具有抗病毒活性、抗生理活性以及抗菌活性。此外,一些特殊的二氢查尔酮有抗肿瘤的作用。查尔酮化合物的存在为新型的二氢查尔酮衍生物的合成提供了条件。杨金会等[49]以2,4,6-三羟基苯乙酮和对羟基苯甲醛为起始原料,经选择性的甲基化、甲氧甲基化、羟醛缩合、还原、脱保护等反应合成了2′,4-二羟基-4′,6′-二甲氧基-二氢查尔酮。
2.4 查尔酮的迈克尔加成反应
查尔酮类化合物可与1,3-二羰基化合物在碱性条件下发生麦克尔加成反应。1,3-二羰基化合物在NaOH,Ba(OH)2,EtONa及KOH等强碱性催化剂催化下,虽然是形成碳碳双键的有效方法,但是总会引起很多副反应降低产率。近年来,新型的碱性催化剂无机载体氟化物在此类有机合成中有着较为广泛的应用。苏州师范大学的王苏惠等[49]成功研究出以KF/Al2O3为催化剂,催化达米酮与查尔酮的麦克尔加成反应。
吴浩等[38]采用高速振动研磨法,以K2CO3为催化剂,高速振动研磨进行无溶剂合成,合成出高产率、高纯度的化合物。其中,1,3-丙二酸二乙酯和乙酰乙酸乙酯与查耳酮以及氮杂查耳酮的固相加成也是用这种方法成功合成的。
2.5 查尔酮与胺类化合物的加成
查尔酮化合物还可以和胺类化合物发生加成反应。Shan等[50]报道了查尔酮类似物N-肉桂酰基吡唑啉与盐酸羟胺在KOH和EtOH混合溶液回流生成异恶唑啉。Jadhav等[51]用查尔酮和水合肼在CH3OH溶液中回流得到吡唑啉。此外,查尔酮类化合物与乙氰乙酰尿素和乙氰乙酰哌啶的迈克尔加成以及肼类物质等有机合成方面均较为广泛的应用。
3 展 望
查尔酮有许多生物活性,如抗氧化、抗肿瘤、防癌、抑菌消炎、抗病毒活性等,在医药、食品等领域有广泛应用。如今,用于合成查尔酮化合物的原料和方法已有很多,但这些方法还存在着不足,常用的强碱如NaOH或RONa溶液催化合成查尔酮,收率较低,而且副产物多。固体超强碱催化剂催化效率高、可回收并重复利用;强酸催化剂催化合成查尔酮,反应时间一般较长,而且产率不高;有机金属合成法一般产率较高,反应速度快,但是催化剂制备较困难,价格也比较昂贵;金属盐催化合成法制备简单,提纯方便,且可反复使用,缺点是反应时间太长,产率不高;离子液体往往价格较高,黏度大,在均相体系存在离子液体催化剂与产物难以分离的问题。因此,开发新的合成工艺、新的催化剂,从绿色化学的原子经济性角度合成查尔酮仍是今后继续研究的方向。
[1] 郑洪伟,牛新文,朱君,等.查尔酮类化合物生物活性研究进展[J].中国新药杂志,2007,16(18):1 445-1 449.
[2] Santos L,Curi Pedrosa R,Correa R.Biological evaluation of chalcones and analogues as hy-polipidemic agents[J].Archiv der Pharmazie,2006,339(10):541-546.
[3] 杨彩霞,田春莲,耿健,等.黄酮类化合物抗菌作用及机制的研究进展[J].中国畜牧兽医,2014,41(9):158-162.
[4] 刘文虎,常晋霞,张建武.含查尔酮结构香豆素衍生物的合成及抗肿瘤增殖活性[J].中国药科大学学报,2014,45(5):522-528.
[5] 邢肖兰,刘婷婷,宋明霞,等.含查尔酮结构N-取代饶丹宁衍生物的合成及抗菌活性研究[J].中国药物化学杂志,2013,23(1):1-7.
[6] 旷春桃,李湘洲,郭远良,等.查尔酮衍生物的合成及其抗菌和抗氧化活性研究[J].中国科技论文,2013,8(9): 862-864.
[7] Murthy Y L N,Viswanath I V K,Pandit E N.Synthesis, Characterization & Antibacterial Activity of 7,41-Dihydroxy,31-Methoxy Flavones[J].International Journal of Chem Tech Reaserch,2010,2(2):1 097-1 101.
[8] 方正,唐伟方,徐芳.萘丁美酮的合成工艺改进[J].中国药科大学学报,2004,35(1):90-91.
[9] 楼定忠,朱坡,刘泽贵.萘丁美酮合成路线图解[J].中国医药工业杂志,1996,27(5):238-239.
[10] 廖头根,汪秋安,方伟琴,等.新型查尔酮类化合物的合成及其生物活性研究[J].有机化学,2006,26(5):685-689.
[11] Kohler E P,Chadwell H M.Synthesis of Chalcone[J].Org Syn,1956,1(1):78-83.
[12] 厉恩振.毛叶假鹰爪素C衍生物的合成与活性评价[D].北京:中国人民解放军军事医学科学院,2012.
[13] 党珊,刘锦贵,王国辉.室温下2′-羟基查尔酮的合成[J].合成化学,2008,16(4):460-463.
[14] 冯丽.含二茂铁基查尔酮的合成研究[D].西安:陕西科技大学,2012.
[15] 程格,甘秋,王跃川.固态缩合反应合成查耳酮[J].化学试剂,2000,22(3):181.
[16] 王存德,郭明珠,周志锋.无溶剂快速合成查耳酮[J].化学试剂,2004,26(1):55.
[17] 钟琦,邵建国,刘长庆.用碲Ylide合成α,β-不饱和酮[J].有机化学,1990(5):459-463.
[18] Khupse R S,Erhardt P W.Practical synthesis of lespedezol A1[J].Journal of Natural Products,2008,71(2):275-277.
[19] Sebti S,Solhy A,Smahi A,et al.Dramatic activity enhancement of natural phosphate catalyst by lithilum nitrate: An efficient synthesis of chalcones[J].Catalysis Communications,2002,3(8):335-339.
[20] Sebti S,Solhy A,Tahir R,et al.Calcined sodium nitrate/natural phosphate: An extremely active catalyst for the easy synthesis of chalcones in heterogeneous media[J].Tetrahedron Letters,2001,42(45):7 953-7 955.
[21] 吴峰,龚飞,杨国青,等.微波辐射合成查尔酮衍生物[J].山地农业生物学报,2014,33(3):88-90.
[22] 李修刚,丁德军,高根之,等.固体超强碱催化合成查尔酮的研究[J].工业催化,2008,16(9):71-74.
[23] 陆文兴,颜朝国,顾惠芬.查尔酮的KF-Al2O3催化合成[J].化学试剂,1995,17(4):253-254.
[24] 王书香,李记太,王振华.研磨法合成α,β-不饱和酮[J].有机化学,2004,24(4):447-449.
[25] 黄丹,江国庆.超声技术在查尔酮合成中的应用研究[J].有机化学,2002,22(12):1 057-1 059.
[26] 曾碧涛,赵志刚,易奉敏,等.微波促进无溶剂合成查尔酮衍生物[J].合成化学,2007,15(5):625-627.
[27] 厉恩振,吴久鸿,张学辉,等.查尔酮类化合物的合成研究进展[J].中国药学杂志,2013,48(6):401-406.
[28] Petrov O,Ivanova Y,Gerova M.SOCl2/EtOH: Catalytic system for synthesis of chalcones[J].Catalysis Communications,2008,9(2):315-316.
[29] 徐琼.生物质炭磺酸的制备及催化性能研究[D].长沙:湖南师范大学,2008.
[30] 关丽萍,尹秀梅,全红梅,等.羟基查尔酮类衍生物的合成[J].有机化学,2004,24(10):1 274-1 277.
[31] Iranpoor N,Kazemi F.RuCl3catalyses Aldol Condensations of aldehydes and ketones[J].Tetrahedron,1998,54(32):9 475-9 480.
[32] 吴春,刘宝殿,吴艳华,等.有机锡试剂在查耳酮合成中的应用[J].黑龙江商学院学报(自然科学版),1994,10(3):52-57.
[33] 徐洲,宛瑜,沈阳,等.四丁基溴化铵存在下水介质中微波促进2-羟基查尔酮的合成[J].徐州师范大学学报(自然科学版),2006,24(1):64-66.
[34] 段宏昌,姜恒,宫红.查耳酮衍生物的绿色合成[J].中国药业,2006,15(15):30-31.
[35] 蒋新宇,赵爱丽.聚乙二醇相转移催化法合成查耳酮[J].广州化学,2006,31(3):1-5,10.
[36] 刘汉文,谭凤姣,李康应.相转移催化合成亚苄基苯乙酮研究[J].化学试剂,2000,22(1):50-51.
[37] Kunde L B,Gade S M,Kalyani V S,et al.Catalytic synthesis of chalcone and flavanone using Zn-Al hydrotalcite adhere ionic liquid[J].Catalysis Communications,2009,10(14):1 881-1 888.
[38] 吴浩,叶红齐,陈东初.绿色合成查尔酮新方法的研究[J].工业催化,2006,14(6):34-37.
[39] 王壮坤.微波促进碱性离子液体催化合成查尔酮[J].合成化学,2015,23(3):202-209.
[40] Hu Xiaoyun,Wei Liyan,Zhong Shishi,et al.A Green Synthesis of Chalcones Catalyzed by An Alkaline Ionic Liquid under Solvent-Free Condition[J].中南民族大学学报(自然科学版),2015,34(4):19-23.
[41] Zhu Y L,Pan Y J.A new Lewis acid system Palladium/TMSCI for catalytic aldol condensation of aldehydes with ketones[J].Cheminform,2004,35(45):668-669.
[42] Engman L,Cava M P.Bis(p-methoxyphenyl)telluroxide, a novel organotellurium aldol catalyst[J].Tetrahedron Letters,1981,22(52):5 251-5 252.
[43] Knatam M L,Prakash B V,Reddy C V.Efficient synthesis of chalcones by a solid base catalyst[J].Synth Commun,2005, 35(14):1 971-1 978.
[44] 赵志刚,李良助,廖戎.应用芳基锂合成查尔酮[J].成都理工学院学报,2000,27(2):217-220.
[45] 侯玲,李依南,刘若灿,等.新型查尔酮类衍生物的合成[J].应用化工,2014,43(7):1 297-1 298,1 302.
[46] 姜文清,邹建平,安礼涛.NKC-9酸性树脂非均相催化合成查耳酮[J].苏州大学学报(自然科学版),2008,24(1):78-79,90.
[47] Cave G W V,Raston C L.Efficient synthesis of Pyridines via a sequential solventless Aldol Condensation and Michael Addition[J].Journal of the Chemical Society Perkin Transactions,2001,1:3 258-3 264.
[48] 张红.新型查尔酮与黄酮醇类化合物的合成及其生物活性研究[D].长沙:湖南大学,2007.
[49] 王苏惠,王香善,史达清,等.KF-Al2O3催化下达米酮与查尔酮的麦克尔加成反应[J].有机化学,2003,23(10):1 146-1 148.
[50] Shan T,Desai V.Synthesis and antibacterial studies of some new isoxazoline derivatives[J].J Serb Chem Soc,2007,72:443-449.
[51] Jadhav S B,Shaltri R A,Gaikwad K V,et al.Synthesis and antimicrobial studies of some novel pyrazoline and isoxazoline derivatives[J].E-J Chem,2009,6:s183-s188.
(责任编辑:朱宝昌)
Synthetic Methods of Chalcone and Its Application in Organic Synthesis
ZHAO Ying, MA Yue, ZHANG Jianping, ZHAO Yongguang
(College of Chemistry Engineering, Hebei Normal University of Science & Technology,Qinhuangdao Hebei,066600,China)
Many catalytic synthesis methods of chalcone compounds were summarized, which was expected to provide guidance for the development of new catalysts and new technology for chalcone synthesis. And the application of these compounds in organic synthesis was also introduced in this paper.
chalcone; catalyst; synthesis
10.3969/J.ISSN.1672-7983.2016.03.010
河北省高等学校科学技术研究青年基金项目(项目编号:QN20131095)。
2016-09-14; 修改稿收到日期: 2016-09-26
TQ244.5
A
1672-7983(2016)03-0055-11
赵莹(1979-),女,硕士, 讲师。主要研究方向:有机合成。

