热解温度及AAEM元素对生物质快速热解焦油的影响
冯冬冬,赵义军,唐文博,张宇,钱娟,孙绍增(哈尔滨工业大学能源科学与工程学院,黑龙江 哈尔滨 150001)
热解温度及AAEM元素对生物质快速热解焦油的影响
冯冬冬,赵义军,唐文博,张宇,钱娟,孙绍增
(哈尔滨工业大学能源科学与工程学院,黑龙江 哈尔滨 150001)
摘要:生物质热解受热解温度、热解速率和碱金属及碱土金属(AAEM)元素影响显著。利用热裂解气相色谱质谱联用法(Py-GC/MS)针对热解温度及AAEM元素对生物质快速热解焦油的影响展开深入研究,通过样品热解前后的失重情况分析了热解温度及AAEM元素对生物质(稻壳和木屑、酸洗稻壳和酸洗木屑)热解特性的影响规律,利用气相色谱质谱仪(GC/MS)对热解焦油组分及含量进行了在线半定量分析,并对热解焦油组分分子量分布情况展开了讨论。结果表明生物质Py-GC/MS快速热解实验,酸洗脱除AAEM元素致使热解失重率减小。500~900℃范围内随温度的升高,大分子焦油成分逐渐减少,逐渐转化为轻质组分。AAEM元素限制了焦油前体的聚合,进一步抑制了含氧杂环类碳环(糠醛等)的生成。稻壳的热解焦油的相对分子质量主要分布在110~129。木屑快速热解焦油产率明显高于稻壳,且热解焦油中分子量分布广泛,含有更多较大分子量(150~209)的化合物成分。
关键词:生物质;快速热解;AAEM;Py-GC/MS;焦油
2015-12-15收到初稿,2016-02-18收到修改稿。
联系人:赵义军。第一作者:冯冬冬(1988—),男,博士研究生。
Received date: 2015-12-15.
Foundation item: supported by the National Natural Science Foundation of China (51206037) and the Postdoctoral Fund in China (2013M541376).
引 言
热解是生物质热化学转化技术中的基础过程[1-2],是生物质在缺氧条件下,生成液体、气体、固体3种产物的热降解过程。快速热解为了提高生物油的产率,在生物质被降解之前迅速达到目标温度,其加热速率高达1000℃·s−1以上[1]。热解的挥发分产物通过扩散和对流被输运到颗粒外部,作为挥发分前体的大分子结构在生物质颗粒内部进行裂解。在高的加热速度下会产生更多的挥发分前体,在生物质颗粒内部形成更高的压力或浓度梯度,从而提高了其扩散和对流的输运驱动力,缩短这些前体在颗粒内部的停留时间,从而缩短前体在颗粒内部的聚合反应和热裂解反应[3]。常规热解法因传热率有限,所得的焦油产物缩聚程度较大,焦油中所能反映出的生物质结构信息与快速热解产生的真实焦油成分有一定的差异。而热裂解气相色谱质谱联用法(Py-GC/MS),升温速率可达20000℃·s−1,有效避免了热解过程中温度的滞后,快速热解条件下所提供的能量足以满足小分子相克服传质所需,使得生物质中的大分子结构尚未对其进行捕获、缩合就逸出了生物质的固相表面[4],因而极大程度地减小了传统快速热解过程中挥发分与焦炭间所存在的二次反应[5-7]。生物质焦油是生物质在热解、气化等反应过程中,部分分子键发生断裂后重新组合,形成的分子量较大的有机可凝结物质[8]。国内外对生物质快速热解及其热解焦油组分进行了大量研究[9-14], 研究结果表明热解温度很大程度地影响着生物质热解产物产率的分布,并且影响着挥发分重质组分的二次裂解[10-11]。随着热解温度的升高,生物质内芳香族化合物和呋喃类物质会发生进一步裂解,而逐渐转化为轻质组分[10-11,13]。生物质内碱金属及碱土金属(AAEM)元素是制约生物质热解及气化反应活性的重要因素之一[15],其影响着反应过程中生物质组分内分子键的断键与重组,从而影响着生物质焦油的形成[16-17]。然而,关于生物质中AAEM元素对热解焦油成分的影响未见相关报道。
基于上述研究现状,本文将多年生植物(木屑)和一年生植物(稻壳)进行了酸洗处理,有效脱除了生物质原料内的AAEM元素,利用Py-GC/MS 在500~900℃热解温度下,对两类生物质原料及两者对应的酸洗原料进行了快速热解的实验研究。通过样品热解前后的失重情况对热解温度及AAEM元素对生物质热解特性的影响规律进行了研究,利用气相色谱质谱仪(GC/MS)对热解焦油组分及含量进行了在线半定量分析,并对热解焦油组分分子量分布情况展开了讨论。
1 实验材料和方法
1.1实验样品制备
本文选取黑龙江省哈尔滨市五常稻壳及小兴安岭核桃楸木屑为原料,研磨筛分至150~250 μm,105℃干燥12 h,即得到生物质原始物料(origin)。将生物质稻壳及木屑原料,按照液固质量比为30:1,与0.2 mol·L−1的硫酸溶液混合,在磁力搅拌器中氩气气氛下搅拌24 h,将混合物进行抽滤并用去离子水反复洗涤,至洗涤液pH恒定,最后将样品再次筛分至150~250 μm,得到生物质酸洗原料(H-form)。稻壳与木屑原始物料的工业分析及元素分析如表1所示,其原始及酸洗物料中AAEM元素含量分析如表2所示。

表1 稻壳与木屑原料的工业分析及元素分析Table 1 Proximate and ultimate analyses of rice husk and sawdust

表2 稻壳与木屑原料AAEM元素含量分析Table 2 AAEM species analyses of rice husk and sawdust/mg·g−1
1.2生物质快速热解焦油Py-GC/MS测试
采用热裂解仪(美国CDS公司CDS5200型Py)和气相色谱-质谱联用仪(美国Agilent公司6890-5975 型GC/MS)联用。利用Py-GC/MS在线分析热解温度及AAEM元素对生物质快速热解焦油的组成与含量的影响。实验过程中每次采用生物质待测原料1.5 mg装入石英反应管内,在20000℃·s−1的升温速率下,快速升温至目标温度(500、600、700、800、900℃),在目标温度下保温30 s。热解焦油组分分析采用裂解仪后置出口与GC/MS联用的测试方法,连接管道保温为300℃。裂解仪(Py)与GC/MS同步激发,选用DB-5ms色谱柱(长30 m,内径0.25 mm, 膜厚0.50 μm),采用的分流比为40:1,进样口温度260℃,氦气作为载气,载气流量选取为1.5 ml·min−1。气相升温程序如下:40℃保温3 min,后以5℃·min−1的升温速率升温至260℃,保温5 min。GC/MS测定峰图归属由NIST峰图库及标准物的停留时间确定,相对分子质量测试范围50~500。
2 实验结果与讨论
2.1生物质快速热解失重率分析
生物质稻壳和木屑快速热解反应前后的失重率对比如表3所示。在500℃条件下,对于稻壳而言,其酸洗样品失重率为68.86%,原稻壳失重率为70.29%;对于木屑而言,样品的热解失重率均明显高于稻壳原料,其酸洗样品失重率为72.00%,原木屑失重率为74.67%,主要原因在于木屑原料的挥发分含量(77.13%)明显高于稻壳原料挥发分含量(58.53%),如表1所示。由表3看出,当热解温度从500℃升高至900℃时,样品失重率逐渐增加,900℃时样品失重率达到最大值。在900℃条件下,酸洗稻壳的失重率为79.61%,原始稻壳的失重率为83.02%。相比于稻壳原料,由于木屑内灰分及AAEM元素含量较低,酸洗对木屑失重率的影响较小,酸洗木屑900℃下的失重率为91.25%,原始木屑的失重率为92.55%。不难发现,随着热解温度的逐渐升高,生物质热解失重率逐渐增大,并且相关文献表明该过程并不利于热解焦油产物的形成[3]。由表3所示,无论稻壳还是木屑原料,在500~900℃条件下,酸洗样品的失重率均小于原始物料的失重率,国内外相关文献对酸洗脱除AAEM物质后煤与生物质原料的热解行为进行了研究,表明酸洗原料在高加热速率下的焦油产量明显高于原始物料在相同条件下的焦油产量[18-20],并且酸洗物料产生的焦油热稳定性较差,在一定条件下发生了二次裂解[18,21-23]。该现象可以解释为,生物质原料经0.2 mol·L−1硫酸溶液洗涤后,生物质内所含AAEM元素含量明显降低,如表2 所示。在生物质的大分子结构中,AAEM元素实际上是以交联点的形式存在[24],并增大了生物质基体的密度[25],使生物质大分子结构中碎片单元的蒸气压降低而抑制其蒸发。在生物质酸洗原料热解脱除挥发分的过程中,生物质炭基质结构的开环断键、自由基再聚合形成焦炭及焦油大分子结构的过程,在没有AAEM存在的条件下变得更加容易。因AAEM元素在生物质热解反应过程中交替地在固相炭基质及气相焦油自由基组分的活性位点上断键、成键,使得碳碳键(C C)的连接位点上出现了AAEM元素变为C AAEM键的连接形式,热解反应过程中碱金属与碱土金属元素以交联点的形式来抑制焦油的形成[26],从而一定程度地阻碍了焦炭或焦油分子芳香环结构聚合的发生,进而解释了酸洗生物质原料热解失重率的降低以及其焦油产率的提高[18]。
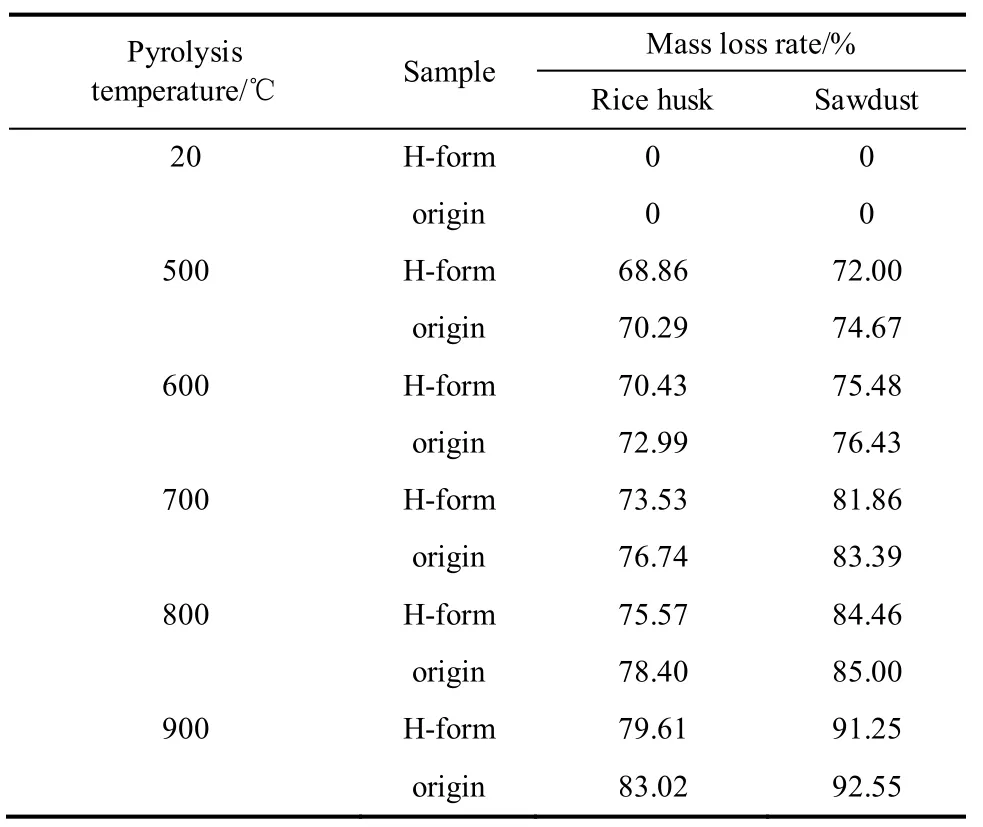
表3 稻壳与木屑热解反应前后失重率对比Table 3 Mass loss rate of rice husk and sawdust before and after pyrolysis
2.2生物质快速热解焦油成分分析
2.2.1稻壳快速热解焦油成分分析图1和表4是不同温度下(500~900℃)稻壳热解焦油图谱及各成分分析结果。可以看出,温度在500~700℃范围内谱峰数量及峰强浓度比例变化不大,这与吴文广[27]得到的结论相一致。而在800~900℃,谱峰的数量及峰强随温度升高而迅速减少,焦油的生成量明显降低。由GC/MS分析图可以看出,在500~900℃范围内随温度的升高,大分子焦油成分含量逐渐减少,更多地形成了小分子的焦油及气体成分。通过比较原始稻壳和酸洗稻壳的谱图可以直接看出,酸洗稻壳快速热解生成的焦油成分与原始稻壳生成的焦油成分并不完全一致,存在新的焦油物种产生,例如12.99 min处的5-甲基糠醛等;与此同时伴随着一些焦油成分的消失,例如11.77 min处的1,2-环戊二酮和15.05 min处的3-甲基环戊烷-1,2-二酮。表明在热解反应过程中,AAEM元素限制了焦油前体的聚合,进一步抑制了含氧杂环类碳环(糠醛等)的生成。在峰强度方面,酸洗稻壳相比于原始稻壳而言,其总的GC/MS峰面积明显增加,表明其热解焦油含量增多,表明通过酸洗将稻壳原料内的AAEM元素脱除,导致热解过程中缺少了AAEM元素通过热解前或热解过程中充当交联点而抑制焦油的形成的重要作用,致使在热解反应过程中有新的焦油成分产生,且原热解焦油产率也相对增加[18]。
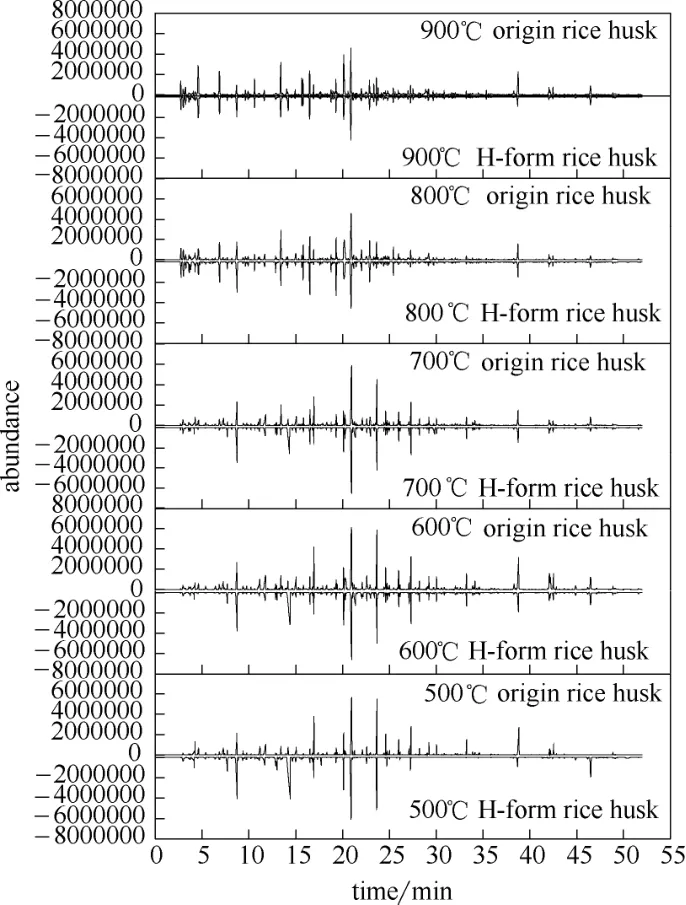
图1 500~900℃所得稻壳Py-GC/MS热解焦油谱图Fig.1 Rice husk pyrolysis tar Py-GC/MS analysis at 500—900℃
由图1可知,生物质Py-GS/Ms法热解反应过程检测到的焦油成分在实验起始的0~25 min内集中析出。由表4可知,表中各数据是稻壳在500~900℃所得Py-GC/MS热解焦油分析结果,为对应成分的面积百分比,表中“—”则表示未被检测。稻壳500~900℃热解焦油成分以含氧成分的烃类或含取代基的低环芳烃为主,由表4可以看出,呋喃甲醛、二甲基苯酚、邻苯二酚、2,3-苯并呋喃、2-羟基-5-甲基苯乙酮和棕榈酸是不同热解温度及稻壳(origin和H-form)共有的主要成分,占总含量的比值均超过3%,部分样品含量比值达到20%以上。
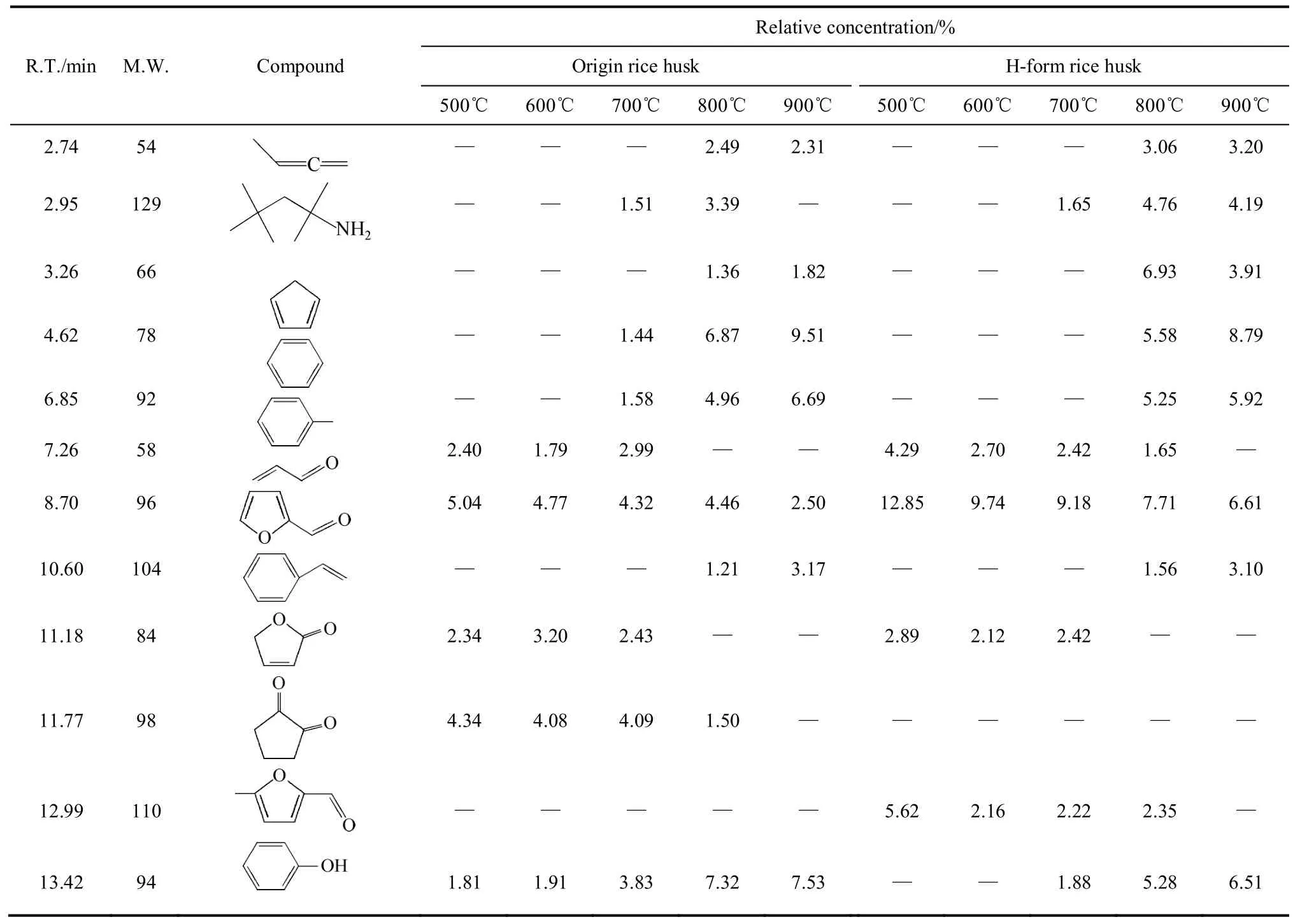
表4 稻壳在500~900℃所得Py-GC/MS热解焦油分析结果Table 4 Py-GC/MS analysis of rice husk pyrolysis tar at 500—900℃

Table 4 (continued)
随着热解温度的升高,呋喃甲醛、2,3-苯并呋喃,2-羟基-5-甲基苯乙酮和棕榈酸占总焦油含量下降显著,原始稻壳热解焦油中呋喃甲醛由500℃时的5.04%下降到900℃时的2.50%,酸洗稻壳焦油中呋喃甲醛由500℃时的12.85%下降到900℃时的6.61%;原始稻壳热解焦油中2,3-苯并呋喃由500℃时的20.32%下降到900℃时的13.05%,酸洗稻壳焦油中2,3-苯并呋喃由500℃时的20.31%下降到900℃时的14.28%;同样,原始稻壳热解焦油中2-羟基-5-甲基苯乙酮由500℃时的11.08%下降到900℃时的5.05%,酸洗稻壳焦油中2-羟基-5-甲基苯乙酮由500℃时的8.88%下降到900℃时的3.30%。在500~600℃范围内新增的焦油成分的形成,以及在较高温度下(700~900℃),焦油成分进一步的分解与转化,致使原始组分比例下降;此外AAEM元素在生物质热解反应过程中交替地在气固相自由基组分的活性位点上断键、成键,通过热解前或热解过程中充当交联点而影响焦油的形成,从而一定程度地影响了热解焦油各组分占总焦油成分的比例。另一部分焦油含量随着热解终温的升高而增大,热解温度的升高使得生物质挥发分更大程度地析出,并且该过程伴随着大分子焦油成分逐渐裂解转化为小分子焦油。例如二甲基苯酚、邻苯二酚等,原始稻壳热解焦油中二甲基苯酚由500℃时的3.02%升高到900℃时的10.03%,酸洗稻壳焦油中二甲基苯酚由500℃时的3.12%升高到900℃时的9.86%;原始稻壳热解焦油中邻苯二酚由500℃时的3.73%升高到900℃时的10.59%,酸洗稻壳焦油中邻苯二酚由500℃时的4.89%升高到900℃时的7.80%。
随着温度的升高,生物质热解焦油由低温下的初级焦油,逐步转化为中温下的次级焦油[28]。结合表4中的焦油成分分析,可以看出在500~600℃下生物质焦油以酚类及其取代同系物的含量最大,以CH3、OCH3等为主要取代基,其在较高温度下会逐渐以气体等形式断键析出,如C O和C O官能团以CO或CO2形式析出,含CH3支链会逐渐转化为CH4析出[29],且焦油的分布情况以次级焦油分布为主。
为了较为清晰地解析生物质热解焦油分子量的分布情况,本文按照焦油组成分子量大小的分布情况对热解焦油进行了研究[27]。利用局部加权的计算方法,将热解焦油分子量进行局部加权,以中间分子量作为平均分子量,得到生物质稻壳热解焦油组分随分子量的分布情况,如图2所示。生物质稻壳快速热解焦油成分随焦油产物分子量的分布情况较为集中,原始稻壳及酸洗稻壳的快速热解焦油产物的相对分子质量分布主要在110~129的范围内,其对应的代表性产物有5-甲基糠醛、N-丁基叔丁胺、2-甲氧基苯酚、邻苯二酚、2,3-苯并呋喃等,在500~900℃对应温度条件下该分子量范围内酸洗稻壳的热解焦油百分比例均高于原始稻壳的焦油产率,这与2.1节分析的酸洗脱除AAEM元素后稻壳焦油产率有所提高的结论相一致。另在90~109和150~169的相对分子质量范围中也含有较多的焦油比重,但该组中焦油种类较多,在此不详细展开陈述。

图2 稻壳热解焦油产物随平均分子量分布规律Fig.2 Rice husk pyrolysis tar distribution with average molecular weight
2.2.2木屑快速热解焦油成分分析图3是不同热解温度对原始木屑及酸洗木屑原料快速热解焦油产物的GC/MS分析谱图,随着热解温度的升高(500~600℃),谱峰变化较小,且丰度值也不大,在700~900℃范围内,GC/MS谱峰数目及丰度值均出现了明显下降,且随温度的升高,明显可以看出热解逐渐产生了较低分子量的有机成分,此变化规律与稻壳相似。与稻壳热解焦油分布(集中在25 min之前)不同,木屑热解焦油具有更为宽泛的析出范围,其热解焦油集中在35 min之前,如图3所示,这也表明木屑焦油中含有更多较大分子量的化合物成分。对于木屑而言,酸洗过程并没有对热解反应过程中木屑原料热解焦油产物产生太大影响,主要原因在于酸洗过程主要脱除生物质原料内的AAEM元素,而AAEM元素主要存在于灰分当中,由表1木屑原料的元素分析及工业分析可知,木屑的灰分含量仅有0.96%,因其含量较低,即AAEM元素在木屑原料内的含量较低,从而导致酸洗木屑及原始木屑原料的快速热解焦油成分相差不大。

图3 500~900℃所得木屑Py-GC/MS热解焦油谱图Fig.3 Sawdust pyrolysis tar Py-GC/MS analysis at 500—900℃
对比两种生物质原料的热解焦油分析发现,木屑的快速热解焦油产率明显高于稻壳,此结论可由反应前后的失重率及反应管颜色变化得出,主要原因如表1所示,木屑原料的挥发分含量高达77.13%,而稻壳原料的挥发分仅有58.53%,因而导致了热解反应过程中两者焦油产量的差异,并且物料中生物质三组分的不同及AAEM元素含量的差异也导致了生物质快速热解焦油差异的存在。
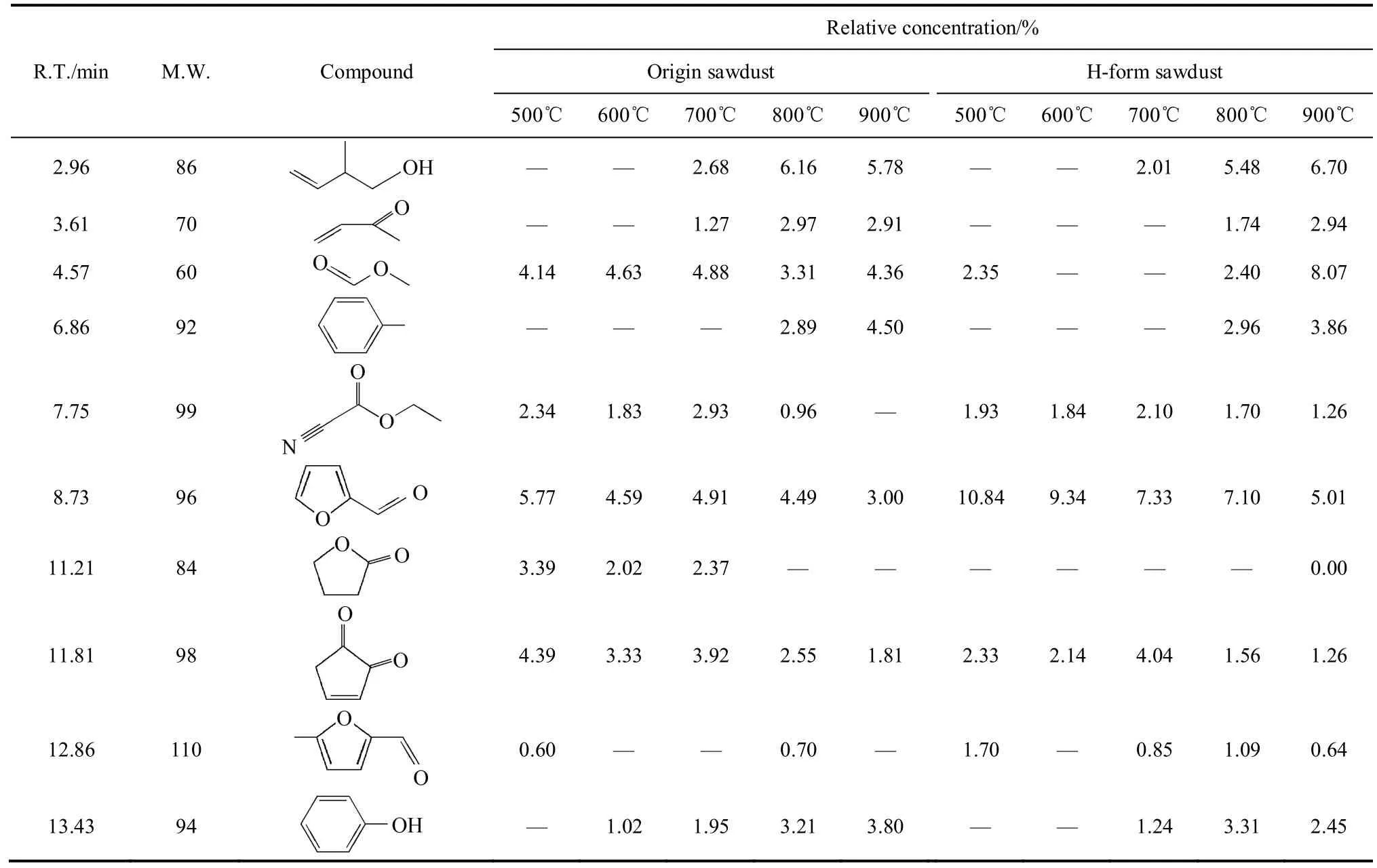
表5 木屑在500~900℃所得Py-GC/MS热解焦油分析结果Table 5 Py-GC/MS analysis of sawdust pyrolysis tar at 500—900℃

Table 5 (continued)

Table 5 (continued)
表5是木屑原料不同温度热解焦油产物生成规律,其主要焦油组成成分包括8.73 min处的呋喃甲醛、11.81 min处的1,2-环戊二酮、14.27 min处的N-丁基叔丁胺、16.94 min处的2-甲氧基苯酚、20.27 min处的邻苯二酚、22.16 min处的2-甲氧基对苯二酚、22.58 min处的4-乙烷基-2-甲氧基苯酚、24.64 min处的2,6-二甲氧基苯酚、27.13 min处的1,2,4-三甲氧基苯等,这些成分基本上占了总热解焦油的50%以上。随着热解终温的升高,呋喃甲醛、1,2-环戊二酮、2,6-二甲氧基苯酚、1,2,4-三甲氧基苯等成分相对浓度逐渐减小。另外,部分焦油成分浓度随着热解终温的升高而增大,如邻苯二酚、4-乙烷基-2-甲氧基苯酚等。该现象可解释为在低温时(500~600℃)热解焦油中存在较多的杂环结构(例如呋喃、五碳糖等),伴随着温度的升高,逐渐发生了分解与转化,进一步变为芳烃环,以代表性的OCH3、CnH2n−1、CnH2n+1等为主。在该条件下温度进一步提升(700~800℃),焦油成分发生芳烃环取代基的脱除反应,转化为稳定的甲基或酚基物质。在800~900℃范围内芳烃环各类取代基团一步步完全脱除,环类物质在高温线发生开环后进一步聚合,从而导致更大分子量的热解焦油产物的形成[30]。

图4 木屑热解焦油产物随平均分子量分布规律Fig.4 Sawdust pyrolysis tar distribution with average molecular weight
对于生物质木屑热解焦油产物随平均分子量分布规律,本文采用与稻壳分析方法相同的局部加权法。如图4所示,木屑焦油分子量的分布情况更加分散,在100、120、140、160、180及200相对分子质量范围内均匀分布。
3 结 论
(1)生物质Py-GC/MS快速热解实验,酸洗脱除AAEM元素致使热解失重率减小。
(2)500~900℃范围内随温度的升高,大分子焦油成分逐渐减少。AAEM元素限制了焦油前体的聚合,进一步抑制了含氧杂环类碳环(糠醛等)的生成。稻壳的热解焦油的相对分子质量主要分布在110~129。
(3)木屑快速热解焦油产率明显高于稻壳,且热解焦油中分子量分布广泛,含有更多较大分子量(150~209)的化合物成分。
References
[1]巴苏. 生物质气化和热解:实际设计和理论 [M]. 北京: 学术出版社, 2010. BASU P. Biomass Gasification and Pyrolysis: Practical Design and Theory [M]. Beijing: Academic Press, 2010.
[2]孙立, 张晓东. 生物质热解气化原理与技术 [M]. 北京:化学工业出版社, 2013. SUN L, ZHANG X D. Biomass Pyrolysis Gasification Principle and Technology [M]. Beijing: Chemical Industry Press, 2013.
[3]李春柱. 维多利亚时代的褐煤的科学进展 [M]. 余江龙,常丽萍, 译. 北京: 化学工业出版社, 2009:109. LI C Z. Advances in the Science of Victorian Brown Coal [M]. YU J L, CHANG L P, trans. Beijing: Chemical Industry Press, 2009:109.
[4]谢克昌. 煤的结构和反应性 [M]. 北京: 科学出版社, 2002:222. XIE K C. Coal Structure and Its Reactivity [M]. Beijing: Science Press, 2002:222.
[5]SONG Y, XIANG J, HU S, et al. Importance of the aromatic structures in volatiles to the in-situ destruction of nascent tar during the volatile-char interactions [J]. Fuel Processing Technology, 2015, 132: 31-38.
[6]KRERKKAIWAN S, FUSHIMI C, YAMAMOTO H, et al. Influences of heating rate during coal char preparation and AAEMs on volatile-char interaction with different sources of biomass volatile [J]. Fuel Processing Technology, 2014, 119: 10-18.
[7]ZHANG S, MIN Z, TAY H L, et al. Effects of volatile-char interactions on the evolution of char structure during the gasification of Victorian brown coal in steam [J]. Fuel, 2011, 90 (4): 1529-1535.
[8]REED T B, GAUR S. A survey of biomass gasification 2000: gasifier projects and manufacturers around the world[R]. Biomass Energy Foundation, 1999.
[9]MUHAMMAD N, OMAR W N, MAN Z, et al. Effect of ionic liquid treatment on pyrolysis products from bamboo [J]. Industrial & Engineering Chemistry Research, 2012, 51 (5): 2280-2289.
[10]LOU R, WU S B, LV G J. Fast pyrolysis of enzymatic/mild acidolysis lignin from moso bamboo [J]. BioResources, 2010, 5 (2): 827-837.
[11]LOU R, WU S B, LV G J. Effect of conditions on fast pyrolysis of bamboo lignin [J]. Journal of Analytical and Applied Pyrolysis, 2010, 89 (2): 191-196.
[12]KANTARELIS E, LIU J, YANG W, et al. Sustainable valorization of bamboo via high-temperature steam pyrolysis for energy production and added value materials [J]. Energy & Fuels, 2010, 24 (11): 6142-6150.
[13]REN X Y, ZHANG Z T, WANG W L, et al. Transformation and products distribution of moso bamboo and derived components during pyrolysis [J]. BioResources, 2013, 8 (3): 3685-3698.
[14]XIAO G, NI M J, HUANG H, et al. Fluidized-bed pyrolysis of waste bamboo [J]. Journal of Zhejiang University Science A, 2007, 8 (9): 1495-1499.
[15]ZHANG L X, KUDO S, TSUBOUCHI N, et al. Catalytic effects of Na and Ca from inexpensive materials on in-situ steam gasification of char from rapid pyrolysis of low rank coal in a drop-tube reactor [J]. Fuel Processing Technology, 2013, 113: 1-7.
[16]JENSEN P A, FRANDSEN F, DAM-JOHANSEN K, et al. Experimental investigation of the transformation and release to gas phase of potassium and chlorine during straw pyrolysis [J]. Energy & Fuels, 2000, 14 (6): 1280-1285.
[17]KEOWN D M, FAVAS G, HAYASHI J I, et al. Volatilisation of alkali and alkaline earth metallic species during the pyrolysis of biomass: differences between sugar cane bagasse and cane trash [J]. Bioresource Technology, 2005, 96 (14): 1570-1577.
[18]SATHE C, PANG Y, LI C Z. Effects of heating rate and ion-exchangeable cations on the pyrolysis yields from a Victorian brown coal [J]. Energy & Fuels, 1999, 13 (3): 748-755.
[19]JAMIL K, HAYASHI J I, LI C Z. Pyrolysis of a Victorian brown coal and gasification of nascent char in CO2atmosphere in a wire-mesh reactor [J]. Fuel, 2004, 83 (7): 833-843.
[20]SATHE C, HAYASHI J I, LI C Z, et al. Combined effects of pressure and ion-exchangeable metallic species on pyrolysis of Victorian lignite [J]. Fuel, 2003, 82 (3): 343-350.
[21]XU W C, TOMITA A. Effect of coal type on the flash pyrolysis of various coals [J]. Fuel, 1987, 66 (5): 627-631.
[22]XU W C, TOMITA A. Effect of temperature on the flash pyrolysis of various coals [J]. Fuel, 1987, 66 (5): 632-636.
[23]MAE K, MAKI T, MIURA K. A new method for estimating the cross-linking reaction during the pyrolysis of brown coal [J]. Journal of Chemical Engineering of Japan, 2002, 35 (8): 778-785.
[24]SCHAFER H N. Pyrolysis of brown coals (Ⅰ): Decomposition of acid groups in coals containing carboxyl groups in the acid and cation forms [J]. Fuel, 1979, 58 (9): 667-672.
[25]SCHAFER H N. Pyrolysis of brown coals (Ⅱ): Decomposition of acidic groups on heating in the range 100—900℃ [J]. Fuel, 1979, 58 (9): 673-679.
[26]HAYASHI J I, TAKAHASHI H, DOI S, et al. Reactions in brown coal pyrolysis responsible for heating rate effect on tar yield [J]. Energy & Fuels, 2000, 14 (2): 400-408.
[27]吴文广. 生物质焦油均相转化及其在焦炭中异相脱除的实验研究[D]. 上海: 上海交通大学, 2012. WU W G. Experimental investigation of homogeneous conversion and heterogeneous decomposition of pyrolytic biomass tar [D]. Shanghai: Shanghai Jiao Tong University, 2012.
[28]REED T B, GAUR S. A survey of biomass gasification [R]. National Renewable Energy Laboratory, 1998.
[29]MASCHIO G, KOUFOPANOS C, LUCCHESI A. Pyrolysis, a promising route for biomass utilization [J]. Bioresource Technology, 1992, 42 (3): 219-231.
[30]BALDWIN R M, MAGRINI-BAIR K A, NIMLOS M R, et al. Current research on thermochemical conversion of biomass at the National Renewable Energy Laboratory [J]. Applied Catalysis B: Environmental, 2012, 115: 320-329.
Effect of temperature and AAEM species on fast pyrolysis of biomass tar
FENG Dongdong, ZHAO Yijun, TANG Wenbo, ZHANG Yu, QIAN Juan, SUN Shaozeng
(School of Energy Science and Engineering, Harbin Institute of Technology, Harbin 150001, Heilongjiang, China)
Abstract:Pyrolysis temperature, heating rate, alkali metal and alkaline earth metal (AAEM) species have significant effects on biomass pyrolysis. In this paper, by using the pyrolysis gas chromatography mass spectrometry (Py-GC/MS), the effect of temperature and AAEM species on fast pyrolysis of the biomass tar was investigated. The influence of pyrolysis temperature and AAEM species on the pyrolysis characteristics of biomass (rice husk and sawdust, H-form rice husk and H-form sawdust) was analyzed by means of mass loss of samples. The online semi quantitative analysis of pyrolysis tar was carried out by gas chromatography mass spectrometry (GC/MS). The distribution of molecular weight of pyrolysis tar was discussed. The results showed that during fast pyrolysis of biomass, the removal of AAEM species reduced the mass loss rate. With increasing pyrolysis temperature in the range of 500—900℃, the tar composition of high molecular weight decreased gradually. The polymerization of the tar precursor was limited by the AAEM species and the formation of the heterocyclic carbon ring was further inhibited. The molecular weight of tar of rice husk pyrolysis was mainly distributed in the range of 110—129. The tar yield of sawdust fast pyrolysis was higher than that of rice husk. The molecular weight distribution of sawdust tar was wide, containing more substances with high molecular weight (150—209).
Key words:biomass; fast pyrolysis; AAEM; Py-GC/MS; tar
中图分类号:X 382.1
文献标志码:A
文章编号:0438—1157(2016)06—2558—10
DOI:10.11949/j.issn.0438-1157.20151907
基金项目:国家自然科学基金项目(51206037);中国博士后基金项目(2013M541376)。
Corresponding author:Prof. ZHAO Yijun, zhaoyijun@hit.edu.cn

