石墨烯@聚希夫碱水凝胶对橙黄G的吸附
张秀青,王 斌,姜 芳
(西华师范大学 化工学化工学院,四川 南充 637009)
石墨烯@聚希夫碱水凝胶对橙黄G的吸附
张秀青,王斌,姜芳
(西华师范大学 化工学化工学院,四川 南充637009)
摘要:通过原位聚合的方法合成了石墨烯@聚希夫碱水凝胶。该水凝胶具备了氧化石墨烯以及聚希夫碱单独存在不具有的特性,简单易得。它可以作为一种新型的橙黄G的吸附剂。接触时间,pH值和初始浓度分别为研究水凝胶吸附橙黄G 三个实验参数。平衡时间是48h。水凝胶对橙黄G吸附的最佳pH值为6。Langmuir,Tempkin和Fruendlich等温线方程被用来模拟吸附过程,对橙黄G染料的吸附符合Langmuir方程。通过假一级、假二级方程分析的吸附动力学数据表明,假二级方程可以精确描述对橙黄G的吸附过程。水凝胶通过过滤器得到大小相同的颗粒。
关键词:水凝胶;吸附;染料;平衡
染料是有毒污染物的其中一种,有三种类型:阴离子型,非离子型和阳离子染料[1-3]。橙黄G是阴离子染料的一部分,并且它属于偶氮染料[1]。由于染料的耐热性和光稳定性,生物降解的问题也随之而来[4,5]。因此,找到一个有效降解染料的方法具有十分重要的意义。目前,除去废水中染料的化学方法包括氧化法[6],光化学氧化法和生物降解法[7,8]。但这些方法可能包含许多制约因素:成本高、效率低下可能造成二次污染等。吸附作为一种有效方法被开发利用,其操作成本低,设计简单可行,高度灵活并且容易再生[9]。
设计合成水凝胶的原理是基于氧化石墨烯和聚希夫碱[10]之间的共轭作用。氧化石墨烯在水热条件下被部分还原成石墨烯,石墨烯是具有单层结构的膜,由于其表面积比起氧化石墨烯要大的多,所以考虑在水热条件下还原氧化石墨烯来提高氧化石墨烯和其他物质的复合材料的吸附性能。合成的混合水凝胶可以置于柱装置中用于水净化的必要成分。众所周知,这不能只由石墨烯或聚希夫碱完成。由于共价键的作用力和还原氧化石墨烯本身为膜的结构特性,这种新材料改善了低吸附能力。更重要的是,它可以低成本合成并且非常容易制备。
1实验部分
1.1实验原料
橙黄G又名橙黄10(阿拉丁),其最大吸收波长是476nm。2mg/mL 的氧化石墨烯分散液(LEADERNANO),4,4'-偶氮基二甲苯实验室合成,二甲基甲酰胺溶液(Sigma-Aldrich),去离子水,甲醛溶液AR(重庆茂业)。
吸附量的计算公式:

(1)
在式(1)中,C0代表橙黄G溶液的初始浓度;Ce代表吸附后溶液的浓度;V是溶液的体积,m是吸附剂的质量。
1.2水凝胶的合成
将0.04 g 聚希夫碱溶于20mL去离子水中,加入2mL 1mol/L的盐酸溶液,在80 W功率下超声1 h。准备一个5 mL的小玻璃瓶,加入2 mL聚希夫碱水溶液和2 mL的氧化石墨烯分散液以及1 mL的甲醛溶液。补加盐酸溶液并迅速摇晃小瓶得到红棕色混合物。然后保持95 ℃油浴。3 h之后观察,混合物开始变为絮状物。6 h之后变为黑色的柱状物浮于水中。然后柱状物随着时间的推移慢慢缩水,体积慢慢减小,最后沉到小瓶底部。整个过程如图 1所示。

2结果与讨论
2.1水凝胶的热稳定性


2.2红外分析

2.3最佳 pH
图4中,当pH值从2.0增加到6.0时,在pH值为6.0时材料对染料的吸附量达到最大值。当pH值很低时,H+浓度很高,其可以与阳离子染料形成竞争,使得染料分子与吸附剂接触的可能性降低。但随着pH值的增加,H+浓度减少,羟基电离形成—O-基团,增加了静电吸引作用而导致染料去除率上升。因此,最适pH值为6.0。

2.4反应时间的影响
从图5可以清楚地观察到,平衡时间是48 h。 48 h后,去除橙黄G百分比是恒定的。水凝胶的用量为5mg,温度保持35℃[10]。pH为6。
2.5初始浓度的影响
从图6中,可以观察到吸附剂对不同浓度的染料的吸附结果。图中,从0到200 mg/L材料对染料的去除量呈上升趋势。因为由于较高的浓度可以促进橙黄G分子扩散进入到水凝胶的微孔中。从200 mg/L到500 mg/L吸附量变得平稳,不再受初始浓度影响。
3吸附平衡曲线的研究
要建立最适合的平衡曲线,三种方程被用来模拟吸附橙色染料,如Langmuir,Freundlich和Tempkin。
3.1Langmuir 模型
它可以由下面的等式来表示:
Langmuir模型:

(2)
其中,Ce和qe分别是浓度和平衡时染料的吸附量。KL为朗缪尔常数和qm代表最大吸附量。如图7,其结果示于表1。
3.2Freundlich 模型
Freundlich等温模型假定吸附过程与吸附剂的非均相吸附表面相关。该模型用下列方程式表示。
Freundlic模型:

(3)
其中,qe是吸附染料的质量,Ce代表平衡浓度。KF是Freundlich平衡常数。如图8,该结果示于表1。

3.3Tempkin 模型
Tempkin 等温吸附模型假定吸附物之间相互作用产生吸附热和结合放出的最大能量。Tempkin等温线是由下式表示:
qe=B1lnKT+B2lnCe,
(4)
其中,KT是Tempkin常数,与最大结合能和B1与吸附热相关。如图9其参数的值在表1。

表1 吸附平衡曲线常数
3.4假一级方程
用以下公式表示:
ln(qe-qt)=lnqe-KFt,
(5)
其中,t是时间,qe是水凝胶对橙黄G的吸附能力,qt是橙黄G在时间t内去除量,KF是假一级模型常数,其参数的值示于图10,R2=0.69085,qe=765.26 与实际测得值相差太大,那么该吸附过程不符合假一级方程。

3.5假二级方程
假二级吸附模型公式:
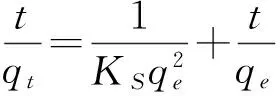
(6)
其中,KS是假二阶模型常数,其数值由t/qt决定。吸附参数的值如图11,R2=0.978。
4结论
作为一种新型的吸附剂,水凝胶对染料的吸附效果是非常有效的。最重要的是,合成水凝胶的过程非常简单可行。分析结果:最适pH值是6,它在48h达到平衡。吸附容量为416.52mg/g。 Langmuir吸附等温线模型可以描述这种吸附过程,动力学研究符合假二级方程。因此,它是用于吸附橙G的一个很好的选择。
参考文献:
[1]BENTOUAMI A, DERRICHE Z, BETTAHAR N. Synthesis and characterization of Mg-Fe layer double hydroxides and its application on adsorption on adsorption of orange G from aqueous solution[J]. Chemical Engineering Journal. 2011, 169(1): 231-238.
[2]SINGHK P, GUPTA S, SINGH A K, et al. Optimizing adsorption of crystal violet dye from water by magnetic nanocomposite using response surface modeling approach[J]. Journal of Hazardous Materials. 2011,186(2): 1462-1473.
[3]LEE J W, CHOI S P, SMHI W G, et al. Evaluation of the performance of adsorption and coagulation process for the maximum removal of reactive dyes[J]. Dyes and Pigment. 2006, 69(3): 196-203.
[4]INDRA D M, VIMAL C S, NITIN K, et al. Removal of orange G and methyl violet dyes by adsorption onto bagasse fly ash- kinetic study and equilibrium isotherm analyses[J]. Dyes and Pigments. 2006,69(3): 210-223.
[5]FORGACS E, CSERHATI T, OROS G. Removal of synthetic dyes from wastewaters: a review[J]. Environment International. 2004, 30(7): 953-971.
[6]ROBINSON T, MULLAN G, MARCHANT R. Remediation of dyes in textile effluent: a critical review on current treatment technologies worth proposed alternative[J]. Bioresource technology. 2001, 77(3): 247-255.
[7]KADIRVELU K, KAVIPRIYA M, KARTHIKA C, et al.Utilization of various agricultural wastes for actived carbon preparation and application for the removal of dyes and metal ions from aqueous solutions[J]. Bioresource Technology. 2003, 87(1): 129-132.
[8]GARG V K, GUPTA R, YADAV A B, et al. Dye removal from aqueous solution by adsorption by adsorption on treated sawdust[J]. Bioresource Technology. 2003, 89(2): 121-124.
[9]KHARE S K, PANDAY K K, SINGH V N, et al. Removal of victoria blue from aqueous solution by ash[J]. Journal of Chemical Technology and Biotechnology. 1987, 38(2): 99-104.
[10]ZHANG L Y., WANG T, WANG H Y, et al. Removal of victoria blue from aqueous solution by ash. Removal of victoria blue from aqueous solution by ash[J]. Chemical Communications. 2013, 49(85): 9974-9976.
Adsorption of Orange G onto Graphene&PolySchiff Base Hydrogel
ZHANG Xiuqing, WANG Bin,JIANG Fang
(College of Chemistry and Chemical Engineering,China West Normal University,Nanchong Sichuan 637009,China)
Abstract:In this paper,a hydrogel was synthesized by a very facile method.It can be used as a novel adsorbent of orange-G.Three effects of experimental parameters such as contact time,pH and initial concentration were studies for the removal of orange-G.The equilibration time was reached within 48 h.The effective pH for the adsorption of orange-G on this hydrogel is 6. Langmuir,Tempkin and Fruendlich isotherm equation were used to model the adsorption rule,and the adsorption of orange-G dye followed langmuir equation.Adsorption kinetic data was analyzed by pseudo-first-order,pseudo-second-order.Kinetic data showed that the adsorption of orange-G could be precisely described by pseudo-second-order.The hydrogel was used without pretreatment except getting the same size of it through filter.
Keywords:hydrogel;adsorption;dye;equilibrium
文章编号:1673-5072(2016)02-0184-05
收稿日期:2015-04-07
基金项目:四川省教育厅自然科学重点项目(12ZA175)
作者简介:张秀青(1990—),女,山东东营人,硕士研究生,主要从事功能高分子材料研究。 通讯作者:王斌(1967—),男,四川雅安人,副教授,博士,主要从事功能高分子材料研究。 E-mail:cwnuwangb@126.com
中图分类号:O634.5
文献标识码:A
DOI:10.16246/j.issn.1673-5072.2016.02.011

