EGFR TKI+TP方案及TP方案对晚期非小细胞肺癌治疗临床效果及肿瘤标志物水平的影响*
梁秋萍,殷 俊
成都市第三人民医院 呼吸内科 (成都 610000)
EGFR TKI+TP方案及TP方案对晚期非小细胞肺癌治疗临床效果及肿瘤标志物水平的影响*
梁秋萍,殷俊
成都市第三人民医院 呼吸内科 (成都610000)
【摘要】目的探究EGFR TKI+TP方案(厄洛替尼联合紫杉醇、顺铂化疗方案)及TP方案(紫杉醇、顺铂化疗方案)对晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)治疗临床效果及肿瘤标志物水平的影响。方法 分析2012年1月至2013年12月在成都市第三人民医院呼吸内科接受治疗的84例晚期NSCLC患者的临床资料,观察组(n=43)给予EGFR TKI+TP方案治疗,对照组(n=41)给予TP方案治疗。观察比较两组临床化疗效果、肿瘤标志物表达情况及生存率。结果两组治疗后血清CEA、CA125及Cyfra21-1水平与治疗前相比明显降低,差异有统计学意义(P=0.002,0.001,0.045);对照组治疗后血清CEA、CA125及Cyfra21-1水平明显高于观察组,差异有统计学意义(P=0.022,0.031,0.036);观察组治疗有效率为81.40%,对照组治疗有效率为48.78%,采用Wilcoxon秩和检验法进行分析,观察组治疗有效率明显高于对照组,差异有统计学意义(Z=3.520,P<0.001);观察组PR、SD、PD患者血清中,CEA、CA125及Cyfra21-1水平明显低于对照组,差异有统计学意义[P=(0.026,0.021,0.014)vs(0.037,0.042,0.029)vs(0.007,0.011,0.018)];观察组不良反应发生率明显低于对照组,差异有统计学意义(P=0.042);通过 Kaplan-Meier生存分析发现,观察组患者生存率明显高于对照组,差异有统计学意义(5/43,11.63% vs14/41,34.15%;Log-rank �2=7.912,P=0.005)。结论EGFR TKI+TP方案化疗联合使用,可明显改善晚期NSCLC的治疗效果,不良反应小,有助于提高患者生存率,有效降低患者血清中肿瘤标志物的浓度,临床上可用于晚期NSCLC 表皮生长因子(EGFR)基因突变患者的治疗。
【关键词】非小细胞肺癌;表皮生长因子;酪氨酸激酶抑制剂;厄洛替尼;紫杉醇;顺铂
非小细胞肺癌(non-small cell lung cancer,NSCLC)是肺癌中常见的病理类型,占肺癌患者的80%,主要以低热、咳嗽、痰血和胸痛为早期临床表现[1]。NSCLC患者细胞分裂速度较慢,发病较隐匿,其中75%老年患者临床分期较差,5年生存率较低,严重危害我国老年患者的生命健康与生活质量[2]。有研究[3]表明,第3代细胞毒性药物合并铂类治疗晚期NSCLC已成为首选的化疗方案,可有效提高患者的中位生存期,提高患者缓解率,但是含铂类治疗方案不良反应率较高,老年人群耐受性较差。近年来,靶向化疗药物的研究已成为晚期NSCLC治疗的研究热点之一,主要通过多种靶向药物联合使用来优化化疗效果,改善患者预后。本研究通过分析两种化疗方案治疗晚期NSCLC的临床效果及患者的生存率,为晚期NSCLC患者治疗提供参考。
1资料与方法
1.1临床资料

表1 两组一般临床资料比较
1.2治疗方案及疗程
对照组给予静脉滴注紫杉醇和顺铂进行治疗(TP方案),使用方法:先用175 mg/m2紫杉醇注射液静脉滴注,密切注意患者化疗情况,休息30 min后,给予75 mg/m2顺铂注射液(20 mg/20mL)静脉滴注,治疗2个月。观察组在对照组治疗的基础上,给予厄洛替尼治疗,使用方法:嘱患者口服盐酸厄洛替尼片(150 mg/片),1片/d,服用2个月。治疗共4个疗程,每个疗程7 d。
1.3观察指标及方法
1.3.1检测方法抽取两组治疗前后清晨静脉血5 mL,以3 000 r/min,离心半径10 cm,离心3 min后,取其上层清液,置于-20 ℃环境中冷冻保存。采用化学发光免疫分析法检测患者血清癌胚抗原(CEA)、糖类抗原(CA125)及细胞角蛋白19片段(Cyfra21-1)含量。
1.3.2观察指标比较两组治疗后血清CEA、CA125及Cyfra21-1水平;比较两组治疗效果、不良反应发生率和生存率。
1.3.3疗效评价近期疗效评价:两组患者治疗4个疗程后,化疗效果评价参照实体瘤的疗效评价标准(RECIST 1.0)[5],具体评价标准如下:完全缓解(CR):目标病灶消失;部分缓解(PR):肿瘤病灶最长径之和与基线状态比较,减少30%以上;疾病稳定(SD):肿瘤直径缩小范围处于PR与SD之间;疾病恶化(PD):肿瘤病灶最长径之和与基线状态比较,增长程度>30%以上。CR+PR+SD定义为治疗有效,PD定义为治疗无效,试验对象中未出现治疗效果为CR的患者。治疗有效率=(CR+PR+ SD)患者数/总病例数×100%。
1.3.4随访方法两组采用电话和门诊随访的方式进行观察,自患者出院后开始随访,记录两组患者死亡时间,随访时间截止到2015年3月。
1.4统计学方法
合理利用安全人机工程学的原理对设备、设施进行优化。注意设备的保养与维护,编制严格、多层次设备的维修和检修规程;尽量采用具有互锁装置的设备,以有效避免人员误操作;对于特殊作业的设备必须满足相应的安全性能,如水下设备须达到相应密封要求,临电全部采用三相五线制,用电设备有漏电保护、接地,同一水平、垂直工作面上下电源实行单向联锁供电装置;合理利用人机工程学中的视觉原理设计安全警示牌,对于特殊环境设置检测装置、联动光电报警装置等,积极探索试行安全“目视化”管理。

2结果
2.1两组治疗前后血清肿瘤标志物水平比较
两组治疗后血清CEA、CA125及Cyfra21-1水平与治疗前相比明显降低,差异有统计学意义(P=0.002,0.001,0.045)。对照组治疗后血清CEA、CA125及Cyfra21-1水平明显高于观察组,差异有统计学意义(P=0.022,0.031,0.036)(图1)。
2.2两组治疗后临床治疗效果及不同疗效下血清肿瘤标志物水平比较
观察组治疗有效率为81.40%(35/43),对照组治疗有效率为48.78%(20/41),采用Wilcoxon秩和检验法进行分析,观察组治疗有效率明显高于对照组,差异有统计学意义(Z=3.520,P<0.001);观察组PR、SD、PD患者血清中CEA、CA125及Cyfra21-1水平明显低于对照组PR、SD、PD患者,差异有统计学意义[P=(0.026,0.021,0.014)vs(0.037,0.042,0.029)vs(0.007,0.011,0.018)]。(表2,图2)。
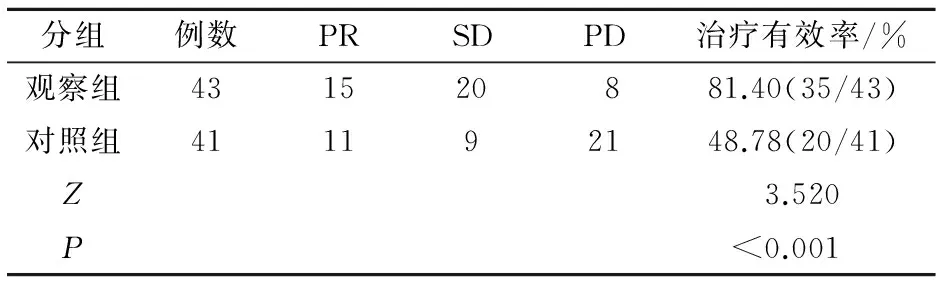
表2 两组临床治疗效果比较(n)
2.3两组不良反应发生情况比较
两组经不同化疗方案治疗后,均出现恶心呕吐、血小板降低和骨髓抑制等不良反应。观察组不良反应发生率明显低于对照组,差异有统计学意义(P=0.042)。
2.4两组不同化疗方式生存率比较
经过两年随访后,对照组中有1例患者退出本试验。观察组死亡5例,死亡率为11.63%,中位生存时间为23个月;对照组死亡14例,死亡率为34.15%,中位生存时间为20个月。通过 Kaplan-Meier生存分析发现,观察组生存率明显高于对照组,差异有统计学意义(Log-rank2=7.912,P=0.005)(图3)。
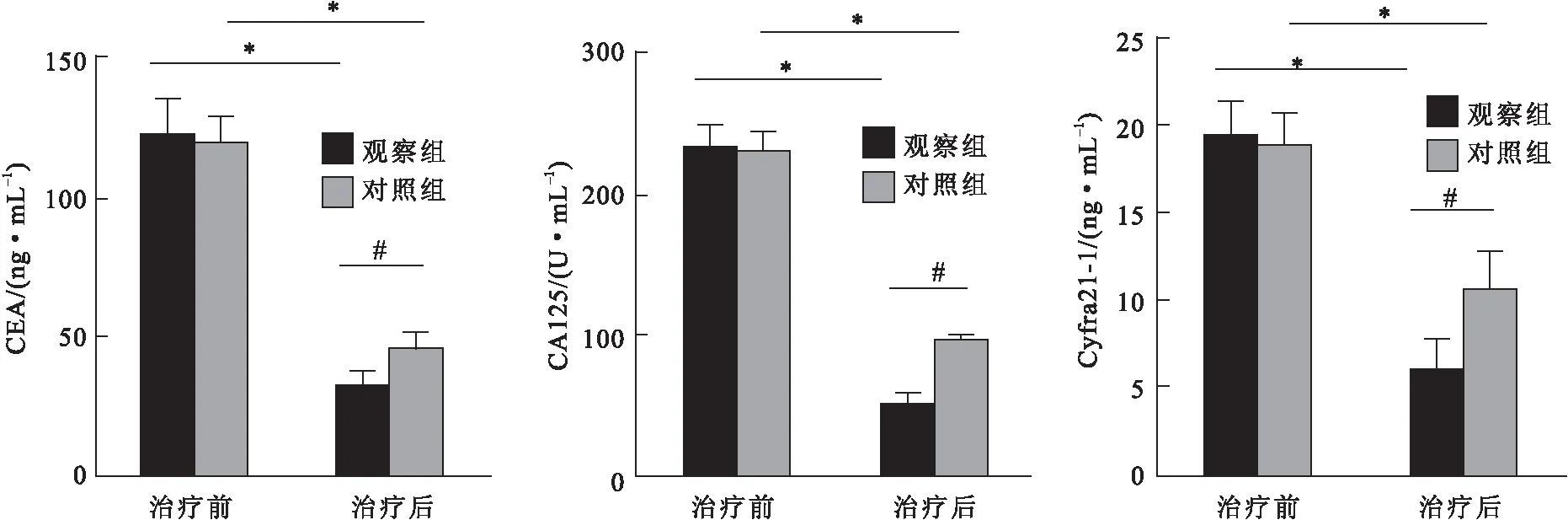
图1两组化疗前后血清肿瘤标志物水平比较
注:与治疗前比较,*P<0.05;与治疗后对照组比较,#P<0.05
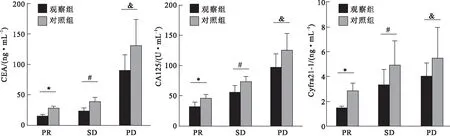
图2两组治疗后不同疗效下血清肿瘤标志物水平比较
注:与对照组PR患者比较,*P<0.05;与对照组SD患者比较,#P<0.05;与对照组PD患者比较,&P<0.05
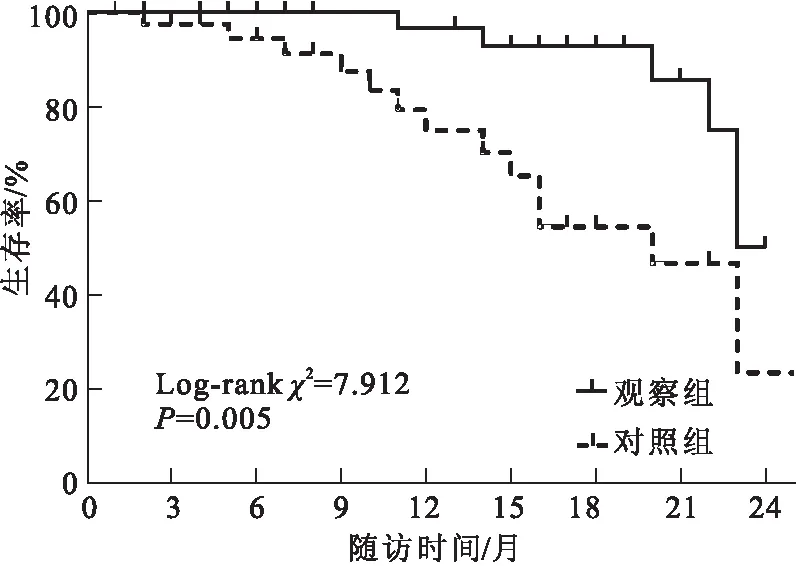
图3两组不同化疗方式生存率比较
3讨论
由于晚期NSCLC患者预后较差,患者常出现肿瘤转移,且施行根除性手术意义不大,临床上主要采用化疗来治疗晚期NSCLC的病人,可有效控制病灶的扩大,提高患者的缓解率以及5年生存率。现如今临床上主要采用含铂类联合化疗方案来治疗NSCLC患者,通过含铂类联合化疗方案对TNM分期较差的患者治疗效果较好,对于老年人群不良反应率较高,患者一般不能全程坚持[6]。
近年来,分子靶向治疗概念的提出,为晚期NSCLC患者治疗提供一个新的方向,表皮生长因子(EGFR) 基因激活突变或间变性淋巴瘤激酶(ALK)基因重排的肿瘤患者可以通过EGFR 和 ALK酪氨酸激酶抑制剂(TKI)进行分子靶向进行治疗。第1代EGFR TKIs药物厄洛替尼可以针对细胞受体、基因,调控分子信号传导为靶点进行治疗,有效促进肿瘤细胞凋亡、抑制血管新生和细胞增殖分化,靶向选择性较高,不良反应较小,临床研究价值较大[7-8]。
CEA是由大肠癌组织分泌的一种糖蛋白,是一种广谱的肿瘤标志物,可用于肺癌疗效判断和预后评估,对恶性肿瘤判断的灵敏性不高[9]。CA125常见于上皮性卵巢肿瘤患者血清中,可作为肺癌、卵巢癌、子宫内膜癌和肠癌患者的诊断和疗效评价[10]。有文献[11]指出,Cyfra21-1在肺鳞癌细胞中高度表达,可作为诊断NSCLC的特异性指标,Cyfra21-1血清浓度与肿瘤临床分期呈现正相关,可用来预测患者放化疗复发情况。本研究发现,两组治疗后血清CEA、CA125及Cyfra21-1水平较治疗前相比明显降低,对照组治疗后血清CEA、CA125及Cyfra21-1水平明显高于观察组,说明两种化疗方案可以有效降低晚期NSCLC患者血清中CEA、CA125及Cyfra21-1水平,应用靶向药物治疗的患者CEA、CA125及Cyfra21-1水平降低的程度较高,这可能是与厄洛替尼可靶向性阻断生长因子受体、加速细胞凋亡、抑制肿瘤浸润转移有关[12]。
有文献[13]报道,使用以顺铂为主的化疗药物对NSCLC患者化疗后,治疗缓解率可达40%~60%,但是对于晚期NSCLC患者治疗缓解率不超过40%,如何选取有效的化疗方案对晚期NSCLC患者治疗效果尤为重要。本研究发现,观察组治疗有效率明显高于对照组,观察组生存率明显高于对照组,说明应用靶向药物治疗晚期NSCLC患者可有效减少病情恶化的患者,抑制患者病情发展,提高患者生存率,对晚期NSCLC稳定病情和改善预后具有重要临床意义。观察组PR、SD、PD患者血清中CEA、CA125及Cyfra21-1水平明显低于对照组,说明血清中肿瘤标志物可评价晚期NSCLC治疗效果,预测患者的预后情况。
应用不同化疗方案对两组患者治疗后发现,两组均出现恶心呕吐、血小板降低和骨髓抑制等不良反应,观察组不良反应率较低。当患者出现不良反应后,给予G-CSF、GM-CSF和止吐药(昂丹司琼)治疗,患者均可耐受化疗。两组经过两年随访后,通过 Kaplan-Meier生存分析发现,观察组生存率明显高于对照组,说明接受EGFR TKI+TP方案化疗的患者死亡率较常规化疗方案治疗的患者明显降低,治疗效果较好。
综上所述,EGFR TKI+TP方案进行化疗可明显改善晚期NSCLC的治疗效果,不良反应小,有助于提高患者生存率,有效降低患者血清中肿瘤标志物的浓度,临床上可用于晚期NSCLC EGFR基因突变患者的治疗。
参考文献
[1]Michelsen L,Sørensen JB.Platinum-Vinorelbine Induction Chemotherapy plus Bevacizumab With and Without Pemetrexed Switch Maintenance in Advanced NSCLC[J].Anticancer Res,2015,35(11): 6255-6259.
[2]Xu L,Lei J,Wang QZ,etal.Clinical characteristics of patients with non-small cell lung cancers harboring anaplastic lymphoma kinase rearrangements and primary lung adenocarcinoma harboring epidermal growth factor receptor mutations[J].Genet Mol Res,2015,14(4): 12973-12983.
[3]Kalikaki A,Voutsina A,Koutsopoulos A,etal.ERCC1 SNPs as Potential Predictive Biomarkers in Non-Small Cell Lung Cancer Patients Treated With Platinum-Based Chemotherapy[J].Cancer Invest,2015,33(4): 107-113.
[4]刘佩佳.EGFR突变与非小细胞肺癌的个体化治疗[J].实用肿瘤学杂志,2011,25(1):79-82
[5]王正,赵瑞峰,王娟,等.18F-FDG PET-CT及实体瘤疗效评价标准评价肺癌早期化疗效果的临床研究[J].肿瘤研究与临床,2015,27(7):488-490.
[6]Zhang T,Zhang DM,Zhao D,etal.Osteopontin expression is associated with platinum-based chemotherapy response and prognosis of patients with advanced non small cell lung cancer[J].J BUON,2014,19(3): 742-748.
[7]胡毅,陶海涛.晚期非小细胞肺癌的药物治疗进展[J].中国药物应用与监测,2014(6):329-333.
[8]彭芳,陈明.放疗联合分子靶向药物治疗非小细胞肺癌的研究进展[J].实用肿瘤学杂志,2012,26(1):42-48.
[9]Yu DH,Li JH,Wang YC,etal.Serum anti-p53 antibody detection in carcinomas and the predictive values of serum p53 antibodies,carcino-embryonic antigen and carbohydrate antigen 12-5 in the neoadjuvant chemotherapy treatment for III stage non-small cell lung cancer patients[J].Clin Chim Acta,2011,412(11-12): 930-935.
[10] Wang XF,Wu YH,Wang MS,etal.CEA,AFP,CA125,CA153 and CA199 in malignant pleural effusions predict the cause[J].Asian Pac J Cancer Prev,2014,15(1): 363-368.
[11] 曹咏,闫吉.NSE、Cyfra21-1、SCCA 和 CEA 在肺癌诊断中的价值[J].中国实验诊断学,2015,19(9):1539-1541.
[12] 张雅军,李红兵,李现东,等.吉非替尼与厄洛替尼二线治疗晚期肺腺癌的临床疗效及安全性[J].中国临床药理学杂志,2015,31(11):899-901.
[13] 冯高华,陈晓峰.不同化疗方案治疗晚期非小细胞肺癌的疗效及对肿瘤标志物水平的影响[J].中国老年学杂志,2014,34(23):6601-6603.
Efficacy and Prognosis Research on EGFR TKI+TP and TP Regimens for Advanced Non-Small Cell Lung Cancer and Impact on Tumor Marker Levels
LiangQiuping,YinJun.
DepartmentofRespiratoryMedicine,ThirdPeople′sHospitalofChengdu,Chengdu610000,China
【Abstract】ObjectiveTo investigate the clinical effect and prognosis of for the patients with advanced non small cell lung cancer by different chemotherapy regimens and its impact on the levels of tumor markers. MethodsThe clinical data of 84 patients with advanced non-small cell lung cancer(NSCLC) for treatment in our hospital from January 2012 to December 2013 were analyzed and divided into observation group(n=43) given erlotinib, paclitaxel and cisplatin for treatment, and control group(n=41) given paclitaxel and cisplatin for treatment. The clinical curative effect, the expression of tumor markers and survival rate in two groups were compared. ResultsAfter treatment, the levels of serum CEA, CA125 and Cyfra21-1 were significantly decreased in the two groups, the differences were statistically significant (P=0.002,0.001,0.045). After treatment, serum CEA, CA125 and Cyfra21-1 level in control group were significantly higher than those of the observation group, the difference had statistical significance (P=0.022,0.031,0.036); In observation group, the treatment effective rate was 81.40%; in control group, the effective rate of the treatment was 48.78%. According to the analysis of Wilcoxon test method, the efficacy in observation group was significantly higher than that of control group, the difference was statistically significant (Z=3.520, P<0.001). CEA, CA125 and Cyfra21-1 levels in PR, SD and PD patients in observation group were significantly lower than those in control group, the differences of which were statistically significant [P= (0.026, 0.021, 0.014) VS (0.037, 0.042, 0.029) VS (0.007, 0.011, 0.018)]. The adverse reactions incidence in observation group were significantly lower than those of control group, the differences were statistically significant (P=0.042). According to the Kaplan Meier survival analysis, the survival rate in observation group was significantly higher than that of the control group, the difference was statistically significant (5/43, 11.63% vs 14/41, 34.15%; Log-rank 2=7.912, P=0.005). ConclusionCombined utilization of EGFR TKI+TP can obviously improve the therapeutic effect of advanced NSCLC, has low adverse reactions, improve patient survival rate, reduce the concentration in serum of patients with tumor markers and can be used clinically for the treatment of patients with advanced NSCLC EGFR gene mutation.
【Key words】Non-small cell lung cancer;EGFR;TKI;Erlotinib;Taxol;Cis-Dichlorodiamineplatinum(II)
doi:10.3969/j.issn.1674-2257.2016.01.009
*基金项目:四川省卫生厅课题 (No:120535)
【中图分类号】R734.2
【文献标志码】A
网络出版地址:http://www.cnki.net/kcms/detail/51.1705.R.20160221.2022.038.html
·论著·

