腔内支架植入术治疗国内Stanford B 型主动脉夹层的系统评价
王俊伟李勇辉李永欣崔 进李 文汪 洋王深明王劲松*
1中山大学附属第一医院血管外科,广州 5100802青岛大学附属医院血管外科,青岛 266001
腔内支架植入术治疗国内Stanford B 型主动脉夹层的系统评价
王俊伟1李勇辉1李永欣2崔 进1李 文1汪 洋1王深明1王劲松1*
1中山大学附属第一医院血管外科,广州 5100802青岛大学附属医院血管外科,青岛 266001
摘要:目的 探讨国内腔内支架植入术治疗Stanford B 型主动脉夹层(aortic dissection,AD)的治疗效果,技术可行性及临床安全性。方法 系统检索PubMed,科学网(Web of Science,WOS)和Cochrane图书馆中的来源于国内英文医学文献及中国生物医学数据库(Chinese Biomedical Database,CBMdisc),中国知网(China National Knowledge Infrastructure,CNKI)和万方数据库中的中文医学文献。本系统评价是基于所有评估腔内支架植入术治疗中国Stanford B型AD的治疗效果的回顾性研究。结果 共有153篇回顾性研究,8 415例B型夹层患者纳入本研究。技术成功率为(99.7±0.1)%。总体并发症发生率为(19.1±0.6)%。术后内漏发生率为(7.2±0.3)%。严重并发症发生率为(3.2±0.2)%,其中神经系统并发症发生率为(1.3±0.1)%。围手术期中风率比截瘫率高(0.8%±0.1% vs 0.1%±0.04%)。总体并发症发生率第1代覆膜支架比第2代覆膜支架高(25.1%±1.2% vs 9.5%±0.9%,P<0.001)。住院死亡率为(1.6±0.1)%。此外,平均随访时间为(29.4±13.5)个月,随访期间晚期死亡率为(1.8±0.2)%。30 d,6个月,1年,2年和5年总体生存率的Kaplan-Meier估计分别是(99.0±0.1)%,(98.5±0.2)%,(98.4±0.2)%,(98.1±0.2)%和(97.9±0.2)%。结论 腔内支架植入术治疗Stanford B型AD切实可行,技术成功率较高,神经系统并发症发生率较低,生存率较高。第2代覆膜支架住院和随访期的治疗效果更好。
关键词:腔内;覆膜支架;Stanford B型;主动脉夹层;系统评价
在最近专家共识中,腔内支架植入术被推荐为复杂型Stanford B型AD的最佳治疗方法[1,2]。而非复杂型B型AD患者,指南推荐保守治疗[1-3]。2项随机对照试验(randomized controlled trials,RCTs)结果显示,与内科治疗相比,腔内支架植入术治疗B型AD能够促进主动脉重塑[4-8],并且增加5年生存率[6]。近期研究也进一步证实了腔内修复术治疗B型AD的效果,技术可行性和临床安全性[9,10]。随着覆膜支架设计的改进和技术经验的积累,国内应用腔内支架置入术治疗B型AD的效果越来越好,临床适应证进一步扩大。目前国内使用支架的现状包括:⑴ 国产和进口支架联合使用;⑵ 支架的长度及尺寸等设计均有改进。然而,这些结果尚未得到系统的、有效的评价。本研究通过系统回顾国内作者发表的文献,评估腔内支架植入术治疗B型AD的效果,技术可行性及临床安全性。
1 材料与方法
1.1文献检索策略
文献检索于2014年8月进行,检索时不限制文献发表时间,类型或者语言。以“主动脉夹层”、“B型”、“DeBakeyⅢ型”、“腔内”和“支架”作为关健词在中国生物医学数据库(Chinese Biomedical Database,CBMdisc),中国知网(China National Knowledge Infrastructure,CNKI)和万方数据库中对中文文献进行了全面检索。同样,以“aortic dissection”,“type B”,“DeBakeyⅢ”,“endovascular”,“stent”和“China”作为关键词在PubMed,科学网(Web of Science,WOS),和Cochrane图书馆对中国人发表的英文文献进行了全面检索。对相关文章的参考文献也进行了手工检索,纳入更多潜在的文献。
1.2纳入与排除标准
文献纳入标准:⑴ Standford B型AD患者接受腔内支架植入术;⑵ 例数≥10例;⑶ 能够提供预定义变量≥25%数据;⑷ 为避免单中心重复报道,仅最近发表或者最大例数发表的文献纳入本研究。文献排除标准:⑴主题不相关的文献;⑵ 无法提供数据的文献,例如病例报告、给编辑的信、社论、综述、会议摘要和动物实验等研究。
1.3数据提取
用于数据提取的标准步骤,参考Eggebrecht等[11]提出的53个有关临床特征、手术数据、住院和随访期治疗效果的预定义变量。每篇纳入研究使用包含了65个预定义变量的改良标准步骤(附录表A1)。2位作者(王俊伟和李勇辉)独立提取和汇总数据。数据提取分歧时由2位高年资的作者协商达成共识。未指明的信息定义为“不可用(not available,NA)”。因此,本文中每个特定变量患者(分母)的数目可能会变化。
1.4统计分析
本研究使用SPSS 13.0统计软件进行统计分析。总的事件数除以可用患者数的总和用来计算事件率。如果权重被定义为特定的研究所提供的可用患者的比例,通过计算不同研究的个体率,并且用加权平均的方法把这些率合并,得到同一的结果。结果用平均值±标准差或者中位数和范围表示。分类变量用卡方检验,连续变量用双侧t检验。Kaplan-Meier非参数检验方法用来估计30 d、6个月、1年、2年和5年的生存率,并且用log-rank检验进行统计推断。只有报告事件发生准确时间的研究才纳入Kaplan-Meier分析。P<0.05差异具有统计学意义。
1.5定义
2种分类方法用来描述AD。Stanford B型AD起源于降主动脉远端至左侧锁骨下动脉的起始端,也称为DeBakeyⅢ型。症状发生时间≤14 d被认为是急性夹层;>14 d出现症状为慢性夹层。有生命危险或者需要紧急处理的并发症,定义为严重并发症,例如中风或者需要外科修复的径路并发症;不需要进一步处理的并发症,定义为轻微并发症,例如径路口的感染,无需透析的一过性肾衰。技术成功定义为技术上成功把假体植入到预定的目标位置。任何突然发生或者无法找到其他原因的死亡,归因于主动脉破裂。再次干预定义为需要额外腔内支架手术或者中转手术。手术相关并发症定义为与腔内支架植入术相关的并发症,例如夹层破裂,逆行夹层,器官或者外周动脉灌注不全,锁骨下动脉闭塞引起中风,Ⅰ型内漏。患者例数>中位数(32)的中心被认为比患者例数<中位数的中心更有经验。此外,对纳入研究的不同出版日期的腔内支架植入术的结果进行比较。2002—2008年发表的研究表示早期经验,2009—2014年发表的研究表示近期经验。国内中心自2009年开始才全面使用改进的第2代国产或者进口覆膜支架;而多数第2代覆膜支架,例如Medronic,Cook自2008年以来才推入中国市场。因而,在2009年前、后进行手术被认为分别使用第1代和第2代覆膜支架。
2 结果
2.1纳入研究
共有153篇研究,包含8 694例AD患者符合纳入和排除标准,纳入最终分析(图1)。其中,8415例(96.8%)为B型AD(附录表A2)。
2.2患者特点
纳入研究的患者特点见表1。8 415例患者中大部分(7 901,93.9%)B型AD接受了腔内修复术。7 775例患者中65例(0.8%)通过CT血管造影、磁共振血管造影或者数字减影血管造影,证实是主动脉破裂。7 072例患者中404例(6.1%)确诊为复杂型B型AD。
2.3手术及住院数据
技术成功率为(99.7±0.1)%。早期中转手术(18/7 901)率为(0.2±0.1)%(表2),辅助性腔内手术发生率为(2.6±0.2)%。住院总体并发症的发生率为(19.1±0.6)%。其中,严重并发症的发生率为(3.2±0.2)%,而轻微并发症的发生率为(16.2±0.6)%。术后内漏的发生率为(7.2±0.3)%,其中Ⅰ型、Ⅱ型、Ⅲ型和Ⅳ型内漏发生率分别为(4.2±0.3)%、(0.3±0.1)%、(0.2±0.1)%和(0.4±0.1)%。手术相关并发症的发生率为(7.1±0.4)%,其中逆行A型AD的发生率为(0.3±0.1)%,径路并发症的发生率为(1.1±0.1)%。总神经系统并发症的发生率为(1.3±0.1)%,其中中风率为(0.8±0.1)%,而截瘫率为(0.10±0.04)%。腔内隔绝术综合征的发生率为(3.8±0.3)%。每个患者平均使用1.1枚支架,如表2所示。Zenith TX-2(Cook,美国)支架是最常用的支架(表3)。
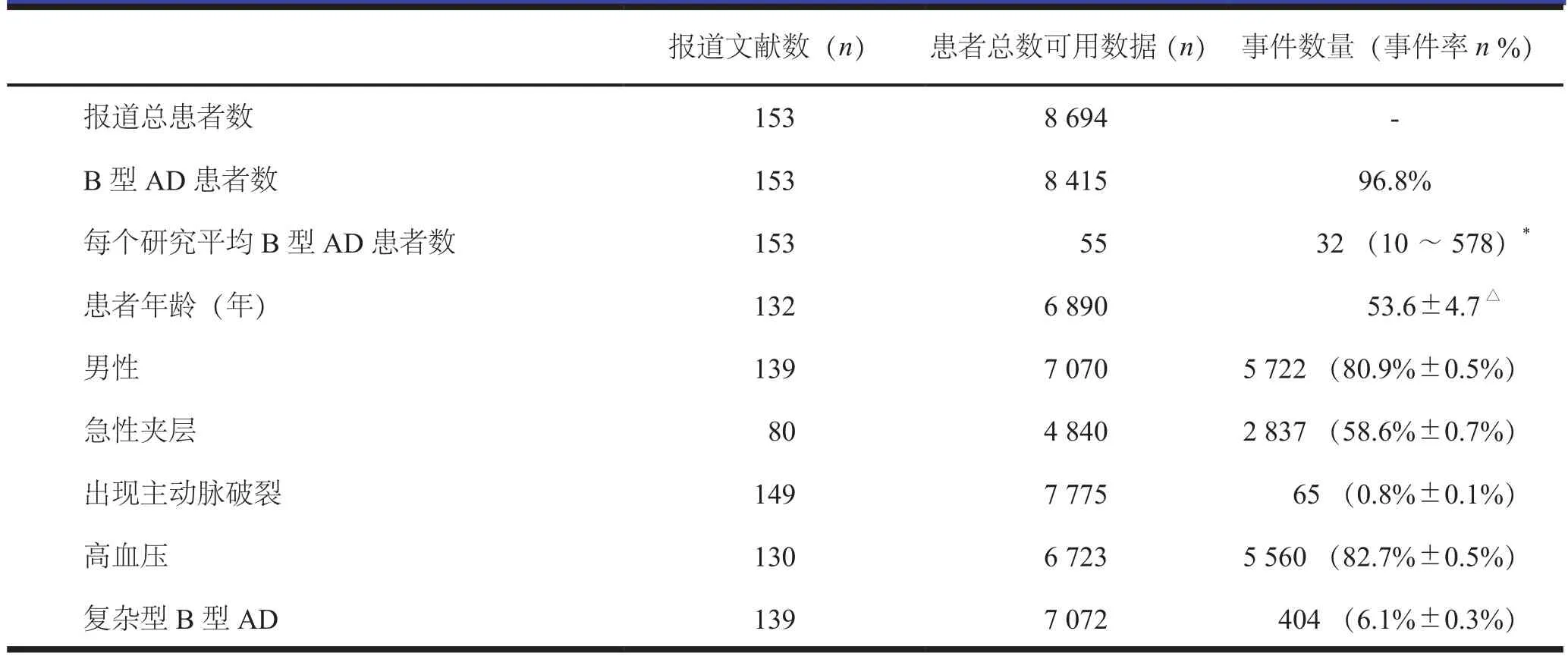
表1 患者特点
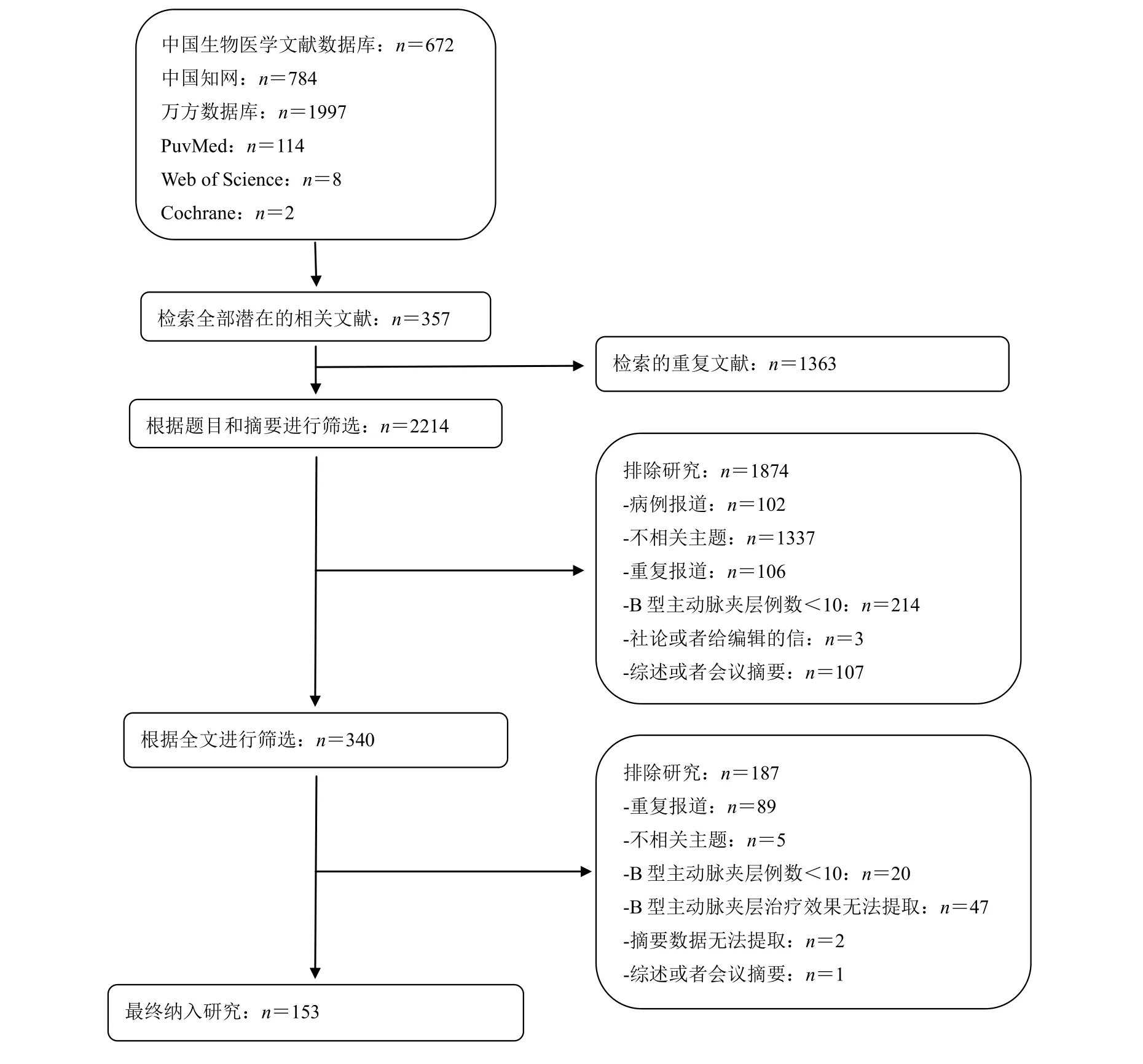
图1 文献纳入和排除流程图
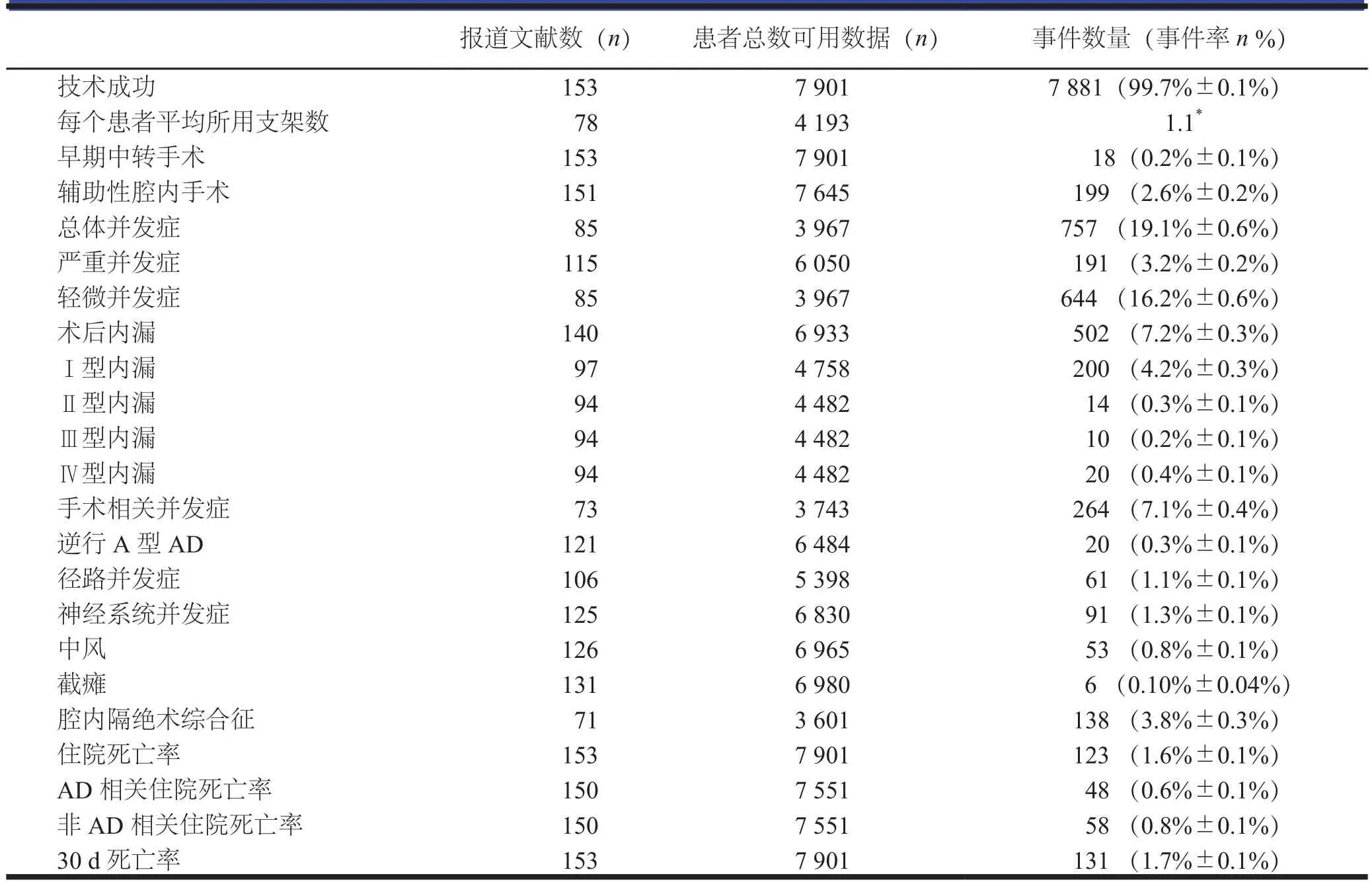
表2 住院期间数据
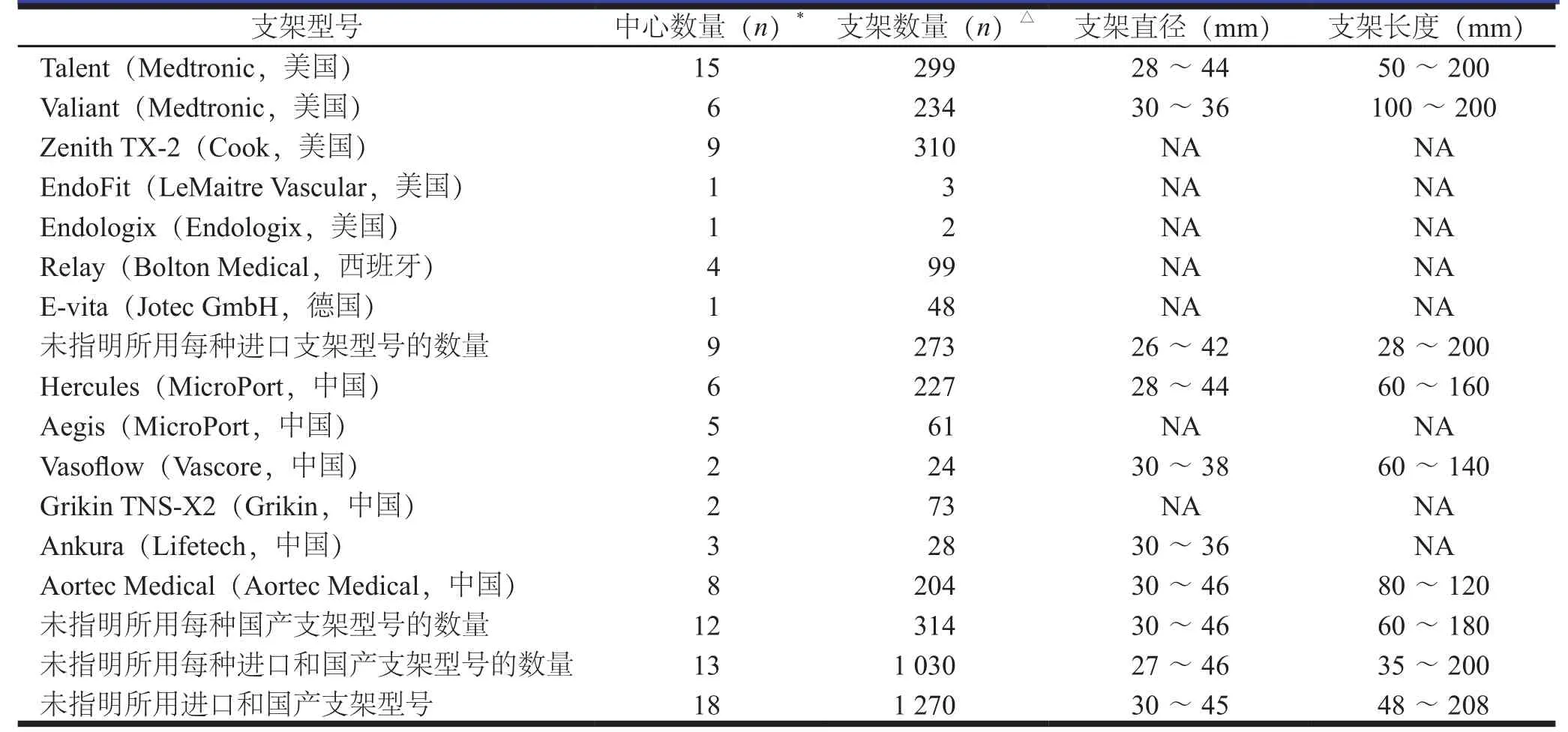
表3 支架型号
7 901例患者中共有123例住院期间死亡,总的住院期间死亡率为(1.6±0.1)%。另有8例患者在30 d内死亡,因此30 d死亡率为(1.7±0.1)%。
2.4随访数据
共有147篇研究(6 970例患者)报道了随访时间,但是只有52篇研究(3 311例患者)报道了平均随访时间,(29.4±13.5)个月(表4)。晚期假腔内血栓形成的发生率为(93.4±0.5)%。晚期中转手术率为(0.4±0.1)%,晚期辅助性腔内手术的发生率为(0.10±0.04)%。因此,随访期总的再次干预率为(0.5±0.1)%。持续内漏和新发内漏的发生率分别为(2.1±0.2)%和(0.5±0.1)%。支架移位的发生率为(0.1±0.04)%。晚期并发症、晚期神经系统并发症和晚期逆行A型AD的发生率分别为(8.3±0.4)%,(0.8±0.1)%和(0.5±0.1)%。新发AD的发生率为(0.3±0.1)%。(1.1±0.1)%患者接受了2次腔内手术。
随访期间主动脉破裂的发生率为(1.2±0.1)%,(1.8±0.2)%患者在随访期间死亡。图2对有确切死亡时间的5 142例患者进行Kaplan-Meier分析。30 d、6个月、1年、2年和5年的生存率分别为(99.0±0.1)%、(98.5±0.2)%、(98.4±0.2)%、(98.1±0.2)%和(97.9±0.2)%。
2.5不同出版日期的腔内支架植入术的结果
总体并发症的发生率在近期出版的研究(2009—2014年)为(18.0±0.7)%,比早期出版的研究(2002—2008年)(24.6±1.7)%(P<0.001)(表5)低。神经系统并发症的发生率在近期研究组中更高(1.5%±0.2% vs 0.5%±0.2%,P=0.006)。技术成功率,30 d或者1年死亡率2组间差异无统计学意义。
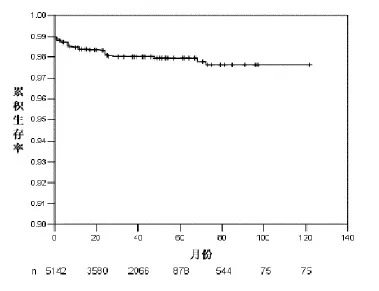
图2 腔内支架植入术治疗AD总体生存率的Kaplan-Meier估计
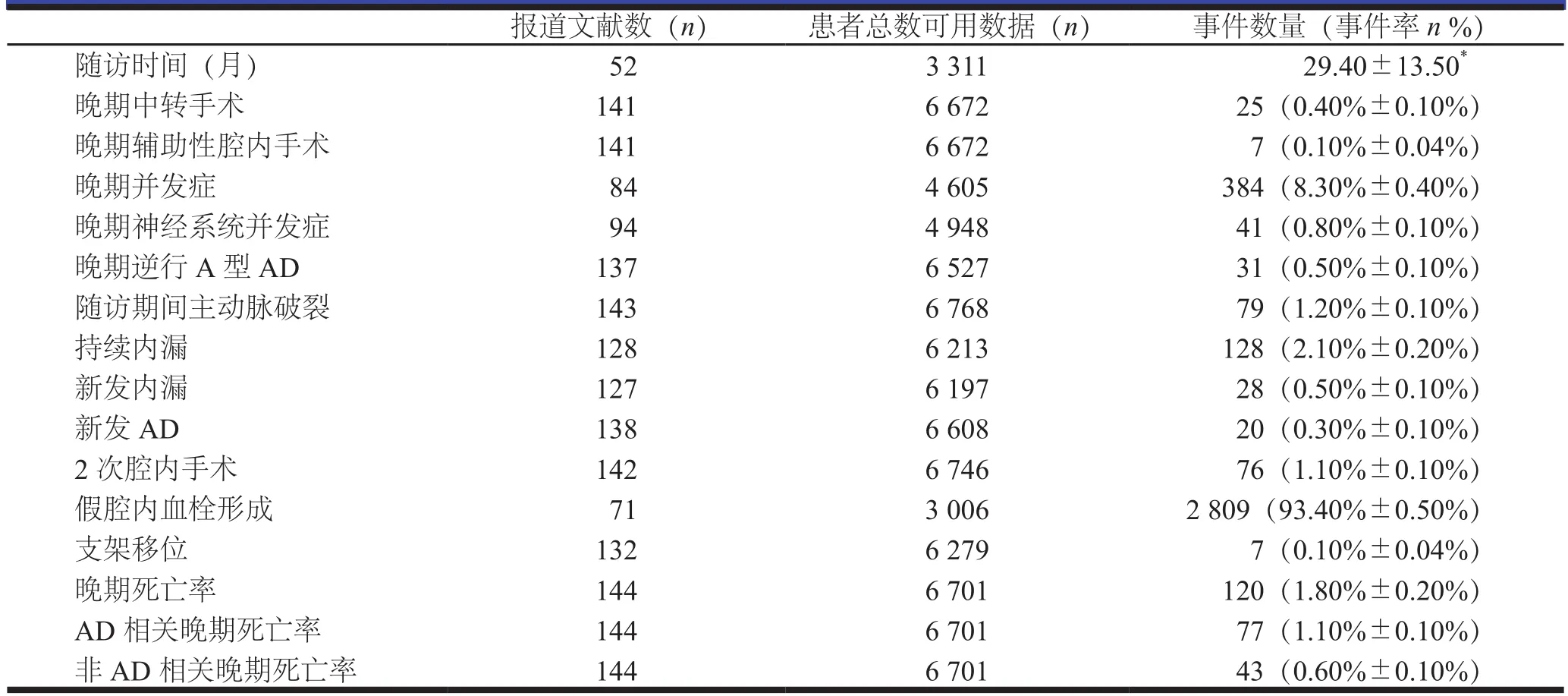
表4 随访期间数据
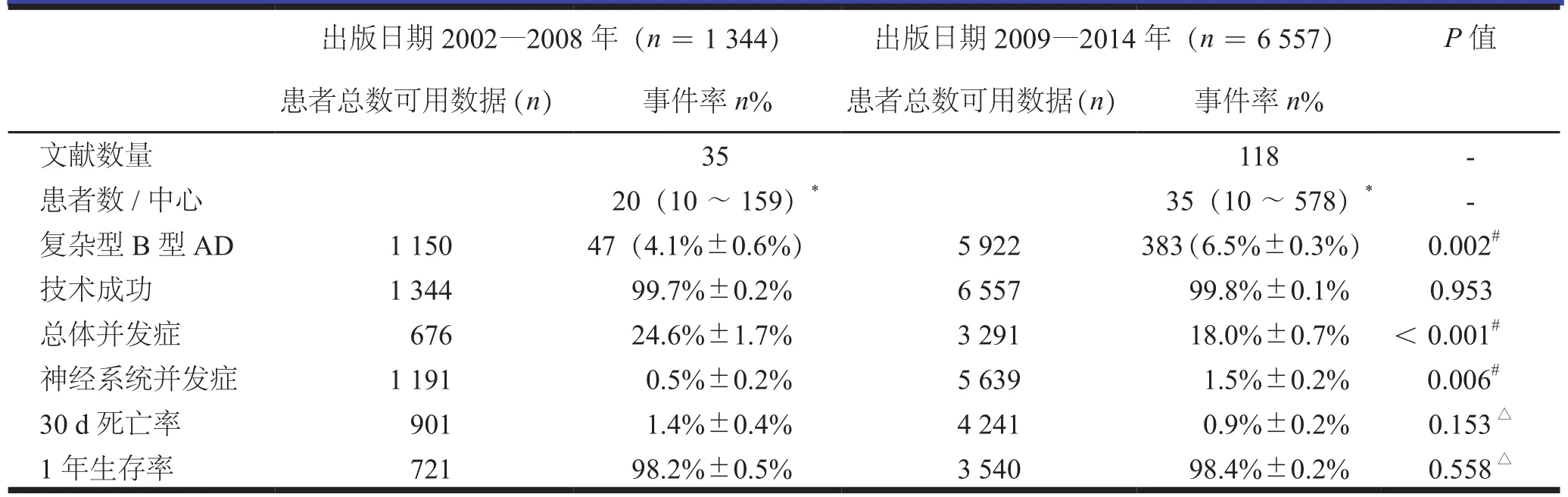
表5 不同出版日期腔内支架植入术的结果
2.6腔内手术经验的影响
腔内手术经验对结果的影响见表6。患者例数>中位数的中心,其总体并发症的发生率和30 d死亡率均比患者例数<中位数的中心低(15.3%±0.7% vs 32.3%±1.6%,P<0.001;0.8%±0.1% vs 1.7%±0.4%,P=0.005)。然而患者例数>中位数的中心,其1年生存率更高(98.7%±0.2% vs 97.5%±0.4%,P= 0.004)。
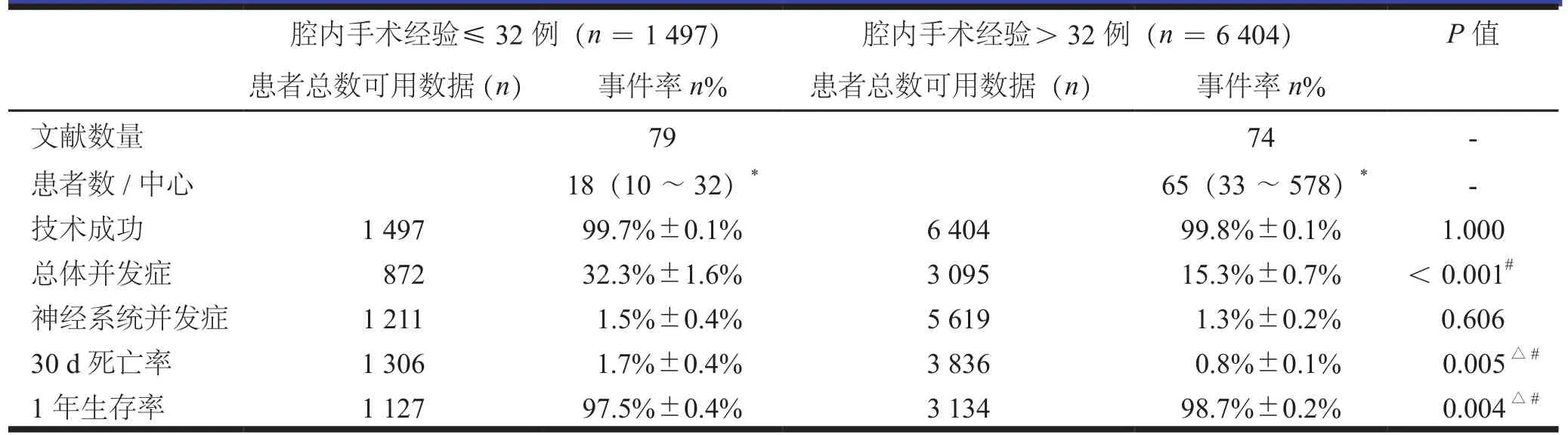
表6 腔内手术经验对结果的影响
2.7第1代和第2代覆膜支架
在总的153篇研究中,61篇(39.9%)研究同时报道第1代和第2代覆膜支架的使用情况,66篇(43.1%)研究报道了第1代覆膜支架的使用情况,26篇(17.0%)研究报道了第2代覆膜支架的使用情况(表7)。第1代和第2代覆膜支架组之间大部分评价指标差异无统计学意义(表7)。第2代覆膜支架组纳入年轻患者的比例更大。第2代覆膜支架组的总体并发症(9.5%±0.9% vs 25.1%±1.2%,P<0.001),严重并发症(2.0%±0.4% vs 3.2%±0.4%, P=0.042),轻微并发症(7.4%±0.8% vs 21.7%±1.1%,P<0.001),术后内漏(5.0%±0.6% vs 8.6%±0.6%,P <0.001),手术相关并发症(3.6%±0.6% vs 6.8%±0.8 %,P=0.001),晚期并发症(5.3%±0.7% vs 9.1%±0.7%,P<0.001),晚期神经系统并发症(0.2%±0.1% vs 0.8%±0.2%,P=0.032)和持续内漏(0.8%±0.3% vs 2.2%±0.3%,P= 0.003)相对较少。然而,辅助性腔内手术和2次腔内手术第2代覆膜支架组相对较多(2.8%±0.4% vs 1.5%±0.2%,P=0.005;2.0%±0.4% vs 0.7%±0.2%,P<0.001)。第1代覆膜支架组的30 d、6个月、1年、2年和5年总体生存率分别为(99.0±0.2)%、(98.6±0.3)%、(98.4±0.3)%、(98.3±0.3)%和(98.1±0.4)%。第2代覆膜支架组的30 d、6个月、1年、2年和5年总体生存率分别为(99.3±0.2)%、(99.1±0.3)%、(99.1±0.3)%、(98.8±0.3)%和(98.8±0.3)%。(表7)
3 讨论
本研究结果表明,腔内支架植入术治疗Stanford B型AD技术成功率较高(>99%),治疗效果较好。腔内修复术的早期、中期和远期生存率分别为99.0%、98.1%和97.9%。INSTEAD试验对比了覆膜支架植入术联合最佳药物治疗(optimal medical therapy,OMT)与单纯OMT治疗慢性非复杂型B型AD的结果提示,覆膜支架联合药物治疗组虽然未能增加术后1年和2年生存率,但是5年生存率明显改善[4-6]。急性主动脉夹层的国际注册(the International Registry of Acute Aortic Dissection,IRAD)试验报道了患者接受药物、手术和腔内治疗3年生存率,结果分别为(77.6±6.6)%、(82.8±18.9)%和(76.2±25.2)%(P=0.61)[12]。事实上,在IRAD试验中手术或者腔内修复术纳入了更多的复杂型AD患者,而OMT用于非复杂型AD患者,组间没有可比性。覆膜支架植入术组生存率似乎比药物治疗组更高,至少能够说明,覆膜支架植入术组死亡率没有增加。可见,Stanford B型夹层可能从腔内修复术中获益。
手术治疗急性B型AD的1年、5年、10年和15年生存率分别为56%、48%、29%和11%,手术治疗慢性B 型AD的生存率分别为78%、59%、45%和27%[13]。另一个IRAD研究发现手术治疗急性B型AD的住院死亡率为31.4%[14]。可见,开放手术治疗B型AD的死亡率较高。据2个荟萃分析报道,腔内修复术与开放手术治疗相比,明显减少了急性B型AD的30 d死亡率[9,15]。可见,腔内支架植入术相比开放手术治疗急性B型AD特定病例的早期存活率似乎更有利,但是在缺乏与开放手术随机直接比较的情况下,结论仍然需要谨慎。
神经系统并发症,特别是截瘫,是手术修复B型AD最严重的并发症。IRAD试验[16]报道手术治疗AD患者神经系统并发症的发生率为23.2%,脑血管意外和截瘫发生率分别为9.0%和4.5%。EUROSTAR(European Collaborators on Stent/Graft Techniques for Aortic Aneurysm Repair)注册的一项研究[17]报道腔内修复术治疗AD患者截瘫率和中风率分别为1.4%和3.3%。一项荟萃分析表明,腔内支架修复术与开放修复术相比,截瘫发生率更低﹝比值比(odds ratio,OR)为0.23,P=0.005)﹞[10]。另一项荟萃分析表明,腔内修复与开放修复相比,截瘫率(OR =0.256,P=0.001)明显减少[9]。Eggebrecht等[11]报道了腔内修复术治疗AD患者的结果,观察到神经系统并发症、中风和截瘫的发生率分别为2.9%、1.9%和0.8%。本研究汇总的数据提示神经系统并发症发生率更低,仅为1.3%(中风率为0.8%,截瘫率为0.1%)。神经系统并发症的发生率较低,其原因可能包括:⑴ 本研究纳入患者的平均年龄及女性患者的比例比其他研究更低[11,17];⑵ 本研究一些危险因素,例如夹层破裂发生率,明显低于Eggebrecht等研究(0.8%±0.1% vs 16.1%±1.2%)[11],这也是获得更好结果的原因之一;⑶ 研究中每个患者平均使用的支架较少,仅1.1枚。覆膜支架数量的减少和主动脉覆盖长度的缩短可能减少截瘫或者中风的风险因素[17,18]。在腔内修复术时如果主动脉T9~T12节段需要覆盖,常规进行脑脊液引流以防止截瘫。在腔内修复胸主动脉病变时覆盖左侧锁骨下动脉而不进行血运重建,会增加截瘫或者中风的风险[17,19,20]。当前左侧锁骨下动脉的重建不频繁,这可能是近期研究神经系统并发症增加的原因之一。2项病例报告分别报道国内应用血管封堵器和室间隔缺损封堵器可以作为Stanford B型AD的另一种微创选择,也可以减少神经系统并发症,但是确切的长期治疗效果仍然有待观察[21,22]。
本研究住院期间总体并发症的发生率为19.1%。这些并发症中约有40%是手术相关并发症。逆行A型AD在住院和随访期间发生率分别为0.1%和0.4%。逆行A型AD归因于多种原因,包括主动脉壁脆弱、病情恶化、导丝/护套的操作和覆膜支架相关因素[23,24]。谨慎选择患者,精心设计覆膜支架设备,规范腔内操作,可防止逆行A型AD的发生。腔内修复术后影像学监测,可以早期发现这种灾难性并发症。本研究中新发AD和2次腔内手术的发生率分别为0.3%和1.1%。作为腔内修复的辅助技术,限制性裸支架可以减少覆膜支架引起的远端再发夹层和再次干预发生率[25]。
本研究表明经验更多的中心1年生存率更高,并发症和30 d死亡率更低。近期研究的总体并发症的发生率<早期研究;近期研究的神经系统并发症却有所增加,其原因在于:⑴ 由于能够做腔内修复术的中心数量和手术的数量增加;⑵ 术者培训也发生了变化;⑶ 随着技术和腔内技术的发展,腰椎引流或者颈动脉锁骨下动脉旁路在国内使用更少;⑷ 随着地级医院医生知识的增加,更多具有挑战性复杂病例被诊断出来;⑸ 腔内修复术的指征已经扩大到高风险患者。这种指征的扩大可能导致早期和中期并发症谱的扩大,包括截瘫或者中风等潜在的灾难性并发症[26]。
覆膜支架技术逐步发展,从第1代远端直筒覆膜支架发展到第2代远端锥形覆膜支架。第1代覆膜支架面临许多问题,包括内漏、支架扭曲、支架移位、逆行A型AD和主动脉破裂等。2009年前,绝大多数国内医生选择使用长度为60~130 mm,oversize为10%~30%覆膜支架。这些长度较短的支架材质较硬,不符合主动脉弓及降主动脉之间接合处形状。根据报道,第1代覆膜支架直径过大可能会对主动脉壁产生较大的径向力,进而增加逆行夹层及远端破口的风险,因此,oversize 10%~15%似乎更合适[23]。2009年后,长度为150~240 mm,oversize为10%~15%覆膜支架,被更频繁地使用。第2代覆膜支架有更长的长度和更合适的oversize可供选择,可以减少因潜在主动脉内膜损伤和撕裂导致内漏和逆行A型AD的风险。新型支架,包括开窗、分支和烟囱支架,使腔内支架植入术治疗那些复杂解剖结构的患者成为可能。
研究结果表明:使用第1或者第2代覆膜支架,腔内支架植入术的技术成功率均较高。第2代覆膜支架没有改善术后5年生存率,但是住院和随访期治疗效果似乎更好。其原因可能是:⑴ 第2代覆膜支架患者平均年龄更年轻,在一定程度上可能有更好的治疗效果;⑵ 大多数覆膜支架相关并发症的减少可能得益于第2代覆膜支架的设计和输送导管的技术改进。第2代覆膜支架的应用可以减少并发症,但是并不能完全消除并发症。未来设计良好,具有更合适的直径和长度的覆膜支架,可以进一步增加治疗效果。
超过一半的研究没有详细描述术后假腔的形态学变化。术后假腔内血栓形成发生率约93%。随访期间主动脉破裂风险约为1.2%。随着时间推移,约3%患者需要行辅助性腔内手术和中转手术。持续假腔通畅与晚期动脉瘤的形成密切相关。良好的重塑可以防止晚期动脉瘤破裂[27]。已经有研究证明,腔内支架植入术可以促进主动脉重塑[4,8,27]。假腔内血栓形成和重塑可以减少晚期动脉瘤形成和再次干预率[7],国内作者似乎只是重视技术上成功和并发症减少,而忽略了随访期间主动脉的形态学变化。在腔内支架植入术后密切、长期影像学随访,应该受到足够的重视。
本研究的缺陷包括以下6个方面:⑴ 所有纳入研究都是回顾性研究;⑵ 缺乏随机和盲法常会增加潜在的偏倚;⑶ 提供完整数据的研究所占的比例相对较低,进一步增加了选择偏差;⑷ 在一些研究中定义和原始数据模棱两可,这可能减少本研究可靠性并且限制统计学功效;⑸ 随访期间影像学资料不完整;⑹ 研究纳入较多年轻患者并且复杂型夹层相对较少,结果可能更适用于年轻或者非复杂型患者。
尽管如此,本研究纳入了足够多国内数据。而且,本研究严格实施系统评价的评估方法,严格执行纳入和排除标准。更为重要的是,本研究为腔内支架植入术治疗B 型AD的技术成功率、潜在优势、并发症、支架进展和生存率等方面,提供了重要的数据参考。
4 结论
综上所述,腔内支架植入术治疗Stanford B型AD切实可行,技术成功率较高,神经系统并发症的发生率较低,生存率较高。第2代覆膜支架住院和随访期治疗效果更好。然而,尽管本研究方法严谨,考虑到纳入研究的固有局限性,引用本研究结论宜谨慎。未来设计良好的多中心RCTs及更完善的随访观察,可能进一步论证本研究的观点。
参考文献
[1] Svensson LG, Kouchoukos NT, Miller DC, et al. Expert consensus document on the treatment of descending thoracic aortic disease using endovascular stent-grafts. Ann Thorac Surg, 2008, 85: S1-41.
[2] Fattori R, Cao P, De Rango P, et al. Interdisciplinary expert consensus document on management of type B aortic dissection. J Am CollCardiol, 2013, 61: 1661-1678.
[3] Glower DD, Fann JI, Speier RH, et al. Comparison of medical and surgical therapy for uncomplicated descending aortic dissection. Circulation, 1990, 82: IV39-46.
[4] Nienaber CA, Rousseau H, Eggebrecht H, et al. Randomized comparison of strategies for type B aortic dissection: the INvestigation of STEnt grafts in aortic dissection (INSTEAD)trial. Circulation, 2009, 120: 2519-2528.
[5] Nienaber CA, Kische S, Akin I, et al. Strategies for subacute/ chronic type B aortic dissection: the investigation of Stent grafts in patients with type B aortic dissection (INSTEAD) trial 1-year outcome. J Thorac Cardiovasc Surg, 2010, 140: S101-108.
[6] Nienaber CA, Kische S, Rousseau H, et al. Endovascular repair of type B aortic dissection: long-term results of the randomized investigation of stent grafts in aortic dissection trial. Circ Cardiovasc Intervent, 2013, 6: 407-416.
[7] Brunkwall J, Lammer J, Verhoeven E, et al. 2012 ADSORB:A study on the efficacy of endovascular grafting in uncomplicated acute dissection of the descending aorta. Eur J Vasc Endovasc Surg, 2012, 44: 31-36.
[8] Brunkwall J, Kasprzak P, Verhoeven E, et al. Endovascular repair of acute uncomplicated aortic type B dissection promotes aortic remodelling: 1 year results of the ADSORB trial. Eur J Vasc Endovasc Surg, 2014, 48: 285-291.
[9] Luebke T, Brunkwall J. Outcome of patients with open and endovascular repair in acute complicated type B aortic dissection: a systematic review and meta-analysis of case series and comparative studies. J Cardiovasc Surg (Torino), 2010, 51: 613-632.
[10] Xenos ES, Minion DJ, Davenport DL, et al. Endovascular versus open repair for descending thoracic aortic rupture:institutional experience and meta-analysis. Eur J Cardio Surg, 2009, 35: 282-286.
[11] Eggebrecht H, Nienaber CA, Neuhäuser M. Endovascular stent-graft placement in aortic dissection: a meta-analysis. Eur Heart J, 2006, 27: 489-498.
[12] Tsai TT, Fattori R, Trimarchi S, et al. Long-term survival in patients presenting with type B acute aortic dissection:insights from the International Registry of Acute Aortic Dissection. Circulation, 2006, 114: 2226-2231.
[13] Fann JI, Smith JA, Miller DC, et al. Surgical management of aortic dissection during a 30-year period. Circulation, 1995,92: 113-121.
[14] Hagan PG, Nienaber CA, Isselbacher EM, et al. The International Registry of Acute Aortic Dissection (IRAD):new insights into an old disease. JAMA, 2000, 283: 897-903.
[15] Zhang H, Wang ZW, Zhou Z, et al. Endovascular stent-graft placement or open surgery for the treatment of acute type B aortic dissection: a meta-analysis. Ann Vasc Surg, 2012, 26: 454-461.
[16] Trimarchi S, Nienaber CA, Rampoldi V. Role and results of surgery in acute type B aortic dissection: insights from the International Registry of Acute Aortic Dissection (IRAD).Circulation, 2006, 114: I357-364.
[17] Buth J, Harris PL, Hobo R, et al. Neurologic complications associated with endovascular repair of thoracic aortic pathology:incidence and risk factors. A study from the European collaborators on Stent/graft techniques for aortic aneurysm repair (Eurostar) registry. J Vasc Surg, 2007, 46: 1103-1111.
[18] Amabile P, Grisoli D, Giorgi R, et al. 2008 Incidence and determinants of spinal cord ischaemia in stent-graft repair of the thoracic aorta. Eur J Vasc Endovasc Surg, 2008, 35: 455-461.
[19] Clough RE, Modarai B, Topple JA, et al. Predictors of stroke and paraplegia in thoracic aortic endovascular intervention. Eur J Vasc Endovasc Surg, 2011, 41: 303-310.
[20] Feezor RJ, Martin TD, Hess PJ, et al. Risk factors for perioperative stroke during thoracic endovascular aortic repairs (TEVAR). J Endovasc Ther, 2007, 14: 568-573.
[21] Tang X, Fu WG, Xu X, et al. Use of a vascular occluder to treat a re-entry tear in a patient with Stanford type B aortic dissection:acute and 1-year results. J Endovasc Ther, 2008, 15: 566-569.
[22] Chang GQ, Wang HS, Chen W, et al. Endovascular repair of a type B aortic dissection with a ventricular septal defect occluder. J Vasc Surg, 2010, 51: 1507-1509.
[23] Dong ZH, Fu WG, Wang YQ, et al. Retrograde type A aortic dissection after endovascular stent graft placement for treatment of type B dissection. Circulation, 2009, 119: 735-741.
[24] Eggebrecht H, Thompson M, Rousseau H, et al. Retrograde ascending aortic dissection during or after thoracic aortic stent graft placement: insight from the European registry on endovascular aortic repair complications. Circulation, 2009, 120: S276-281.
[25] Feng JX, Lu QS, Zhao ZQ, et al. Restrictive bare stent for prevention of stent graft-induced distal redissection after thoracic endovascular aortic repair for type B aortic dissection. J Vasc Surg, 2013, 57: 44S-52S.
[26] Eggebrecht H, Baumgart D, Radecke K, et al. Aortoesophageal fistula secondary to stent-graft repair of the thoracic aorta. J Endovasc Ther, 2004, 11: 161-167.
[27] Conrad MF, Crawford RS, Kwolek CJ, et al. Aortic remodeling after endovascular repair of acute complicated type B aortic dissection. J Vasc Surg, 2009, 50: 510-517.

附录表A1 腔内支架植入术治疗B型AD患者临床特点,住院、手术和随访期间数据
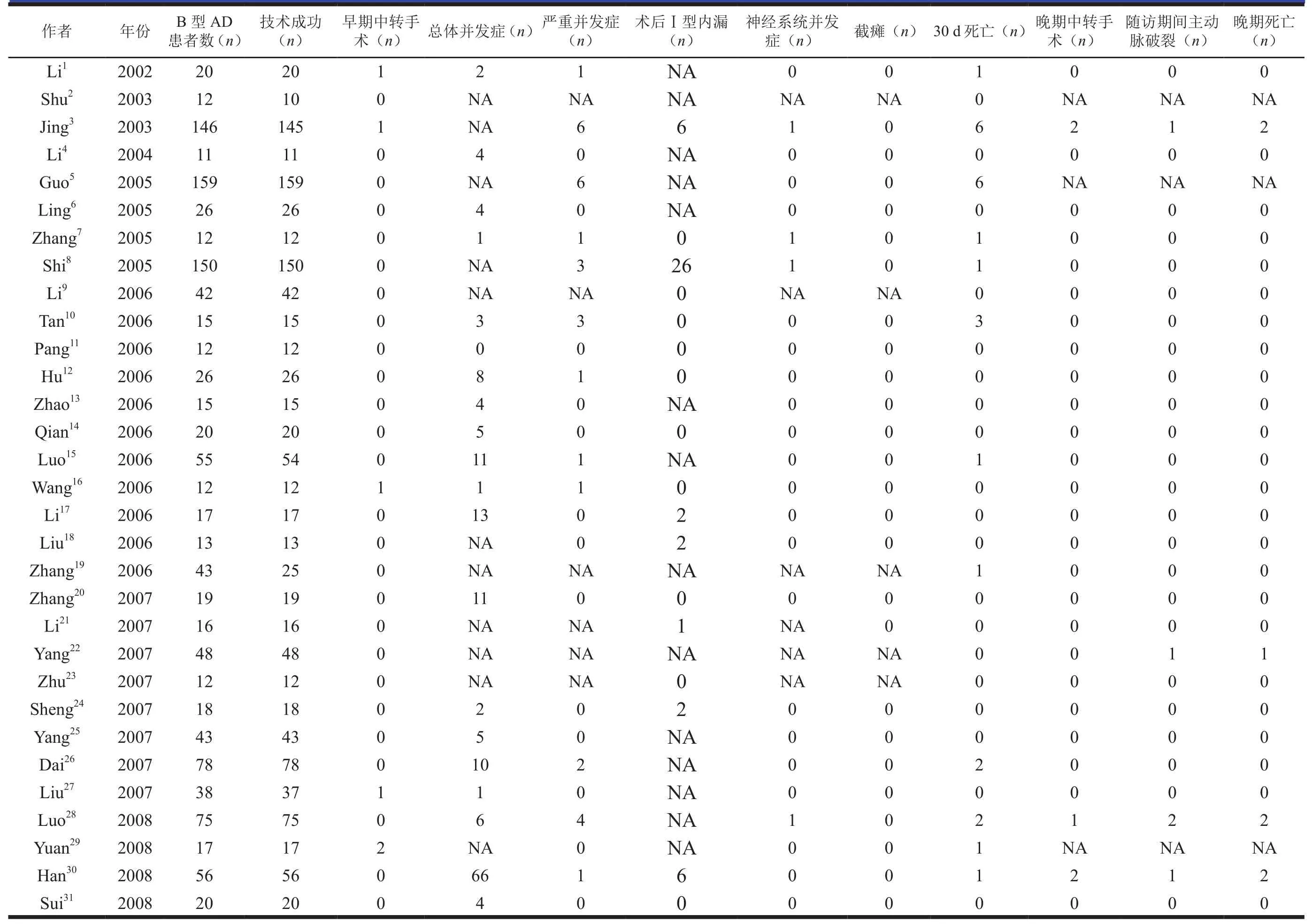
附表A2 纳入文献部分数据的概况(1)
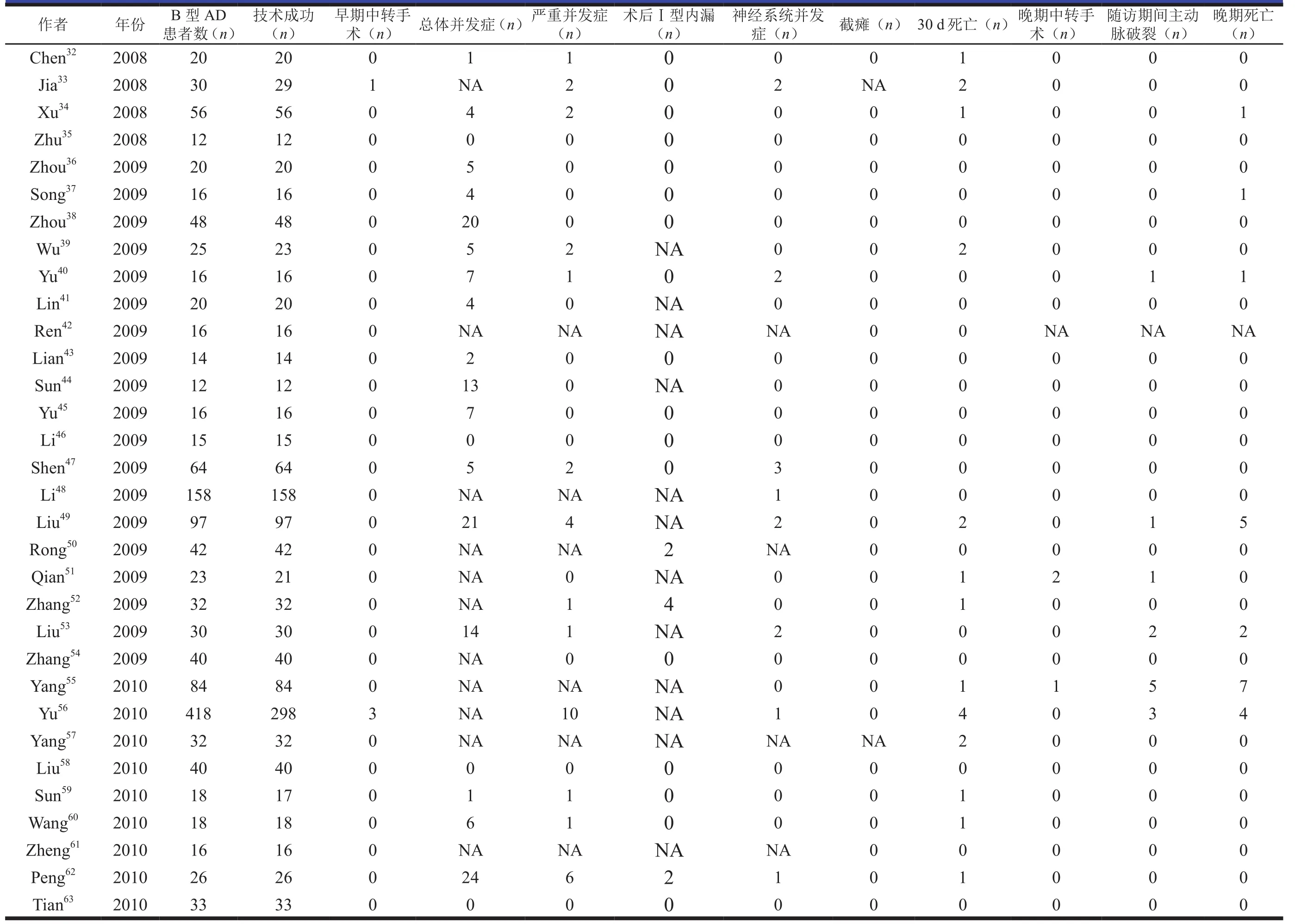
附表A2 纳入文献部分数据的概况(2)
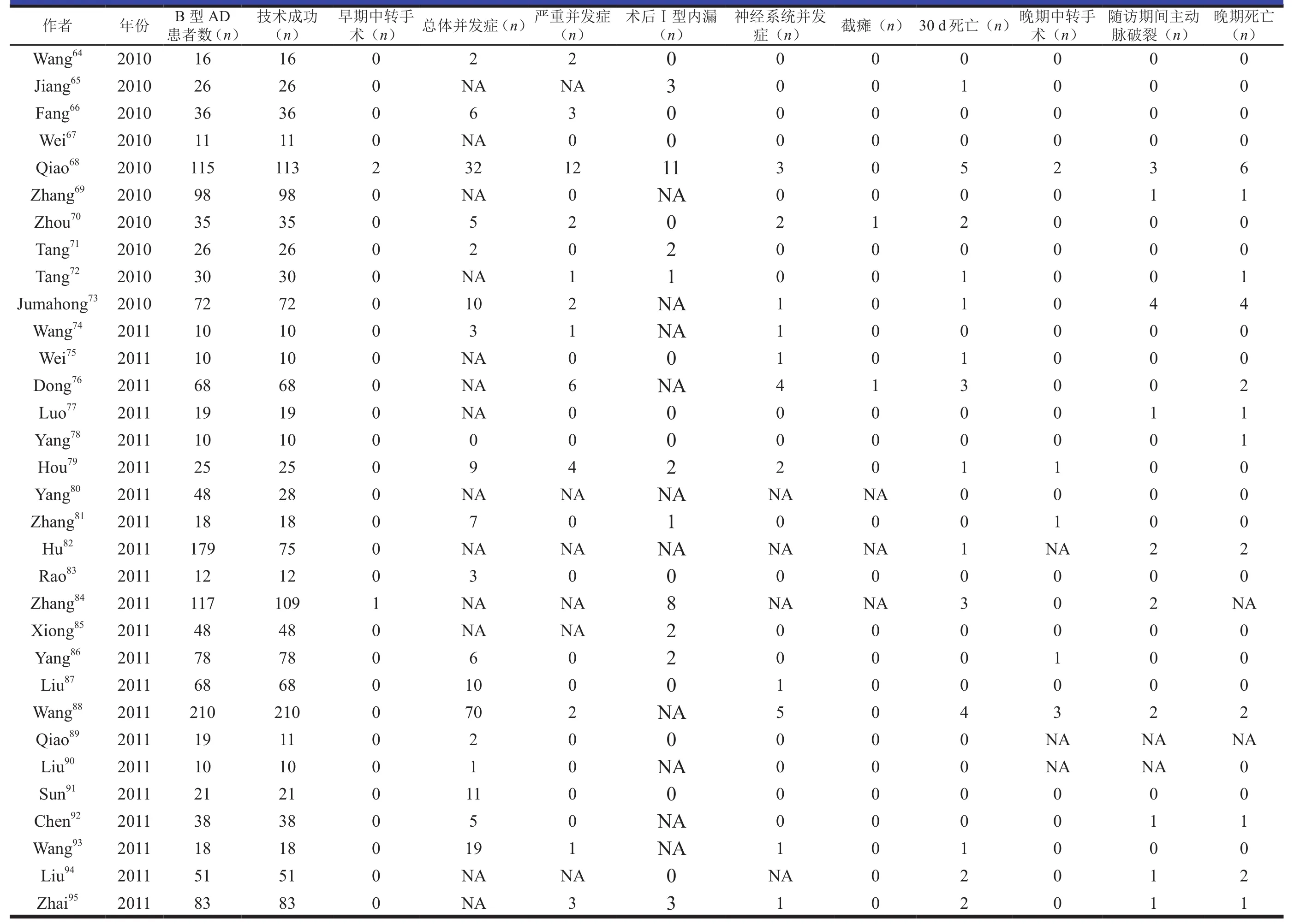
附表A2 纳入文献部分数据的概况(3)
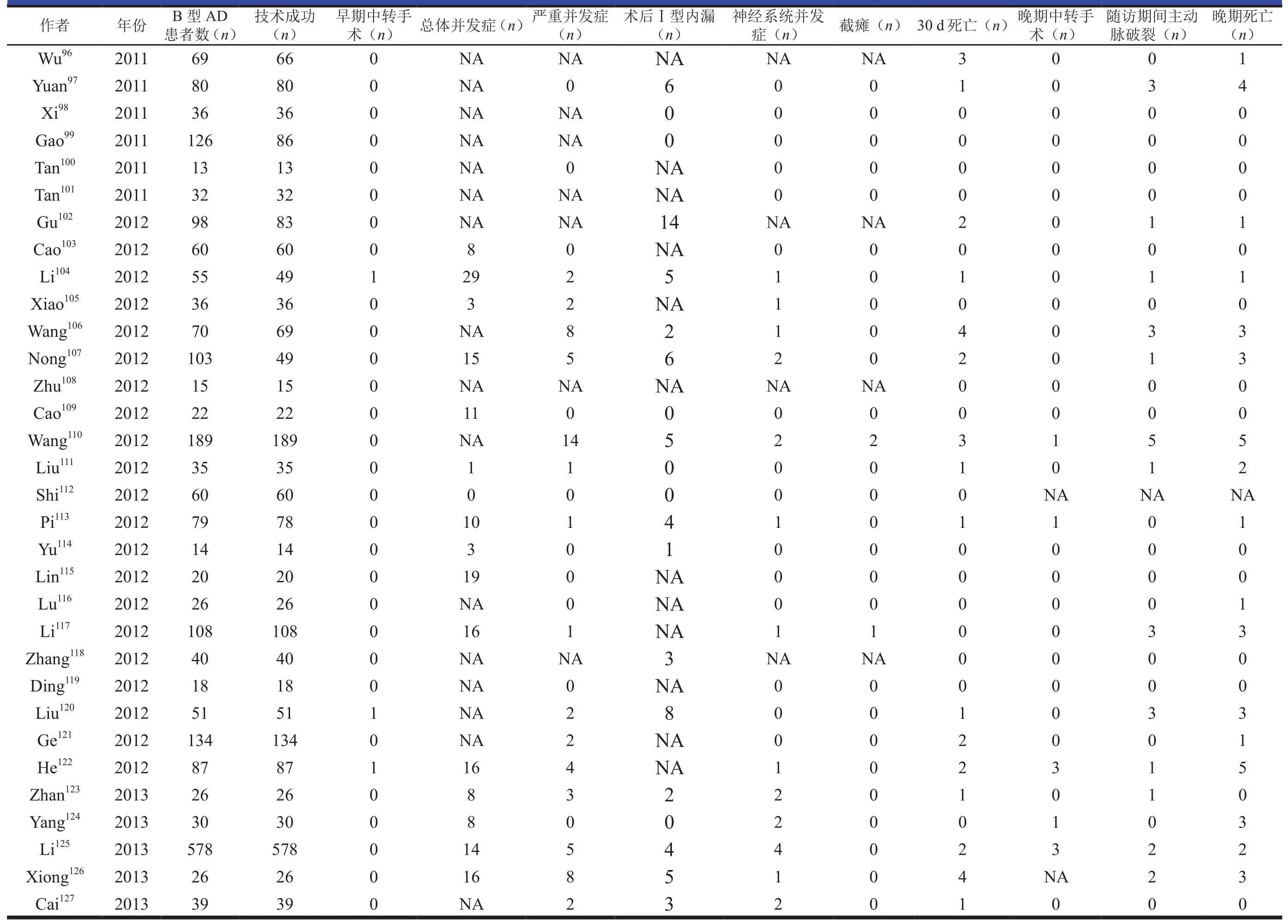
附表A2 纳入文献部分数据的概况(4)
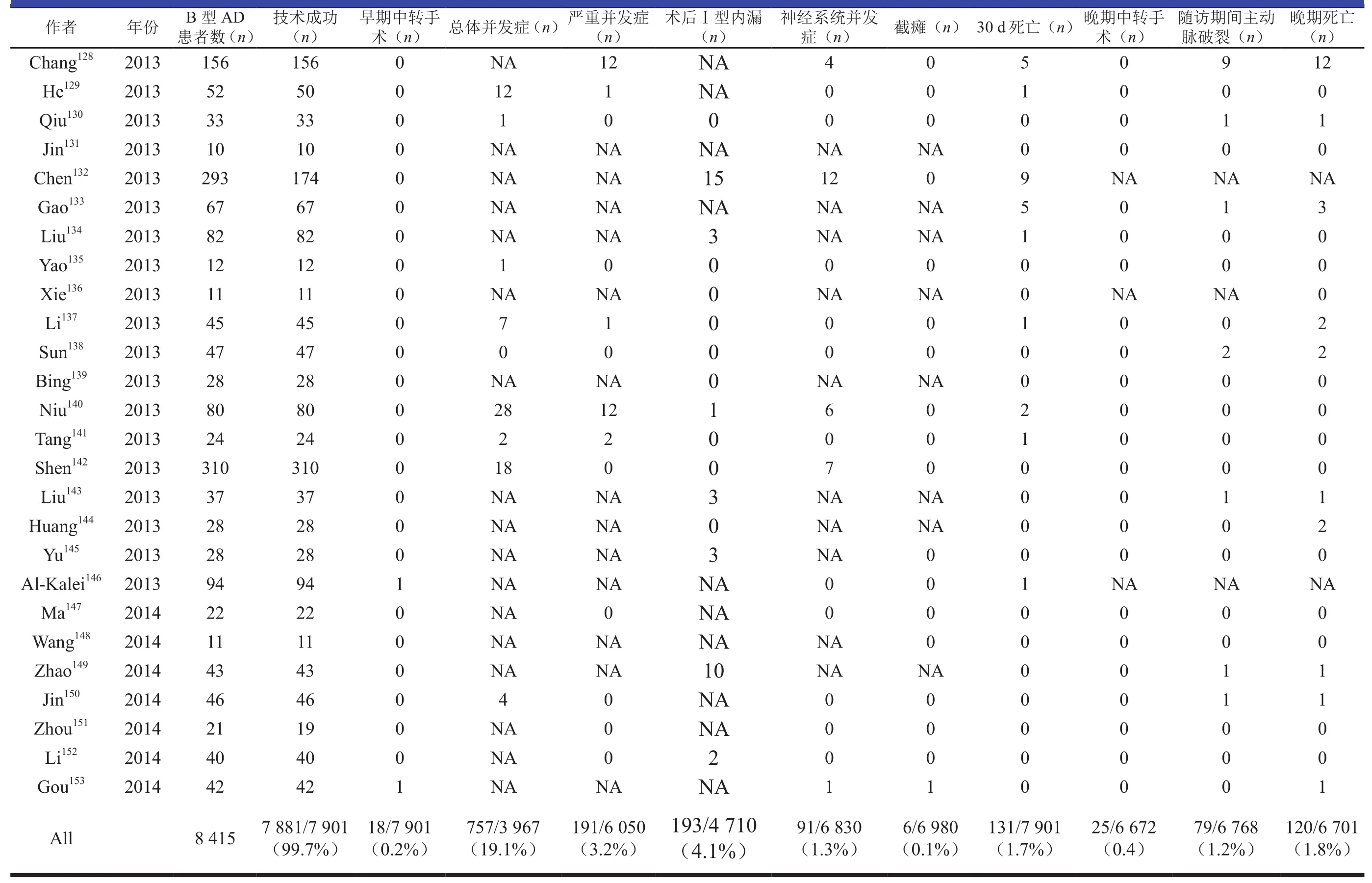
附表A2 纳入文献部分数据的概况(5)
Endovascular stent-graft placement for the treatment of Stanford type B aortic dissection in China: A systematic review
WANG Jun-wei1LI Yong-hui1LI Yong-xin2CUI Jin1LI Wen1WANG Yang1WANG Shen-ming1WANG Jin-song1*1Department of Vascular Surgery, the First Affliated Hospital of Sun Yat-sen University, Guangzhou 510080, China2Department of Vascular Surgery, the Affliated Hospital of Qingdao University, Qingdao 266001, China
Abstract:Objective To summarize the efficacy, technique feasibility, and clinical safety of endovascular repair for Stanford type Baortic dissection (AD) in China. Methods We comprehensively searched the English-language medicalliterature in PubMed, Web of Science, and the Cochrane Library and the Chinese-language medical literatures in CBMdisc (Chinese Biomedical Database), CNKI (China National Knowledge Infrastructure), and Wanfang Data. This systematic review was based on all retrospective studies assessing outcomes of Stanford type BAD treated with endovascular stent-graft placement in China. Results A total of 153 retrospective studies that included 8 415 cases of type B AD were analyzed in this study. Procedure success was reported in (99.7±0.1)% of patients. Overall complications were reported in (19.1±0.6)% of patients. Postoperative endoleak occurred in (7.2±0.3)% of patients. Major complications were reported in (3.2±0.2)% of patients, with a neurological complication rate of (1.3±0.1)%. Periprocedural stroke occurred more frequently than paraplegia (0.8%±0.1% versus 0.1%±0.04%). Overall complications was signifcantly greater in patients treated with frst-generation stents compared with second-generation stents (25.1%±1.2% versus 9.5%±0.9%, P<0.001). The in-hospital mortality rate was (1.6±0.1)%. Additionally,(1.8±0.2)% of patients died during a mean follow-up period of (29.4±13.5) months. The Kaplan-Meier estimates of the overall survival rate were (99.0±0.1)% at 30 days, (98.5±0.2)% at 6 months, (98.4±0.2)% at 1 year, (98.1±0.2)% at 2 years, and (97.9±0.2)% at 5 years. Conclusions Endovascular stent-graft placement is feasible and has a high technique success rate and favorable neurological complication and survival rates in treating Stanford type B AD. Technique improvements in stent-graft design and device delivery catheters have attempted to address previously encountered diffculties. The second-generation of stent-grafts has better in-hospital and follow-up outcomes.
Key words:endovascular; coated stent graft; Stanford type B; aortic dissection; systematic review
中图分类号:R543.1
文献标志码:A
文章编号:2096-0646.2016.02.02.09
基金项目:国家自然科学基金(81070257)
*通信作者:王劲松,E-mail:wangjs@mail.sysu.edu.cn

