特发性高嗜酸性粒细胞综合征累及心脏的超声心动图诊断
姚 静,许 迪(南京医科大学第一附属医院超声医学科,江苏 南京 210029)
特发性高嗜酸性粒细胞综合征累及心脏的超声心动图诊断
姚 静,许 迪
(南京医科大学第一附属医院超声医学科,江苏 南京 210029)
特发性高嗜酸性粒细胞增多综合征(idiopathic hypereosinophilicsyndrome,IHES)是指无明确致病因素的血液和/或细胞中嗜酸性粒细胞持续性增多,并伴有脏器损害的一种疾病。IHES累及心脏可引起左心室收缩功能和(或)舒张功能降低、心内血栓、心肌炎、心内膜心肌纤维化、限制性心肌病、心律失常、冠状动脉病变等,致死率及致残率高。因相关症状缺乏特异性,临床易漏诊、误诊。超声心动图在IHES心脏受累的临床诊断中具有重要作用。本文就IHES伴心脏受累的病理、临床表现及超声心动图诊断进行阐释。
嗜酸性粒细胞;特发性高嗜酸性粒细胞综合征;超声心动图描记术
特发性高嗜酸性粒细胞增多综合征(idiopathic hypereosinophilic syndrome,IHES)是指无明确致病因素的血液和/或细胞中嗜酸性粒细胞持续性增多,并伴有脏器损害的一种疾病[1]。IHES可累及各器官,其中以心脏、神经系统、皮肤以及呼吸道受累常见[2]。IHES累及心脏时致死率及致残率高。因相关症状缺乏特异性,临床易漏诊、误诊。超声心动图在本病的临床诊断中具有重要作用。本文就IHES伴心脏受累的病理、临床表现及超声心动图诊断进行阐释。
1 嗜酸性粒细胞增多及IHES
正常人外周血中嗜酸性粒细胞计数为(0.05~0.50)×109/L,当外周血嗜酸性粒细胞计数≥1.5×109/L,且持续1个月以上,即为嗜酸性粒细胞增多[3]。根据病因,嗜酸性粒细胞增多可分为家族性和获得性,后者又可分为原发性和继发性。原发性主要包括急性白血病等克隆性疾病和IHES。继发性主要与寄生虫感染、过敏、药物、肿瘤及免疫炎症等疾病相关[1~4]。嗜酸性粒细胞增多临床较少见,但预后较差,该病5年生存率为80%,10~15年生存率为42%[5]。
1968年Hardy与Anderson首次报道IHES[6]。Chusid等1975年提出IHES的具体诊断标准[7]。IHES的诊断标准如下:①嗜酸性粒细胞增多(≥1.5×109/L)持续6个月以上;②无引起嗜酸性粒细胞增多的潜在原因,如寄生虫感染、变态反应等;③嗜酸性粒细胞可浸润器官及引起功能障碍;④无克隆性嗜酸性粒细胞的证据;⑤无免疫表型异常[8]。
2 IHES心脏受累病理及临床表现
2.1 概述 IHES可发生于各年龄段,其中以40~50岁青壮年较多,男女比例为9∶1[2]。嗜酸性粒细胞相关的脏器损害可发生于各个器官,文献报道病例中45%~60%为心脏、神经系统、脾脏或肺受累,而肝脏、眼睛或消化系统受累相对较少见(20%~30%)[9],亦有文献报道IHES患者中心脏受累者高达54%~82%[2]。IHES累及心脏可引起左心室收缩功能和(或)舒张功能降低、心内血栓、心内膜炎症、心肌纤维化、限制性心肌病、心律失常、冠状动脉病变等[10],致死率及致残率高。1936年Wilhelm Löffer于1936年最早描述IHES心脏受累,此后将IHES累及心脏出现心内膜炎称为Löffer心内膜炎。
2.2 病理及分期 正常人体嗜酸性粒细胞一般只存在于胃肠道,IHES患者嗜酸性粒细胞则选择性地在外周血或任何组织内聚积,心脏受累时以嗜酸性粒细胞浸润和介质(如碱性蛋白)释放造成的损害为特征。病理学改变包括急性嗜酸细胞心肌炎、纤维样心肌炎、冠状动脉腔内纤维样脉管炎(可导致管腔痉挛、闭塞)、心内膜受损部位的附壁血栓形成、心室闭塞伴心内膜纤维化增厚和心内膜心肌纤维化[2,11],见图1。
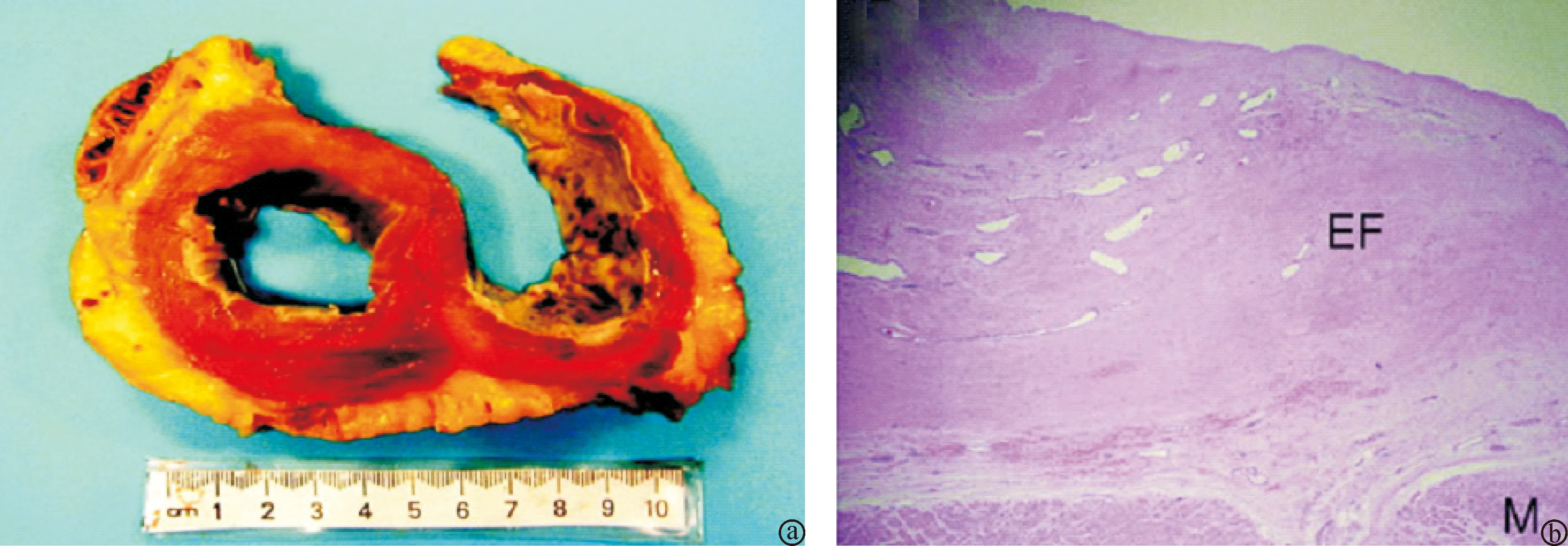
图1 IHES心脏病理改变 a.IHES患者大体解剖心脏横切面显示左室心肌增厚,以及心内膜纤维化,多处表面出血;b.组织学显示明显的心内膜纤维化(EF)伴新生血管形成[14]。
IHES引起的心脏病理损伤可分为三个阶段:急性坏死期、血栓形成期、纤维化期。急性坏死期表现为心肌嗜酸性粒细胞浸润,该期持续时间短(平均5.5周),临床上较难发现。在血栓形成期,附壁血栓可出现于各个心腔。冠状动脉受累患者出现节段性室壁运动障碍时,相应受累节段的内膜面易形成附壁血栓。Von Willebrand因子(vWf),以及胶原和组织因子(TF)释放在血栓形成早期起到重要作用[12]。研究显示嗜酸颗粒蛋白可激活IHES患者的凝血因子Ⅻ、血小板以及单核细胞,从而促进凝血[13]。因此,IHES患者处于高凝状态,这一因素参与了此类患者的心腔血栓形成。在左、右心室腔,心内膜表面(尤其在心尖部心内膜表面)的血流相对较缓慢,而在合并节段性室壁运动障碍时,相应室壁内膜面血流更加缓慢。血流缓慢可激活凝血因子,是血栓形成的重要因素。血栓附着于室壁,并可被纤维组织所替代,且心内膜心肌出现纤维化改变,从而进入第三期,即纤维化期,最终形成限制性心肌病,瓣膜亦可受累,功能障碍加重。
2.3 临床表现 IHES临床表现多样,患者可无症状,亦可能出现严重症状。症状通常非特异性,可表现为疲乏、咳嗽、呼吸困难、消化功能紊乱、搔痒、皮疹、血管神经性水肿,其中以皮疹、咳嗽、呼吸困难最为常见。IHES心脏受累的症状、体征主要是充血性心力衰竭、心内血栓形成/栓塞、心肌缺血、瓣膜受累、冠脉受累、心律失常以及心包炎等引起的相应症状和体征。
3 IHES心脏受累超声心动图诊断
IHES心脏受累早期,超声心动图可无明显异常,或可由于心肌炎症、水肿而出现心肌增厚,随着病程进展,心脏受累加重,超声心动图可发现各种心脏受累征象。
3.1 心腔内血栓形成 IHES心腔内血栓可见于左心室和(或)右心室,多发于心尖部(图2),并可导致受累心腔心尖闭塞,血栓发生纤维化、机化后可与心内膜粘连,而易被误诊为肥厚型心肌病(HCM)、心肌致密化不全(NVM)。IHES患者心尖部心肌搏动正常(除非合并冠脉内血栓形成而出现累及心尖部的心肌梗死),但由于心尖部血栓固定,超声检查时易将其误认为心尖部节段性室壁运动障碍。心腔声学造影可清晰显示心尖部(图3),有助于IHES心脏受累与上述疾病的鉴别。根据病理研究及病案报道,血栓形成为IHES心脏受累的较早期改变,而在此时若能及时、正确诊断,并采取合理的治疗可延缓疾病进展,并使血栓消退[15]。
3.2 Löffler心内膜炎及心肌纤维化 嗜酸性粒细胞浸润心脏组织,脱颗粒释放碱性蛋白和阳离子蛋白引起组织损伤,可引发急性心包炎、心肌炎或心内膜炎,即上文所述的坏死期。进入纤维化期时则可表现受累部位心内膜心肌纤维化,心内膜纤维化超声心动图诊断及评估标准见表1,心内膜纤维化定义为达到2项主要诊断标准,或达到1项主要标准+2项次要标准。总评份小于8分提示轻度心内膜纤维化,8~15分为中度,大于15分为重度。典型的IHES伴发心内膜纤维化时,超声心动图可表现为心内膜回声增强,增厚>2 mm。此外,瓣膜纤维化可影响瓣膜功能,出现瓣膜僵硬、明显反流(图4),极少数情况下,房室瓣活动受限还可产生狭窄,超声心动图可用于瓣膜形态及活动度的显示,以及瓣膜反流和(或)狭窄的定量/半定量分析;心脏传导系统纤维化则可出现各种心律失常。

图2 IHES患者超声心动图影像表现 a:治疗前见左室心尖部血栓;b:治疗6个月后左室心尖部血栓缩小;c:治疗2年后左室心尖部血栓消失[11]

图3 左室声学造影显示左室心尖部血栓充填 a:心尖四腔图;b:心尖短轴图(箭头)[11]

表1 心内膜纤维化超声心动图诊断及评估标准[16]
a 根据房室瓣返流严重性进行评分;b指M型超声显示的运动模式,在心内膜纤维化时由于左室心尖闭塞或限制性运动模式伴二尖瓣返流
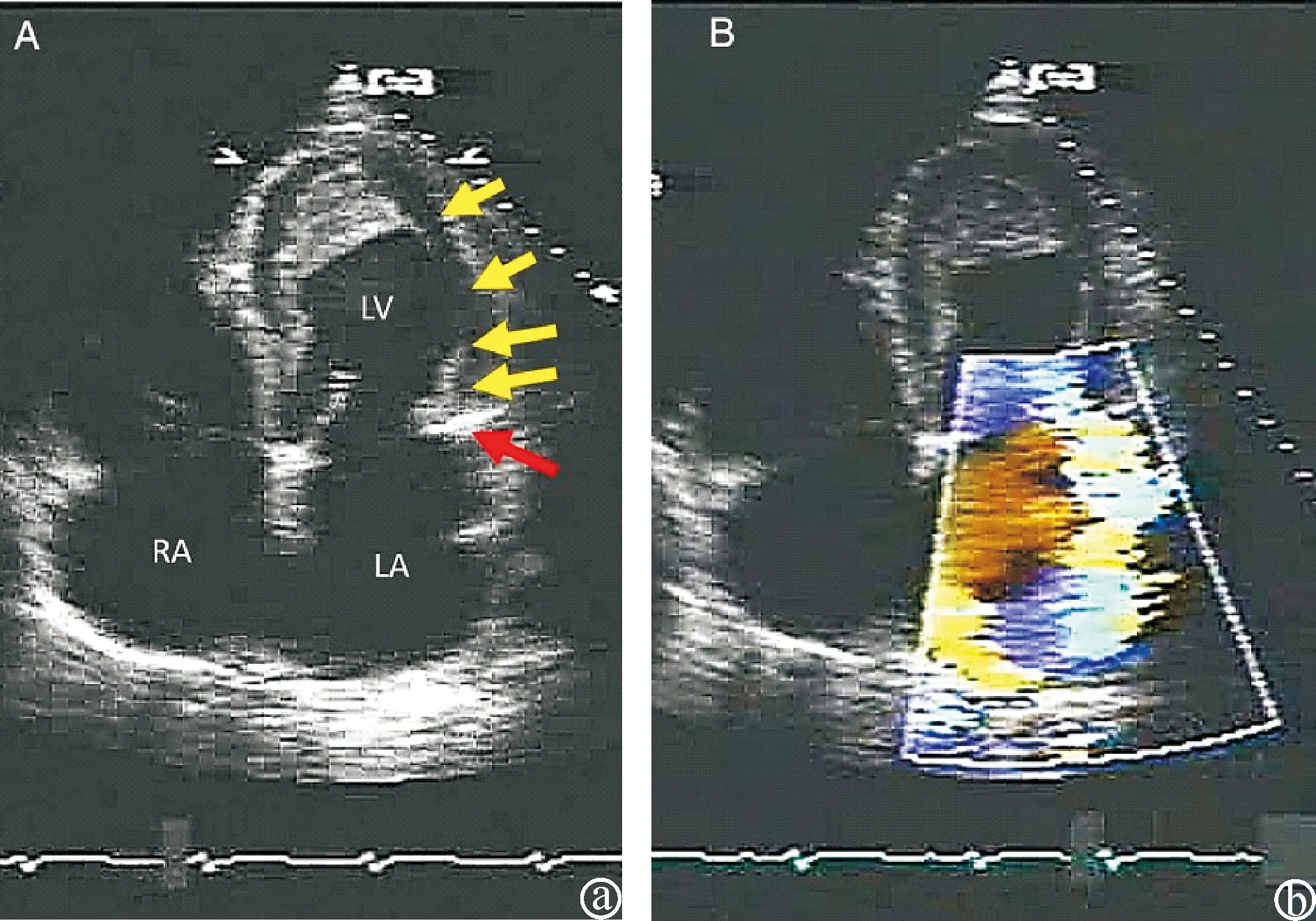
图4 IHES体发心内膜纤维化超声影像改变a.心尖四腔切面显示左室侧壁(黄色箭头)心内膜心纤维化,并累及二尖瓣后叶,从而出现重度偏心性二尖瓣返流;b.心尖部血栓形成[11]
3.3 冠脉病变导致节段性室壁运动障碍 部分IHES患者心脏受累主要表现为冠状动脉病变,临床可以心绞痛或心肌梗死为首发症状。有尸检报告,约60%的IHES患者合并冠状动脉炎症,考虑与嗜酸性粒细胞炎性浸润导致冠状动脉内皮细胞受损后血栓形成有关[17]。超声心动图可表现为节段性室壁运动障碍,根据病变节段可以大致判断受累冠脉。
3.4 舒张功能障碍 IHES患者出现心内膜心肌纤维化、限制性心肌病时,二尖瓣血流频谱可以表现为限制性充盈模式(图5)。
3.5 超声心动图的监测及随访 IHES患者若超声心动图检查无明显异常征象,建议3~6个月复查。大部分患者不出现心内膜纤维化的征象,但约1/3患者可出现左室及右室心内膜纤维化;约30%患者出现心包积液。约50%患者多次随访,超声心动图无明显异常,此类患者则预后较好,发生栓塞及心力衰竭的可能性较小

图5 IHES出现限制性心肌病超声心动图血流频谱表现 a:二尖瓣口舒张早期峰值流速(E峰)为0.79m/s;b:二尖瓣环舒张早期运动速度峰值为0.05m/s
3.6 IHES心脏受累病例
病例1:男,55岁,因“反复胸闷气短伴心前区疼痛一年余”于2011年10月21日入院。患者于入院前一年反复于劳累后出现胸闷气短,伴心前区疼痛,为刺痛,持续约4~5分钟自行缓解,半年前出现皮肤瘙痒,感全身肌肉酸疼,头晕乏力。3年前有颈静脉血栓病史,否认高血压、糖尿病史。体格检查:T 36.2 ℃ P 56次/分 R 20次/分Bp 94/58 mmHg,神志清。全身皮肤粘膜无黄染,无出血点及瘀斑,全身浅表淋巴结未触及肿大。双肺呼吸音清,未闻及干湿性罗音。心率56次/分,律齐,心尖部可闻及3/6级收缩期杂音。双下肢轻度水肿。入院后查血常规示:WBC 13.7×109/L,EO 5.85×109/L,LY% 16.20,NE% 36.60%。外周血涂片示:白细胞总数增高,分类分叶核比例大致正常、淋巴细胞比例减低,嗜酸性粒细胞占36%,成熟红细胞大致正常。骨髓涂片检查结果示:①HES;②建议FIP1LI-PDGFRa融合基因检查。超声心动图检查可见左房左室右房增大(左房内径45 mm,左室舒张末期内径69 mm,左室收缩末期内径44 mm,右房内径43 mm,右室内径38 mm),LVEF 64.5%,左室心尖部局部增厚(考虑血栓形成并与心内膜面融合所致)(图6)伴中-重度二尖瓣反流,中度三尖瓣反流。
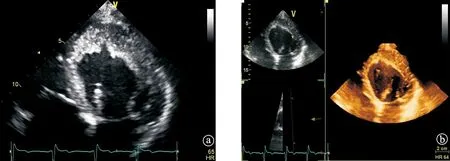
图6 IHES合并左室心肌局部增厚超声心动图影像改变 心尖四腔观显示左室心尖部局部增厚(考虑血栓形成并与心内膜面融合所致) a:二维;b:实时三维
病例2:男,32岁,因“突发胸痛半小时”于2015年2月15日入院。患者于半小时前突发胸痛,疼痛较剧烈,向左肩放射。5年因“急性心肌梗死”行急诊冠脉造影+支架植入术。嗜酸性粒细胞增高病史25年,未规则诊治。血常规示:WBC 20.6×109/L,EO 8.90×109/L,NE% 43.20%。心电图检查示:窦性心律,Ⅱ、Ⅲ、aVF导联ST段抬高。超声心动图检查示左房增大(内径44 mm),左室内径正常(舒张末期内径50 mm),左室心尖部探及一枚约36 mm×12 mm稍低回声团块,与心内膜境界不清,内侧缘回声增强(图7),左室下壁及后室间隔中上段搏动减弱,LVEF60%。患者入院后急诊行冠状动脉造影,显示左主干正常,左前降支内径正常,血流缓慢,未见明显狭窄,左回旋支内径正常,血流缓慢,原支架处未见明显狭窄,右主干自近段起完全闭塞,可见血栓影,抽出血栓,复查造影血流灌注良好。
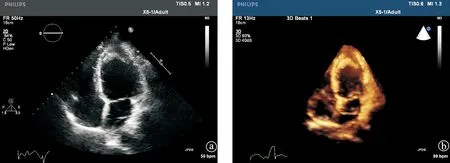
图7 IHES合并血栓超声心动图影像改变 超声心动图心尖四腔观显示左室心尖部探及一枚约36mm×12 mm稍低回声团块,与心内膜境界不清,内侧缘回声增强 a:二维;b:实时三维
4 小结
IHES伴发心脏受累时病理学改变包括急性嗜酸细胞心肌炎、纤维样心肌炎、冠状动脉腔内纤维样脉管炎(可导致管腔痉挛、闭塞)、心内膜受损部位的附壁血栓形成、心室腔闭塞伴心内膜纤维化增厚和心内膜心肌纤维化,从而引起相应的临床症状,预后差。临床表现多样,缺乏特异性,超声心动图可显示心腔内血栓、心尖部闭塞、心内膜心肌纤维化,且可定量评估心室收缩和(或)舒张功能、瓣膜反流程度,因此在本病的临床诊断及随访中具有重要作用。
[1] Tefferi A. Blood eosinophilia: a new paradigm in disease classification,diagnosis,and treatment [J]. Mayo ClicProc,2005,80(1):75-83.
[2] Kleinfeldt T,Nienaber CA,Kische SC. Cardiac manifestation of the hypereosinophilic syndrome: new insights[J]. Clin Res Cardiol,2010,99(7):419-427.
[3] Valent P,Klion AD,Horny HP,et al. Contemporary consensus proposal on criteria and classification of eosinophilic disorders and related syndromes [J]. J Allergy Clin Immunol,2012,130(3):607-612.
[4] Chang HW,Leong KH,Koh DR,et al. Clonality of isolated eosinophils in the hypereosinophilicsyndrome[J]. Blood,1999,93(5):1651-1657.
[5] Lefebvre C,Bletry O,Degoulet P,et al. Prognostic factors of hypereosinophilicsyndrome. Study of 40 cases [J].Ann Med Interne. 1989,140(4):253-257.
[6] Hardy WR,Anderson RE. The hypereosinophilicsyndrome[J].Ann Inern Med,1968,68(6):1220-1229.
[7] Chusid MJ,Dale DC,West BC,et al. The hyperesinophilic syndrome analysis of fourteen cases with review of the literature [J]. Medicine,1975,54(1):1-27.
[8] Tefferi A,Gotlib J,Pardanani A. Hypereosinophilic syndrome and clonal eosinophilia: point-of-care diagnostic algorithm and treatment update[J]. Mayo ClinProc,2010,85(2):158-164.
[9] Roufosse F,Cogan E,Goldman M. Recent advances in pathogenesis and management of hypereosinophilicsyndromes[J]. Allergy,2004,59(7):673-689.
[10] Tsugu T,Nagatomo Y,Yamada Y. The significance of early screening with echocardiography in eosinophilicgranulomatosis with polyangiitis[J]. J Med Ultrason,2016.[Epub ahead of print]
[11]Mankad R,Bonnichsen C,Mankad S. Hypereosinophilic syndrome: cardiac diagnosis and management[J]. Heart,2016,102(2):100-106.
[13]Ruggeri ZM. Platelet interactions with vessel wall components during thrombogenesis [J]. Blood Cells Mol Dis,2006,36(2):145-147.
[13]Rohrbach MS,Wheatley CL,Slifman NR,et al. Activation of platelets by eosinophil granule proteins[J]. J Exp Med,1990,172(4):1271-1274.
[14]Korczyk D,Taylor G,McAlistair H,et al. Heart transplantation in a patient with endomyocardial fibrosis due to hypereosinophilicsyndrome[J]. Transplantation,2007,83(4):514-516.
[15]Pillar N,Halkin A,Aviram G. Hypereosinophilic syndrome with cardiac involvement: early diagnosis by cardiac magnetic resonance imaging[J]. Can J Cardiol,2012,28(4): e11-e13.
[16]Braunwald E. The cardiomyopathies[M]//Zipes D. Braunwald’s heart disease,7th edn.Saunders,Philadelphia
[17]Sato Y,Fukunaga T,Hayashi T,et al. Hypereosinophilic syndrome associated with occlusive coronary thrombosis and right ventricular thrombus [J]. Pathol Int,2008,58(2):138-141.
Cardiac involvement in idiopathic hypereosinophilic syndrome: diagnosis by echocardiography
YAOJing,XUDi
(DepartmentofUltrasound,TheFirstAffiliatedHospitalofNanjingMedicalUniversity,Nanjing210029,China)
XUDi
Idiopathic hypereosinophilic syndrome (IHES) is a disease with persistently elevated eosinophil count in peripheral blood or tissues accompanied by organ damage. The disease had no identifiable cause. Cardiac involvement is a major cause of morbidity and mortality. It may present as left ventricular systolic and/or diastolic dysfunction, intra-cardiac thrombus, eosinophilic myocarditis, endomyocardial fibrosis, restrictive cardiomyopathy and arrhythmia as well as coronary artery disease. The clinic features are rather diverse and nonspecific. Echocardiography plays an important role in diagnosis of cardiac involvement in IHES. The pathogenesis, clinic manifestation and echocardiographic diagnosis of cardiac involvement in IHES were discussed in this review.
Eosinophilic cell; Idiopathic hypereosinophilic syndrome; Echocardiograhpy
许 迪,男,主任医师,教授,博士生导师。中华医学会超声分会常务委员,中国医师协会超声分会常务委员,中国医师协会心血管内科医师分会超声心动图专业委员会副主任委员,中国医师协会超声医师分会超声心动图专业委员会副主任委员,海峡两岸医药卫生交流协会超声医学专家委员会副主任委员,江苏省医学会超声医学专科分会前任主任委员,江苏省医师协会超声分会前任主任委员,江苏省声学学会副理事长,江苏省声学学会医学超声学专业委员会主任委员,江苏省超声医学工程学会副理事长。研究方向:超声心动图在心血管疾病中的基础和临床研究。
R540.4+5
A
1672-6170(2016)05-0019-05
2016-07-20)

