千金止带丸中染色剂金胺O的检测方法研究
赵梦杰,魏伯平,孙韬
·炮制制剂·
千金止带丸中染色剂金胺O的检测方法研究
赵梦杰,魏伯平,孙韬
目的:建立千金止带丸中染色剂金胺O的检测方法。方法:采用HPLC-PDA法对千金止带丸中金胺O进行筛查,并采用HPLC- Q-TOF/MS对阳性样品进行确证。结果:对来自7家企业的71批次样品进行筛查和确认发现:有2家企业的11批次样品中检出金胺O;金胺O进样在0.082~82.08 μg.mL-1范围内有良好的线性关系。结论:本方法准确可靠,可作为千金止带丸中金胺O的检测方法。
千金止带丸;金胺O;液相色谱法;液相色谱质谱联用法
千金止带丸由党参、白术、当归、白芍、延胡索等17味药材配伍制成,具有健脾补肾、调经止带等功效,用于脾肾两虚所致的月经不调、带下病的治疗[1]。本方来源于孙思邈的《千金方》,现收载于《中华人民共和国药典》2015年版一部。其处方中有一味原料药延胡索,市场上发现常被非法染料金胺O染色,使得千金止带丸有金胺O残留的风险[2,3]。金胺O属于工业染色剂,可刺激皮肤黏膜,引起结膜炎、皮炎和上呼吸道刺激症状,人接触或者吸入金胺O会引起中毒。且金胺O较难以自然降解,体内残留物具有致癌、致突变、致畸等毒性,我国在2008年发布的《食品中可能违法添加的非食用物质和易滥用的食品添加剂品种名单(第一批)》中将其列为非食用物质[4-8]。为保证用药安全,有必要对千金止带丸中金胺O建立检测方法。本文采用HPLC-PDA对千金止带丸中的染色剂金胺O进行筛查,并采用液相色谱-质谱联用(HPLC-Q-TOF/MS)法对阳性结果进行确认。结果:来自7家企业的71批次样品进行筛查和确认发现:有2家企业的11批次样品中检出金胺O;建立了千金止带丸中的染色剂金胺O的检测方法,为打击千金止带丸原料中的非法染色行为提供了技术手段。
1 仪器与试药
高效液相色谱仪(美国Waters 2695),二级管阵列检测器(美国Waters PDA 2996);液相色谱联用仪(美国Agilent 1290 ,美国Agilent 6540 Q-TOF/ MS);BP211D型电子天平(德国Sartorius公司);腈、乙酸铵为色谱纯,水为超纯水,其余试剂均为分析纯。金胺O(中国药品生物制品检定所,批号111770-200701);千金止带丸样品来源于全国7个生产企业的71批次样品。
2 方法与结果
2.1 HPLC-PDA筛查
2.1.1 供试品溶液制备 本品,研细,取约2.0 g,精密称定,置锥形瓶中,加60%甲醇20 mL,称定重量,超声处理20 min,取出,放冷,再称定重量,用60%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.1.2 对照品溶液制备 取金胺O对照品适量,加60%甲醇制成每1 mL含2 µg的溶液。
2.1.3 色谱条件与系统适用性试验 采用Waters Xbridge C18色谱柱(4.6 mm×250 mm,5 µm);流动相:乙腈-0.01 mol/L乙酸铵溶液(40:60);流速:1 mL.min-1;柱温:35 ℃;检测波长为438 nm。理论塔板数按金胺O色谱峰计算,应不得低于3000。取对照品溶液和供试品溶液各5 µL,注入液相色谱仪,记录色谱图。结果见图1。

图1 金胺O对照品(A)、阳性供试品(B)的HPLC图
2.1.4 专属性试验
2.1.4.1 HPLC-PDA法 采用二极管阵列检测器比较相应色谱峰在300~650 nm波长范围的紫外-可见吸收光谱,千金止带丸阳性样品与金胺O对照的紫外-可见光谱基本一致。结果见图2。

图2 金胺O对照品(A)、阳性供试品(B)的PDA吸收光谱图
2.1.4.2 HPLC- Q-TOF/MS法 离子源:ESI正离子模式;毛细管电压:4500V;干燥气流速:9 L/min ;干燥气温度:350℃;扫描范围:100~500m/z ;起始加速电压:100V (一级);100V (二级) ;碰撞电压:10~30V; 采样锥电压:60V;其他色谱条件同上。准分子离子与碎片的质谱图见图3。

图3 金胺O对照品(A)、阳性供试品(B)的准分子离子(Ⅰ)与碎片(Ⅱ)的质谱图
2.1.5 筛查结果 共筛查7家企业的71批千金止带丸样品,其中2家企业的11批样品色谱中检出与金胺O对照品色谱保留时间相同的色谱峰,该峰在300~650 nm波长范围的紫外-可见吸收光谱与对照品基本一致,见表1。
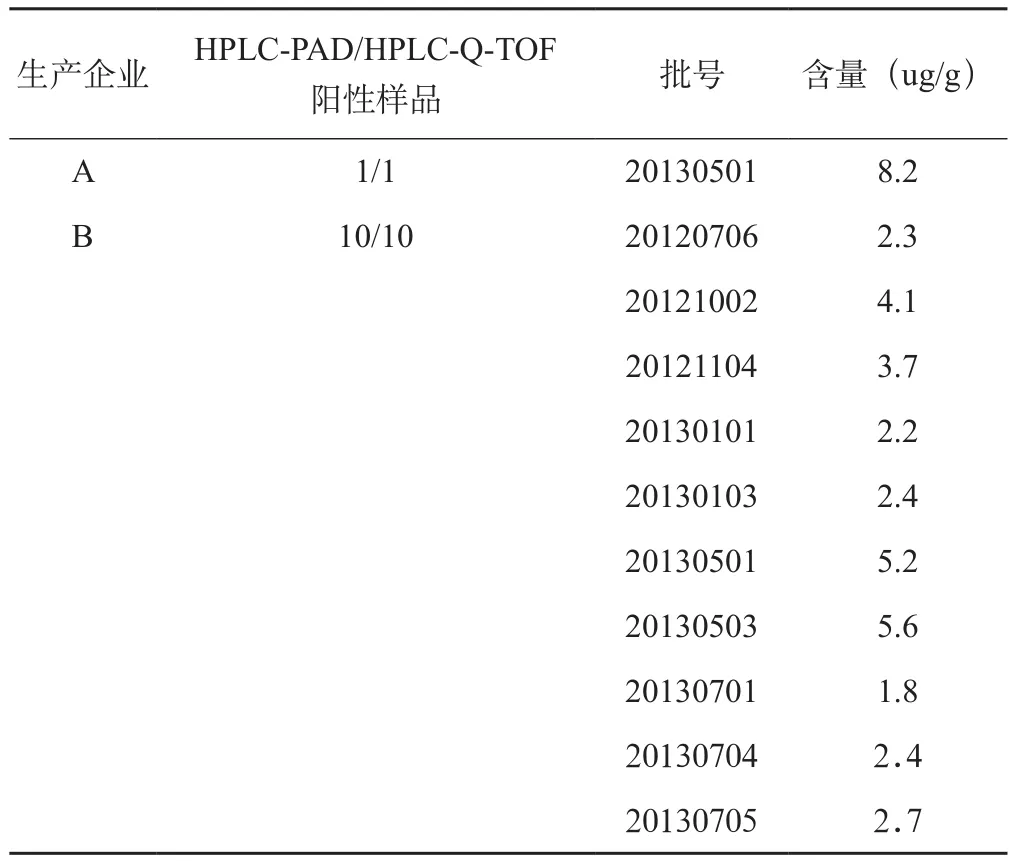
表1 千金止带丸样品筛查结果
2.1.6 阳性样品确认 2家企业的11批千金止带丸样品采用HPLC-Q-TOF/MS进行确认,在与金胺O对照品色谱保留时间相同的位置出现色谱峰,且与对照的准分子离子和碎片离子质谱图基本一致。
2.2 HPLC含量测定
供试品溶液、对照品溶液的制备及色谱条件同上“2.1”项下各项。
2.2.1 线性关系考察 取金胺O对照品溶液适量, 加60%甲醇依次稀释为每1mL含金胺O 0.08208、0.4104、1.642、8.208、41.04、82.08 μg.mL-1的标准溶液, 分别取5µL,注入液相色谱仪分析, 以对照品峰面积Y对进样量X(ng)进行线性回归计算,结果:回归方程为Y=9666X-9804, r=0.9995 ,表明金胺O在进样0.082~82.08μg.mL-1的浓度范围内线性关系良好。
2.2.2 精密度试验 精密吸取上述浓度为1.642 μg.mL-1的对照品溶液5 µL,连续进样6针,分别记录峰面积,结果金胺O的RSD为1.1%,表明进样精密度良好。
2.2.3 重复性试验 取千金止带丸,制备供试品溶液各6份,分别注入液相色谱仪,测定并计算,结果金胺O含量平均值为2.4 μg.g-1,RSD为2.1%,表明方法重复性良好。
2.2.4 稳定性试验 取“2.2.3”项下的同一千金止带丸供试品溶液,室温下放置,精密吸取5 µL,分别在0、2、4、8、16、24h注入液相色谱仪。金胺O色谱峰面积的RSD为1.5%,说明供试品溶液在24h内稳定性良好。
2.2.5 加样回收试验 精密称取未检出金胺O的千金止带丸样品2 g,共称定6份,置具塞锥形瓶中,加入41.04 μg.mL-1的金胺O标准溶液0.1 mL,挥干溶剂后,同“2.1.1”项下制备供试品溶液并测定,计算回收率,结果金胺O平均回收率为102.04%,RSD为2.88%,表明该方法的准确度良好,见表2。
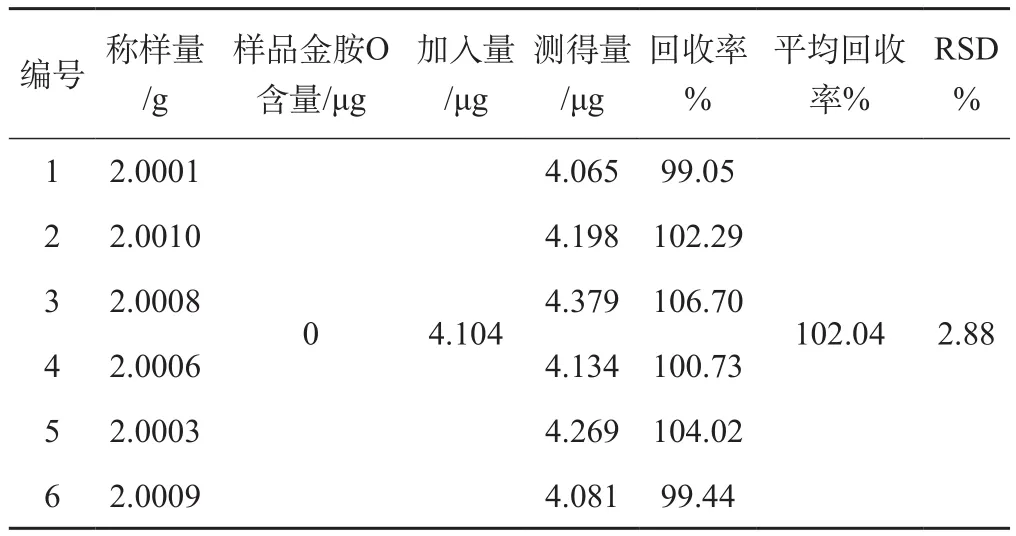
表2 加样回收试验结果
2.2.6 检出限和定量限 取“2.1”项下的金胺O对照品溶液,用60%甲醇进行逐步稀释,进样5µL,在选定的色谱条件下, 按信噪比的3倍值和10倍值计算, 测得金胺O的检出限0.02 μg.mL-1,定量限为0.06 μg.mL-1。
2.2.7 样品测定 取千金止带丸阳性样品,照“2.1.1”项下制备供试品溶液并测定,用外标法计算含量,测定结果见表1。
3 讨论
3.1 金胺O裂解碎片分析 碎片离子是二级质谱的重要鉴别点,金胺O的准分子离子m/z268击碎后,一般会产生m/z252、m/z 147,见图4。
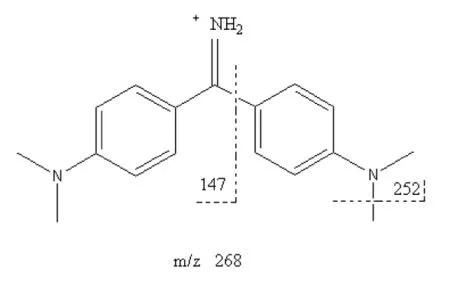
图4 金胺O裂解碎片离子
3.2 流动相系统的选择 有文献[8][9]采用乙腈-0.025moL.L-1磷酸盐缓冲液(含0.2%的三乙胺,用磷酸调节pH到3.0)(30:70)分离测定金胺O, 本文采用了更为简单流动相乙腈-0.01moL.L-1乙酸铵溶液(40:60),也取得了满意的分离效果,且可以直接适用于液质联用仪,更为方便。
3.3 本文建立的千金止带丸中金胺O的检测方法,准确迅速,可以有效打击在千金止带丸原料中添加金胺O的违法行为,从结果看,有2家企业的11批次的样品检出金胺O染色剂,表明千金止带丸有被非食用化工染色剂污染的风险,提示企业应定期对影响原料质量的风险因素进行监测分析,监管部门也应定期开展监督检查,防范非食用化工染色剂污染中成药制剂。
[1] 国家药典委员会.中国药典2015年版[S].一部.北京:中国医药科技出版社,2015:509.
[2] 肖聪,饶伟文,钟名诚.染色延胡索中金胺O的检测方法研究[J].中国药师,2010,13(9):1235.
[3] 肖凌,侯俊杰,聂晶,等.元胡止痛系列制剂中金胺O的检测[J].药物分析杂志, 2012,32(11):2008.
[4] 余新启,何轶,鲁静,等.金胺O染色物在中成药中的检测方法研究[J].药物分析杂志,2014, 34 (1):130.
[5] 杨新玮.罗钰言,肖刚,等.化工产品手册-染料[M].第四版.北京:化学工业出版社,2005:219.
[6] 卢士英,邹明强.食品中常见的非食用色素的危害与检测[J]中国仪器仪表,2009(8):45.
[7] 钟金汤.偶氮染料及其代谢产物的化学结构与毒性关系的回顾与前瞻[J ].环境与职业医学,2004,21(1):58.
[8] 段营辉,陈惠玲,王志林,等.胃康宁胶囊中金胺O染色物的检测方法研究[J ].中国药物评价,2016, 33(2):77.
[9] 赵纯玉,饶伟文,莫连峰.蒲黄中金胺O的HPLC测定[J].药物分析杂志,2007,27(12):1956.
(责任编辑:李芸霞)
Detection of dye auramine O in Qianjinzhidai pill
/ZHAO Meng-jie1, WEI Bo-ping2, SUN Tao2/(1. School of Pharmacy, Chengdu University of Traditional Chinese Medicine; Key Laboratory of Standardization for Chinese Herbal Medicine, Ministry of Education; National Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources, Chengdu 611137, Sichuan; 2. Sichuan Institute for Food and Drug Control, Chengdu, 610097, Sichuan)
Objective:To establish a method for detection of dye auramine O in Qianjinzhidai pills.Method:HPLC-PDA was used as a screening method for auramine O .The positive results were further confirmed by HPLC- Q-TOF/MS.Result:71 batches of qianjinzhidai pills from 7 manufacturer were detected and confirmed. Auramine O was detected from 11 batches of samples in 2 manufacturers. Auramine O had considerable linear relationship in range of 0.082~82.08 μg.mL-1.Conclusion:This method is accurate and reliable, and can be used as the detection method for auramine O in Qianjinzhidai pill.
Qianjinzhidai pill; auramine O; HPLC; HPLC-MS
R 283
A
1674-926X(2016)05-006-03
1. 成都中医药大学药学院 中药材标准化教育部重点实验室 四川省中药资源系统研究与开发利用重点实验室——省部共建国家重点实验室培育基地,四川 成都 611137; 2.四川省食品药品检验检测院,四川 成都 610097
赵梦杰,女,在读硕士,主要从事中药药效物质基础及其安全性评价研究
Tel:18224472725 Email: 846684378@qq.com
魏伯平,男,主管药师,主要从事中药质量控制与安全性研究 Email:weiboping@gmail.com
2016-03-09

