手性固定相AD、AS和OD的拆分性能
李丽群, 范 军*, 张 晶, 陈晓东, 王 泰, 贺建峰, 章伟光,*
(1. 华南师范大学化学与环境学院, 广东 广州 510006; 2. 广州研创生物技术发展有限公司, 广东 广州 510663)
手性固定相AD、AS和OD的拆分性能
李丽群1,范军1*,张晶1,陈晓东2,王泰2,贺建峰1,章伟光1,2*
(1. 华南师范大学化学与环境学院, 广东 广州 510006; 2. 广州研创生物技术发展有限公司, 广东 广州 510663)
摘要:手性固定相-高效液相色谱法在手性药物、手性农药等的分离分析中应用广泛。本文采用3种多糖衍生物的手性固定相(即EnantioPak AD、AS和OD)对20种手性化合物开展手性分离研究,进而探讨样品分子结构、多糖骨架和衍生基团对手性分离的影响。结果表明,除化合物13外,其余化合物在EnantioPak AD上均实现基线分离,分离度多在2.0以上,在正己烷-醇流动相中加入酸碱添加剂可改善和优化酸性或碱性化合物的分离效果;芳香醇(化合物13~16)随着侧链碳数增加在色谱柱上的保留减弱,其分离度呈现增加的趋势;对比8种化合物在3种手性固定相上的分离结果可知,EnantioPak AD表现出更优的分离性能。这为深入研究和了解多糖手性固定相、拓展其手性分离应用提供了参考。
关键词:多糖手性固定相;高效液相色谱;手性识别;分离机理
手性异构体在生物体环境中可能表现截然不同的生物活性、药理和毒性等,因此对天然化合物、手性药物、农药化学品及中间体进行手性分析检测是非常必要的。近几十年,手性固定相-高效液相色谱法成为手性分离分析的重要手段之一[1-4]。
在多糖分子(如直链淀粉和纤维素等)中,葡萄糖单元通过氢键形成螺旋链结构,进而形成高度有序的超分子手性区域,与手性化合物产生手性识别作用;在多糖骨架上引入取代基(如苯氨基甲酸酯等)形成多糖衍生物后,其手性识别能力得到显著地提高;同时,糖单元的结构及衍生基团的性质对多糖手性固定相的分离性能影响明显[5-11]。靳红卫等[12]发现,普萘洛尔对映体在Chiralpak AD、Chiralcel OD和OJ等色谱柱上的分离度分别为8.97、9.24和1.76,而在Chiralpak AS柱上无分离趋势;袁黎明等[13]研究38种手性化合物在Chiralcel OD、Chiralpak AD和IA、(S,S)-Whelk-O1等色谱柱上的分离时发现,Chiralpak AD柱可拆分其中21种(约占55%),而22种化合物在Chiralcel OD柱上实现基线分离。本课题组也相继开发了单脲键、多脲键的环糊精手性固定相[14,15]、脲键型多糖手性固定相[16,17]等,研究了它们对手性金属配合物、氨基酸及衍生物、β-阻断剂等手性药物的拆分性能。
本文则研究了20种手性化合物在EnantioPak AD、OD和AS等3种手性固定相上的分离,探讨糖单元、取代基等对手性分离的影响。3种多糖衍生物的结构示意图见图1。
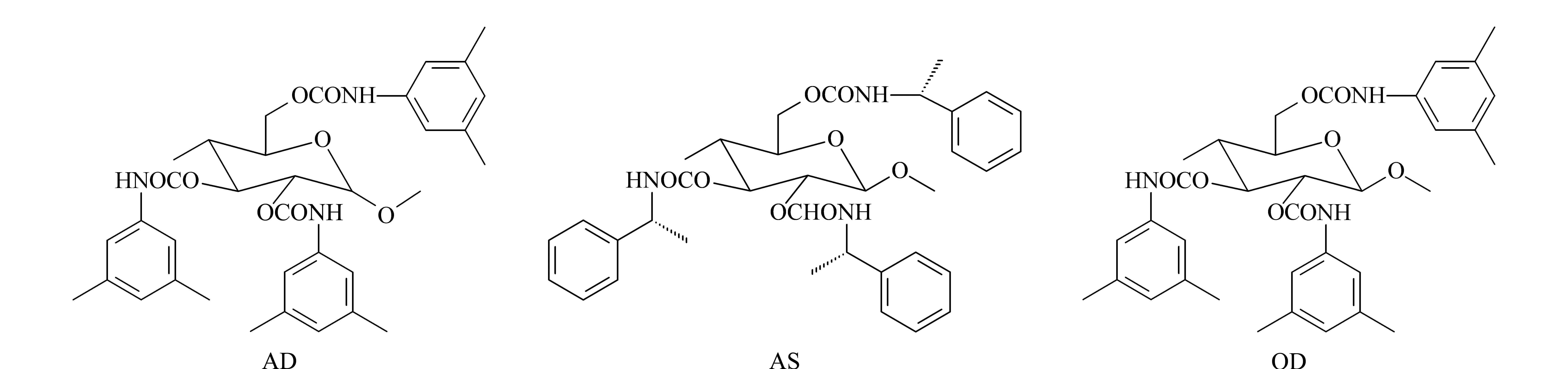
图1 3种多糖衍生物的结构示意图Fig. 1 Molecular structures of the three polysaccharide derivatives AD: amylose tri(3,5-dimethylphenylcarbamate); AS: amylose-tris[(S)-α-phenylethylcarbamate]; OD: cellulose-tris(3,5-dimethyphenylcarbamate).
1实验部分
1.1仪器与试剂
安捷伦1200系列高效液相色谱系统,配有紫外检测器、真空脱气机、四元泵、100 μL定量环的自动进样器、柱温箱和安捷伦化学工作站软件(美国安捷伦)。
正己烷、异丙醇、乙醇(色谱纯,天津科密欧化学试剂有限公司),乙二胺(DEA)、三氟乙酸(TFA)(色谱纯,上海晶纯生化科技股份有限公司); 20种手性化合物(见图2)、EnantioPak AD、OD和AS手性固定相由广州研创生物技术发展有限公司提供,硅胶填料的粒径为5 μm,孔径为100 nm,色谱柱规格为150 mm×4.6 mm。
1.2色谱分离实验
如无特殊说明,手性化合物均用乙醇溶解;流动相使用前经过滤并超声脱气处理;在安捷伦高效液相色谱系统上,25 ℃下以1.0 mL/min的流速进行色谱分离实验。
保留因子k按公式k=(tR-t0)/t0计算,其中tR为化合物的保留时间(min),t0为死时间(min);分离因子(α)按k2/k1计算得到;分离度(Rs)按2 (tR2-tR1)/(w2+w1)计算得到,其中tR2和tR1分别为第二个和第一个洗脱对映异构体的保留时间(min),w2和w1分别为相应异构体色谱峰的半峰宽[14]。
2结果与讨论
2.1EnantioPak AD手性固定相的分离性能
在正相色谱条件下研究了EnantioPak AD手性固定相对化合物1~12的分离情况,流动相条件和分离结果见表1。可以看出,这些化合物在EnantioPak AD柱上都实现了基线分离(Rs>2.0);在流动相的选择方面,化合物1~4没有典型的酸性或碱性官能团,在正己烷-醇流动相中即可实现分离;化合物6~9上带有羧基或羟基官能团,在流动相中添加少量TFA增强其洗脱能力,达到更好的分离效果(如化合物7);化合物10~12中含有氨基,在流动相中同时添加TFA-DEA后得到分离。

图2 20种手性化合物的结构示意图Fig. 2 Molecular structures of the 20 chiral compounds
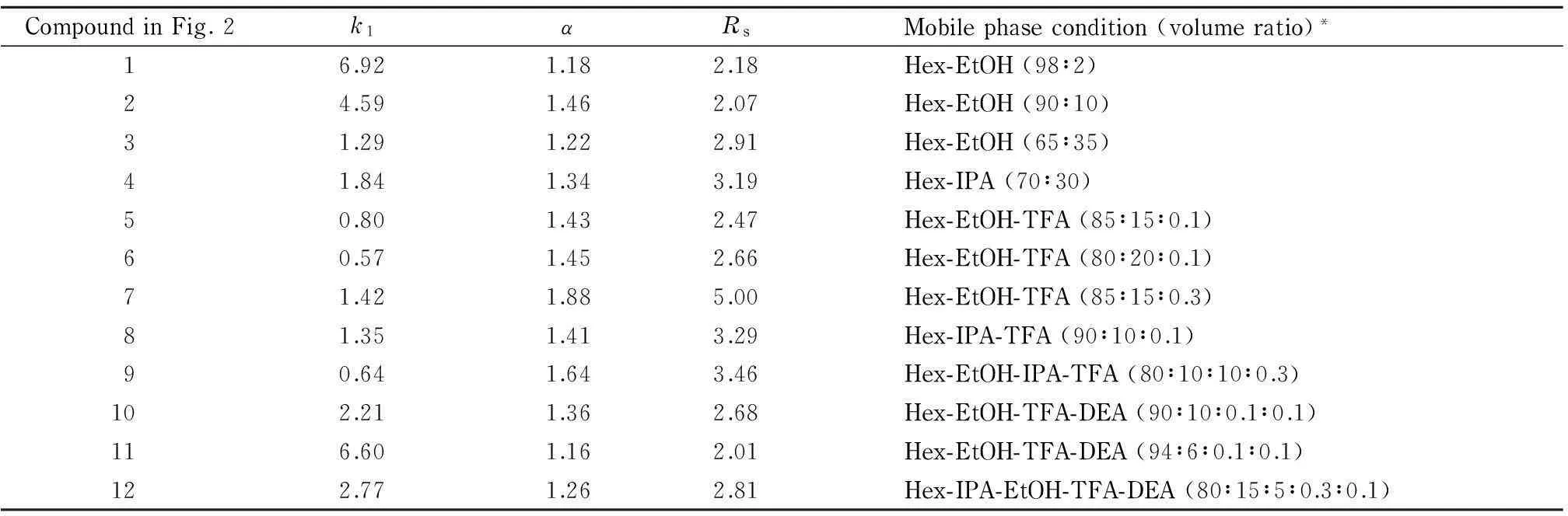
CompoundinFig.2k1αRsMobilephasecondition(volumeratio)*16.921.182.18Hex-EtOH(98∶2)24.591.462.07Hex-EtOH(90∶10)31.291.222.91Hex-EtOH(65∶35)41.841.343.19Hex-IPA(70∶30)50.801.432.47Hex-EtOH-TFA(85∶15∶0.1)60.571.452.66Hex-EtOH-TFA(80∶20∶0.1)71.421.885.00Hex-EtOH-TFA(85∶15∶0.3)81.351.413.29Hex-IPA-TFA(90∶10∶0.1)90.641.643.46Hex-EtOH-IPA-TFA(80∶10∶10∶0.3)102.211.362.68Hex-EtOH-TFA-DEA(90∶10∶0.1∶0.1)116.601.162.01Hex-EtOH-TFA-DEA(94∶6∶0.1∶0.1)122.771.262.81Hex-IPA-EtOH-TFA-DEA(80∶15∶5∶0.3∶0.1)
* Hex: hexane; EtOH: ethanol; IPA: isopropanol; TFA: trifluoroacetic acid; DEA: diethylamine.
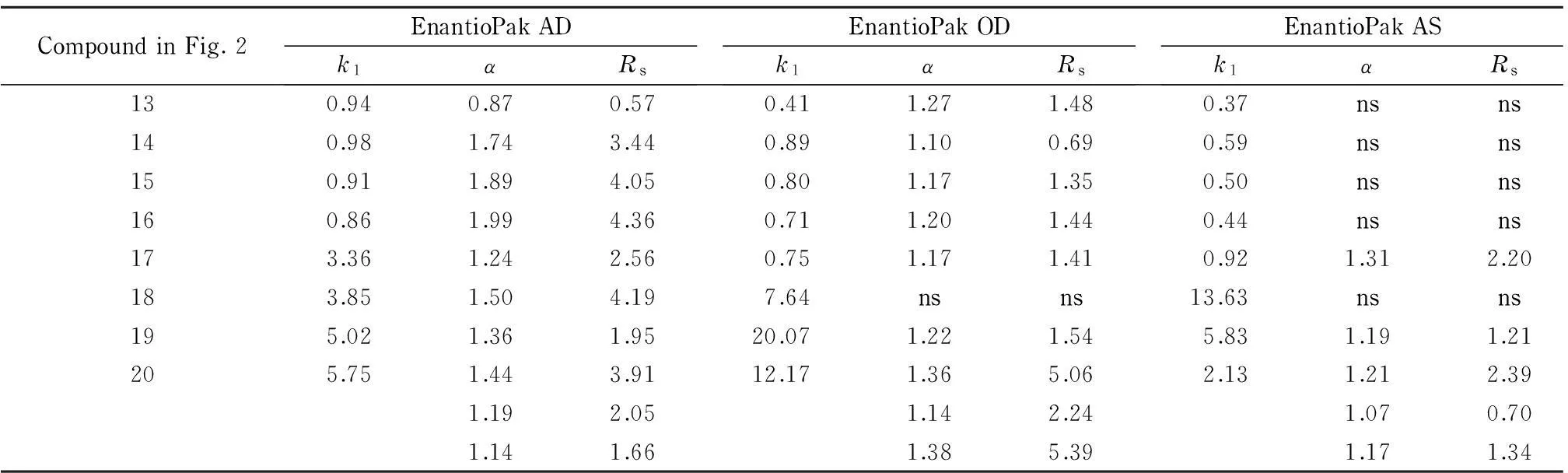
表 2 化合物13~20在3种手性柱上的HPLC分离结果
13-16: Hex-EtOH (95∶5, v/v), detection wavelength 220 nm; 17, 18: Hex-EtOH (90∶10, v/v), detection wavelength 220 nm; 19: Hex (0.1%TFA)-EtOH (80∶20, v/v), detection wavelength 290 nm; 20: Hex (0.1%TFA)-IPA (97∶3, v/v), detection wavelength 220 nm. ns: no separation.
在正相模式下的分离主要通过Dalgliesh的“三点相互作用”理论[18]来解释。手性分子中的羟基、氨基或酯基等官能团可与手性固定相上的苯氨基甲酰基产生相互作用而形成非对映异构体配合物。由于手性异构体空间结构的差异影响两者结合的空间立体效应及非对映体配合物的稳定性,最终实现异构体的手性分离。
2.2芳香醇碳链长度对EnantioPak AD手性固定相分离性能的影响
化合物13~16均为芳香醇,结构相似,侧链长度不同。对它们在EnantioPak AD柱上的分离进行了研究,结果见表2。
结果表明,随着侧链碳链长度的增加,化合物在色谱柱上的保留减弱,分离度和选择因子呈现增加的趋势。如前所述,手性固定相与化合物分子间的手性识别主要通过分子间弱相互作用(如氢键、π-π作用、疏水作用等)实现;同时,手性中心附近的基团产生的立体位阻也会影响手性分离[19]。在化合物13~16中,随着烷基侧链碳数依次增加,空间位阻的增大使得手性分子与手性固定相间的氢键作用减弱;另一方面,手性化合物与流动相间疏水作用增强,加速了样品从手性固定相上洗脱,进而对样品的手性分离产生影响。
2.33种手性固定相的拆分性能比较
2.3.1多糖骨架结构的影响
EnantioPak AD和OD手性固定相具有相同的取代基(即3,5-二甲基苯氨基甲酰基)(见图1),但多糖结构不同,前者为直链淀粉,后者为纤维素。以化合物13~20比较研究其分离性能差异(见表2),化合物17和20的色谱图见图3。
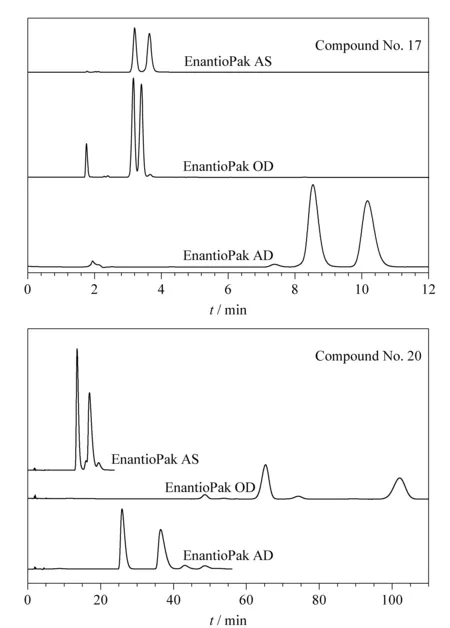
图3 手性化合物17和20的色谱图Fig. 3 HPLC chromatograms of chiral compounds 17 and 20 17: Hex-EtOH (90∶10, v/v), detection wavelength 220 nm; 20: Hex (0.1%TFA)-IPA (97∶3, v/v), detection wavelength 220 nm.
结果表明,除化合物13外,其余化合物在EnantioPak AD柱上均实现基线分离(Rs>1.5);化合物13和20在EnantioPak OD柱的分离优于EnantioPak AD柱,而化合物14~19的分离度均比在EnantioPak AD柱上差,化合物18则无分离趋势。
这些差异可归因于多糖葡萄糖单元的构象和空间结构的不同。本课题组曾对比研究键合型纤维素和直链淀粉手性固定相的分离性能[16]。直链淀粉是由D-葡萄糖单元通过α-1,4-糖苷键形成的链状聚合物,为右手4/3螺旋结构;而纤维素则是由D-葡萄糖单元通过β-1,4-糖苷键链接形成的,为左手3/2螺旋结构;在多糖衍生物中,3,5-二甲苯氨基甲酰基围绕着主链形成一个螺旋沟槽,与手性分子形成氢键、偶极-偶极和π-π堆积等分子间相互作用而实现手性识别。
2.3.2衍生基团的影响
表2亦给出化合物13~20在EnantioPak AS柱上的分离结果。结果表明,化合物17、19和20在EnantioPak AS柱上得到一定的分离,其他未有分离趋势。显然EnantioPak AS对这些化合物的分离能力比EnantioPak AD和OD差。
EnantioPak AD和AS均为直链淀粉衍生物手性固定相,其骨架结构、硅胶基质和结合方式相同,但葡萄糖单元上的取代基不同。在EnantioPak AD中,苯环上甲基的推电子作用使其具有较高的π电子密度,可与手性底物形成强的π-π堆积作用,同时苯氨基甲酰基C=O电子云密度增大,促使固定相与手性化合物(如13~16)中的羟基形成氢键,进而实现手性拆分[15];在EnantioPak AS中,苯环与氨基甲酰基通过烷基连接,空间位阻影响手性固定相与手性分子间的相互作用[20],手性化合物在EnantioPak AS上的保留要弱于EnantioPak AD。
3结论
在正相模式下研究了20种手性化合物在多糖手性固定相EnantioPak AD、AS和OD上的分离,探讨了化合物的结构、多糖骨架和衍生基团等对手性分离的影响。结果表明,除化合物13外,其余化合物在EnantioPak AD上都获得良好的分离;对酸性或碱性化合物,在正己烷-醇流动相中加入三氟乙酸或二乙胺等添加剂可改善分离;比较了8种化合物在3种手性固定相上的分离,EnantioPak AD表现出最优的分离性能。
参考文献:
[1]Chankvetadze B. J Chromatogr A, 2012, 1269: 26
[2]Ye J, Wu J, Liu W P. TrAC-Trends Anal Chem, 2009, 28(10): 1148
[3]Cheng B, Xie Y F, Hu Y M, et al. Chinese Journal of Chromatography, 2015, 33(6): 647
成斌, 谢一凡, 胡优敏, 等. 色谱, 2015, 33(6): 647
[4]Li L, Zhou S S, Jin L X, et al. J Chromatogr B, 2010, 878(17/18): 1264
[5]He X M, Yao Y Y, Ndorbor T, et al. Chinese Journal of Analytical Chemistry, 2013, 41(8): 1188
何小梅, 姚誉阳, Ndorbor T, 等. 分析化学, 2013, 41(8): 1188
[6]Chankvetadze B, Yashima E, Okamoto Y. J Chromatogr A, 1995, 694(1): 101
[7]Lin X J, Gong R J, Li P, et al. Chinese Journal of Chromatography, 2014, 32(8): 880
林小建, 龚如金, 李平, 等. 色谱, 2014, 32(8): 880
[8]Zhang C, Jin L X, Zhou S S, et al. Chirality, 2011, 23(3): 215
[9]Sun X, Wu D, Shao B, et al. Anal Sci, 2009, 25(7): 931
[10]Ikai T, Okamoto Y. Chem Rev, 2009, 109(11): 6077
[12]Zhao J, Zou W, Jin H W, et al. Chinese Journal of Spectroscopy Laboratory, 2011, 28(1): 7
赵静, 邹卫, 靳红卫, 等. 光谱实验室, 2011, 28(1): 7
[13]Zhang M, Xi W H, Yuan L M, et al. Chinese Journal of Analytical Chemistry, 2010, 38(2): 181
张美, 奚文汇, 袁黎明, 等. 分析化学, 2010, 38(2): 181
[14]Lin C, Liu W N, Fan J, et al. J Chromatogr A, 2013, 1283: 68
[15]Lin C, Fan J, Liu W N, et al. J Pharmaceut Biomed Anal, 2014, 98: 221
[16]Tan Y, Fan J, Lin C, et al. J Sep Sci, 2014, 37(5): 488
[17]Tu H S, Fan J, Tan Y, et al. Chinese Journal of Chromatography, 2014, 32(5): 452
涂鸿盛, 范军, 谭艺, 等. 色谱, 2014, 32(5): 452
[18]Dalgliesh C E. J Chem Soc, 1952, 137: 3940
[19]Lin C, Luo W J, Zhang S, et al. J Sep Sci, 2010, 33(11): 1558
[20]Maher H M. J Chromatogr Sep Tech, 2014, 5(4): e123
Enantioseparation behavior of chiral stationary phases AD, AS and OD
LI Liqun1, FAN Jun1*, ZHANG Jing1, CHEN Xiaodong2,WANG Tai2, HE Jianfeng1, ZHANG Weiguang1,2*
(1. School of Chemistry and Environment, South China Normal University, Guangzhou 510006, China;2. Guangzhou Research & Creativity Biotechnology Co. Ltd., Guangzhou 510663, China)
Abstract:Over the past decades, HPLC enantioseparation with chiral stationary phases (CSPs) has been widely applied in chiral analysis and preparation of new pharmaceuticals, pesticides, food, etc. Herein, enantioseparation of 20 chiral compounds have been carried out on three polysaccharide-based CSPs (EnantioPak AD, AS and OD) with normal phases by HPLC, separately. The influences of skeletal structure and the kinds of derivative groups on separation behaviors of these CSPs have been studied in detail. As results indicated, except for compound 13, the other compounds were baseline separated on EnantioPak AD, with most of resolution over 2.0; in addition, better separation for acidic or basic compounds was achieved through adding acidic/basic additives into the mobile phase of hexane-alcohol. For four aromatic alcohols (compounds 13-16), their retention in the EnantioPak AD column showed a weakening tendency with increase of carbon number in side chain group, and the reverse trend of their resolution was observed. Furthermore, EnantioPak AD showed much better separation performance for eight compounds (13-20) than the others. In short, these results have provided some references for further investigation of separation behavior and applications of polysaccharide-based CSPs.
Key words:polysaccharide-based chiral stationary phases; high performance liquid chromatography (HPLC); chiral recognition; separation mechanism
DOI:10.3724/SP.J.1123.2015.10035 [11]Shen J, Okamoto Y. Chem Rev, 2015, 10.1021/acs. chemrev.5b00317
*收稿日期:2015-10-24
基金项目:国家自然科学基金项目(21171059,21571070);科技部中小型企业技术创新基金项目(13C26214404534);广东省科技计划项目(2014A010101145,2012B010900043);广州市科技计划项目(2013J4400027,201508020093).
中图分类号:O658
文献标识码:A
文章编号:1000-8713(2016)01-0108-05
色谱手性分离专刊·研究论文
*通讯联系人:Tel:(020)39310187,E-mail:wgzhang@scnu.edu.cn(章伟光); E-mail:fanj@scnu.edu.cn(范军).
Foundation item: Project of National Natural Science Foundation of China (21171059, 21571070); Innovation Fund for Technology Based Firms, Ministry of Science and Technology, China (13C26214404534); Science and Technology Project of Guangdong Province, China (2014A010101145, 2012B010900043); Guangzhou Science and Technology Project, China (2013J4400027, 201508020093).

