大肠杆菌氮代谢调节蛋白GlnG与固氮施氏假单胞菌氮代谢调节蛋白NtrC的功能互补研究
柯琪陈清华战嵛华陆伟燕永亮
(1.西南科技大学生命科学与工程学院,绵阳 621010;2.中国农业科学院生物技术研究所,北京 100081)
大肠杆菌氮代谢调节蛋白GlnG与固氮施氏假单胞菌氮代谢调节蛋白NtrC的功能互补研究
柯琪1,2陈清华2战嵛华2陆伟2燕永亮2
(1.西南科技大学生命科学与工程学院,绵阳 621010;2.中国农业科学院生物技术研究所,北京 100081)
旨在围绕大肠杆菌DH10B(Escherichia coli DH10B)中氮代谢调节蛋白GlnG与施氏假单胞菌A1501(Pseudomonas stutzeri A1501)中氮代谢调节蛋白NtrC在一般氮代谢调控网络中是否存在功能互补展开研究。利用DH10B菌的glnG基因回补A1501菌的ntrC突变株,以及A1501菌的ntrC基因回补DH10B菌的glnG突变株,对所获得的功能互补株分别展开生理生化表型测定。结果表明,在以硝酸钾或尿素为唯一氮源的培养条件下,DH10B glnG基因可以回补A1501 ntrC突变株的氮源利用能力,并且部分恢复ntrC突变株的固氮酶活性(约为野生型A1501固氮酶活性的45%);与DH10B glnG突变株相比,A1501菌的ntrC基因回补了DH10B glnG突变株以精氨酸为唯一氮源的生长能力。以上结果说明DH10B菌的GlnG蛋白与A1501菌的NtrC蛋白不仅在进化关系上紧密联系而且在所测试的氮代谢途径中存在功能互补。
施氏假单胞菌A1501 NtrC;大肠杆菌DH10B GlnG;一般氮代谢;功能互补
生物固氮是微生物在某些特定的条件下将空气中的氮气还原为铵的过程[1],是自然生态系统中氮的主要来源,在氮素的生态平衡和农、林生产业中发挥重要作用,而对于生物固氮调控过程的研究是目前微生物研究领域的热点之一。
氮源是自然环境中影响生物固氮效率的一个重要的限制性因素,固氮微生物能否高效利用环境中的氮源,使生物固氮仅发生在有利和必要的条件下是关键性问题。目前已有研究表明在大肠杆菌(Escherichia coli)、鼠伤寒沙门氏菌(Salmonella typhimurium)、克雷伯氏菌(Klebsiella)和肺炎克氏杆菌(Klebsiella pneumoniae)中氮素吸收和氮源代谢由NtrBC(Nitrogen regulation,ntr)双组份系统全局调控[2]。NtrBC双组份系统(亦称GlnLG双组份系统)在革兰氏阴性菌中广泛存在,由组氨酸激酶NtrB和转录调控因子NtrC构成。在细菌所处生长环境缺乏氮源时,NtrB能够自身磷酸化,并且发挥激酶作用将NtrC磷酸化,磷酸化以后的NtrC转录激活氮源转运吸收和代谢相关基因的表达[3]。其中NtrC 蛋白(在固氮施氏假单胞菌A1501中由ntrC基因编码)是固氮施氏假单胞菌A1501中固氮岛基因表达激活的关键调节蛋白。在大肠杆菌中,GlnG蛋白(在DH10B菌中由glnG基因编码)是氮限制条件下氮源选择性同化途径的全局激活子[4]。研究表明假单胞菌中的NtrC蛋白是激活一系列编码参与氮源吸收和利用的蛋白基因表达所必需的因素[5],包括自身操纵子glnA-ntrBC及atzDEF操纵子。同时NtrC在施氏假单胞菌中也参与固氮调控过程[6],也有许多研究表明肠杆菌中的氮调节系统与假单胞菌很多相同之处[6,7]。大肠杆菌的代谢调控网络目前研究较为透彻,具有可进行厌氧生长、易于培养以及遗传操作方便等显著优点。而作为第一株完成测序的联合固氮菌,施氏假单胞菌A1501含有一全长49 kb的固氮岛,含有59个编码基因,其中传统的20多个固氮相关基因是其实现生物固氮的遗传基础[8]。本实验室已经成功将A1501的固氮岛基因转入大肠杆菌DH10B获得了具有固氮酶活性的重组大肠杆菌,使得联合固氮菌摆脱了遗传背景不清楚的局限。然而重组大肠杆菌的固氮酶活性只有野生型A1501的1/10,因此,研究固氮条件下大肠杆菌内的氮代谢相关基因与施氏假单胞菌固氮岛内相关基因的表达调控是否具有相关性,是提高重组大肠杆菌固氮能力的关键。
本研究通过构建DH10B glnG回补A1501 ntrC突变株的功能互补株和A1501 ntrC回补DH10B glnG突变株的功能互补株,对突变株和功能互补株在唯一氮源条件下生长能力进行分析,旨在为揭示DH10B GlnG与A1501 NtrC两蛋白在细菌一般氮代谢过程中是否具有调控功能的相关性奠定理论基础,也为进一步提高重组菌固氮酶活性提供理论依据。
1 材料与方法

表1 实验所用菌株
1.1 材料
1.1.1 本研究中所涉及的细菌菌株主要是固氮施氏假单胞菌野生型及相关突变株和互补株(表1)。
1.1.2 培养基及生化试剂 LB培养基(固体培养基含1.5%琼脂粉):0.5%酵母提取物,1.0%胰蛋白胨,1.0%氯化钠,pH7.0。改良K培养基(固体培养 基 含1.5%琼 脂 粉 ):0.04% KH2PO4,0.01%K2HPO4,0.01% NaCl,0.02% MgSO4·7H2O,0.001% MnSO4·H2O,0.001% Fe2(SO4)3·H2O,0.001% Na2MoO4·H2O,0.6% C3H5NaO3,0.04%(NH4)2SO4,pH6.8 。M9培养基(固体培养基含1.5%琼脂粉):20% 5×M9盐溶液,0.2% 1 mol/L MgSO4,20%葡萄糖,0.01% 1 mol/L CaCl2。5×M9盐溶液:6.4% Na2HPO4,1.5% KH2PO4,0.25% NaCl,0.5% NH4Cl。1.1.3 引物合成和测序 由北京擎科生物技术有限公司及六合华大基因有限公司完成。
1.2 方法
1.2.1 三亲结合实验 活化供体菌(大肠杆菌JM109)、受体菌(A1501)以及含有助质粒pRK2013的大肠杆菌,转接至相应液体培养基中。过夜培养后接至新鲜的液体培养基中,30℃,220 r/min荡培养至OD600=0.6-0.8。吸取1.5 mL液离心收集菌体沉淀。用0.85%的生理盐水洗涤菌体2次,并将3管相同的菌液合为一管,离心收集菌体沉淀后加入100 μL 0.85%的生理盐水将3种菌液稀释成同一浓度,按供体菌∶受体菌∶助质粒为2∶2∶1的比例将3种混合均匀离心收集菌体沉淀。用50-100 μL 0.85%的生理盐水重悬菌体并点于LB(无任何抗性)平板中央,风干后放于30℃培养箱。培养24-48 h后将所有菌苔刮下,用0.85%的生理盐水倍比稀释各取100 μL涂在加相应抗生素的K培养基平板上,30℃培养至单菌落长到合适大小。
1.2.2 以10 mmol/L硝酸钾和10 mmol/L尿素为唯一氮源条件下的生长曲线测定 活化菌株A1501、ΔntrC、ntrC-comp、glnG-comp,接种至新鲜的K培养基中,30℃过夜培养,离心收集菌体沉淀。用0.85%的生理盐水洗涤菌体2次。用以10 mmol/L硝酸钾和10 mmol/L尿素为唯一氮源的液体培养基重悬菌体,并调节菌液初始OD600为1.0。将2 mL菌液接种于18 mL以10 mmol/L硝酸钾和10 mmol/L尿素为唯一氮源的液体培养基,30℃,220 r/min震荡培养,每个体系3个重复。分别于2、4、6、8、10、12、14、16、18、20、22和24 h取样,测定各菌液的OD600。
1.2.3 施氏假单胞菌固氮酶活测定 活化菌株A1501、ΔntrC、ntrC-comp、glnG-comp,接种至新鲜无氮培养基中,30℃过夜培养,离心收集菌体沉淀。用0.85%的生理盐水洗涤菌体2次。用液体无氮培养基K重悬菌体,并调节菌液初始OD600为1.0。将1 mL菌液接种于9 mL无氮K培养基中,封口后每瓶充5 min氩气并注入0.5%的氧气和10%的乙炔,30℃,220 r/min震荡培养,每个体系3个重复。分别于4、6、8、10 h取样250 μL气体进行气谱检测,并记录乙烯的峰面积。
利用公式 固氮酶活=乙烯峰面积×(摇瓶中气相总体积/进样量)/(1 nmol标准乙烯峰面积×反应时间×蛋白量)计算固氮酶活性。其中摇瓶中气相总体积为70 mL,1 nmol标准乙烯峰面积为1 962.9,蛋白量为0.68 mg。
1.2.4 以精氨酸为唯一氮源条件下的生长曲线测定 活化菌株DH10B、ΔglnG、ntrC-comp-E,接种至液体培养基M9中,37℃过夜培养。离心收集菌体。用0.85% 的生理盐水洗涤菌体2次。用以精氨酸为唯一氮源的液体培养基重悬菌体,并调节菌液初始OD600为1.0。接种200 μL菌液于19.8 mL以精氨酸为唯一氮源的液体培养基,37℃,220 r/min震荡培养,每个体系3个重复。分别于2、4、6、8、10、12、14、16、18、20、22和24 h取样,测定各菌液的OD600。
1.2.5 引物设计 根据NCBI数据库的GenBank中获得大肠杆菌DH10B及施氏假单胞菌A1501的基因组序列后分别找到目标基因glnG和ntrC,用Primer premier 5.0设 计 引 物glnG(F)/glnG(R)和 ntrC(F)/ntrC(R)。glnG(F):5'-CAAAGCTT CCACTCGATACCAGATTA-3'和 glnG(R)5'-CGGGATCC AGGAAATAAAGGTGACG-3',下划线分别为Hind III和BamH I酶切位点。ntrC(F):5'-TTTAAGCTTTGTCGCAGGTCGGAT-3',和ntrC(R):5'-TTGGATCCAGAACATCATCAGTCAG-3',下划线分别为Hind III和BamH I酶切位点。以基因组DNA为模板用引物glnG(F)/glnG(R)和ntrC(F)/ntrC(R)扩增glnG和ntrC基因片段。PCR扩增条件:95℃10 min;95℃ 30 s,54-62℃ 1.5 min,72℃ 30 s,30个循环;72℃ 10 min。
2 结果
2.1DH10B GlnG和A1501 NtrC的生物信息学及理化性质分析
在 NCBI数 据 库 中(http://blast.ncbi.nlm.nih. gov/Blast.cgi)分别检索DH10B GlnG及A1501 NtrC两蛋白质的氨基酸序列,获得序列后利用DNAMAN软件对两个序列进行序列比对分析,比对结果(图1)显示两个蛋白的一级结构相似,氨基酸序列相似性为63.5%。

图1 DH10B GlnG与A1501 NtrC蛋白质氨基酸序列比对
利用 ExPASy(Expert Protein Analysis System)数据库中进行氨基酸理化参数计算的工具ProtParam(http://expasy.org/tools/protparam.html)对两个蛋白质进行了比较分析。结果(表2)显示两个蛋白的分子量、等电点等都非常接近。以上结果表明DH10B GlnG蛋白与A1501 NtrC蛋白在结构上具有一定相似性,两蛋白可能具有功能相关性。

表2 A1501 NtrC与DH10B GlnG理化性质比较(预测)
2.2 glnG互补ΔntrC功能互补株的构建及表型分析
本实验室已经采用广宿质粒pLAFR3通过双酶切成功构建了pLAFR3-glnG重组质粒,本研究通过三亲结合的方法将重组质粒 pLAFR3-glnG导入ΔntrC中。在含有四环素(Tc)和氯霉素(Cm)双抗性的固体限制性培养基K上进行阳性克隆筛选,再利用引物glnG(F)/glnG(R)进行菌落PCR验证(图2),得到glnG互补ΔntrC的功能互补株(glnG-comp)。
图2 菌落PCR验证glnG基因
为了研究GlnG能否替代NtrC在ΔntrC一般氮代谢过程中行使功能,我们构建了glnG互补ΔntrC的功能互补株并进行了相应功能表型测定。因本实验室已经证实ΔntrC不能在以硝酸钾或尿素为唯一氮源的培养基上生长,所以本研究测定了A1501、A1501ΔntrC、ntrC-comp以及glnG-comp在培养基K中以硝酸钾和尿素为唯一氮源的生长曲线(图3)。从图中可以看到ΔntrC能够利用硝酸钾和尿素为唯一氮源进行生长,野生型A1501在该条件下生长良好。而不论是用ntrC还是用glnG回补ΔntrC都能使其恢复一定的生长能力。结果表明,glnG已在ΔntrC中成功表达,并能够替代ntrC实现对硝酸钾和尿素功能的利用,这一结果表明GlnG蛋白与NtrC蛋白在氮代谢过程中具有功能相关性。

图3 四种菌株在以10 mmol/L硝酸钾(A)及10 mmol/L尿素(B)为唯一氮源条件下的生长曲线
为了进一步验证 GlnG蛋白与NtrC蛋白在固氮调控过程中是否具有功能相关性,我们对A1501、ΔntrC、ntrC-comp及glnG-comp的固氮酶活性进行了测定。结果(图4)发现ntrC突变以后使菌株的固氮酶活性基本丧失,而glnG-comp具有一定的固氮酶活性,约为野生型A1501的45%。说明在固氮过程中,glnG能够部分互补ntrC的调节功能,使菌株表现出固氮酶活性。结果表明,在重组大肠杆菌中GlnG参与了固氮表达调控,与NtrC蛋白具有功能相关性。
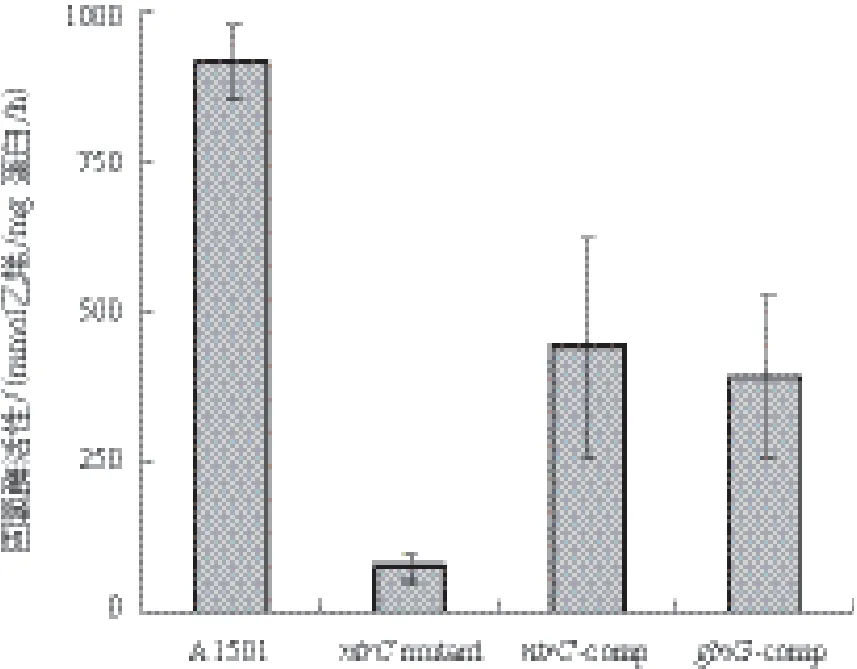
图4 四种菌株固氮酶活性的测定
2.3 ntrC互补ΔglnG功能互补株的构建及表型分析
本实验室已成功地将A1501ntrC片段克隆到广宿主质粒载体pLAFR3上,构建了A1501 NtrC蛋白的表达载体 pLAFR3-ntrC。本研究首先提取了重组质粒 pLAFR3-ntrC,然后通过电击转化将重组质粒pLAFR3-ntrC导入到ΔglnG中,再利用含有四环素(Tc)和卡那霉素(Km)双抗性的固体LB平板进行阳性克隆筛选。最后利用ntrC(F)/ntrC(R)引物进行菌落PCR验证(图5),得到ntrC回补ΔglnG的功能互补株(ntrC-comp-E)。

图5 菌落PCR验证ntrC基因
为了研究NtrC蛋白能否在 E.coli DH10B中代替GlnG在一般氮代谢过程中行使功能,我们对ΔglnG和ntrC-comp-E进行了相应表型测定。因为有研究表明ΔglnG不能在以精氨酸为唯一氮源的条件下进行生长[9],所以本研究测定了E.coli DH10B、ΔglnG以及ntrC-comp-E在培养基M9中以精氨酸为唯一氮源条件下的生长曲线。结果(图6)显示 ΔglnG在M9培养基中不能够以精氨酸为唯一氮源进行生长,野生型E.coli DH10B在该条件下生长良好。而当用ntrC互补ΔglnG突变株时,功能互补菌株基本恢复了生长能力。结果表明,ntrC已在ΔglnG中成功表达,并能够替代glnG在E.coli DH10B菌的一般氮代谢过程中行使功能,实现对精氨酸利用功能的互补。
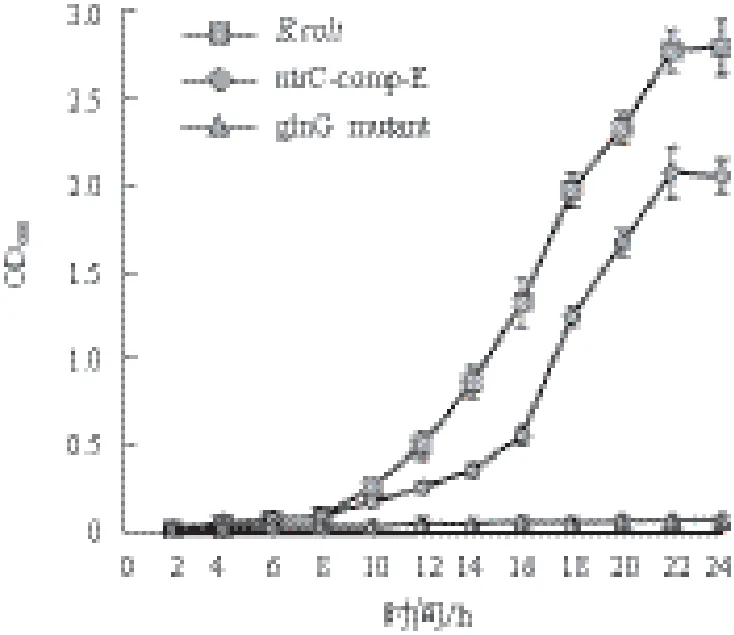
图6 三种菌株在以精氨酸为唯一氮源条件下的生长曲线
3 讨论
氮调节是涉及多个信号转导和效应蛋白的复杂调控网络,该领域在肠道菌中已经进行了深层研究。假单胞菌的氮代谢系统与肠细菌相比有很多共同特点,均含有典型的氮代谢调节系统即NRII-NRI双组分调节系统[3],该系统由尿苷转移酶(GlnD)、PII(GlnB、GlnK)、NRII(GlnL/NtrB)和 NRI(GlnG/NtrC)等具有双功能的蛋白组成。然而,施氏假单胞菌的氮调节与大肠杆菌也有很多不同之处。首先,施氏假单胞菌中Ntr系统的功能仅由glnK基因编码的PII蛋白调控,其产物直接编码高亲和力转运蛋白的amtB基因相互作用。而在大肠杆菌中,glnB和glnK都编码PII蛋白,其中组成型表达的GlnB蛋白由glnB编码,由于GlnK的转录依赖于NRI,因此glnK编码的GlnK蛋白只在低氮条件下表达,GlnB和 GlnK的功能也部分重叠[10]。
Schumacher等[5]研究表明,NRI(NtrC)的存在导致恶臭假单胞菌中glnK和amtB的表达受氮源调控,其功能仅在氮限制的条件下由NtrC激活[5]。体外纯化蛋白实验表明,glnK的转录直接被 NtrC激活[5]。通过对施氏假单胞菌A1501中glnK基因的序列分析,发现在glnK基因的启动子上游-12/-24处具有与σ54结合位点相似的序列。在低氮的条件下,依赖于σ54的启动区开始转录后glnK 基因开始表达,该表达受NtrC蛋白调控;在高氮条件下,glnK基因可能在一个不依赖于σ54和NtrC蛋白调控的启动子区开始转录并进行低水平表达[11]。
在大肠杆菌中,glnK基因上游区域也含有一个 σ54结合位点,一个 NRI(GlnG)结合位点,操纵子表达也依赖GlnG同时也受到氮素调控[12,13]。另外,与大肠杆菌glnKp不同的是恶臭假单胞菌glnKp开放复合物的形成强烈依赖于IHF,这在体内才能观察到。并且IHF的参与,加上其螺旋的同一侧存在两个连续的NtrC结合位点,表明恶臭假单胞菌glnKp的转录激活对低浓度的NtrC是敏感的。这两个不同点可能与缺乏组成型GlnB蛋白进行高效氮抑制有关[14]。其次,大肠杆菌氮调节的操纵子也包含能被 σ70RNA聚合酶全酶识别的启动子[15],这些操纵子的转录受到氮同化控制蛋白(Nac)-LysR 型调节子的调控。在大肠杆菌中受Nac激活的基因和操纵子涉及氮化分子的转运[16],这也可能作为氮的来源。然而施氏假单胞菌A1501全基因组数据表明其不含有nac基因[17],并且已测序的假单胞菌基因组表明该属菌中不含有Nac同源物[18]。有研究证实在恶臭假单胞菌中,由NtrC直接激活的基因同时含有σ54依赖型启动子和Nac激活基因同源物,这避免了需要一个适配器来共同调节σ54和σ70依赖型基因[19]。进而推测通过Nac介导的依赖σ70的级联氮调控不是肠杆菌所必须的,因为许多菌中不含有nac基因。在沙门氏菌中,最近发现似乎Nac也丢失了,因为在响应氮的情况下它不能控制依赖σ70基因的表达。然而沙门氏菌中hutC基因的启动子仍易受克雷伯氏菌Nac的激活[20,21]。相反在恶臭假单胞菌中,这些基因有的仍然响应氮的调控,但是它们的启动子依赖σ54,直接受到NtrC的调控,从而避免了额外的调控[22]。由此可知施氏假单胞菌A1501中由氮介导的调控网络也是大肠杆菌中氮调控网络的简化模式:只含有一个PII蛋白,没有Nac参与的级联调控[23],这可能是造成DH10B GlnG和A1501 NtrC调控功能差异的因素。
本研究证实了DH10B GlnG和A1501 NtrC蛋白在一级结构、理化性质以及功能上都具有很大的相似性。这些数据表明,在大肠杆菌和施氏假单孢菌中的NRI蛋白的功能是高度保守的,两个蛋白可以进行相互替换。同时也发现,DH10B glnG互补A150 ntrC突变株时,在一般氮代谢方面的功能互补性高于调控固氮过程的功能互补性,推测这可能与大肠杆菌和施氏假单胞菌中氮介导的调节网络的不同有关,也可能是在进化过程中,由于大肠杆菌所处的环境营养条件优越,造成其一般氮代谢调节蛋白GlnG在功能上产生了分化。
4 结论
本研究成功构建了DH10B glnG回补A1501 ΔntrC的功能互补株和A1501ntrC回补DH10B ΔglnG的功能互补株,并对互补株和突变株与野生型的氮源利用和生物固氮能力等方面进行了比较分析,结果显示DH10B glnG能够互补A1501 ntrC在氮源利用和氮限制条件下的调节功能,而A1501 ntrC能够互补DH10B glnG在氮源条件下的生长能力,这一结果表明DH10B菌中的GlnG可能通过互补A1501菌中 NtrC蛋白在氮限制条件下的调节功能进而参与到一般氮代谢调控网络过程中。
[1] Halbleib CM, Ludden PW. Regulation of biological nitrogen fixation[J]. J Nutr, 2000, 130(5):1081-1084.
[2]Li W, Lu CD. Regulation of carbon and nitrogen utilization by CbrAB and NtrBC two-component systems in Pseudomonas aeruginosa[J]. J Bacteriol, 2014, 59(4):524-592.
[3] Arcondeguy T, Jack R, Merrick M. P(II)signal transduction proteins, pivotal players in microbial nitrogen control[J]. Microbiol Mol Biol Rev, 2001, 65(1):80-105.
[4]Vidangos NK, Heideker J. DNA recognition by a σ(54)transcriptional activator from Aquifex aeolicus[J]. J Mol Biol, 2014, 175(19):667-684.
[5] Schumacher J, Behrends V, Pan ZS, et al. Nitrogen and carbon status are integrated at the transciptional level by the nitogen regulator BtrC in vivo[J]. Microbiology, 2013, 149(Pt 8):251-262.
[6] Hervas AB, Canosa I, Santero E. Transcriptome analysis of Pseudomonas putida in response to nitrogen availability[J]. J Bacteriol, 2008, 190(1):416-420.
[7]Desnoues N, Lin M, Guo X, et al. Nitrogen fixation genetics and regulation in a Pseudomonas stutzeri strain associated with rice[J]. Microbiology, 2003, 149(Pt 8):2251-2262.
[8]Yan Y, Yang J, Dou Y, et al. Nitrogen fixation island and rhizophere competence traits in the genome of root-associated Pseudomonas stutzeri A1501[J]. Proc Natl Acad Sci USA, 2008, 105(21):7564-7569.
[9] Mcfarland N, Mccarter L, Artz S, et al. Nitrogen regulatory locus "glnR" of enteric bacteria is composed of cistrons ntrB and ntrC:identification of their protein products[J]. Proc Natl Acad Sci USA, 1981, 78(4):2135-2139.
[10] Williams KJ, Bennett MH, Barton GR, et al. Adenylylation of mycobacterial GlnK(PII)protein is induced by nitrogen limitation[J]. Tuberculosis(Edinb), 2013, 49(Pt 8):1251-1262.
[11]Chen B, Doucleff M, Wemmer DE, et al. ATP ground- and transition states of bacterial enhancer binding AAA+ ATPases support complex formation with their target protein, sigma54[J]. Structure, 2007, 15(4):429-440.
[12] Benkert P, Biasini M, Schwede T. Toward the estimation of the absolute quality of individual protein structure models[J]. Bioinformatics, 2010, 27(3):343-350.
[13] Jiang H, Shang L, Yoon SH, et al. Optima production of polygamma-glutamic acid by metabolically engineered Escherichia coli[J]. Biotechnol Lett, 2006, 29(2):631-647.
[14]Hervas AB, Canosa I, Little R, et al. NtrC-dependent regulatory network for nitrogen assimilation in Pseudomonas putida[J]. J Bacteriol, 2009, 181(4):1056-1062.
[15] Abbas MM, Mohie-Eldin MM, EI-Manzalawy Y. Assessing the effects of data selection and representation on the development of reliable E. coli sigma 70 promoter region predictors[J]. PLoS One, 2015, 162(19):3028-3039.
[16] Zeng J, Spiro S. Finely tuned regulation of the aromatic amine degradation pathway in Escherichia coli[J]. J Bacteriol, 2013, 195(22):5141-5150.
[17] Babaer P, Marashi SA, Asad S. Genome-scale reconstruction of the metabolic network in Pseudomonas stutzeri A1501[J]. RSC Publishing, 2015, 41(13):3082-3088.
[18]Yan Y, Ping S, Peng J, et al. Global transcriptional analysis of nitrogen fixation and ammonium repression in root-associated Pseudomonas stutzeri A1501[J]. BioMed Central, 2010, 115(21):7543-7565.
[19] Melchiorsen CR, Jokumsen KV, Villadsen J, et al. The level of pyruvate-formate lyase controls the shift from homolactic to mixedacid product formation in Lactococcus lactis[J]. Appl Microbiol Biotechnol, 2002, 58(3):338-344.
[20]Utrilla J, Gosset G, Martinez A. ATP limitation in a pyruvate formate lyase mutant of Escherichia coli MG1655 increases glycolytic flux to D-lactate[J]. J Ind Microbiol Biotechnol, 2009, 36(8):1057-1062.
[21] Sieira R, Arocena GM, Zorreguieta A, et al. A MarR-Type regulator directly activates transcription from the Brucella abortus virB promoter by sharing a redundant role with HutC[J]. J Bacteriol, 2012, 73(13):6143-6158.
[22] Vidangos NK, Heidiker J, Lyubimov A, et al. DNA recognition by a σ(54)transcriptional activator from Aquifex aeolicus[J]. J Mol Biol, 2014, 114(3):1162-1169.
[23]Hasona A, Kim Y, Healy FG, et al. Pyruvate formate lyase and acetate kinase are essential for anaerobic growth of Escherichia coli on xylose[J]. J Bacteriol, 2004, 186(22):7593-7600.
(责任编辑 马鑫)
Functional Complement Between General Nitrogen Regulator GlnG in Escherichia coli and General Nitrogen Regulator NtrC in Pseudomonas
KE Qi1,2CHEN Qing-hua2ZHAN Yu-hua2LU Wei2YAN Yong-liang2
(1. School of Life Science and Engineering,Southwest University of Science and Technology,Mianyang 621010;2. Biotechnology Research Institute,Chinese Academy of Agricultural Sciences,Beijing 100081)
This study aims to investigate whether or not there is functional complement in general nitrogen-regulation network between nitrogen metabolism regulator GlnG from Escherichia coli DH10B and NtrC from Pseudomonas stutzeri A1501. Using gene glnG of DH10B to complement gene ntrC of A1501 or vice versa,the physiological and biochemical phenotypes of the obtained functionally complementary strains were measured. The results showed that while nitrate or urea as the sole nitrogen source,DH10B’s glnG complemented the nitrogenutilizing ability and partially restored the nitrogenase activity(about 45% of wild type)of mutant A1501’s ntrC. Comparing with DH10B’s glnG,A1501’s ntrC only complemented mutant DH10B glnG while arginine as sole nitrogen source. Above results revealed that not only was there close phylogenetical relationship,but also the functional complement in the tested nitrogen metabolism between DH10B’s GlnG and A1501’s NtrC.
Pseudomonas stutzeri A1501 NtrC;Escherichia coli DH10B GlnG;general nitrogen metabolism;functional complement
10.13560/j.cnki.biotech.bull.1985.2016.04.025
2015-12-17
国家“973”项目(2015CB755700),国家自然科学基金项目(31470174),广东省引进创新创业团队计划项目(2013S033)
柯琪,女,硕士,研究方向:固氮微生物与基因工程,E-mail:543274382@qq.com;陈清华为本文并列第一作者
燕永亮,博士,副研究员,硕士生导师,研究方向:固氮微生物分子生物学及基因工程;E-mail:yanyongliang@caas.cn
——固氮微生物

