基于单针三电极的动态血糖传感器研制
刘亮泽, 岳瑞峰
(清华大学 微电子学研究所,北京 100084)
基于单针三电极的动态血糖传感器研制
刘亮泽, 岳瑞峰
(清华大学 微电子学研究所,北京 100084)
摘要:研制了一种基于单根空心微针的新型植入式葡萄糖传感器,用于对人体血糖变化趋势进行连续监测。单根空心微针由结构相同的两个沿轴向磨去半边的不锈钢针管通过绝缘胶粘结而成,其分别作为传感器的工作电极与辅助电极;参比电极是置于该微针通孔之中的Ag/AgCl细丝;葡萄糖氧化酶(GOD)置于针尖的通孔处。测试结果表明:传感器的线性范围为3~22 mmol/L,灵敏度为1.11 μA/mmol/L,响应时间为10 s,且具有较好的抗干扰性。
关键词:葡萄糖氧化酶; 葡萄糖传感器; 连续监测
0引言
糖尿病患者的血糖值受饮食、运动等的影响在一天中会有较大波动,往往需要多次对其进行检测以及时调整给药量和治疗策略。目前主要通过采指血的方法进行体外血糖检测,每天多次检测无疑会给患者带来剧痛和诸多不便。近年来,用于实时连续监测的血糖传感器已经成为研发的热点,其中,针型葡萄糖传感器由于其结构简单、可植入性强等优点而受到广泛的关注[1-5]。由于体内环境复杂多变和电活性物质的干扰,如何增强传感器的抗干扰能力、提高灵敏度和响应时间与线性范围等已成为植入式检测研发的重点[6~8]。前期曾报道过一种基于微针阵列的连续监测葡萄糖传感器[9],其采用三根微针组成的三电极结构,分别用作工作电极、辅助电极和参比电极;测试结果表明其具有很好的抗干扰性与线性范围,鉴于三根微针之间的间距设置的比较大(2 mm),灵敏度(0.575 μA/mm)和响应时间(16 s)等性能还有待改进。
为了进一步提高灵敏度、降低响应时间并减小刺入创口与疼痛,本文研制了一种由三电极结构组成的单针葡萄糖传感器。单针结构不仅可以进一步降低对人体的刺入创伤,且因大大缩小了电极间距而提升了灵敏度、降低了响应时间。三电极体系可构成差分结构,能够有效排除一些人体内电活性物质对传感器的干扰,有利于提高抗干扰性。
1原理与设计
1.1传感器工作原理
本文设计的葡萄糖传感器是基于酶促反应[10]来实现葡萄糖的电化学检测的。葡萄糖在葡萄糖氧化酶(GOD)的催化作用下可被氧分子氧化生成葡萄糖酸和过氧化氢(H2O2),而H2O2浓度与待测葡萄糖浓度之间具有严格的化学计量关系。通过电学方式测量H2O2的产生量即可获得待测葡萄糖的浓度信息,其反应原理如图1所示。
在酶膜层发生的化学反应式为
(1)
在一定电位下,金属Pt对H2O2具有催化分解作用,电极处发生的反应式为
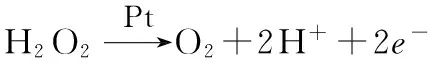
(2)

图1 酶电极工作原理图Fig 1 Working principle diagram of enzyme electrode
产生的电荷转移到酶电极会形成电流,电流大小与H2O2浓度呈正比,从而可以得出其与葡萄糖浓度的关系。
1.2结构设计
设计的葡萄糖传感器如图2所示的单根空心微针上的三电极结构。其中,单根空心微针是采用结构相同的两个沿轴向磨去半边的不锈钢针管通过绝缘硅橡胶粘结组装而成,在室温下4 h即可固定牢固,其分别作为传感器的工作电极与辅助电极,它们的表面均溅射有Ti/Pt金属薄膜;参比电极是置于该微针通孔之中的Ag/AgCl细丝;葡萄糖氧化酶置于空心微针针尖的通孔处以防止在刺入过程中导致酶膜的脱落。辅助电极与工作电极之间的区别仅在于工作电极针尖上的葡萄糖氧化酶具有活性,而辅助电极针尖上的葡萄糖氧化酶已经失活。通过这种三电极差分的形式可望有效去除体内一些电活性物质的干扰,提高传感器测试的准确性和稳定性。
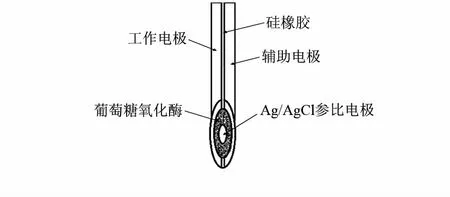
图2 单针三电极结构示意图Fig 2 Diagram of single needle with three electrodes structure
2传感器的制备
2.1工作电极和辅助电极的制备
首先,将数根外径为450 μm且表面溅射了20 nm/200 nm厚Ti/Pt薄膜的不锈钢空心微针固定在模具之中,借助模具沿与针管轴心平行的方向研磨微针,直至磨去1/2针管为止。将这些微针取出后,分别侵入丙酮、无水乙醇和去离子水中进行超声清洗。待烘干后,将微针放入磷酸盐缓冲液中加100 mV/s低电压进行循环扫描,使微针中的电活性杂质溶出,直至响应电流稳定为止。这些结构相同的微针将作为工作电极或辅助电极备用。
本文采用戊二醛—牛血清蛋白交联法对葡萄糖氧化酶进行固定。戊二醛的醛基可以与蛋白质的氨基发生缩合反应,形成交联薄膜实现GOD在电极的固定。实验中取GOD(活性为340 U/mg)按1.8 mg分装成若干份,置于-4 ℃冷藏保存。使用时,用磷酸盐缓冲液(PBS溶液)配置,使其活性达到6.8 U/μL。取GOD(活性为6.8 U/μL)、牛血清蛋白BSA和2 %的戊二醛溶液,按溶液体积比5︰5︰1的比例混合(GOD与BSA先混合后,再加入戊二醛溶液)并摇匀[11]。将经过预处理的上述微针电极的断面凹腔朝上置于洁净的橡胶垫上。用移液枪将少量配置好的GOD溶液涂覆在针尖处的凹腔之中,然后将其置于室温洁净的培养皿中静置2 h晾干,并在4 ℃下储存。
虽然辅助电极的形状、材质与工作电极完全相同,同时也敷有GOD,但其氧化酶是处于失活状态的。由于GOD的最佳工作温度为30~50 ℃,70 ℃以上GOD会逐渐失去活性。因此,本文采用加热法处理固定在辅助电极针尖处的GOD,通过循环伏安测试发现其已没有明显的氧化还原峰值,说明其涂覆的GOD已经失活。所以,设计的辅助电极测得的电流应仅是溶液中的背景电流,不会产生响应电流。
2.2Ag/AgCl参比电极的制备
采用电解法制备Ag/AgCl参比电极。首先用细砂纸对直径为150 μm的实心银丝进行打磨以去除表面的氧化物。然后用去离子水将浓度为37 %的浓盐酸稀释至0.1 mol/L,并将处理后的Ag丝作为阳极侵入稀释后的浓盐酸中,阴极也固定Ag丝置于溶液之中。在两电极间施加5 V电压,避光电解5 min,即可制备出致密均匀的白色Ag/AgCl参比电极。将阳极制备好的Ag/AgCl细丝取出,用去离子水清洗后,置于饱和的KCl溶液中避光保存。
2.3传感器的组装
首先在针尖上固定有GOD的工作电极与辅助电极的半圆凹槽内与研磨断面处分别涂覆一薄层绝缘硅橡胶,然后将工作电极与辅助电极分别贴覆在Ag/AgCl参比电极两侧形成如图2所示结构,并放于洁净培养皿中室温固化24 h。各电极之间的绝缘由涂覆的绝缘硅橡胶完成,待完全固化后,在微针后端引线以备测试使用。
3传感器性能测试
3.1电极循环伏安测试
将传感器微针电极侵入1 mmol/L的葡萄糖溶液中,在工作电极和参比电极之间施加-0.3~0.9 V、变化速率为100 mV/s的三角波电压,并记录电流变化,如图3所示。从图中可明显看出:电极的氧化还原峰值出现在0.7 V附近,故以后的测试均以0.7 V电压作为最佳反应电压。
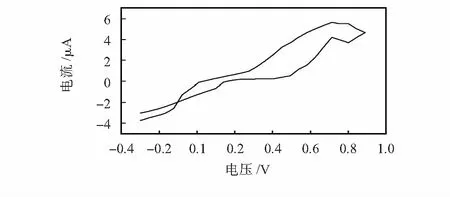
图3 工作电极循环伏安曲线Fig 3 Cyclic voltammetric curve of working electrode
3.2滴加响应台阶测试
为了保证实验环境接近人体环境,所有体外实验均在37 ℃的恒温水浴池中进行。将微针探头侵入6 mL的PBS溶液中,对工作电极和辅助电极均施加0.7 V电压。待电流响应稳定后开始计时,每隔3 s向溶液中滴加一定量浓度为30 mmol/L的葡萄糖溶液,被测试溶液每次浓度变化为1 mmol/L。测得的传感器的响应曲线如图4所示,至第22次滴加时传感器响应均变化明显,继续滴加溶液响应趋于饱和,整体趋势符合Michaelis-Menten的酶传感器特性,其线性范围在22 mmol/L左右。

图4 滴加响应曲线Fig 4 Dropwise response curve
3.3线性范围和灵敏度测试
将微针探头侵入一定量的PBS缓冲溶液中,施加0.7 V电压,待响应电流稳定后,开始进行实验。葡萄糖传感器在不同浓度的葡萄糖溶液中的响应电流如图5所示。通过线性拟合法分析响应曲线,可以得出拟合方程为Y=1.11X+2.13,校正决定系数,R2=0.998 7。从而可以得出:该传感器的零位为2.13 μA,灵敏度为1.11 μA/mmol/L,线性范围为3~22 mmol/L。

图5 传感器对不同浓度葡萄糖溶液的响应曲线Fig 5 Response curve of sensor to glucose solution with different concentration
3.4响应时间测试
传感器的响应时间是表征其性能的重要参数。测试时先将葡萄糖传感器侵入在3 mmol/L的葡萄糖溶液中,待反应稳定后,向溶液中滴加一定高浓度的葡萄糖溶液,并做稍许搅拌,此时溶液浓度可以迅速提升达到10 mmol/L。由加入溶液后开始反应到其响应电流稳定,所经历时间约为10 s,如图6所示。
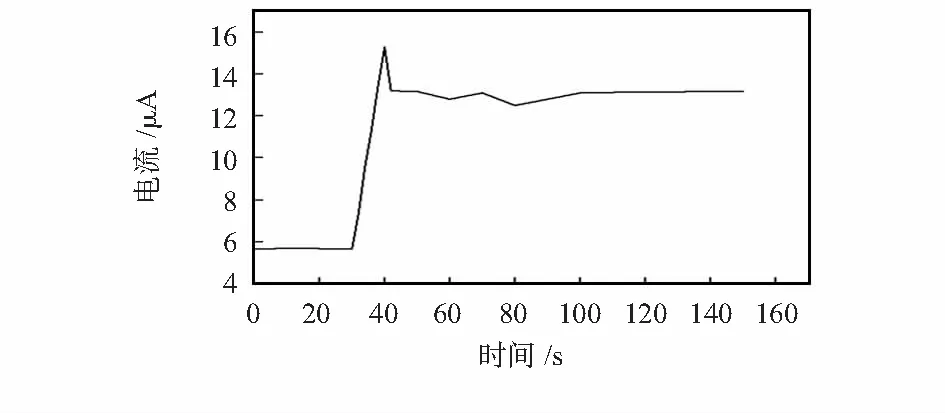
图6 传感器响应时间曲线Fig 6 Response time curve of sensor
4抗干扰能力测试
人体正常的血糖变化范围为3.9~6.1 mmol/L(空腹),本文取6 mmol/L葡萄糖溶液作为测试基液。先将葡萄糖传感器置于6 mL的PBS基液中,待响应稳定后开始测试。30 s后滴加一定量30 mmol/L的葡萄糖溶液,此时基液浓度可达6 mmol/L。90 s后滴加一定量浓度(0.2 mmol/L)的抗坏血酸溶液。从测试结果可以看出:三电极结构产生的干扰电流为0.65 μA,没有辅助电极的双电极结构产生的干扰电流为3.71 μA,如图7所示,说明三电极结构传感器具有较强的抗干扰能力。

图7 抗坏血酸对葡萄糖传感器的影响Fig 7 Effects of ascorbic acid on glucose sensor
5结论
本文提出了一种基于单微针三电极结构的新型葡萄糖传感器,通过对初期样品进行体外测试评价结果表明:该传感器的线性范围为3~22 mmol/L并具有较强的干扰能力;单针结构中的电极间距变小直接导致了响应时间更短、灵敏度更高;以针壁作为电极,氧化酶覆在针尖凹腔之中,探针刺入皮肤时可望有效保护GOD以免其脱落,而采用单针结构则能在很大程度上减少传感器刺入时造成的创伤。
参考文献:
[1]Albisser A M,Leibel B S,Ewart T G,et al.Clinical control of diabetes by the artificial pancreas[J].Diabetes,1974,23(5):397-404.
[2]Shichiri M,Yamasaki Y,Kawamori R,et al.Wearable artificial endocrine pancreas with needle-type glucose sensor[J].The Lancet,1982,320(8308):1129-1131.
[3]Dilbir S Bindra,Zhang Yanan,Wilson George S.Design and in vitro studies of a needle-type glucose sensor for subcutaneous monitoring[J].Analytical Chemistry,1991,63(17):1692-1696.
[4]Moussy Francis,Harrison D Jed,O’Brien Darryl W,et al.Performance of subcutaneously implanted needle-type glucose sensors employing a novel trilayer coating [J].Analytical Chemistry,1993,65:2072-2077.
[5]曹大均,周敏.针形葡萄糖传感器的研究[J].化学传感器,1996,16(1):26-31.
[6]Zimmermann S,Fienbork D,Stoeber B,et al.A microneedle-based glucose monitor:Fabricated on a wafer-level using in-device enzyme immobilization[C]∥The 12th International Conference on Solid-State Sensors,Actuators and Microsystems, 2003:99-102.
[7]Takaoka Hiroki,Yasuzawa Mikito.Fabrication of an implantable fine needle-type glucose sensor using γ-polyglutamic acid[J].Analytical Sciences,2010,26:551-555.
[8]Koh A,Lu Y,Schoenfisch M H.Fabrication of nitric oxide-releasing porous polyurethane membranes-coated needle-type implan-table glucose biosensors[J].Analytical Chemistry,2013,85(21):10488-10494.
[9]刘尚,岳瑞峰.基于空心微针阵列的连续监测葡萄糖传感器[J].传感器与微系统,2015,34(1):97-100.
[10] Updike S J,Hicks G P.The enzyme eletrode [J].Nature,1967,214:986- 988.
[11] 张先恩.生物传感器[M].北京:化学工业出版社,2005:60-64.
Study and fabrication of dynamic glucose sensor based on single needle with three electrodes
LIU Liang-ze, YUE Rui-feng
(Institute of Microelectronics,Tsinghua University,Beijing 100084,China)
Abstract:A new type of implantable glucose sensor based on hollow micro-needle is studied and fabricated used for continuous monitoring on human blood glucose concentration.The hollow micro-needle is constituted by two same slot-type stainless steel needles used as working electrode and auxiliary electrode respectively,which glued together with silicone rubber,a Ag/AgCl filament is placed in the hollow micro-needle as reference electrode,and glucose oxidase is placed on the tip of the micro-needle.The experimental results show that linear range of the sensor is 3~22 mmol/L with glucose concentration,sensitivity is 1.11 μA/mmol/L,response time is 10s,and with good anti-jamming performance.
Key words:glucose oxidase(GOD); glucose sensor; continuous monitoring
DOI:10.13873/J.1000—9787(2016)02—0078—03
收稿日期:2015—05—26
中图分类号:TP 212.3
文献标识码:A
文章编号:1000—9787(2016)02—0078—03
作者简介:
刘亮泽(1989-),男,北京人,硕士研究生,研究方向为生物传感器。

