HPLC法测定利伐沙班有关物质
王明珊

摘 要:目的 研究HPLC法测定利伐沙班有关物质。方法 利用流动相:水-乙腈(70∶30);色谱柱:Kromasil C18柱(250×4.6 mm,5 m);柱温:30 ℃;检测波长:241 nm;流速:1.0 mL/min;进样量:20l。结果 该品有关物质检查色谱条件的系统适用性试验较好。利伐沙班的定量限为1.033 ng,检测限为0.310 ng;吗啉酮的定量限为0.527 ng,检测限为0.158 ng;杂质Ⅰ的定量限为1.041 ng,检测限为0.364 ng;杂质Ⅱ的定量限为1.012 ng,检测限为0.304 ng。吗啉酮、杂质Ⅰ、杂质Ⅱ的校正因子均在0.9~1.1,因此,该品的有关物质检查中吗啉酮、杂质Ⅰ、杂质Ⅱ的杂质含量可以采用主成分自身对照法进行计算,重复性精密度良好。结论 HPLC法测定利伐沙班有关物质具有快速检测,方法简便的特点,特别适合于对产品质量的中控和工艺摸索阶段的快速响应调整。
关键词:利伐沙班 有关物质 HPLC法 测定
中图分类号:R927.2 文献标识码:A 文章编号:1674-098X(2016)01(b)-0159-02
利伐沙班是由强生和拜耳公司研制开发的一种高度选择性和可竞争性直接抑制Xa因子的口服抗凝药,具有生物利用度的Xa因子抑制剂,其选择性地阻断Xa因子的活性位点,且不需要辅因子(例如:抗凝血酶Ⅲ)以发挥活性。2008年在欧盟及加拿大等地上市,2009年6月在中国正式上市,2011年7月1日在美国上市,至今拜瑞妥(利伐沙班片)已在全球50多个国家上市。作为一种新型抗凝药,在疗效和安全性上可与华法林媲美,又不会产生药物间的相互作用,而且不需治疗监测。所以对其中间体在原料药中残留的控制是具有重要的实际意义的。
1 仪器与材料
仪器:LC-10A型高效液相色谱仪(SPD-10A紫外检测器,日本岛津公司)。
工作站:奥泰(CSChrom Plus)色谱工作站。
天平:BP-211D型电子天平(十万分之一,德国赛多利斯公司)。
利伐沙班样品批号:20150801;利伐沙班对照品批号:20150901(纯度:99.91%);来源:南京佳核鑫医药科技有限公司。
3-吗啉酮批号:20150925(纯度:100.0%);杂质Ⅰ的批号:20151012(纯度:99.74%)杂质Ⅱ的批号:20151025(纯度:98.56%)来源:南京佳核鑫医药科技有限公司。
乙腈(Honeywell,色谱纯)。
纯净水(哇哈哈有限公司)。
其他所用试剂(分析纯,国药集团化学试剂有限公司)。
2 方法与结果
2.1 色谱条件
流动相:水-乙腈(70∶30);色谱柱:Kromasil C18柱(250×4.6 mm,5 ?m);柱温:30 ℃;检测波长:241 nm;流速:1.0 mL/min;进样量:20 ?l。
2.2 溶液配制
取该品,加乙腈适量溶解,用流动相定量稀释制成每1 mL中约含0.5 mg的溶液,作为供试品溶液。取供试品溶液适量,用流动相定量稀释制成每1 mL中约含5 ?g的溶液,作为对照溶液。分别精密称取吗啉酮和杂质Ⅰ、杂质Ⅱ适量,分别加乙腈适量溶解,分别用流动相定量稀释制成每1 mL中约含50 μg的溶液,分别作为吗啉酮、杂质Ⅰ、杂质Ⅱ的贮备溶液;精密量取各杂质贮备溶液1 mL,分别置10 mL量瓶中,加流动相稀释至刻度,摇匀,分别作为吗啉酮和杂质Ⅰ、杂质Ⅱ的定位溶液。精密称取该品约10 mg,置20 mL量瓶中,加乙腈适量溶解,分别加入吗啉酮和杂质Ⅰ、杂质Ⅱ贮备溶液各2 mL,加流动相稀释至刻度,摇匀,作为系统适用性溶液。
2.3 系统适应性
将系统适用性溶液连续进样6次,利伐沙班峰、吗啉酮峰、杂质Ⅰ峰、杂质Ⅱ峰相互之间的分离度均大于1.5,理论板数按利伐沙班峰计为12 595,连续进样6次各成分峰的保留时间及峰面积的RSD均小于2.0。
2.4 空白干扰及专属性试验
分别取供试品溶液、各杂质定位溶液及系统适用性溶液各20 ?L,分别注入液相色谱仪。结果供试品溶液的主峰保留时间为13.571 min,色谱峰峰行较好,保留时间适宜;另取流动相20 ?L,注入液相色谱仪,记录色谱图,结果如图1、图2所示,空白溶剂对主峰及各杂质峰的检测无干扰。表明该品有关物质检查色谱条件的系统适用性试验较好。
(吗啉酮定位溶液的主峰保留时间为3.088 min,杂质Ⅰ定位溶液的主峰保留时间为11.321 min,杂质Ⅱ定位溶液的主峰保留时间为8.533 min)。
2.5 定量限及检测限
量取利伐沙班对照品溶液和吗啉酮、杂质Ⅰ、杂质Ⅱ的杂质储备液适量,加乙腈溶解,加流动相逐级稀释至适当浓度,进样,考察利伐沙班、吗啉酮、杂质Ⅰ、杂质Ⅱ的定量限和检测限。利伐沙班的定量限为1.033 ng,检测限为0.310 ng;吗啉酮的定量限为0.527 ng,检测限为0.158 ng;杂质Ⅰ的定量限为1.041 ng,检测限为0.364 ng;杂质Ⅱ的定量限为1.012 ng,检测限为0.304 ng。
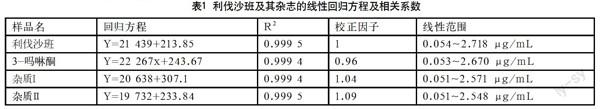
2.6 线性及范围
取利伐沙班、吗啉酮、杂质Ⅰ、杂质Ⅱ对照品适量,精密称定,加乙腈适量溶解,用流动相定量稀释制成每1 mL中约含利伐沙班、吗啉酮、杂质Ⅰ、杂质Ⅱ各50 μg的混合溶液,作为线性储备溶液,精密量取线性贮备溶液0.1 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL分别置100 mL量瓶中,加流动相稀释至刻度,摇匀,作为各线性溶液,取各线性溶液20 μL,分别注入色谱仪,记录色谱图。并以浓度C(μg/mL)为横坐标,峰面积A为纵坐标,进行线性回归,并计算相关系数r。结果如表1所示,吗啉酮在范围内,浓度与色谱峰面积之间的线性关系良好。根据线性试验计算得到的吗啉酮、杂质Ⅰ、杂质Ⅱ的校正因子均在0.9~1.1,因此,该品的有关物质检查中吗啉酮、杂质Ⅰ、杂质Ⅱ的杂质含量可以采用主成分自身对照法进行计算。
2.7 精密度(重复性试验)
取利伐沙班(20150801)适量,加乙腈溶解后流动相稀释制成每1 mL含0.5 mg的溶液作为供试品溶液,同法配制,共制得6份供试品溶液。照利伐沙班有关物质测定方法测定,并于6份样品测定结果的RSD考察该品有关物质的重复性。利伐沙班有关物质检查重复测定6次结果的RSD小于2.0%,表明此有关物质检查方法的重复性较好。
3 结语
该方法针对利伐沙班中部分杂质进行的开发研究,具有快速检测,方法简便的特点,特别适合于对产品质量的中控和工艺摸索阶段的快速响应调整。对于杂质限度的确定,可以依据《药品杂质分析指导原则》的要求,根据实际的工艺水平讨论制定。
参考文献
[1] 崔萍,纪安成,张爱华,等.利伐沙班及其光学异构体的HPLC法分离与测定[J].中国医药工业杂志,2015,46(11):1220-1222.
[2] 程璐,陈军.液-质联用法测定人血浆中利伐沙班的浓度[J].中国医院药学杂志,2014,34(19):1653-1656.

