蕹菜叶过氧化物酶功能基团的化学修饰
王红扬, 孙才云, 黄 忙, 唐云明(西南大学生命科学学院,重庆400715)
蕹菜叶过氧化物酶功能基团的化学修饰
王红扬,孙才云,黄忙,唐云明*
(西南大学生命科学学院,重庆400715)
摘要:为研究蕹菜叶面的的功能基团,将分离纯化得到的电泳纯的蕹菜过氧化物酶,分别用乙酰丙酮、顺丁烯二酸酐,二巯基苏糖醇、氯胺-T、溴代乙酸、对氯汞苯甲酸、苯甲基磺酰氟、N-乙酰咪唑选择性地对其进行化学修饰,并测定修饰前后酶活力变化。结果表明:精氨酸残基、赖氨酸残基、组氨酸残基和巯基可能是蕹菜过氧化物酶发挥活性的必需基团,而甲硫氨酸硫醚基、丝氨酸残基和酪氨酸酚羟基可能不是蕹菜过氧化物酶活性中心的必需基团。
关键词:蕹菜;过氧化物酶;功能基团;化学修饰
过氧化物酶(Peroxidase,POD)是一类在生物体内普遍存在的以血红素为辅基可催化由过氧化氢(H2O2)参与的氧化还原反应的氧化酶,例如参与胺类[1]和酚类[2]化合物的氧化反应。POD作为一种抗氧化剂,参与分解吲哚乙酸[3]、合成木质素[4]和植物体内防御反应[5]等多种生理反应。当今,该酶不仅广泛用于免疫印迹[6]、酶联反应[7]和电镜技术[8]等生物学研究,而且在污水处理[9]、生物传感器[10]等领域发挥重要作用。
蛋白质化学结构和空间结构共同决定其生物活性,在大多数情况下,蛋白质化学结构的改变将导致生物活性的下降,甚至完全丧失[11]。蛋白质的化学修饰中侧链基团的修饰是最成熟、最广泛使用的技术,包括巯基修饰、氨基修饰、羧基修饰和其它侧链修饰。因此,作者采用特定的化学修饰剂,分别为乙酰丙酮、二硫苏糖醇、氯汞苯甲酸、顺丁烯二酸酐、氯胺-T、苯甲基磺酰氯、N-乙酰咪唑和溴乙酸,破坏或者掩蔽侧链基团,通过测定该蛋白酶的酶活力是否受到抑制,判断该侧链基团与该酶发挥活性的必需基团的关系。由于该酶的主要来源辣根生长条件苛刻,在我国种植范围有限,价格昂贵,因此选取蕹菜这种种植范围广、产量高的植物作为提取原料分离纯化过氧化物酶,并且对其功能基团进行化学修饰,为深入了解其理化性质及进一步大规模工业生产提供理论基础。
1 材料与方法
1.1实验材料
作者所在实验室分离纯化得到的蕹菜叶过氧化物酶纯品,其中该酶的比活力为35 972.96 U/mg。
1.2主要试剂与设备
对氯汞苯甲酸:Sigma公司产品;苯甲基磺酰氟:Merck公司产品;溴代乙酸、二巯基苏糖醇、乙酰丙酮、顺丁烯二酸酐、氯胺-T、N-乙酰眯唑以及其余试剂:国产分析纯。UV-2550分光光度计:岛津;Mill-Q plus超纯水仪:Millipore;SevenEasy精密pH计:Mettler-Toledo。
1.3实验方法
分别配置浓度为10 mmol/L的NAI、BD、pCMB、PMSF、BrAc、DTT、顺丁烯二酸酐、氯胺-T溶液,作为母液。参考陈贻竹[12]等的方法,反应体系为3 mL,包括2.775 mL、50 mol/L磷酸盐缓冲液(pH 7.0)、0.1 mL、1% H2O2、0.1 mL 4%愈创木酚和0.025 mL酶液。将各种母液按一定比例分别加入到测酶活力缓冲体系中,得到不同浓度的化学修饰剂溶液,最后加入蕹菜POD,25℃下作用30 min后,测定过氧化物酶的活性。
酶活测定过程如下:在加入底物和缓冲液后,再加入0.025 mL酶液并混匀,在25℃下测定2 min 内OD470的变化值。以测定条件下每分钟光吸收值变化0.01所需要的酶量作为一个酶活力单位(U)。以相同条件下不加化学修饰剂时测得的酶活力作为100%对照。
2 结果与分析
2.1精氨酸胍基的化学修饰
在碱性条件下,蛋白质分子中的精氨酸残基与乙酰丙酮(BD)能够特异性地作用,影响侧链基团的结构,进而改变整个蛋白质分子的性质。在pH 8条件下,用乙酰丙酮(BD)处理蕹菜POD,结果表明:随着乙酰丙酮(BD)浓度的增大,酶活力逐渐下降,当浓度达到5 mmol/L时,活力只剩50%左右,见图1。由此说明精氨酸残基可能是蕹菜叶POD活性中心的必需基团。
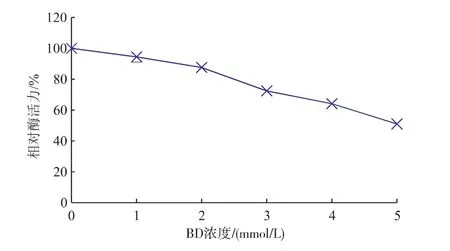
图1 BD浓度对蕹菜叶POD酶活力的影响Fig. 1 Effect of BD on activity of POD from Ipomoea aquatica Forsk leaves
2.2赖氨酸残基的化学修饰
顺丁烯二酸酐与蛋白质氨基酸残基侧链上的氨基相互作用,可以与氨基共价结合或者发生脱氨基作用,从而将氨基屏蔽起来[13]。结果表明:随着浓度的增大,酶活逐渐降低。说明赖氨酸残基有可能是该酶活性中心的必需基团,见图2。
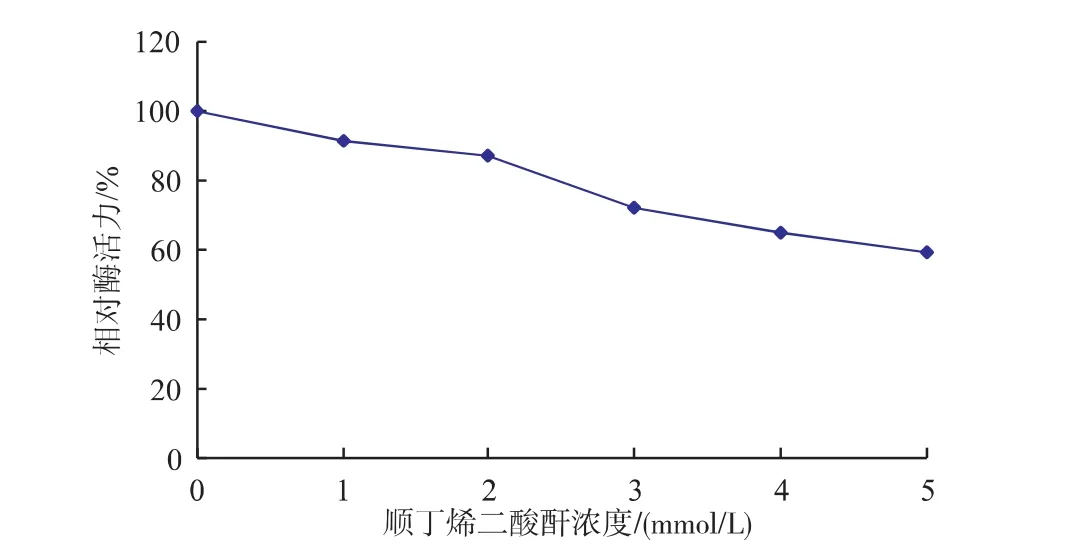
图2 顺丁烯二酸酐浓度对蕹菜叶POD酶活力的影响Fig. 2 Effect of maleic anhydride on activity of POD from Ipomoea aquatica Forsk leaves
2.3组氨酸残基的化学修饰
溴乙酸(BrAc)在偏酸性的条件下与组氨酸中的咪唑基相互作用,生成羧甲基衍生物[14]。在pH 6条件下,用溴乙酸(BrAc)处理蕹菜。实验结果显示:随着BrAc浓度的增加,酶活力急剧降低,当BrAc浓度为0.3 mmol/L时,酶活接近于0。由此说明组氨酸残基可能是该酶活性中心的必需基团,见图3。
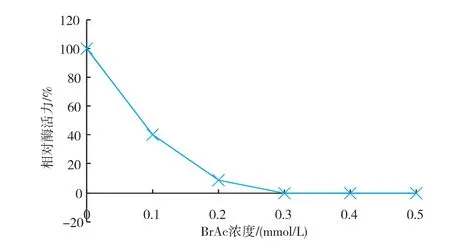
图3 BrAc浓度对蕹菜叶POD酶活力的影响Fig. 3 Effect of BrAc on activity of POD from Ipomoea aquatica Forsk leaves
2.4巯基的化学修饰氯汞苯甲酸(pCMB)做为巯基的常用修饰剂[15],在酸性条件下,与蛋白质分子中的巯基反应。在pH 5条件下,用氯汞苯甲酸(pCMB)处理蕹菜POD。随着氯汞苯甲酸(pCMB)浓度的增大,酶活急剧降低,在pCMB浓度为0.5 mmol/L时,酶活几乎为零。说明巯基很有可能是该酶活性中心的必需基团,见图4。
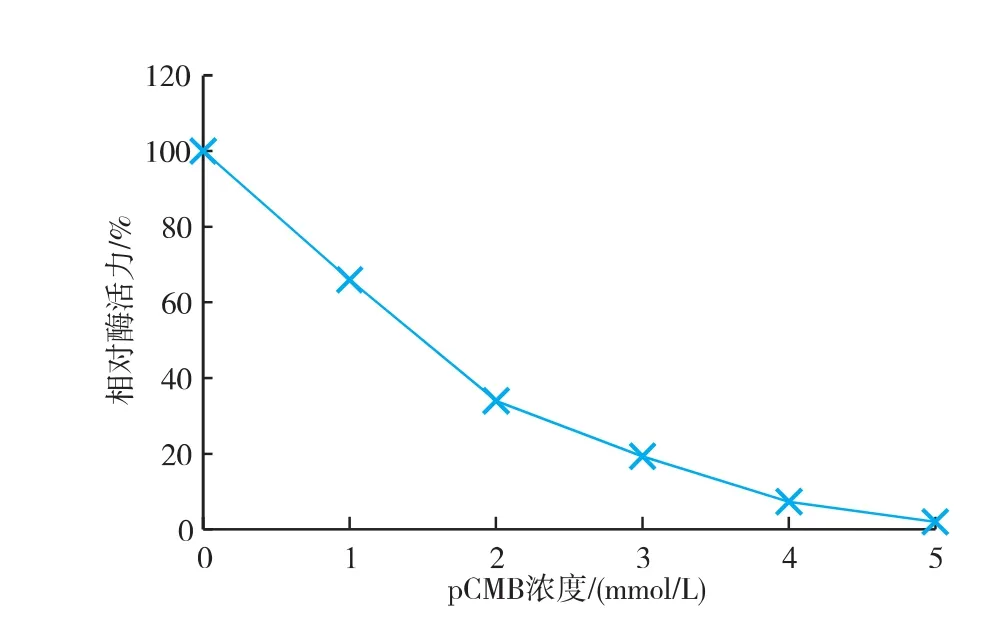
图4 pCMB浓度对蕹菜叶POD酶活力的影响Fig. 4 Effect of pCMB on activity of POD from Ipomoea aquatica Forsk leaves
2.5甲硫氨酸硫醚基的化学修饰
氯胺-T能在碱性条件下与甲硫氨酸的硫醚基相互作用。当pH 8时,用氯胺-T处理蕹菜POD,结果表明:氯胺-T对酶活无影响,说明甲硫氨酸硫醚基可能不是该酶活性中心的必需基团,见图5。
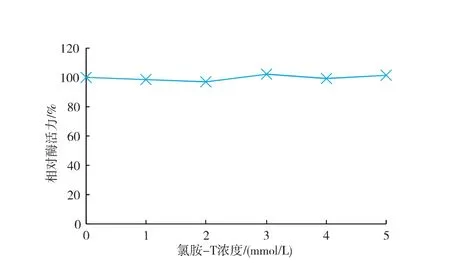
图5 氯胺-T浓度对蕹菜叶POD酶活力的影响Fig. 5 Effect of Chloramine-T on activity of POD from Ipomoea aquatica Forsk leaves
2.6丝氨酸残基的化学修饰
苯甲基磺酰氟(PMSF)可以与蛋白质中的丝氨酸残基相互作用[16]。实验结果表明:PMSF对蕹菜叶POD酶活几乎无影响,说明丝氨酸残基可能不是该酶活性中心的必需基团,见图6。
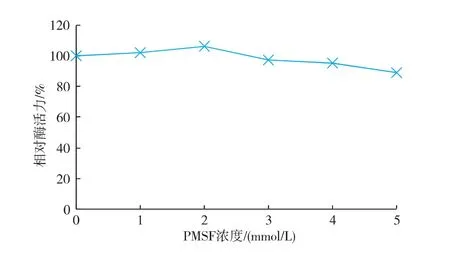
图6 PMSF浓度对蕹菜叶POD酶活力的影响Fig. 6 Effect of PMSF on activity of POD from Ipomoea aquatica Forsk leaves
2.7酪氨酸酚羟基的化学修饰
N-乙酰咪唑(NAI)能对蛋白质中酪氨酸残基的酚羟基进行修饰,从而改变蛋白质的空间构象和特性[17]。实验结果表明:N-乙酰咪唑(NAI)对蕹菜叶POD活性几乎无影响,见图7。由此说明酪氨酸的酚羟基可能不是该酶活性中心的必需基团。
2.8二硫键的化学修饰
巯基化合物二硫苏糖醇(DTT)是一种强的还原剂,能特异性的与蛋白质中二硫键作用,阻止半胱氨酸之间形成分子内或分子间二硫键,并稳定了蛋白质内部的巯基。当DTT浓度升高时,酶活力逐渐升高,进一步说明巯基很有可能是蕹菜POD活性中心的必需结构,见图8。
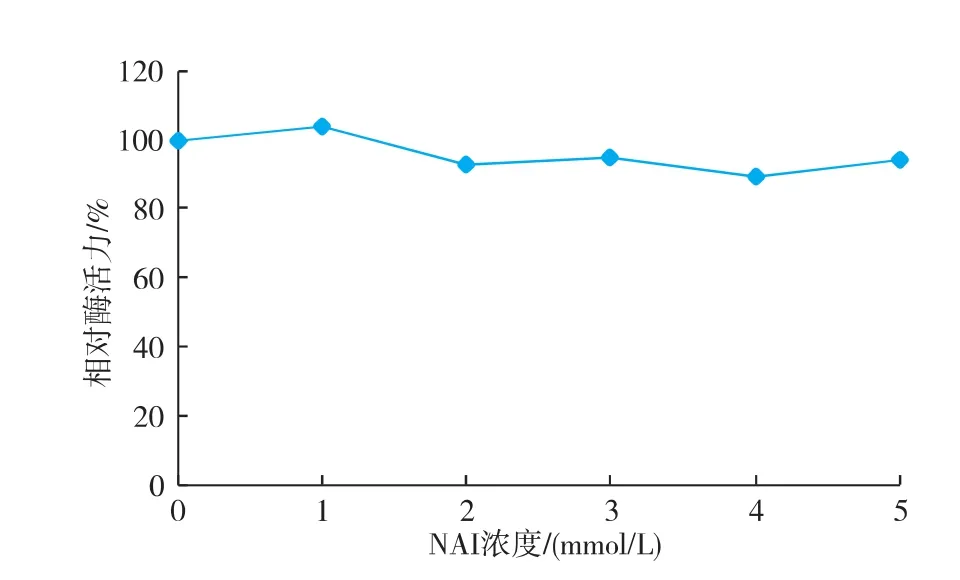
图7 NAI浓度对蕹菜叶POD酶活力的影响Fig. 7 Effect of NAI on activity of POD from Ipomoea aquatica Forsk leaves
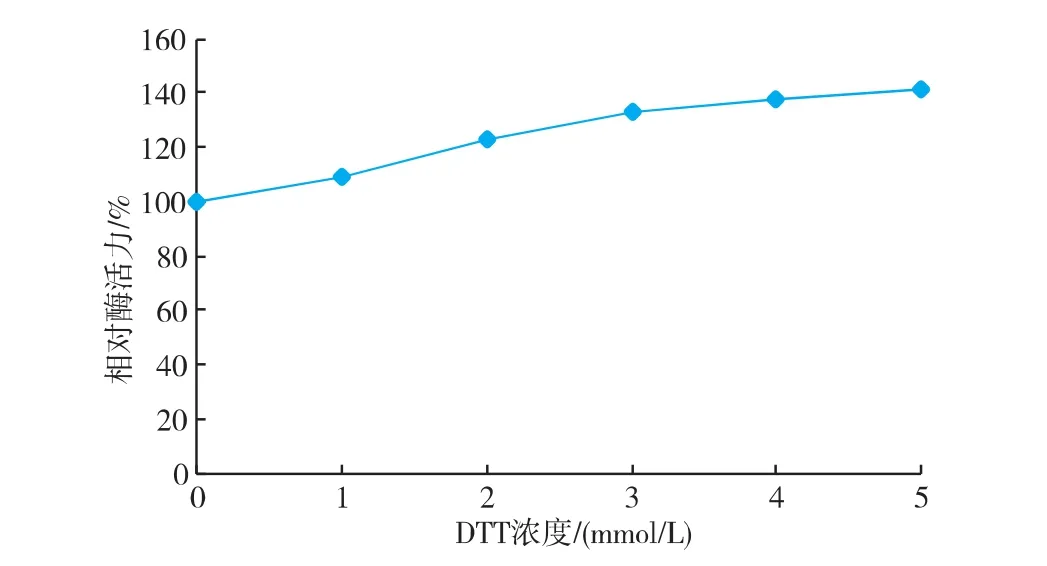
图8 DTT浓度对蕹菜叶POD酶活力的影响Fig. 8 Effect of DDT on activity of POD from Ipomoea aquatica Forsk leaves
3 结语
蛋白质化学结构和空间结构共同决定其生物活性,如果其化学结构不变,而空间结构遭到破坏从而导致蛋白质生物学功能的丧失,称为蛋白质变性或去折叠;反之,如果蛋白质化学结构发生改变才称为蛋白质的化学修饰。在有些情况下,蛋白质化学结构改变并不影响本身的活性,这些修饰是非必需部分的修饰。但是在大多数情况下,蛋白质化学结构的改变将导致生物活性的下降,甚至完全丧失[11]。因此,为了分析蛋白质中处于活性部位并为蛋白质发挥特定功能所必需的氨基酸,人们研制出各种小分子化学修饰剂。常见的修饰剂包括乙酰咪唑、卤代乙酸、N-乙基马来酰亚胺、焦碳酸二乙酯、四硝基甲烷、聚乙烯吡咯烷酮、乙二酸/丙二酸的共聚物、羧甲基纤维素、乙烯/顺丁烯二酰肼共聚物、聚氨基酸、葡聚糖、环糊精、PEG等[18-19]。
作者利用专一性化学修饰剂乙酰丙酮(BD)、二巯基苏糖醇(DTT)、氯胺-T、溴代乙酸(BrAc)、对氯汞苯甲酸(PCMB)、苯甲基磺酰氟(PMSF)、N-乙酰咪唑(NAI)分别对精氨酸残基、二硫键、甲硫氨酸硫醚基、组氨酸残基、巯基、赖氨酸残基、丝氨酸、酪氨酸酚羟基进行了修饰。结果表明:精氨酸残基、赖氨酸残基、组氨酸残基和巯基是蕹菜过氧化物酶发挥活性的必需基团,而甲硫氨酸硫醚基、丝氨酸残基和酪氨酸酚羟基可能不是蕹菜叶过氧化物酶活性中心的必需基团。
参考文献:
[ 1 ] Liu W,Kumar J,Tripathy S,et al. Enzymatically synthesized conducting polyaniline[J]. J Am Chem Soc,1999,121(1):71-78.
[ 2 ] Nakamoto S,Machida N. Phenol removal from aqueous solutions by peroxidase 2 catalyzed reaction using additives [J]. Wat Res,1992,26(1):49-54.
[ 3 ] Zheng X,Van Huystee R B. Oxidation of tyrosine by peroxidase isozymes derived from peanut suspension culture medium and by isolated cell walls[J]. Plant Cell,Tissue and Organ Culture,1991,25:35-44.
[ 4 ] Christensen J H,Bauw G,et al. Purification and characterization of peroxidases correlated with lignification in poplar xylem[J]. Plant Physiology,1998,118:125-135.
[ 5 ] Passardi F,Penel C,Dunand C. Performing the paradoxical:how plant peroxidases modify the cell wall [J]. Trends in Plant Science,2004,9:534-540.
[ 6 ]丁薪源,曹建康.果蔬过氧化物酶酶学特性研究进展[J].食品科技,2012,37(10):62-66. DING Xinyuan,CAO Jiankang. Characteristics of peroxidase from fruit and vegetable research progress [J]. Food Science,2012,37(10):62-66.(in Chinese)
[ 7 ]李宗妍,曹立民,林洪,等.水产品中恩诺沙星残留的一步法酶联免疫检测研究[J].食品科学,2009,30(10):231-235. LI Zongyan,CAO Limin,LIN Hong,et al. Development of one-step enzyme-linked immunoassay for determining enrofloxacinresidues in sea foods[J]. Food Science,2009,30(10):231-235.(in Chinese)
[ 8 ]钟薇,秦培勇,刘长霞,等.辣根过氧化物酶修饰电极的电化学研究[J].北京化工大学学报:自然科学版,2009,36(2):18-22. ZHONG Wei,QIN Peiyong,LIU Changxia,et al. Electrochemistry of horseradish peroxidase immobilized on a modified electrode [J]. Journal of Beijing University of Chemical Technology:Natural Science Edition,2009,36(2):18-22.(in Chinese)
[ 9 ] LA ROTTA C E,BON E P. 4-Chlorophenol degradation by chloroperoxidase from Caldariomyces fumago:formation of insoluble products[J]. Applied Biochemistry and Biotechnology,2002,98(3):191-204.
[10]冯东,李雪梅,王丙莲,等.用辣根过氧化物酶生物传感器测定啤酒中的过氧化氢[J].酿酒科技,2011,12:37-39. FENG Dong,LI Xuemei,WANG Binglian,et al. Determination of hydrogen peroxide in beer by immobilized horseradish peroxidase biosensor[J]. Liquor-making Science&Technology,2011,12:37-39.(in Chinese)
[11]严锐,黄金营.蛋白质化学修饰的研究进展[J].化学工业与工程,2005,22(1):53-55,76. YAN Rui,HUANG Jinying. Progress in chemical modification of protein [J]. Chemical Industry and Engineering,2005,22 (1):53-55,76.(in Chinese)
[12] CHEN Y Z,WANG Y R. A study on peroxidase in latches pericarp [A]. In:Acta Botanical Austro Sinica Vol.5 [C]. Beijing:Science Press,1989:47-52.(in Chinese)
[13]郭勇.酶工程[M].北京:科学出版社,2004:162.
[14] William M,Eberhard U M. Chemical modification of histidine residues of rabbit hemopexin [J]. Archives of Biochemistry and Biophysics,1976,176(2):431-441.
[15]陈清西,陈素丽,朱凌翔,等.长毛对虾碱性磷酸酶功能基团的研究[J].厦门大学学报:自然科学版,1996,35(4):587-591. CHEN Qingxi,CHEN Suli,ZHU Lingxiang,et al. Functional group research of alkaline phosphatase from Penaeu spenicillatus [J]. Journal of Xiamen University:Natural Science,1996,35(4):587-591.(in Chinese)
[16]张洪渊,刘克武,姜云,等.背角无齿蚌碱性磷酸酶的功能基团研究[J].水生生物学报,1997,21(4):347-352. ZHANG Hongyuan,LIU Kewu,JIANG Yun,et al. Functional groups research of alkaline phosphatase from anodonta woodiana heude[J]. Acta Hydrobiologica Sinica,1997,21(4):347-352.(in Chinese)
[17]刘稳,方靖,高培基.豆壳过氧化物酶的盐酸胍变性与化学修饰研究[J].中国生物化学与分子生物学报,1999,15(5):804-805.LIU Wen,FANG Jing,GAO Peiji.The effects of Guanidine Hydrochloride on denature and chemical modification of Soybeanhull peroxidase(SHP)[J]. Chinese Journal of Biochemistry and Molecular Biology,1999,15(5):804-805.(in Chinese)
[18] Inada Y 1,Furukawa M,Sasaki H,et al. Biomedical and biotechnological applications of PEG- and PM-modified proteins[J]. Trends Biotechnol,1995,13(3):86-91.
[19] Veronese F M. Peptide and protein PEGylation:a review of problems and solutions[J]. Biomaterials,2001,22(5):405-417.
Chemical Modification of Functional Groups of Peroxidase from Leaves of Ipomoea aquatica Forsk
WANG Hongyang,SUN Caiyun,HUANG Mang,TANG Yunming*
(School of Life Science,Southwest University,Chongqing 400715,China)
Abstract:In order to identify the functional groups of peroxidase from the leaves of Ipmoea aquatica Forsk,peroxidas were isolated,purifiedandselectively modified by using BD,DTT,pCMB,Maleic anhydride,Chloramine-T,PMSF,NAI and BrAc separately and the change on activity were determined. The result showed that Arg,Lys,His and sulfhydryl involving in the composition of the enzyme active center should be considered as indispensable functional groups of peroxidase,while Met,Ser and Tyr residues should not be because they were not directly related to the activity of peroxidase from Ipomoea aquatica Forsk.
Keywords:Ipomoea aquatica Forsk,peroxidase,functional groups,chemical modification
*通信作者:唐云明(1960—),男,四川武胜人,农学博士,教授,主要从事蛋白质与酶工程方面的研究。E-mail:tbright@swu.edu.cn
基金项目:重庆市重点科技攻关项目(CSTC,2011AB1027)。
收稿日期:2014-07-29
中图分类号:Q 55
文献标志码:A
文章编号:1673—1689(2016)02—0192—05
——蕹菜

