髂股静脉血栓综合征的腔内治疗
杨心蕊 陆信武叶开创 殷敏毅 李维敏 黄新天 陆 民 秦金保 蒋米尔上海交通大学医学院附属第九人民医院血管外科 上海交通大学血管病诊治中心,上海 200011
髂股静脉血栓综合征的腔内治疗
杨心蕊 陆信武*叶开创 殷敏毅 李维敏 黄新天 陆 民 秦金保 蒋米尔
上海交通大学医学院附属第九人民医院血管外科 上海交通大学血管病诊治中心,上海 200011
摘要:目的评价腔内支架植入术治疗髂股静脉血栓形成后遗症的治疗效果。方法回顾性分析2007-12—2013-12上海交通大学医学院附属第九人民医院血管外科收治的179例髂股静脉PTS患者(187条肢体),评价近中期支架通畅率及临床改善情况。结果技术成功率为95.2%,平均植入支架2.0枚。术中发现血管穿孔38例,均为自限性,无围手术期死亡、肺栓塞及出血等严重并发症。术后随访平均33个月,3年一期通畅率为69.6%,二期通畅率为92.0%。Villalta评分由术前(21.0±5.1)分至术后(9.7±3.5)分(P<0.001),差异具有统计学意义。结论目前腔内支架植入术可以作为治疗中重度PTS患者的首选方案。
关键词:深静脉血栓形成后综合征;髂股静脉;支架植入术
深静脉血栓形成后综合征(Postthrombotic syndrome,PTS)是继发于下肢深静脉血栓形成(Deep vein thrombosis,DVT)后,由于静脉回流障碍,下肢静脉高压而引起一系列症状和(或)体征。DVT患者即使经过正规抗凝治疗,也将有20%~50%患者发生PTS,PTS在髂股段或者全肢血栓者发生率更高[1,2]。PTS系列症状包括下肢肿胀、静脉性跛行、慢性疼痛以及色素沉着及难愈性溃疡等[3],严重影响患者生活质量,导致劳动力丧失和增加医疗负担[4-7]。既往采用开放性手术治疗PTS患者,但是该方法创伤大并且通畅率偏低,应用受到限制[8]。近年随着血管腔内理念和技术的发展成熟,支架植入术开通髂股静脉闭塞段,改善静脉流出道阻塞已经逐步广泛应用于临床。2007-12—2013-12本中心收治179例髂股静脉PTS患者(187条肢体),采用腔内治疗方法,治疗效果满意。
1 资料与方法
1.1一般资料
回顾性分析2007-12—2013-12上海交通大学医学院附属第九人民医院血管外科收治的179例髂股静脉PTS患者(187条肢体),男性52例,女性127例,年龄28~78岁,平均年龄为(54.4±12.7)岁。左侧下肢148例,右侧下肢39例。CEAP分级:C2者5例(2.6%),C3者54例(28.9%),C4者47例(25.1%),C5者6例(3.2%),C6者75例(40.1%)。Villalta评分为(21.0±5.1)分,所有患者Villalta评分均≥10分,即中重度PTS[910]。DVT病史平均为7.3年(0.5~40年)。所有患者术前均行下肢深静脉顺行造影,明确存在髂股静脉闭塞(图1)。

图1 患者男性,61岁,DVT病史20余年,左侧下肢肿痛伴浅静脉曲张13年。下肢深静脉顺行造影可见左侧髂静脉闭塞,盆腔大量侧支形成
1.2治疗方法
所有操作在数字减影血管造影(Digital substraction angiography,DSA)室完成。根据病变范围选择入路,通常当病变仅为髂静脉时选择病变同侧股总静脉入路,而累及髂股静脉的病变则常以腘静脉作为穿刺入路。腘静脉穿刺点位于腘窝横行皮肤皱褶腘动脉搏动点的外侧0.5~1.0 cm,在临床操作中采用超声或者“路途”透视下直接穿刺,准确度更高。在成功穿刺置管后予以推注肝素(80 U/kg),全身肝素化后行DSA造影检查,确认病变情况。采用强支撑导管配合0.035″Stiff导丝或者0.018″导丝通过病变段,导丝可呈袢状向前推进,从阻力最薄弱处突破,通过闭塞段。导丝在行进过程中可能引起管壁穿孔,如果发现少量造影剂外渗仍然可以继续手术,应旋转球管,调整导丝导管方向,结合髂静脉正常解剖走向,尝试其他通道通过病变段,若有大量造影剂外渗时需要终止手术,可以在几周后再次尝试。在导丝成功通过病变段后跟进导管,退出导丝,在导管内造影,确认导丝导管进入静脉真腔内(图2);有时导管难以跟进,继续跟进导丝,如果导丝位于管腔内,行进过程中应该无阻力感,直至右侧心房可见导丝随心搏跳动。在确认导丝导管位于真腔后,取球囊(直径4~16 mm,长度60~220 mm)自“小”到“大”分步扩张病变部位,开通闭塞静脉(图3)。再取自膨式支架(直径10~16 mm,长度60~150 mm)视病变长度及部位,使用1个或者多个支架全程覆盖病变段(图4、5)。如果在支架释放后扩张不充分,则予以后扩。最终保证静脉血流通畅并且病变血管残余狭窄<30%。术后患者均接受抗凝治疗,3 d低分子肝素(4000 IU/12 h)桥接华法林口服抗凝,调整国际标准化比率(International normalized ratio,INR)至2~3。出院后接受治疗剂量华法林>6个月。

图2 导丝导管通过病变段后,导管内造影证实导丝导管位于下腔静脉内
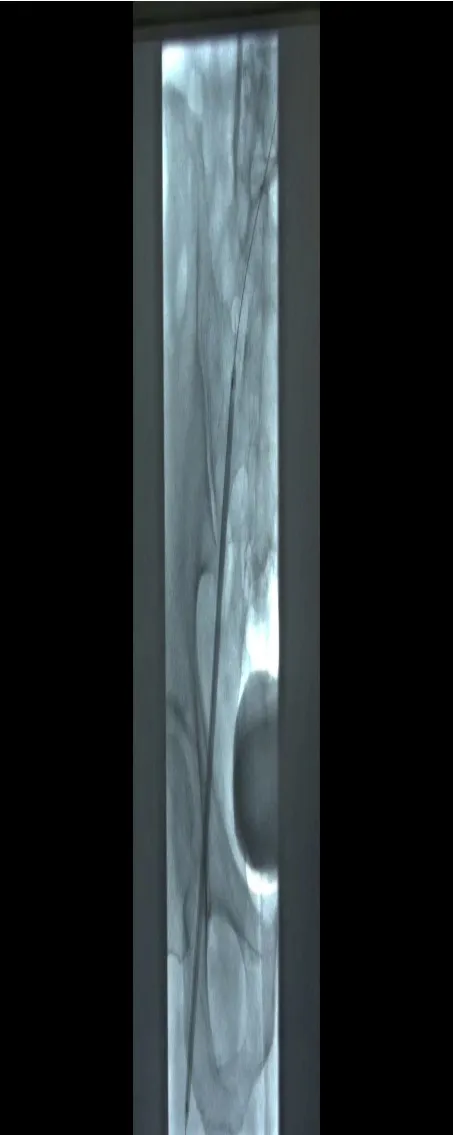
图3 取长球囊,直径由小到大,分步扩张病变段,防止血管撕裂

图4 “路径”引导下准确定位,取WallStent支架(12 mm×90 mm)自病变远心段开始释放,覆盖侧支开口处,保证开通后主干有足够血流量

图5 再取E-Luminexx (12 mm×120 mm)支架,与前一支架重叠3 cm,覆盖病变全程。支架释放后可见股总、髂外、髂总静脉连续性显影,侧支基本消失
1.3随访方法
患者分别于术后3、6、12个月及随后每年门诊随访一次,随访时询问病史并体检,予以超声评估支架通畅情况。如果超声发现支架狭窄/闭塞,行CT血管造影或者静脉造影检查进一步明确病变情况。通畅率为检查度评价狭窄<50%。
1.4统计学分析
连续性变量采用均数±标准差表示,治疗前后采用配对t检验。通畅率应用Kaplan-Meier法进行分析。应用IBM SPSS 22.0软件进行数据分析,P<0.05差异具有统计学意义。
2 结果
共有178条患肢成功开通闭塞静脉并且植入支架,技术成功率为95.2%。另9例失败原因为难以通过闭塞静脉段。平均植入支架2枚(1~3枚)。术中发现血管穿孔38例,均为自限性,回撤导丝后取另一通道上行。无围手术期死亡、肺栓塞及出血等严重并发症。在术后1个月内9例(5.1%)出现支架内早期血栓形成,接受再次腔内治疗。
术后随访平均33个月(1~60个月),失访共18例。3年一期通畅率为69.6%,二期通畅率为92.0%。患者症状体征明显改善,C0-1级者31例(19.4%), C2者7例(4.4%),C3者29例(18.1%),C4者41例(25.6%),C5者33例(20.6%),C6者19例(11.9%)。Villalta评分为(9.7±3.5)分(P<0.001),术前与术后差异具有统计学意义。
3 讨论
PTS是DVT发生后最常见的远期并发症,开通闭塞静脉流出道,改善静脉回流障碍,对中重度PTS患者症状的改善及生活质量的提高具有重要意义。目前国内外资料统计,PTS支架术后1年一期通畅率为79%,二期通畅率为94%[11-13]。本中心随访数据显示3年一期通畅率为69.6%,二期通畅率为92.0%,并发症发生率低,临床症状及体征改善明显。结果提示腔内支架成形术技术成功率高,创伤小,安全有效。
腔内支架植入术应该严格掌握适应证:⑴ 术前影像学检查发现腘静脉和/或以上部位,深静脉存在闭塞而静脉流入道通畅(对髂股静脉段而言,大隐静脉、股浅静脉或者股深静脉均可以作为流入道,应该注意术前评估);⑵ 患肢需要满足Villalta评分≥10分或者临床症状≥C3级,能够定期检测出凝血功能者。目前国内外常用的PTS评价标准是Villalta评分,其结合症状(疼痛、痉挛、沉重感、感觉异常、瘙痒)及体征(胫前水肿、皮脂硬化、色素沉着、浅静脉炎、静脉曲张、腓肠肌压痛、静脉性溃疡),评估PTS病情的严重程度。Villalta评分<5分可以排除PTS,5~9分为轻度,10~14分为中度,≥15分为重度,存在愈合或者未愈合的静脉性溃疡评定为重度PTS[14]。中重度PTS患者可以接受支架成形术治疗,而轻度PTS患者建议穿着弹力袜保守治疗[15]。
保证主干静脉存在足够管腔和回流量,是维持支架通畅的重要因素。PTS是静脉慢性闭塞性疾病,管腔内炎性改变形成纤维束带,单纯的球囊扩张彻底打开,使其贴壁,短期内可能再次闭塞,因此支架植入是必要的。为避免支架内再狭窄,支架两端应该定位于相对正常的血管段,以覆盖病变全程为原则,这是维持术后管腔通畅的关键。必要时支架可以跨过腹股沟韧带,甚至置入股浅/股深静脉[16]。在支架释放后充分后扩,可以增加开通主干静脉管径,减少残余狭窄。Ye等[17]研究发现,在支架释放后侧支显影与早期支架内血栓形成关系密切。因此,支架应该覆盖侧支开口,封闭“分支”,保证主干静脉血流量。
目前最常用的静脉支架是WallStent支架,其编织型结构保证了良好的柔顺性,但是在释放过程中支架前段可能发生短缩,因此在定位时最好突入下腔静脉2~3 cm,以不碰到对侧为宜,避免支架移位和近髂静脉分叉部位支架的再狭窄/闭塞,突入下腔静脉的支架不影响对侧血流。但是在治疗髂股静脉长段病变时单个支架往往难以覆盖全程病变,并且Wallstent支架径向支撑力较差,在治疗PTS病变时即使后扩,支架往往难以充分扩张(尤其在腹股沟韧带处、髂内动脉压迫及髂总动脉处)。本中心经验是在弹性回缩或者压迫明显处选用支撑力强的动脉型支架复合应用;多支架释放顺序由远心段至近心段,由小直径至大直径依次释放,相邻支架首尾重叠,防止支架移位,2支架之间重叠应≥3 cm,以避免再狭窄发生。跨关节支架应该选用柔顺性良好的支架,例如Wallstent支架,可以减少行走活动引起折断的风险。
对中重度PTS患者而言,腔内支架植入术结合规范抗凝治疗能取得良好近中期治疗效果,可以作为目前治疗中重度PTS患者治疗的首选治疗方案[18]。
参考文献
[1]Kahn SR, Shrier I, Julian JA, et al. Determinants and time course of the postthrombotic syndrome after acute deep venous thrombosis. Ann Intern Med, 2008, 149(10): 698-707.
[2]Prandoni P, Lensing AWA, Cogo A, et al. The long-term clinical course of acute deep venous thrombosis. Ann Intern Med, 1996, 125: 1-7.
[3]Enden T, Haig Y, Kløw NE,et al. Long-term outcome after additional catheter-directed thrombolysis versus standard treatment for acute iliofemoral deep vein thrombosis (the CaVenT study): a randomised controlled trial. Lancet, 2012,379(9810): 31-38.
[4]Gillespie DL, Writing Group IIIotPVS, Kistner B, et al. Venous ulcer diagnosis, treatment, and prevention of recurrences. J Vasc Surg, 2010, 52(5 Suppl): 8S-14S.
[5]Kahn SR, Shbaklo H, Lamping DL, et al. Determinants of health-related quality of life during the 2 years following deep vein thrombosis. J Thromb Haemost, 2008, 6(7): 1105-1112.
[6]Guanella R, Ducruet T, Johri M, et al. Economic burden and cost determinants of deep vein thrombosis during 2 years following diagnosis: a prospective evaluation. J Thromb Haemost, 2011, 9(12): 2397-2405.
[7]倪冷,叶炜,刘昌伟,等. 深静脉血栓后综合征的诊治策略[J]. 临床外科杂志,2012,20(5):365-367.
[8]Jost CJ, Gloviczki P, Cherry KJ Jr, et al. Surgical reconstruction of iliofemoral veins and the inferior vena cava for nonmalignant occlusive disease. J Vasc Surg, 2001, 33(2): 320-327.
[9]Villalta S, Bagatella P, Piccioli A, et al. Assessment of validity and reproducibility of a clinical scale for the post-thrombotic syndrome. Haemostasis, 1994, 24(Suppl. 1): 157a.
[10] 田锦林,王伟,李云松,等. 下肢深静脉血栓后综合征的诊断及预测因素[J]. 血栓与止血学,2015,(2):122-124.
[11]Razavi MK, Jaff MR, Miller LE. Safety and Effectiveness of Stent Placement for Iliofemoral Venous Outflow Obstruction: Systematic Review and Meta-Analysis. Circ Cardiovasc Interv, 2015, 8(10): e002772.
[12]Rosales A1, Sandbaek G, Jørgensen JJ. Stenting for chronic post-thrombotic vena cava and iliofemoral venous occlusions: mid-term patency and clinical outcome. Eur J Vasc Endovasc Surg, 2010, 40(2): 234-240.
[13]Raju S, Darcey R, Neglén P. Unexpected major role for venous stenting in deep reflux disease. J Vasc Surg, 2010, 51(2): 401-408.
[14]Kahn SR, Comerota AJ, Cushman M, et al. The postthrombotic syndrome: evidence-based prevention, diagnosis, and treatment strategies: a scientific statement from the American Heart Association. Circulation, 2014, 130(18): 1636-1661.
[15]Yin M, Shi H, Ye K, et al. Clinical Assessment of Endovascular Stenting Compared with Compression Therapy Alone in Postthrombotic Patients with Iliofemoral Obstruction. Eur J Vasc Endovasc Surg, 2015, 50(1): 101-107.
[16]Mahnken AH, Thomson K, de Haan M, et al. CIRSE standards of practice guidelines on iliocaval stenting. Cardiovasc Intervent Radiol, 2014, 37(4):,889-897.
[17]Ye K, Lu X, Jiang M, et al. Technical details and clinical outcomes of transpopliteal venous stent placement for postthrombotic chronic total occlusion of the iliofemoral vein. J Vasc Interv Radiol, 2014, 25(6):,925-932.
[18]Raju S. Best management options for chronic iliac vein stenosis and occlusion. J Vasc Surg, 2013, 57(4): 1163-1169.
Endovenous treatment for postthrombotic syndrome
YANG Xin-ruiLU Xin-wu*YE Kai-chuangYIN Min-yiLI Wei-minHUANG Xin-tianLU MinQIN Jin-baoJIANG Mi-er
Department of Vascular Surgery, Shanghai Ninth People’s Hospital Affiliated to Shanghai JiaoTong University School of Medicine, and Vascular Center of Shanghai JiaoTong University, Shanghai 200011, China
Abstract:ObjectiveTo evaluate the efficacy of endovenous stenting for postthrombotic syndrome (PTS) in iliac-femoral veins. Methods179 patients (187 limbs) with iliac-femoral vein stenosis/occlusion were treated by stent implantation from December 2007 through December 2013 were retrospectively reviewed. Patency rate and clinical improvements were analyzed. ResultsTechnical success rate was 95.2%. The mean number of stent implantation was 2.38 perforation were found during the procedures, they were all self-limited. No severe complications and peri-operative deaths were occurred. Mean follow-up was 33 months. Primary patency rate and secondary patency rate at 3 years were 69.6% and 92.0%. Villalta Score was 9.7 nica after operations, which was significantly increased (P<0.001). ConclusionsStent implantation in iliac-femoral veins can be a first-line treatment for moderate-severe PTS patients.
Key words:Postthrombotic syndrome; Iliac-femoral vein; Stent
*通信作者:陆信武,E-mail:luxinwu@aliyun.com
基金项目:国家自然科学基金(81370423);上海市科学技术委员会引导类项目(134119a2100);上海市科学技术委员会引导类面上项目(15411967300)
文章编号:2096-0646.2016.02.01.06

