生物过程工程研究在创新生物医药开发中应用的驱动力
——生物反应器
孙杨,聂简琪,刘秀霞,杨艳坤,戴晓峰,白仲虎(粮食发酵工艺与技术国家工程实验室,江南大学,江苏 无锡 214122)
生物过程工程研究在创新生物医药开发中应用的驱动力
——生物反应器
孙杨,聂简琪,刘秀霞,杨艳坤,戴晓峰,白仲虎
(粮食发酵工艺与技术国家工程实验室,江南大学,江苏 无锡 214122)
摘要:近年创新生物医药在生物产业中的比重逐渐增大,也给生物产业带来了巨大的经济效益,靶点筛选及分子构建等上游技术的进步是促进生物医药进步的主要原因。随着目前细胞培养技术在生物医药生产中的广泛应用,对细胞培养技术的要求也不断提高,同时细胞培养技术的实现载体——生物反应器的技术改进和创新也越发凸显其重要性。本文介绍了生物反应器在创新生物医药产业中的应用种类、发展趋势及发展驱动力,回顾了全球范围内新型生物反应器的发展成果,包括新型反应器技术及过程分析技术在生物医药中的应用,最后,分析了中国生物反应器的发展现状与问题,指出了生物反应器的发展与进步应以提高生物培养过程的稳定性最终提高产品的质量而不是以提高产量为主要目标。本文详细阐述现代生物反应器技术及基于“质量源于设计”的质量控制理念在其中所起到的关键作用,以及生物反应器的技术发展的现状和未来走向。
关键词:生物反应器;生物过程工程;质量源于设计;过程分析技术;创新生物医药;生物工程;微反应器
第一作者:孙杨(1988—),男,博士研究生,研究方向主要为生物过程工程研究及高通量技术应用。联系人:白仲虎,教授,博士生导师,研究领域包括QbD导向的生物过程工程优化策略及高通量生物反应器的研发、治疗性抗体片段药物的开发、临床免疫分析技术产品的研发等。E-mail baizhonghu@jiangnan.edu.cn。
近20年来全球工业生物技术产业发展迅猛,尤其是生物医药和大宗化学品的生物制造技术产业。全球生物医药产业迅速发展,据美国相关机构2013年统计全球生物医药产值约1997亿美元[1-2],在2010—2020年间将保持年均速13.5%左右,到2020年接近5000亿美元的产值[3]。而基于“细胞培养”技术的蛋白质医药已成为生物医药的重要组成部分[4],中国生物医药市场未来5~10年的发展主流也将会与世界生物技术药物发展方向一样,重点发展重组蛋白药物,尤其是基于哺乳细胞培养生产人源化和全人源治疗性抗体产业的显著进步[5-6],目前辉瑞、葛兰素史克、强生等国际创新生物医药研发机构在细胞培养过程工程研究中确实取得了巨大的进步和发展。这些发展也同样推动了生物医药开发中过程工程研究从方法学到技术手段的飞速进步。生物医药过程工程开发、研究策略和方法的发展体现在硬件技术平台和理念两个方面。硬件方面指的是实施规模化生物反应的核心装置生物反应器,理念指的是ICH Q8、Q10和Q11中所提倡的“设计决定质量”(quality by design,QbD),并在产品质量和稳定性为主要目标下达到生物医药生产过程研发和产品质量控制的目的[7-10]。本文从生物医药产业的发展现状、市场规模、未来发展趋势入手,阐述现代生物反应器技术及基于QbD的质量控制理念在其中所起到的关键作用,以及生物反应器的技术发展的现状和未来走向。
1 生物反应器在创新生物医药开发应用中的种类、发展驱动力与发展趋势
1.1生物反应器的类型与应用
目前生物医药开发技术的基础研究和工业化技术在过去十几年里突飞猛进,鉴于生物反应体系的多样性和目标的复杂性,生物反应器发展出诸多的种类。截至目前,应用于创新医药开发的生物反应器的相关基础技术研究、产品设计创新、制造技术革新是一个全球范围内的关注热点。表1根据主要生物反应器的生物技术应用领域对生物反应器的分类做出简要总结。
1.2全球范围内生物反应器发展的驱动力
全球生物医药产业和新型治疗技术手段日新月异的发展对规模化哺乳细胞培养技术提出了更高的要求。包括生产效率的提高、产品质量的稳定、生产过程成本的控制。例如在人源化治疗性抗体的发展,全球治疗性抗体市场在2011年已达到446亿美元,并保持5.3%的年增速,预计在2016年将达到600亿美元市场总值。
各种细胞培养技术在现代生物医药技术中占据了绝对控制的地位。从1995—2011年间,欧盟医药管理局(EMA)所批准的所有生物医药中,78.3%需要用细胞培养技术来生产,而生物反应器是实现各类细胞培养的基石。CHO细胞、大肠杆菌、酵母细胞占到了欧盟EMA所批准的生物药生产用细胞系的83.4%以上。各种细胞培养技术对生物反应器有着不一样的技术要求和培养规模需要[12]。
全球生物过程工程的研发理念进步巨大。目前国际上生物医药研发巨头如辉瑞、GSK、强生等医药生产研发公司等在推动创新生物医药发展过程中,也推动了动物细胞培养过程工程的研究理念和方法的进步。这些进步是从技术手段、方法、研究理念和目标等方面与传统工业生物技术的开发有所区别。其中主要的理论来源是人用药物注册技术要求国际协调会议ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use)公布的标准 Q8、Q10和Q11中提倡的“质量源于设计”的概念,其主要是指在具体实施生物医药生产过程研发及质量控制的过程中,要以产品的稳定性和质量为最高的目标,其具体的实施过程是前期通过实验设计(design of experiment,DoE)、多变元参数分析(multivariate analysis,MVA)和过程分析技术(process analytical technology,PAT)以及对细胞动态代谢生理学的研究基础上对细胞培养生长的整个过程有一个深入的了解,通过以上技术手段确定产品生产过程中与质量相关的关键过程参数(critical process attributes,CPAs),收集多次细胞培养过程的过程参数,建立培养过程批式模型,最终建立细胞培养过程关键过程参数和保证产品质量的过程设计空间,以获得在产品生产过程细胞培养控制的可执行方案,最终实现在生物医药生产过程中,对产品质量的控制不只是对最终产品的质量检测控制,主要是实现培养过程的空间设计及过程监控。但是在实施多变元批式模型的建立过程中,考虑到生物医药过程研究高成本的因素,希望建立一个合适合理的过程缩小(scale down)策略,通过实验室规模的细胞培养建立过程空间模型来指导生产规模控制。而这些过程缩小策略也必须依赖于生物反应器的技术进步,最新的生物反应器技术手段发展包括:细胞株筛选与评价中采用高通量培养技术,基于微型生物反应器的平行培养技术,以及基于微流控的微型生物反应器技术。生物过程工程研究理念的革新,可以大大提高生物过程工程研究的效率。目前在蛋白质医药研究的过程开发中,可以达到在数月内,快速实现“从DNA到成熟工艺”的整个开发过程。
1.3生物反应器的技术发展趋势与市场
1.3.1一次性生物反应器
在实现细胞培养工艺要求的条件下,为提高生产过程的灵活性、降低过程污染、减少规定设备的巨大资金投入、有效控制产品开发的风险,近10年来,一次性生物反应器(disposable bioreactor)是生物医药产业中生物反应器的最为突出的发展方向[13-15]。用于悬浮细胞培养的搅拌式(STR)一次性生物反应器的工作体积已经可以达到2000L的规模;波浪式(wave bag)一次性生物反应器的体积也可以达到1000L的规模;用于贴壁细胞培养的固定床式的一次性生物反应器体积也已达到500L的规模。图1总结了目前国外的几种主要一次性生物反应器和其工作体积。
近年来由于免疫细胞治疗技术在临床应用方面取得了突破性的进展,比如DC-CIK细胞治疗和嵌合抗原受体T细胞技术(CAR-T)[16-17]针对病人个体的T细胞扩增培养,也进一步扩展了一次性生物反应器的应用范围。事实上体积相对较小的一次性生物反应器对细胞免疫治疗这个新兴治疗技术的广泛临床应用将起到巨大的技术支撑作用。

图1 国外几种主要供应商生产的细胞培养用一次性生物反应器
全球一次性生物反应器的市场规模在2014年就达到了2.02亿美元,并将保持18.4%的增长,预计在2019年达到4.7亿美元。目前一次性生物反应器的市场主要集中在北美和西欧,预计在未来的5年内,新兴国家的一次性生物反应器市场会快速增长[18]。国际上的主要一次性生物反应器供应商为:Thermo Fischer Scientific,Inc.(美国),Sartorius AG(德国),Merck KGaA(德国),GE Healthcare(美国)以及Pall Corporation(美国)。我国在此技术领域尚属刚刚起步阶段,尚无规模化生产能力。
1.3.2高通量微型生物反应器
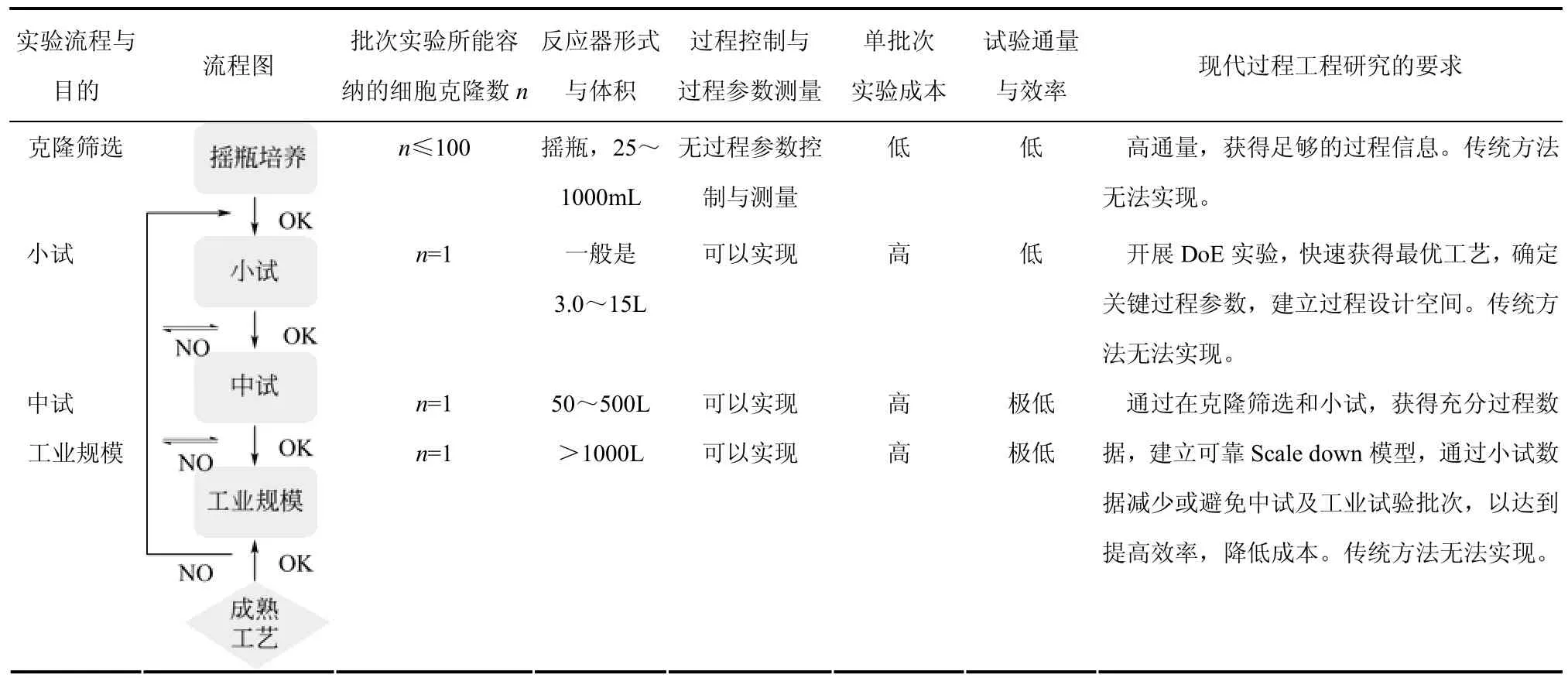
表2 传统生物过程工程研究中的技术手段及实验流程与现代生物过程工程研究需要的矛盾对比
微型生物反应器的技术进步是生物反应器产业的另一个显著特点。研究生物反应器的微型化、平行化以及自动化,以适应与生物过程工程研究的高通量需求,是近10年来生物过程工学科内相关科学仪器研究的一个热点[19-21]。其驱动力来自传统意义上的过程研究技术手段已无法满足现代生物过程工程的技术需求。传统的生物过程工程研究流程与技术手段与现代生物过程研究需要的矛盾总结于表2。由表中可以发现,传统方法采用的是“串行”流程,效率和针对细胞克隆研究的通量均较低,无法满足现在生物过程工程研究的需要。针对表2中指出的这些矛盾,目前国外在高通量平行细胞培养仪器研究主要集中在两个核心点:①为提高培养的通量,尽量减小反应器体积,即采用不同形式的微型(毫升甚至微升级)生物反应器[22];②为对细胞培养过程有深刻的理解,在高通量培养过程中,尽量实现多个不同形式的高通量平行细胞培养系统被报道,或者已经成功商业化。但是,限于目前工业技术和相关基础科学发展的现状,鲜见能够完美地同时解决上述两个问题的系统。也有一些系统为了同时考虑到解决这两个方面的需要,降低仪器系统的普适性,仅针对一类细胞的培养,比如美国的SIMCELLTM(Bioprocessors,Woburn,MA 01801,USA)微流体反应器系统仅适用于哺乳细胞,英国的Ambr(TPA Biosystems,UK)微反应器细胞培养系统也仅针对哺乳细胞培养。
2 全球范围内新型生物反应器发展成果
2.1用于生物过程开发的微型生物反应器和一次性生物反应器
高通量的微型生物反应器在生物过程工程开发中起着越来越重要的作用[23]。近10年来,已商业化生产的该类生物反应器种类繁多,比如10mL级的微型生物反应ambrTM15和ambrTM250系统(Sartorius)、100mL级的德国Dasgip平行细胞培养系统、Applikon的Mini-bioreactor、瑞士Inforis公司的平行细胞培养系统等。这种形式的生物反应器具有高度的过程操作灵活性,可以完全模拟大型规模化反应器内的细胞生长环境,可以平行开展多个培养条件下的过程,可以实施批式、流加批式、连续培养等多种培养方式。该形式的反应器可用于疫苗生产的悬浮细胞培养和微载体细胞培养过程,也可以应用于CHO细胞培养的治疗性抗体生产和各种微生物细胞的培养。以病毒疫苗生产为例,在MDCK细胞培养生产流感病毒疫苗[24],VERO细胞悬浮培养生产HSV I和Polio I病毒疫苗[25]的生产过程,VERO细胞微载体悬浮培养生产流感病毒疫苗[26],HEK293悬浮细胞培养生产狂犬病毒疫苗[27]等。
2.1.1纤维载体的固定床反应器(ATMI LifeSciences 的iCELLis™)
ATMI LifeSciences的iCELLis™是第一个完全一体化,一次性使用的高细胞密度生物反应器[28]。它是由医用级的聚脂微纤维(polyester microfibers)作为微载体,微载体压缩后固定于固定床上,纤维状载体比表面积非常高,相对于传统的STR反应器来说,达到相同数目的细胞的基础上,可以使细胞培养体积降低20倍以上(表3)。反应器设计操作极为简单方便,大大降低了传统STR反应器用于微载体细胞培养过程中的一些耗时操作,比如设备灭菌、微载体的处理等[29-31]。在使用iCELLis用于细胞培养可以省去逐级培养放大过程,可以在较低的细胞浓度下接种,比如,使用6个传统滚动瓶培养(1750cm2)就足够用于接种iCELLis 1000生物反应器(55L)。在培养过程中磁力搅拌驱动培养基在固定床中均匀分布,这种搅拌形式可以有效地减小细胞受到剪切力的机械损伤,从而可以增大培养过程活细胞比例。iCELLis的氧传递模式是一种独特的“瀑布”式传氧策略,这种形式是使培养基由反应器底部运动到反应器顶部,再由顶部以薄膜的形式从外壁滑落,使固定床上的载体能不断的充分与新鲜的培养基接触,实现氧的传递,保证了反应器内的传氧系数kLa保持较高水平。并且iCELLis采用了一次性固定床反应系统,下游纯化阶段无需离心分离细胞,iCELLis反应器系统的固定床结构如图2所示。
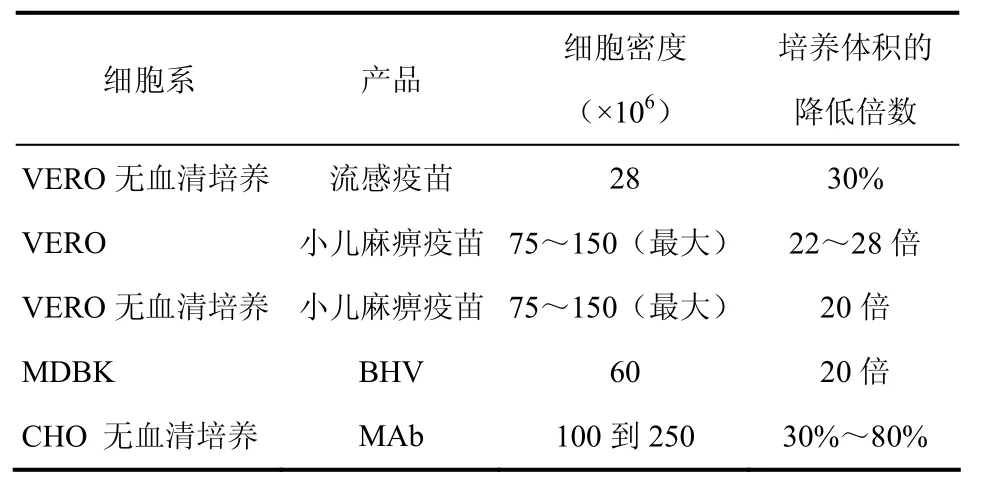
表3 iCELLis固定床细胞培养反应器验证研究结果
2.1.2一次性细胞培养生物反应器
一次性生物反应器以其独特的优势在以细胞培养为基础的生物医药研发生产中逐渐的得到推广与应用,例如一次性波浪式细胞培养袋是由Wave Bioreactor公司在十几年前(现在属于GE Healthcare)引入的一种独特的一次性细胞培养反应器[32-33]。在实现大规模的悬浮细胞培养时可以实施平行的多数量的该种形式的反应器(multiple bag-type bioreactors),类似的产品也有好多种,例如:荷兰Applikon公司的AppliFlex、CELLution Biotech的CELL-tainer,德国Sartorious的BIOSTAT CultiBag、MetBio、PadReactor公司的Optima and OrbiCell培养袋等。
这种形式的一次性细胞培养反应器已被用于临床细胞免疫治疗[34-35]中的T细胞培养,这种反应器由于体积小、全封闭、一次性使用,特别适合临床上对多个病人的个体细胞进行独立培养扩增,它将对细胞免疫治疗,包括CAR-T这种新兴的个体化医疗手段的普及,起到巨大的支撑作用。
由一次性细胞培养袋开始,目前一次性生物反应器的规模可以达到吨级,形式也拓展到STR的形式[36]。比如GE的Xcellerex[37]一次性STR生物反应器XDR-50~2000。它是单容器模块化的、可放大的一次使用生物反应器,具有标准搅拌式反应器的表现,可以满足从工艺开发到生产的全过程需要。


图2 iCELLis细胞培养反应器系统的固定床结构图
一次性的生物反应器已成为了动物细胞培养技术的发展趋势之一,尤其是生物技术本身的发展,显著提高了细胞系的表达量,比如CHO细胞培养生产治疗性抗体的表达水平已经可以达到10 g/L的水准,所以生产上对于培养体积的要求显著减少,因而一次性生物反应器的培养规模已经可以用于规模化生产。图3总结了一次性细胞培养反应器的发展历程。这种生物反应器在个性化治疗的免疫细胞培养过程中有很好的应用前景[38]。
根据Genetic Engineering & Biotechnology News(GEN)在2015年7月做的调查报告显示一次性生物过程工程装置(包括上、下游)在2013— 2018期间的年增长率将保持38%。50%被调查的公司表示使用量最大的和增长最快的一次性生物过程装置为配液系统,其次是哺乳细胞培养生物反应器,排在第三位的是生物反应器的辅助设备——一次性在线过程参数检测传感器,令人惊讶的是有20%的被调查公司认为一次性微生物生物反应器将保持快速增长。
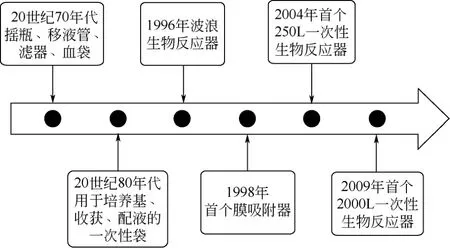
图3 一次性细胞培养生物反应器的发展历程
2.1.3微流体培养系统
微流体培养系统(microfluidic culture system):微流体技术目前在生物行业的到了广泛的应用,如基因芯片、蛋白质芯片、基于流式细胞仪的单液滴细胞分选等,而在用于细胞培养的微流体装置被称为微型生物反应器[39],比如Smart Biosystems公司生产的IVFLAB-6微流体细胞培养系统,CellASCIS公司开发的ONIX微流体灌注细胞培养系统,美国Bioprocessors公司的SimCellTM微型生物反应器系统和Hurel公司的HurelFlow微流控生物反应器等。这些基于微流控的微型生物反应器系统主要用于开展细胞培养过程的优化研究和细胞克隆的高通量筛选,可以显著提高细胞克隆筛选过程的效率与生产过程优化效率。
例如SimCell高通量细胞培养系统,该系统是由4个独立模块组成:①反应器的温控和混合搅拌是由5个培养箱模块控制;②传感器模块通过非接触式pH、溶氧(DO)电极提供溶氧和pH参数的测量;③取样模块功能为从指定反应器内取样并转移到标准多孔板,用于离线参数的分析;④加液模块实现同时向每个反应器内滴加8种液体溶液。实现补料、流加培养基、pH控制时的酸碱补加等功能;⑤第五个模块是自动化机器人系统,实现以上4个模块的整合及自动化操作。SIMCELL的微反应器工作体积为300~800μL,可开展平行培养的最大细胞克隆通量可达1260个/批次。图4是该系统微型生物反应器、系统操作模块的简要示意图。高通量微型生物反应器开展细胞水平培养的过程工程研究,是生物医药过程工程研究技术的发展方向之一。
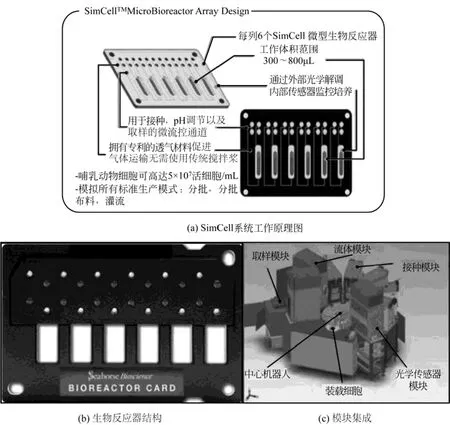
图4 SimCell系统(美国Bioprocessors公司)工作原理图、及生物反应器结构和模块集成

图5 常州英德高通量培养系统
2.1.4高通量细胞培养系统
我国在此领域尚属起步阶段,目前国内高通量微型生物反应器主要处于研发推广阶段,主要有常州英德生物科技有限公司推出的高通量细胞培养系统,如图5,包括高通量细胞培养摇床及与之结合实现自动化移液、接种、取样等功能的高通量移液工作站。该系统可实现基于“三明治板盖”培养方式的高通量平行细胞培养,并可在移液工作站的配合下实现快速的取样以便用于检测,从而实现对细胞库的快速评价,最高通量可实现同时对4608个克隆进行筛选,但此系统无法进行在线参数监控与控制。
2.2生物过程分析技术的进步
2.2.1过程分析技术的概念
生物反应器广泛采用过程分析技术(process analytical technology,PAT)[40-41]以提高人们对反应器内复杂生物反应过程的及时、准确、深入的理解,进而达到控制生物过程质量的目的,是近年来全球范围内生物反应器技术的一个显著进步。
过程分析技术在化学药物和生物医药生产过程中广泛采用的主要推动者是美国FDA和欧盟EMA。他们对PAT的定义是:一种通过及时测量影响关键质量参数(critical quality attributes,CQA)的关键过程参数(critical process attributes,CPAs)的一系列技术,来实现对制药过程的分析、设计和控制。PAT的概念实际上定位于关键过程参数的及时监测(在线、在位和离线),在生物反应过程中的最大价值是实现对生物反应过程本身的质量控制,而不是传统意义上的仅对最终产品的质量进行控而不是传统意义上的仅对最终产品的质量进行控制,以达到所谓设计决定质量的效果。所以可以这样认为:PAT不单单是系列技术手段,它是一种以QbD为核心的技术理念[42- 43]。
2.2.2过程分析技术与装置
较为传统的检测技术和新近发展起来的在线、在位、离线检测技术总结于表4。这些检测技术的联合使用,通过及时理解细胞的生长、代谢、生产的生理学状态参数和反应器内物化环境参数,可以对给定的生物过程有一个较为全面的理解。
目前最显著的发展趋势是使用光谱分析技术,通过在反应器内在反应器内安置传感器,通过光纤传输光谱信号,实现对反应器内细胞的生长、代谢、生产的生理学状态参数的实时在线分析,应用最广泛的是拉曼光谱和近远红外光谱(NIR)。这两个PAT技术手段是以QbD为导向的生物过程研究与实际操作的重要支撑。

表4 传统的检测技术和新近发展起来的在线、离线检测技术总结
国际上主要的拉曼光谱在线检测装置供应商是Kaiser Optical Systems公司,产品为RamanRxn3™。NIR的一个主要供应商是Sartorius Stedim North America,该公司的主要NIR在线检测系统是BioPAT®Spectro。BioPAT Spectro每15s间隔,在950~1750nm波长范围内对生物反应器内培养液做一次扫描,再通过预先建立的数学模型对营养物、代谢产物、产品、细胞活性等过程参数实施实时监测。NIR光谱和拉曼光谱数据会产生巨大的数据,这些数据结合其他检测技术所获得的在线、位、离线参数,作为输入变量组,输入MVA软(SIMCA,件瑞典Umetrics公司)[44],通过研发阶段的多次数据收集,建立过程批式模型和过程操作空间。在实际生产过程中,操作者可以通过实时PAT检测,通过MVA数据分析,对过程状态进行实时综合判断,并可以及时分析出导致过程偏差的原因。这种PAT技术加上多变元分析手段,可以使我们在实际生产中进行真正意义上的生物过程质量检测、分析与控制。MVA技术是PAT技术应用的数据处理基础。这种关系详见图6。

图6 PAT技术与MVA数据处理手段在过程质量控制中的应用
3 我国生物反应器产业的现状与问题
中国作为生物发酵产品大国,生物医药的需求大国,以及潜在的生物医药创新与生产大国,生物反应器产业具有极大发展潜力。但是不可否认的事实是在我国生物技术产业化平台中,细胞大规模培养技术等中下游技术是我国最薄弱的技术环节,我国生物医药等领域产业化与先进国家的差距较大,滞后的一个重要原因就是缺乏配套工艺的工业化放大技术和相应的以生物反应器为核心装备的技术支撑系统。我国目前主要生产一些中低档生物反应器,并且这些反应器主要针对于工业生产中的微生物培养。而在生物医药生产用的高端哺乳细胞培养生物反应器研发与制造方面,跟踪国际上生物反应器的技术进步所做的努力非常有限。这主要由两方面原因:一方面是国家政策导向,尤其是新药审批政策的导向问题;另一方面是生物医药产品的高附加值使得生产企业可以承受较高的设备成本,导致生产企业不愿冒险尝试国产生物反应器装置,对于反应器生产企业而言市场驱动力不大。可以说,目前我国生物医药产业中用于哺乳细胞培养方法生产治疗性抗体和人用疫苗的生物反应器几乎完全依赖进口,主要供应商集中在国际上几个著名公司,包括Sartorius、GE、Simens、Eppendorf、Applikon,只是最近在哺乳细胞培养工艺生产畜用疫苗领域有了一些突破,即在2015年,成都英德生物医药装备技术有限公司为我国的口蹄疫疫苗生产线(兰州中农威特),完全自主生产、设计、安装了单罐批培养体积达到6000 L的VERO细胞悬浮培养生物反应器和配套装置。并且目前我国对于生物医药过程工程的研究理念与发达国家也有一些差距,我国目前还停留在以提高产量为目的的基础上,但对于生物医药产品,生产过程的稳定性、最终产品的质量比产量更重要,而质量的控制在工艺开发阶段就要得到重视,我国就需要在此集中力量,努力改变此领域的现状。
4 结语
生物反应器技术的发展与进步必定会促进生物医药开发的进步,而创新生物医药的发展,在促进国民经济发展,完善疾病治疗手段及方案的同时,也会促进生物过程工程研究的进步,由此带来的进步表现在:硬件上,PAT技术在生物反应器技术上的不断开发及应用;软件上,QbD理念在生物医药生产中的推广和应用。目前,随着一次性生物反应器,微型生物反应器等新型生物反应器的发展与启示,在生物医药技术作为国家发展核心竞争力而越来越得到重视之时,如何实现技术创新、产业创新、产品创新,值得大家思考和共同努力。
参考文献
[1]陳美恩,刘恩廷,陈鹏.全球生物产业发展主要模式及对我国的启示[J].未来与发展,2015(1):27-029.
[2]杨宝盈.全球生物产业的发展模式及对加快我国生物产业集聚的启示[J].经济师,2013(4):60-61.
[3]SAVAGE P,MAHMOUD S. Development and economic trends in cancer therapeutic drugs:a 5-year update 2010—2014[J]. Br. J. Cancer,2015,112(6):1037-1041.
[4]WALTHER J,GODAWAT R,HWANG C,et al. The business impact of an integrated continuous biomanufacturing platform for recombinant protein production[J]. J. Biotechnol.,2015,213:3-12.
[5]TREE J A,RICHARDSON C,FOOKS A R,et al. Comparison of large-scale mammalian cell culture systems with egg culture for the production of influenza virus A vaccine strains[J]. Vaccine,2001,19 (25-26):3444-3450.
[6]LANGER E S. Trends in capacity utilization for therapeutic monoclonal antibody production[J]. MAbs,2009,1(2):151-156.
[7]LEBRUN P,GIACOLETTI K,SCHERDER T,et al. A quality by design approach for longitudinal quality attributes[J]. J. Biopharm. Stat.,2015,25(2):247-259.
[8]RATHORE A S,PATHAK M,GODARA A. Process development inthe QbD paradigm:role of process integration in process optimization for production of biotherapeutics[J]. Biotechnol. Prog.,2015,10.1002/btpr.2209.
[9]YU L X. Pharmaceutical quality by design:product and process development,understanding,and control[J]. Pharmaceutical Research,2008,25(4):781-791.
[10]YU L X,BAKER J,BERLAM S C,et al. Advancing product quality:a summary of the Inaugural FDA/PQRI Conference[J]. AAPS J.,2015,17(4):1011-1018.
[11]CLINCKE M F,MOLLERYD C,ZHANG Y,et al. Very high density of CHO cells in perfusion by ATF or TFF in WAVE bioreactor. Part I. Effect of the cell density on the process[J]. Biotechnology Progress,2013,29(3):754-767.
[12]SARANTOS K,CLEO K. Analysis of the landscape of biologically-derived pharmaceuticals in Europe:dominant production systems,molecule types on the rise and approval trends[J]. European Journal of Pharmaceutical Sciences,2013,48(3):428-441.
[13]LOFFELHOLZ C,KAISER S C,KRAUME M,et al. Dynamic single-use bioreactors used in modern liter- and m(3)- scale biotechnological processes:engineering characteristics and scaling up[J]. Disposable Bioreactors Ii,2014,138:1-44.
[14]EIBL R,KAISER S,LOMBRISER R,et al. Disposable bioreactors:the current state-of-the-art and recommended applications in biotechnology[J]. Applied Microbiology and Biotechnology,2010,86(1):41-49.
[15]EIBL R,LöFFELHOLZ C,EIBL D. Disposable bioreactors for inoculum production and protein expression[J].Methods Mol. Biol.,2014,1104:265-284.
[16]ENBLAD G,KARLSSON H,LOSKOG A S. CAR T-cell therapy:the role of physical barriers and immunosuppression in lymphoma[J]. Hum. Gene Ther.,2015,26(8):498-505.
[17]DAVENPORT A J,JENKINS M R,RITCHIE D S,et al. CAR-T cells are serial killers[J]. Oncoimmunology,2015,4(12):e1053684.
[18]BARBAROUX M,GERIGHAUSEN S,HACKEL H. An approach to quality and security of supply for single-use bioreactors[J]. Adv. Biochem. Eng. Biotechnol.,2014,138:239-272.
[19]LONG Q,LIU X X,YANG Y K,et al. The development and application of high throughput cultivation technology in bioprocess development[J]. Journal of Biotechnology,2014,192:323-238.
[20]BAREITHER R,BARGH N,OAKESHOTT R,et al. Automated disposable small scale reactor for high throughput bioprocess development:a proof of concept study[J]. Biotechnol. Bioeng.,2013,110(12):3126-3138.
[21]AMANULLAH A,OTERO J M,MIKOLA M,et al. Novel micro-bioreactor high throughput technology for cell culture process development:reproducibility and scalability assessment of fed-batch CHO cultures[J]. Biotechnology and Bioengineering,2010,106(1):57-67.
[22]HORTSCH R,STRATMANN A,WEUSTER-BOTZ D. New milliliter-scale stirred tank bioreactors for the cultivation of mycelium forming microorganisms[J]. Biotechnology and Bioengineering,2010,106(3):443-451.
[23]HORTSCH R,WEUSTER-BOTZ D. Milliliter-scale stirred tank reactors for the cultivation of vicroorganisms[J]. Advances in Applied Microbiology,2010,73:61-82.
[24]AGGARWAL K,JING F,MARANGA L,et al. Bioprocess optimization for cell culture based influenza vaccine production[J]. Vaccine,2011,29(17):3320-3328.
[25]PAILLET C,FORNO G,KRATJE R,et al. Suspension-Vero cell cultures as a platform for viral vaccine production[J]. Vaccine,2009,27(46):6464-6467.
[26]CHEN A,POH S L,DIETZSCH C,et al. Serum-free microcarrier based production of replication deficient Influenza vaccine candidate virus lacking NS1 using Vero cells[J]. Bmc. Biotechnology,2011,11:81.
[27]SHEN C F,LANTHIER S,JACOB D,et al. Process optimization and scale-up for production of rabies vaccine live adenovirus vector (AdRG1.3)[J]. Vaccine,2012,30(2):300-306.
[28]KNOWLES S,DRUGMAND J C,LENNAERTZ A,et al. Virus production with the ICELLIS (R) single-use bioreactor[J]. Human Gene Therapy,2014,25(11):A84-A.
[29]RAJENDRAN R,LINGALA R,VUPPU S K,et al. Assessment of packed bed bioreactor systems in the production of viral vaccines[J]. AMB Express,2014,4:25.
[30]VENTINI-MONTEIRO D,DUBOIS S,ASTRAY R M,et al. Insect cell entrapment,growth and recovering using a single-use fixed-bed bioreactor. Scaling up and recombinant protein production[J]. J. Biotechnol.,2015,216:110-115.
[31]LESCH H P,VALONEN P,HEIKKILA K M,et al. iCELLis (R) fixed-bed technology provides an efficient scalable system for viral vector production[J]. Human Gene Therapy,2015,26(10):A25.
[32]EIBL R,WERNER S,EIBL D. Bag bioreactor based on wave-induced motion:characteristics and applications[J]. Disposable Bioreactors,2009,115:55-87.
[33]CLINCKE M F,MOLLERYD C,ZHANG Y,et al. Very high density of CHO cells in perfusion by ATF or TFF in WAVE bioreactor. Part I. Effect of the cell density on the process[J]. Biotechnol. Prog.,2013,29(3):754-767.
[34]SWAIKA A,HAMMOND W A,JOSEPH R W. Current state of anti-PD-L1 and anti-PD-1 agents in cancer therapy[J]. Mol. Immunol.,2015,67(2):4-17.
[35]LUSSIER D M,O'NEILL L,NIEVES L M,et al. Enhanced T-cell immunity to osteosarcoma through antibody blockade of PD-1/PD-L1 interactions[J]. J. Immunother,2015,38(3):96-106.
[36]SHUKLA A A,GOTTSCHALK U. Single-use disposable technologies for biopharmaceutical manufacturing[J]. Trends Biotechnol.,2013,31(3):147-154.
[37]MINOW B,SEIDEMANN J,TSCHOEPE S,et al. Harmonization and characterization of different single-use bioreactors adopting a new sparger design[J]. Engineering in Life Sciences,2014,14(3):272-282.
[38]LEVINE L H. Vaccine manufacturing facilities of the future[R]. London:Vaccines Europe,2010.
[39]ANDERSSON H,VAN DEN BERG A. Microfluidic devices for cellomics:a review[J]. Sensors and Actuators B:Chemical,2003,92(3):315-325.
[40]LANGEMANN T,MAYR U B,MEITZ A,et al. Multi-parameter flow cytometry as a process analytical technology (PAT) approach for the assessment of bacterial ghost production[J]. Appl. Microbiol. Biotechnol.,2016,100(1):409-418.
[41]LOPES J A,COSTA P F,ALVES T P,et al. Chemometrics in bioprocess engineering:process analytical technology (PAT) applications[J]. Chemometrics and Intelligent Laboratory Systems,2004,74(2):269-275.
[42]AKSU B,DE BEER T,FOLESTAD S,et al. Strategic funding priorities in the pharmaceutical sciences allied to quality by design (QbD) and process analytical technology (PAT)[J]. Eur. J. Pharm. Sci.,2012,47(2):402-405.
[43]SCHAEFER C,CLICQ D,LECOMTE C,et al. A process analytical technology (PAT) approach to control a new API manufacturing process:development,validation and implementation[J]. Talanta,2014,120:114-125.
[44]WHEELOCK A M,WHEELOCK C E. Trials and tribulations of 'omics data analysis:assessing quality of SIMCA-based multivariate models using examples from pulmonary medicine[J]. Mol. Biosyst.,2013,9(11):2589-2596.
综述与专论
Pioneering application of biological process engineering in innovative bio-pharmaceutical development——bioreactors
SUN Yang,NIE Jianqi,LIU Xiuxia,YANG Yankun,DAI Xiaofeng,BAI Zhonghu
(National Engineering Laboratory for Cereal Fermentation Technology,Jiangnan University,Wuxi 214122,Jiangsu,China)
Abstract:In recent years,the proportion of innovative biomedical in the biotechnology industry has been increasing gradually,which is mainly due to the improvement of upstream technology such as target screening and molecule construction and brings tremendous economic benefit. With the increasing applications of cell culture technology in biomedical industry,demand for its innovation has been increasing. And so it is with the equipment bioreactors. This review introduced the categories,development trend and driving force of bioreactors in biomedical industry. The achievements of novel bioreactors including the applications of novel bioreactor technology and process analytical technology are also summarized. Finally,we discussed the development status and problems of bioreactor industry in China and pointed out that increasing the product quality rather than production is the goal of bioreactor development. This review also expounded the key role of modern bioreactor technology and the “Quality by Design”principles of ,as well as the developmenet status and trend of bioreactor technology.
Key words:bioreactor; biological process engineering; quality by design; PAT; innovative biopharmaceutical; biological engineering; microreactor
中图分类号:Q 815
文献标志码:A
文章编号:1000–6613(2016)04–0971–10
DOI:10.16085/j.issn.1000-6613.2016.04.001
收稿日期:2015-12-16;修改稿日期:2016-01-06。
基金项目:国家高技术研究发展计划(2015AA020802)及中央高校基本科研业务费专项资金(JUSRP51401A)项目。

