雪上一枝蒿总碱凝胶中雪甲素经皮药动学研究
吴玉梅 陈晓兰 刘文 杨芳芳 唐红艳 戴雅洁

[摘要]该研究结合UPLCMS/MS联用技术,比较雪上一枝蒿总碱凝胶和雪上一枝蒿总碱微乳凝胶中雪上一枝蒿甲素(雪甲素)在小鼠皮肤、血液中的药物浓度随时间的变化过程,并对其药代动力学参数进行比较分析。以探讨微乳制剂在透皮给药制剂中可行性。该试验建立UPLCMS/MS同时测定血浆和皮肤中雪甲素的方法,灵敏度高,符合透皮给药药动学研究要求。微乳凝胶通过皮肤进入血液的主要药动学参数Cmax为(3762±1431) μg·L-1,Tmax为(340±134) h,AUC0∞为(1 0277±260) μg·L-1·h-1,MRT为(3480±1231) h,MRTlast为(1068±057) h,t1/2为(2311±920) h;普通凝胶通过皮肤进入血液的主要药动学参数Cmax为(5223±1590) μg·L-1,Tmax为(400±000) h,AUC0∞为(72860±28080) μg·L-1·h-1,MRT为(2069±398) h,MRTlast为(934±042) h,t1/2为(1469±315) h。结果表明,微乳凝胶较普通凝胶透皮吸收较平稳,作用时间长,生物利用度高,显示微乳凝胶具有良好而稳定的透皮效果。微乳凝胶和普通凝胶中雪甲素在皮肤中的生物利用度差异不明显。
[关键词]雪上一枝蒿总碱;微乳凝胶;普通凝胶;药动学
[Abstract]In this study, the changes of bullatine A in plasma and skin of mice with time in microemulsion gel and ordinary gel of Aconitum brachypodum total alkaloids were compared through UPLCMS/MS, and their pharmacokinetic parameters were also compared and analyzed, to investigate the feasibility of microemulsion agent in the transdermal drug delivery UPLCMS/MS method for simultaneous determination of bullatine A in plasma and skin had high sensitivity and was in line with the pharmacokinetic study requirements for transdermal drug delivery The main pharmacokinetic parameters for microemulsion gel in the plasma were as follows: Cmax=(3762±1431) μg·L-1, Tmax=(340±134) h, AUC0∞=(1 0277±260) μg·L-1·h-1, MRT=(3480±1231) h, MRTlast=(1068±057) h, t1/2=(2311±920) h; main pharmacokinetic parameters for ordinary gel in the blood: Cmax=(5223±1590) μg·L-1, Tmax=(400±000) h, AUC0∞=(72860±28080) μg·L-1·h-1, MRT=(2069±398) h, MRTlast=(934±042) h, t1/2=(1469±315) h The results showed that the microemulsion gel had more stable transdermal absorption, longer duration of action and higher bioavailability than ordinary gel, indicating that the microemulsion gel had a good and stable transdermal effect There was no significant difference in bioavailability of bullatine A in skin between microemulsion gel and ordinary gel
[Key words]Aconitum brachypodum total alkaloids; microemulsion gel; ordinary gel; pharmacokinetic
doi:10.4268/cjcmm20160827
雪上一枝蒿性温,味苦、辛,有大毒,有祛风除湿、通利关节、消肿止痛的功效。其生物碱类成分是其有毒成分且具有活血、镇痛、抗炎等药理作用[12] 。 雪甲素是雪上一枝蒿的主要成分之一,属于二萜类生物碱。现代药理实验研究表明具有镇痛、抗炎、镇静的功效。微乳作为载体透皮给药,与其他剂型相比具有独特优势,能提高药物的透皮能力,可在角质层和真皮形成药物储库,明显缓释药物,达到长时间高剂量的释放[3],从而提高药物的生物利用度,达到增效减毒的目的。 在前期工作中,本团队完成了雪上一枝蒿微乳的研制[4]。但由于微乳黏度低,导致微乳直接涂抹于动物皮肤上时容易流失,造成给药剂量不准确等。因此,本试验将雪上一枝蒿微乳制备成微乳凝胶,在此基础上本文建立了经皮给药后大鼠血和皮肤中雪甲素的UPLCMS/MS含量测定方法,考察了雪上一枝蒿总碱凝胶和微乳凝胶经皮给药后不同时间点雪上一枝蒿甲素在皮肤及血药中的浓度,并计算相应的药代动力学参数,为雪上一枝蒿经皮给药系统的新制剂开发提供实验依据。
1材料
UPLCTQD三重四级杆串联质谱仪(美国Waters);TYXHⅡ型涡旋混合器(无锡沃信仪器有限公司);HC2062型高速离心机(安徽中科中佳科学仪器有限公司);MTN2800型氮吹浓缩装置(天津奥特赛恩斯仪器有限公司);AE/240型电子天平(上海梅特勒仪器有限公司)。
色谱纯乙腈、甲醇(Merck公司);雪上一枝蒿总碱微乳凝胶(自制,批号20150810);雪上一枝蒿总碱普通凝胶(自制,批号20150810);雪上一枝蒿甲素(纯度≥98%,中国食品药品检定研究院,批号110895200404);盐酸帕罗西汀(纯度为974%,中国食品药品检定研究院,批号100357201303);甲酸(CNY Technologies);水为屈臣氏蒸馏水;其余试剂均为分析级。
昆明种小鼠80只,雄性,体重18~22 g,清洁级,由重庆滕鑫生物有限公司提供,合格证号SCXK(渝)20120003。
2方法
21血浆与皮肤中雪甲素浓度的UPLCMS/MS检测方法
211色谱条件
Waters BEH C18色谱柱(21 mm×50 mm,17 μm);流动相02%甲酸水(A)02%甲酸乙腈(B),梯度洗脱,0~2 min,15%~50% B,2~3 min,50%~15% B,4~5 min,15% B,流速03 mL·min-1;进样体积为1 μL,柱温45 ℃。
212质谱条件
电喷雾电离源(ESI);毛细管电离电压3 kV;离子源温度120 ℃;去溶剂气温度550 ℃;喷雾气与反吹气为氮气,去溶剂气流速650 L·h-1,反吹气流速50 L·h-1;扫描方式为多反应监控离子模式(MRM),用于定量分析监测的离子对反应为:m/z 344→580(雪甲素)和m/z 330→192(盐酸帕罗西汀);锥孔电压为54 V;碰撞能量为50 eV。
22样品制备
221血样处理
将小鼠背部用脱毛膏脱毛(15 cm×25 cm),生理盐水洗净,在其脱毛处给以雪上一枝蒿总碱凝胶或微乳凝胶03 g,摘眼球取血,于4 000 r·min-1离心10 min,取血浆200 μL,加入10 μL质量浓度为440 μg·L-1的盐酸帕罗西汀内标溶液,加入乙腈590 μL[5],涡旋混合1 min,1万 r·min-1离心10 min,取上清液600 μL氮气吹干,加入50%乙腈[6]100 μL复溶,涡旋混合1 min,13 000 r·min-1离心10 min,取上清液进样。
222皮肤处理
取完血后,将小鼠脱颈处死。先用干棉花将背部剩余的药擦掉,再用蘸有生理盐水的棉花擦拭皮肤,用干棉花擦拭,重复擦拭3次,剪下给药处皮肤。将皮肤剪碎,加入1 mL 50%乙腈,涡旋混合3 min,匀浆,涡旋混合3 min,8 000 r·min-1离心10 min,取上清液500 μL,加入10 μL质量浓度为44 mg·L-1的盐酸帕罗西汀内标液,加入50%乙腈490 μL,涡旋混合3 min,1万 r·min-1离心10 min,上清液经022 μm微孔滤膜滤过,取续滤液进样。
23方法可行性考察
231色谱考察
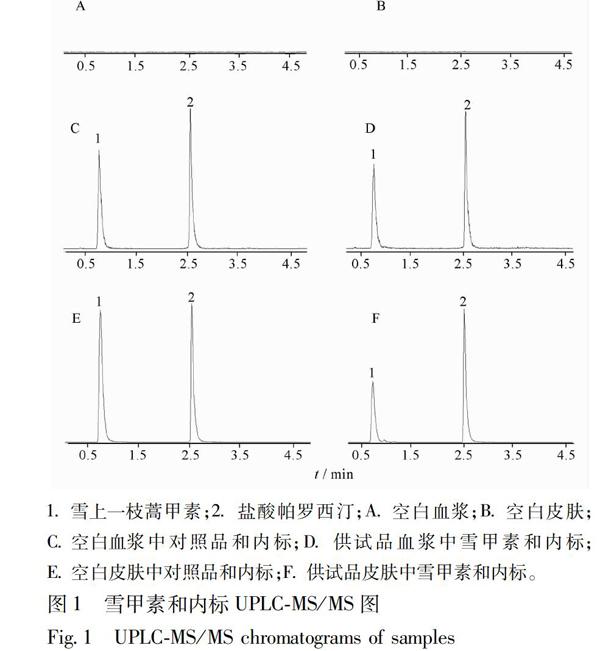
按照拟定的色谱条件,将221中的空白样品、供试品血浆和制备的对照溶液(含雪甲素50 mg·L-1和盐酸帕罗西汀50 mg·L-1)分别进样,结果见图1。雪甲素、盐酸帕罗西汀与血浆中的其他成分分离良好,其保留时间分别为077,25 min,空白血浆中与雪甲素、盐酸帕罗西汀相应的时间处无杂质峰。
232雪甲素标准曲线的绘制
取质量浓度为58,116,290,580,1 160,2 900,5 800 μg·L-1的雪甲素对照品溶液10 μL,加入200 μL空白血浆,使其含雪甲素为29,58,145,29,58,145,290 μg·L-1,按221项下处理后,分别测定雪甲素和盐酸帕罗西汀的峰面积。以雪甲素浓度为横坐标,雪甲素峰面积和内标峰面积比为纵坐标,进行回归处理,平行制备3条标准曲线,得平均的回归标准曲线方程为Y=0011X-0048,r=0999 5。
取质量浓度为1078,2156,539,1078,2156,539,8624 mg·L-1的雪甲素对照品溶液10 μL,加入500 μL空白皮肤匀浆液,使其含雪甲素为0215 6,0431 2,1078,2156,4312,1078,17248 mg·L-1,按222项下处理后,分别测定雪甲素和盐酸帕罗西汀的峰面积。以雪甲素浓度为横坐标,雪甲素峰面积和内标峰面积比为纵坐标,进行回归处理,平行制备3条标准曲线,得平均的回归标准曲线方程为Y=0202X+0115,r=0999 5。
233回收率测定
2331血浆回收率测定向空白血浆中加入一定量的雪甲素对照溶液,分别制得含雪甲素58,29,232 μg·L-1的血浆溶液(n=5)。按221方法处理,UPLCMS/MS测定峰面积比值和该浓度对照品50%乙腈溶液峰面积比值,分别得提取回收率为(8673±692)%(8647±215)%,(8534±240)%。
将上述含雪甲素58,29,232 μg·L-1的血浆处理溶液(n=5)所测定的峰面积比值分别与该浓度对照品用同法制备的血浆处理溶液(n=5)的峰面积比值比较,分别得方法回收率为(9323±977)%,(10578±423)%,(10196±1011)%。
2332皮肤回收率测定向空白皮肤匀浆液中加入一定量的雪甲素对照品溶液,分别制得含雪甲素0431 2,2156,17248 mg·L-1的皮肤溶液。按222方法处理,UPLCMS/MS测定峰面积比值与该浓度对照品50%乙腈溶液峰面积比值比较,分别得提取回收率为 (8995±893)%,(8480±234)%,(9592±187)%。
将上述含雪甲素0431 2,2156,17248 mg·L-1的皮肤处理溶液(n=5),所测定的峰面积分别与该浓度对照品用同法制备的皮肤处理溶液(n=5)的峰面积比较,分别得方法回收率为(9739±170)%,(11252±347)%,(9832±212)%。
234精密度测定
以2331方法,制得含雪甲素58,29,232 μg·L-13种质量浓度的血浆溶液(n=5),测定日内精密度RSD分别为80%,62%,99%;日间精密度RSD分别为10%,82%,96%。
以2332方法,制得含雪甲素0431,2156,17248 mg·L-13种质量浓度的皮肤溶液(n=5),测定日内精密度RSD分别为39%,28%,21%;日间精密度RSD分别为46%,31%,47%。
235稳定性考察
配制含雪甲素高(232 μg·L-1)、中(29 μg·L-1)、低(58 μg·L-1)3个质量浓度的血浆对照液以及高(17248 mg·L-1)、中(2156 mg·L-1)、低(0431 mg·L-1)3个质量浓度的皮肤匀浆液各15份(每项实验n=5),分别按血浆样品处理项下和皮肤匀浆项下操作,考察室温放置6 h和冻融3次的稳定性。结果表明,室温下雪甲素血药浓度变化RSD分别为92%,20%,47%;雪甲素在皮肤匀浆液中浓度变化RSD分别为31%,37%,41%;雪甲素血药浓度变化RSD分别为11%,95%,94%;雪甲素在皮肤匀浆液中浓度变化RSD为10%,93%,10%。上述测定结果表明,雪甲素血浆样品及皮肤匀浆液样品各项稳定性试验结果均符合要求。
24实验分组
取雄性SPF小鼠80只,体重18~22 g,随机分为2组,分为雪上一枝蒿总碱微乳凝胶组(Ⅰ)和普通凝胶组(Ⅱ),每组40只,于实验前12 h禁食,自由饮水。将小鼠背部用脱毛膏脱毛,生理盐水洗净,分别称取03 g微乳凝胶或普通水凝胶(含雪上一枝蒿总碱510 mg和雪甲素0561 mg)紧贴于小鼠背部。给药后,分别于05,1,2,4,6,8,12,24 h摘取眼球取血,每个时间点各5只小鼠。按照221项下处理脱颈处死,取皮肤后,-20 ℃保存,备用。
25数据处理
实验数据以±s表示,用Kinetica 44软件进行统计分析。
3结果
31小鼠血浆中雪甲素浓度的测定
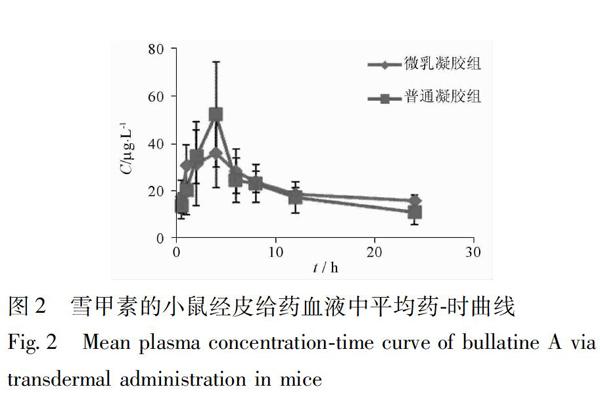
按221项下处理血样后,取1 μL进样,UPLCMS/MS测定其中雪甲素浓度,平均药时曲线见图2。
32小鼠皮肤中雪甲素浓度的测定
按222项下方法处理皮肤,取1 μL进行UPLCMS/MS测定其中雪甲素浓度,平均药时曲线见图3。
33小鼠药动学参数和皮肤分布
用Kinetica 44软件处理雪甲素在血浆和皮肤
中浓度数据,经自动拟合,小鼠经皮给药符合非房室模型。相关药动学参数见表1,2。
4结论
本研究结合文献[6]优化出了一种检测血浆和皮肤中雪甲素的UPLCMS/MS法,在处理和测定过程中,选择了盐酸帕罗西汀作为内标物,减少了操作和测定可能带来的误差。
试验过程中发现微乳和溶液直接给药时,药液会流失,造成给药剂量不准确。因此,本试验将微乳和溶液加入适量黄原胶,制备成适合给药的凝胶,通过透射电子显微镜和激光粒度测定仪测定,发现微乳在凝胶中仍为微乳,凝胶基质并不影响其形态与粒径,其工艺和质量标准研究另文报道。
由表1和图2可以看出,雪上一枝蒿总碱微乳凝胶经皮给药,血液中雪甲素达峰时间(34 h)较普通凝胶组(40 h)快,MRT大于普通凝胶组,药时曲线下面积明显高于普通凝胶组,但Cmax明显低于普通凝胶组,说明微乳凝胶组在体内吸收较普通凝胶组快且平稳,而消除较慢,证明微乳可在角质层和真皮层形成药物储库,使其在皮内的一定深度缓慢释药,因此具有作用平缓、血药浓度更加平稳的优点,与体外经皮渗透性实验结论一致[7]。由图3和表2可以看出,普通凝胶组皮肤中雪甲素浓度较微
乳凝胶组增加快速,达峰后药物浓度降低也较快速。
说明药物在皮肤中的浓度变化与在血液中的浓度变化有一定的相关性。由此可见,雪上一枝蒿总碱微乳凝胶经皮给药,具有稳定血药浓度,提高生物利用度等优点。
[参考文献]
[1]高绍阳,喻萍,陈武元,等RPHPLC法测定雪上一枝蒿中雪上一枝蒿甲素含量[J]药物分析杂志,2005,25(11):1382
[2]朱任宏中国乌头之研究:雪上一枝蒿中的生物碱[J]化学学报,1964,30(2):139
[3]M E Dalmora, S L Dalmora, A G Oliveira Inclusion complex of piroxicam with βcyclodextrin and incorporation in cationic microemulsion In vitro drug release and in vivo topical antiinflammatory effect[J] Int J Pharm,2001,222(1): 45
[4]吴玉梅,陈晓兰,林亚平,等雪上一枝蒿总生物碱微乳的研制与质量评价[J]中国实验方剂学杂志,2015,21(23):7
[5]陈晓兰,陆洋,杜守颖,等HPLC测定丹皮中丹皮酚在大鼠体内血药浓度及药动学研究[J]中国中药杂志,2010,35(21):2826
[6]王毅,刘子秋,王炯,等 UPLCMS/MS法测定人血中雪上一枝蒿甲素[J]中国司法鉴定,2013(6):50
[7]魏文珍,陈晓兰,吴玉梅,等雪上一枝蒿微乳体外透皮及影响因素研究[J]时珍国医国药,2015,26(9):2132
[责任编辑曹阳阳]

