不同电子受体作用下微生物降解多环芳烃研究进展
侯晓鹏,李春华,叶春,许士洪,郑向勇
1. 中国环境科学研究院,北京 100012
2. 东华大学环境科学与工程学院,上海 201620
3. 浙江省水环境与海洋生物资源保护重点实验室,浙江 温州 325035
不同电子受体作用下微生物降解多环芳烃研究进展
侯晓鹏1,2,李春华1*,叶春1,许士洪2,郑向勇3
1. 中国环境科学研究院,北京 100012
2. 东华大学环境科学与工程学院,上海 201620
3. 浙江省水环境与海洋生物资源保护重点实验室,浙江 温州 325035
电子受体作为微生物代谢过程中的必需物质,对不同类型微生物的数量及其代谢能力有重要影响。分析了不同电子受体对微生物降解多环芳烃的影响。对好氧降解(氧气为电子受体)多环芳烃微生物种类及降解途径进行了总结;厌氧降解方面,概述了硝酸盐、硫酸盐、金属离子〔Fe(Ⅲ)或Mn(Ⅳ)〕和碳酸盐为电子受体微生物降解多环芳烃的研究进展。此外,对微生物降解多环芳烃的研究存在的问题以及未来的发展方向进行了简述与展望。
多环芳烃;电子受体;微生物降解;降解效率;降解途径
多环芳烃(polycyclic aromatic hydrocarbons)是由2个及以上苯环以线状、角状或簇状排列而成的芳香族化合物[1-2]。由于其广泛分布于大气、水体、植被和土壤中[3],且具有潜在的“三致”效应以及生物富集性,多环芳烃对农产品安全和人类健康构成了严重威胁[4-5]。多环芳烃可能的转化或去除方式有吸收吸附、挥发、化学降解、光分解和微生物降解等[6],其中微生物降解被认为是最主要和最有效的方法。尽管研究表明大多数的多环芳烃均能被微生物降解,但在实际环境中其降解速率较慢,主要有2方面原因:1)多环芳烃的憎水亲脂性限制了其传质过程,导致生物利用率降低;2)现有环境影响因子无法为微生物降解多环芳烃创造适宜的外部条件。一般认为添加表面活性剂〔如十二烷基磺酸钠(SDS)[7-8]〕能改善多环芳烃的水溶性,从而使其生物利用率增大。影响多环芳烃降解的环境因子(如温度、pH、营养盐、含氧量、湿度)已被广泛总结,研究表明:温度为24~30 ℃,pH为7.0~7.8,C∶N∶P为100∶10∶1,含氧量为10%~40%,湿度为30%~90%时,有利于微生物降解多环芳烃[9]。然而,从电子受体角度去考察微生物对多环芳烃的降解却鲜有报道。

氧化还原电位可反映在某一反应体系中电子受体得电子的能力,生物体内的电子传递一般是从氧化还原电位低的物质到高的物质,例如NAD→黄素酶→细胞色素C系→O2。不同电子受体还原反应的氧化还原电位和释放能量见表1[16-17]。在有氧条件下氧气优先获得电子;在无氧条件下,硝酸盐、硫酸盐、碳酸盐或CO2、Mn(Ⅳ)、Fe(Ⅲ)等可作为微生物降解多环芳烃的电子受体[18-22]。在活细胞中,好氧性细胞的氧化还原电位高于厌氧性细胞,氧化还原电位还会影响酶的活性、细胞同化能力和微生物的生长发育等。环境中的氧气是微生物降解多环芳烃的重要影响因素:1)氧气的含量决定微生物的群落结构;2)由于氧气的氧化能力强,在还原反应中释放的能量多,故好氧微生物对多环芳烃的降解效率较高。大多数厌氧微生物对电子受体的利用都有单一选择性,有研究[23]将微生物厌氧降解多环芳烃的反应体系分为反硝化还原反应体系(硝酸盐为电子受体)、硫酸盐还原反应体系(硫酸盐为电子受体)、金属还原反应体系〔Mn(Ⅳ)和Fe(Ⅲ)等为电子受体〕和产甲烷还原反应体系(碳酸盐或CO2为电子受体)等。无氧条件下微生物降解多环芳烃对特定外源电子受体的需求量有最适范围,电子受体供给量过高或过低都会对降解产生抑制作用。此外,不同外源电子受体对特定微生物厌氧降解多环芳烃反应有不同的促进作用[24]。

表1 不同电子受体还原反应的氧化还原电位和释放能量(pH=7)[16-17]
1 以氧气为电子受体
对好氧条件下微生物降解多环芳烃已经有较广泛的研究,主要集中在降解菌种的筛选与鉴定、对多环芳烃的降解效率及降解条件优化、多环芳烃的降解途径、多环芳烃的酶促降解反应4个方面。大量能够降解多环芳烃的细菌、真菌和藻类从土壤和水体底泥中被筛选出,其中发挥主要作用的是细菌[25]。常见的好氧微生物有:从毛单胞菌属(Comamonassp.)[26]、巴氏杆菌属(Pasteurellasp.)[27]、伯克氏菌属(Burkholderiasp.)[28]、分枝杆菌属(Mycobacteriumsp.)[29]、氧化节杆菌属(Arthrobacteroxydanssp.)[30]、热带根瘤菌属(Rhizobiumtropicisp.)[31]、克雷伯氏菌属(Klebsiellasp.)[32]、不动杆菌属(Acinetobactersp.)[6]、假单胞菌属(Psuedomonassp.)[33]和解环菌属(Cycloclasticussp.)[34]等,这些微生物对不同的多环芳烃表现出不同的降解效果。一般而言,对低分子量的多环芳烃(如萘、蒽、菲、芴等)降解速率较高;对高分子量的多环芳烃降解很慢,主要是由于其分子结构复杂,电子云密度高,很难被氧化,水溶性差,热稳定性强[35]。Guo等[36]从红树林底泥中分离出的一株降解菌(PseudomonasSKDOP),7 d内对菲的降解率可达60%以上,而在14 d的试验期内对芘基本无降解。张杰等[37]在降解菲试验中加入适合浓度的共代谢底物(葡萄糖),发现混合菌系对菲的降解速率由67.85%增加到86.34%。

图1 好氧微生物(真菌和细菌)降解菲的一般途径[38]Fig.1 Proposed pathways for phenanthrene degradation by aerobic microorganisms (fungi and bacteria)
好氧降解多环芳烃的途径已有较多研究,普遍认为是细菌在双加氧酶作用下或真菌在单加氧酶作用下,使芳香环羟基化后,再使之开环进行下一步降解,一般会形成中间产物——邻苯二酚或取代邻苯二酚,然后通过1,2-双加氧酶催化的邻裂途径或者2,3-双加氧酶催化的间裂途径裂解开环进入三羧酸循环(TCA),实现最终降解。以菲为例[38],真菌对菲的降解途径仍不清楚,而细菌对菲的降解途径已有研究。首先在菲双加氧酶作用下形成顺式-3,4-二羟基-3,4-二氢菲,在脱氢酶作用下形成顺式-3,4-二羟基菲,随后在一系列酶作用下转化为1-羟基-2-萘甲酸,不同的菌种会通过不同的途径进行下一步降解,主要是水杨酸代谢途径或邻苯二甲酸代谢途径或二者都有,最后进入TCA循环降解为CO2和H2O(图1),降解过程中羟基化碳的初始位置可以不同。好氧降解过程会产生有毒中间产物,很难被生物利用。Luan等[39]使用红树林湿地中富集到的多环芳烃降解菌群好氧降解芴时,共检测到4种单羟基化中间产物(1-羟基芴,2-羟基芴,3-羟基芴及9-羟基芴),但只有9-羟基芴得到较完全降解,最终转化为邻苯二甲酸,而其他3种中间产物浓度逐渐升高,且无进一步降解趋势。 在微生物降解多环芳烃过程中有多种酶参与,目前研究较多的酶有3种,反应过程见表2[40]。一些加氧酶作用下产生的中间产物分子量比母体多环芳烃大,只有部分能被完全转化为无毒、低分子产物,其他大部分仍滞留在环境中,造成更大的危害。如芘在双加氧酶作用后形成的二氢二醇芘会转化成一种更有毒的中间体二醇芘,并造成毒性累积[41]。
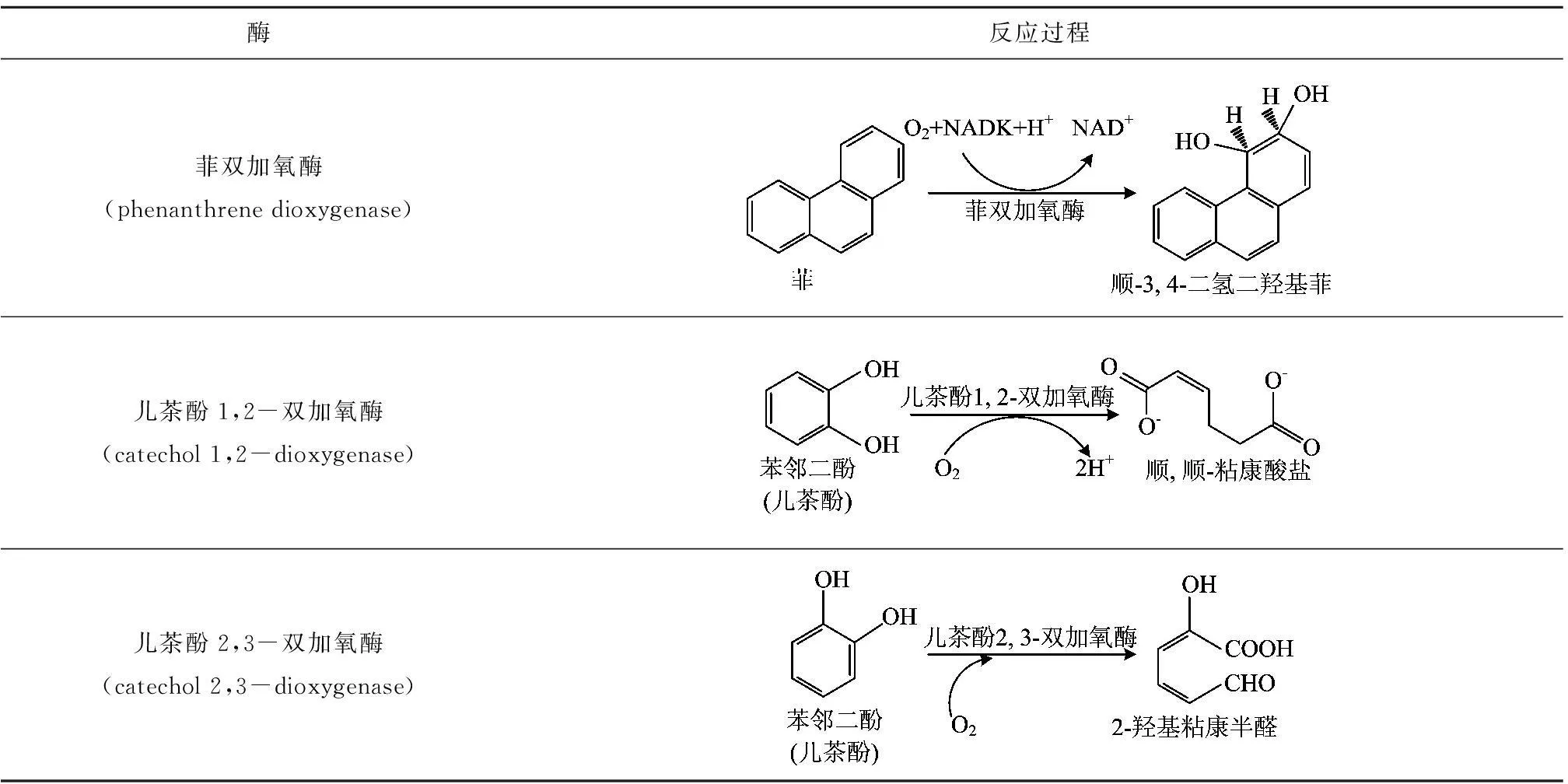
表2 3种双加氧酶反应过程
2 以硝酸盐为电子受体
厌氧降解多环芳烃研究中,以硝酸盐或硫酸盐为电子受体的研究相对较多。Mihelcic等[42]于1988年首次发现反硝化还原反应体系对萘的降解现象,随后越来越多能降解多环芳烃的反硝化菌株或菌群逐渐被分离。Dou等[24]从土壤中分离得到萘降解菌,在厌氧条件下纯培养试验发现,合理控制硝酸盐的投入量能在一定程度上提高对萘的降解率和降解速率。然而,反硝化还原反应体系对多环芳烃的降解效率一直有很大争议。Mihelcic等[42-43]的研究表明多环芳烃或多或少都有被降解;Lei等[8,44]的研究表明多环芳烃完全没有被降解。以硝酸盐为电子受体的微生物降解多环芳烃研究主要集中在低分子多环芳烃,对4环以上的高分子多环芳烃的降解鲜有报道。Mcnally等[45]以硝酸盐为电子受体在严格的厌氧纯培养条件下发现,不同多环芳烃的降解速率依次为蒽>菲>芘,说明厌氧条件下多环芳烃的降解难易程度与好氧条件下一致。
3 以硫酸盐为电子受体
由于硫酸盐广泛存在于各类自然环境中,以硫酸盐为电子受体的还原反应体系对多环芳烃的降解更普遍。研究发现[20,46]添加硫酸盐可以加强环境中微生物对多环芳烃的去除效果,并且相较其他电子受体,硫酸盐为电子受体时微生物对多环芳烃的降解效率最高。Hayes等[47]在研究硫酸盐还原反应体系对多环芳烃的降解时,添加硫酸盐抑制剂导致多环芳烃不再被降解,从而说明硫酸盐是降解的关键因素。硫酸钙是硫酸盐还原反应体系中最佳的电子受体,主要因为硫酸钙水溶性低,在环境中不会形成较高的盐度而抑制细菌的活性。不同浓度的硫酸盐对降解多环芳烃也有影响,一般最佳浓度为10~50 mmolL,目前普遍采用的浓度为20 mmolL。Rothermich等[48]在研究海洋沉积物中的多环芳烃降解时,用14C标记法首次发现硫酸盐还原反应体系下对苯并[a]芘的降解,同时发现高分子多环芳烃的降解速率低于低分子多环芳烃。以硫酸盐为电子受体时降解多环芳烃产生的中间产物比氧气为电子受体时更简单、毒性更小且分解更完全[49-50]。Tsai[51]对芴的降解产物研究中没有发现高分子中间产物,而是大量低分子苯酚,且很快完全转化为CO2和H2O(图2)。Zhang等[52]在产硫菌群对萘和菲的厌氧降解研究中提出,羧基化可能是该系统降解反应的第一步,并用14C标记法证明萘和菲最终被降解为CO2。
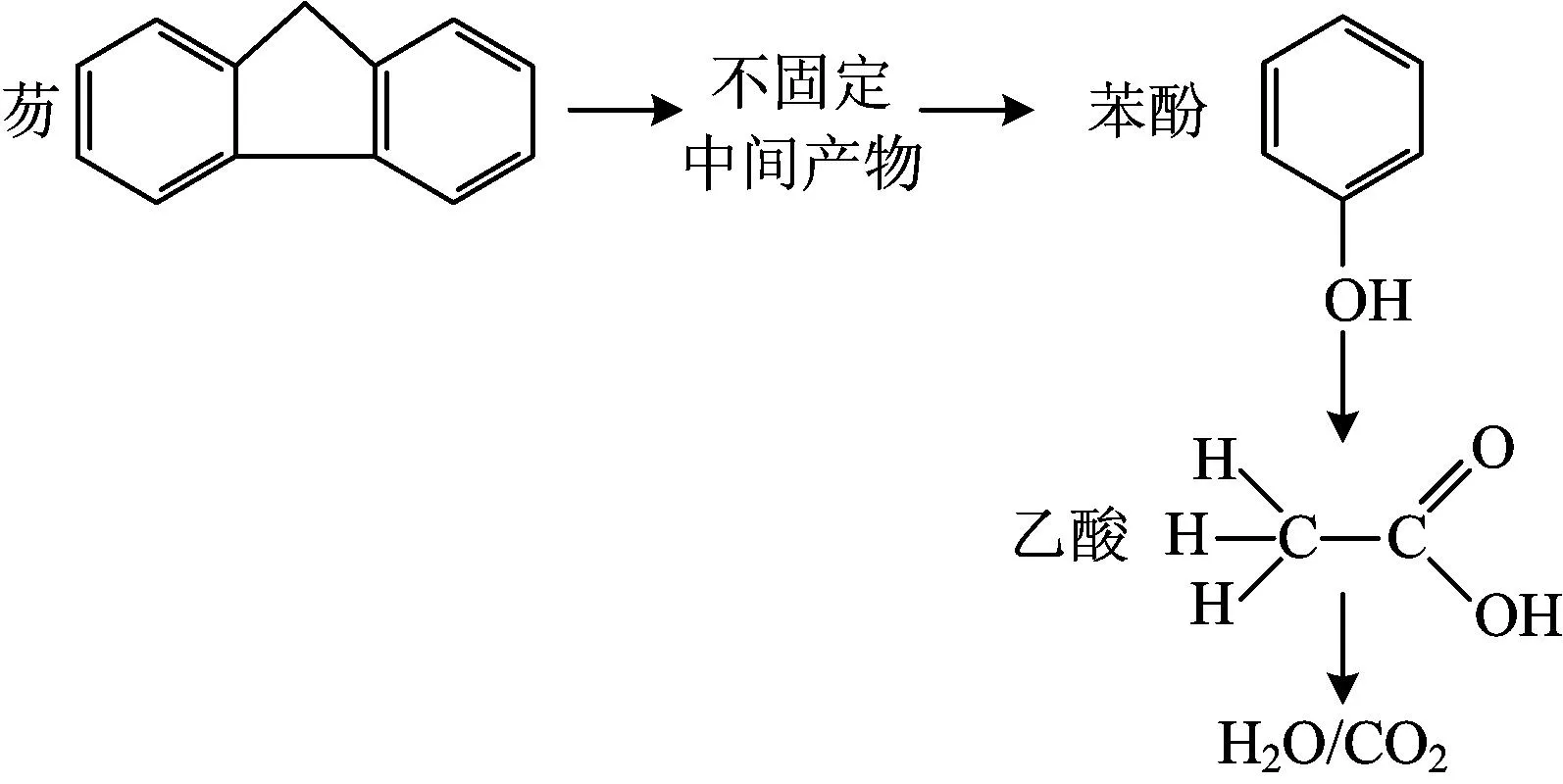
图2 硫酸盐为电子受体下微生物对芴的降解途径[51]Fig.2 Biodegradation pathways of fluorene with amendment of sulfate
4 以金属离子〔Fe(Ⅲ)或Mn(Ⅳ)〕为电子受体
目前对于金属离子作为电子受体的微生物降解多环芳烃的研究较少,主要集中在Fe(Ⅲ)和Mn(Ⅳ)的研究上。研究表明[43,53],添加高浓度Fe(Ⅲ)有利于降解多环芳烃,特别是5环和6环的多环芳烃。Fe(Ⅲ)的形式对降解多环芳烃也有影响,Kraig[53]研究表明,磷酸铁(FePO4)对大多数微生物降解多环芳烃有抑制作用,而柠檬酸铁则没有。Li等[18]的研究发现,在硫酸盐非常丰富时,添加Fe(Ⅲ)对微生物厌氧降解4种多环芳烃(芴、菲、荧蒽和芘)并无显著影响,这或许是因为该环境下硫酸盐的得电子能力高于Fe(Ⅲ)。
对于Mn(Ⅳ)为电子受体的微生物降解多环芳烃鲜有报道,可能是由于Mn(Ⅳ)容易被多种自然存在的有机污染物所利用,而不是被Mn还原菌利用[12]。仅有的研究结果也不统一:有研究表明[12],Mn(Ⅳ)对微生物厌氧降解萘有一定作用,而对芘没有显著影响;也有研究表明[54],Mn(Ⅳ)对微生物降解芴、菲、荧蒽和芘有显著的抑制作用。这可能是由于降解菌种的不同所致,有的菌种能利用Mn(Ⅳ)促进自我生长,而有的菌种会受到Mn(Ⅳ)的毒害而被抑制生长。
5 以碳酸盐或二氧化碳为电子受体
某些产甲烷菌在厌氧还原体系中具有一定降解或者促进其他厌氧微生物降解多环芳烃的能力。由于产甲烷菌广泛分布于高有机碳负荷的还原环境中(氧化还原电位为-600~-200 mV),其在多环芳烃的生物修复中起着重要作用。产甲烷还原反应体系下降解多环芳烃的研究并不深入细致,大多集中在对低分子多环芳烃的研究[14,55],该反应体系中高分子多环芳烃没有减少或消失[46,53]。Chang等[56]以萘和菲为降解对象研究产甲烷和厌氧降解之间的联系时,通过添加产甲烷抑制剂发现多环芳烃降解被部分抑制,从而证明产甲烷在厌氧降解多环芳烃过程中发挥重要作用。Genthner等[55]在研究被木溜油污染的底泥中的多环芳烃时,添加CO2碳酸氢盐缓冲作为电子受体,发现有甲烷产生并且多环芳烃有一定程度的去除,但4环和5环的多环芳烃没有被降解。产甲烷还原反应体系降解萘的途径(图3)[57]与单环烃相似。Chang等[20,58]对5种多环芳烃在不同厌氧还原反应体系下研究表明:对多环芳烃降解效果的促进作用由强到弱依次为硫酸盐还原反应体系>产甲烷还原反应体系>硝酸盐还原反应体系;微生物对多环芳烃的降解速率常数由高到低依次为菲>芘>蒽>芴>苊。然而,Li等[59]研究表明,添加NaHCO3对红树林底泥中微生物降解多环芳烃无促进作用,这可能是由于红树林底泥中其他电子受体浓度较高所致。
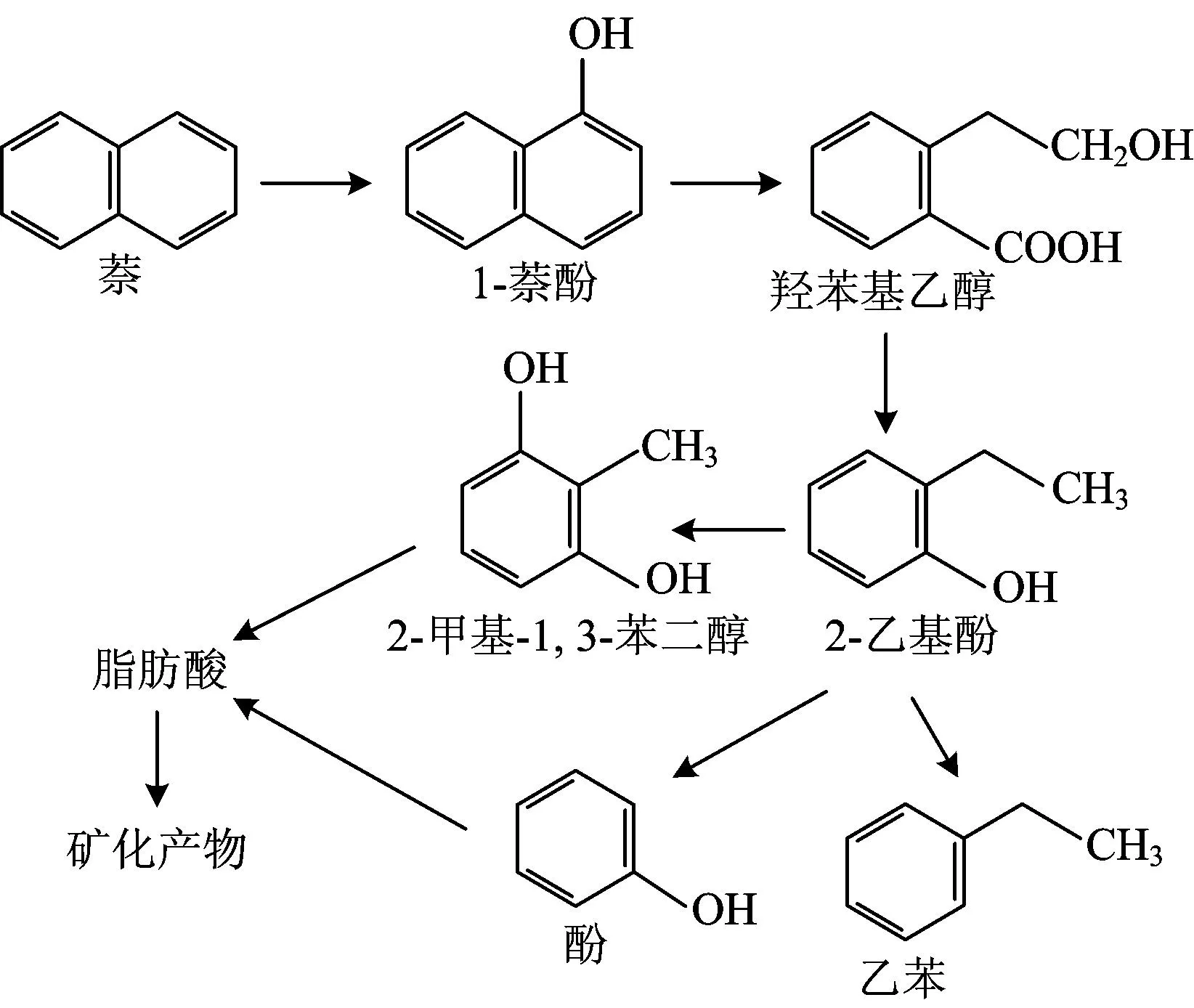
图3 产甲烷还原反应体系降解萘的途径[57]Fig.3 Methane-producing degradation pathways of naphthalene
6 结论与展望
近年来,以氧气为电子受体对多环芳烃的微生物降解(即好氧降解)研究广泛,主要集中在好氧菌种的筛选、多环芳烃的降解速率及影响因素、降解途径和降解的酶系4个方面。而无氧条件下的微生物降解多环芳烃研究相对薄弱,主要是以硝酸盐和硫酸盐为电子受体的厌氧降解,以Fe(Ⅲ)和Mn(Ⅳ)为电子受体的研究较少。不同外源电子受体对多环芳烃降解促进效果不同,无氧条件下对不同多环芳烃降解的难易程度与好氧条件下一致。多环芳烃的好氧降解速率较厌氧降解高,二者的降解途径也不同,好氧降解产生有毒大分子中间产物,并滞留在环境中,而厌氧降解多生成小分子低毒易降解中间产物。
对多环芳烃的微生物降解存在以下关键问题,需进一步研究。
(1)不同电子受体下的多环芳烃厌氧降解菌较少,降解途径目前还不十分清楚,故需加大对厌氧高效降解菌种的筛选,系统研究和总结不同电子受体下微生物厌氧降解多环芳烃的途径。
(2)厌氧条件广泛存在于水体底泥和土壤深处,深入研究厌氧环境下的多环芳烃降解影响因素从而优化降解条件,对采用工程方法去除环境中多环芳烃有重要意义。
(3)多环芳烃好氧降解会产生有毒、难降解的中间产物,其滞留在环境中可能造成更大的危害,对该类中间产物的研究将成为关注的热点。
(4)合理构建内部厌氧降解菌种与外部好氧降解菌种共存的菌胶团结构,将好氧降解的高效率与厌氧降解终产物的低毒易分解相结合,为实际工程中多环芳烃的高效生物修复应用奠定理论基础。
[1] MINAI-TEHRANI D,MINOUI S,HERFATMANESH A.Effect of salinity on biodegradation of polycyclic aromatic hydrocarbons(PAHs) of heavy crude oil in soil[J].Bulletin of Environmental Contamination and Toxicology,2009,82(2):179-184.
[2] 陈明华,李春华,叶春,等.多环芳烃在低氧沉积物环境中的分布状况[J].环境污染与防治,2013(2):104-110.
CHEN M H,LI C H,YE C,et al.Distribution of polycyclic aromatic hydrocarbons in hypoxic sediment environments[J].Environmental Pollution & Control,2013(2):104-110.
[3] 岳敏,谷学新,邹洪,等.多环芳烃的危害与防治[J].首都师范大学学报(自然科学版),2003(3):40-44.
YUE M,GU X X,ZOU H,et al.Killer of health-polycyclic aromatic hydrocarbons[J].Journal of Capital Normal University (Natural Science Edition),2003(3):40-44.
[4] ZHANG Y,WANG J.Distribution and source of polycyclic aromatic hydrocarbons(PAHs) in the surface soil along main transportation routes in Jiaxing City,China[J].Environmental Monitoring and Assessment,2011,182(1234):535-543.
[5] LI J,LIU G,YIN L,et al.Distribution characteristics of polycyclic aromatic hydrocarbons in sediments and biota from the Zha Long Wetland,China[J].Environmental Monitoring and Assessment,2013,185(4):3163-3171.
[6] YUAN H,YAO J,MASAKORALA K,et al.Isolation and characterization of a newly isolated pyrene-degradingAcinetobacterstrain USTB-X[J].Environmental Science and Pollution Research,2014,21(4):2724-2732.
[7] JAHAN K,AHMED T,MAIER W J.Modeling the influence of nonionic surfactants on biodegradation of phenanthrene[J].Water Research,1999,33(9):2181-2193.
[8] LEI L,KHODADOUST A P,SUIDAN M T,et al.Biodegradation of sediment-bound PAHs in field-contaminated sediment[J].Water Research,2004,39(2):349-361.
[9] 陈春云,岳珂,陈振明,等.微生物降解多环芳烃的研究进展[J].微生物学杂志,2007(6):100-103.
CHEN C Y,YUE K,CHEN Z M,et al.Advances in microbial degradation of polycyclic aromatic hydrocarbons (PAHs)[J].Journal of Microbiology,2007(6):100-103.
[10] 周群英,王士芬.环境工程微生物学[M].北京:高等教育出版社,2008.
[11] RABUS R,WIDDEL F.Anaerobic degradation of ethylbenzene and other aromatic hydrocarbons by new denitrifying bacteria[J].Archives of Microbiology,1995,163:96-103.
[12] NIEMAN J K C,SIMS R C,MCLEAN J E,et al.Fate of pyrene in contaminated soil amended with alternate electron acceptors[J].Chemosphere,2001,44:1265-1271.
[13] MACRAE J D,HALL K J.Biodegradation of polycyclic aromatic hydrocarbons(PAH) in marine sediments under denitrifying conditions[J].Water Science and Technology,1998,38:177-185.
[14] CHANG W.Anaerobic biodegradation of polycyclic aromatic hydrocarbon[D].Maryland:University of Maryland,2003.
[15] PIEPE D H,SANTOS V M,GOLYSHIN P N.Genomic and mechanistic insights into the biodegradation of organic pollutants[J].Current Opinion in Biotechnology,2004,15(3):215-224.
[16] LEVETT P N.Anaerobic bacteria:a functional biology[M].Milton Keynes:Open University Press,1990.
[17] ZEHNDER B A J.Biology of anaerobic microorganisms[M].New York:John Wiley and Sons Inc,1988.
[18] LI C H,WONG Y S,TAM N F.Anaerobic biodegradation of polycyclic aromatic hydrocarbons with amendment of iron(Ⅲ) in mangrove sediment slurry[J].Bioresour Technol,2010,101(21):8083-8092.
[19] AMBROSOLI R,PETRUZZELLI L,LUIS M J,et al.Anaerobic PAH degradation in soil by a mixed bacterial consortium under denitrifying conditions[J].Chemosphere,2005,60(9):1231-1236.
[20] CHANG B V,CHANG S W,YUAN S Y.Anaerobic degradation of polycyclic aromatic hydrocarbons in sludge[J].Advances in Environmental Research,2003,7(3):623-628.
[21] ROTHERMICH M M,HAYES L A,LOVLEY D R.Anaerobic,sulfate-dependent degradation of polycyclic aromatic hydrocarbons in petroleum-contaminated harbor sediment[J].Environmental Science & Technology,2002,36(22):4811-4817.
[22] COATES J D,WOODWARD J,ALLEN J,et al.Anaerobic degradation of polycyclic aromatic hydrocarbons and alkanes in petroleum-contaminated marine harbor sediments[J].Applied and Environmental Microbiology,1997,63(9):3589-3593.
[23] 孙明明,滕应,骆永明.厌氧微生物降解多环芳烃研究进展[J].微生物学报,2012(8):931-939.
SUN M M,TENG Y,LUO Y M.Progresses in anaerobic biodegradation of polycyclic aromatic hydrocarbons:a review[J].Acta Microbiologica Sinica,2012(8):931-939.
[24] DOU J,LIU X,DING A.Anaerobic degradation of naphthalene by the mixed bacteria under nitrate reducing conditions[J].Journal of Hazardous Materials,2009,165:325-331.
[25] HARITASH A K,KAUSHIK C P.Biodegradation aspects of polycyclic aromatic hydrocarbons(PAHs):a review[J].Journal of Hazardous Materials,2009,169(123):1-15.
[26] GOYAL A K,ZYLSTRA G J.Molecular cloning of novel genes for polycyclic aromatic hydrocarbon degradation fromComamonastestosteroni GZ39[J].Applied and Environmental Microbiology,1996,62(1):230-236.
[27] SEPIC E,BRICELJ M,LESKOVSEK H.Biodegradation studies of polyaromatic hydrocarbons in aqueous media[J].Journal of Applied Microbiology,1997,83(5):561-568.
[28] WONG J W C,LAI K M,WAN C K,et al.Isolation and optimization of PAH-degradative bacteria from contaminated soil for PAHs bioremediation[J].Water Air and Soil Pollution,2002,139(1234):1-13.
[29] DANDIE C E,THOMAS S M,BENTHAM R H,et al.Physiological characterization ofMycobacteriumsp strain 1B isolated from a bacterial culture able to degrade high-molecular-weight polycyclic aromatic hydrocarbons[J].Journal of Applied Microbiology,2004,97(2):246-255.
[30] PENG H,YIN H,DENG J,et al.Biodegradation of benzo a pyrene byArthrobacteroxydans B4[J].Pedosphere,2012,22(4):554-561.
[31] YESSICA G P,ALEJANDRO A,RONALD F C,et al.Tolerance,growth and degradation of phenanthrene and benzo a pyrene byRhizobiumtropici CIAT 899 in liquid culture medium[J].Applied Soil Ecology,2013,63:105-111.
[32] PING L,ZHANG C,ZHANG C,et al.Isolation and characterization of pyrene and benzo a pyrene-degradingKlebsiellapneumonia PL1 and its potential use in bioremediation[J].Applied Microbiology and Biotechnology,2014,98(8):3819-3828.
[33] MASAKORALA K,YAO J,CAI M,et al.Isolation and characterization of a novel phenanthrene(PHE) degrading strainPsuedomonassp. USTB-RU from petroleum contaminated soil[J].Journal of Hazardous Materials,2013,263:493-500.
[34] CUI Z,XU G,GAO W,et al.Isolation and characterization ofCycloclasticusstrains from Yellow Sea sediments and biodegradation of pyrene and fluoranthene by their syntrophic association withMarinobacterstrains[J].International Biodeterioration & Biodegradation,2014,91:45-51.
[35] 姜岩,杨颖,张贤明.典型多环芳烃生物降解及转化机制的研究进展[J].石油学报(石油加工),2014(6):1137-1150.
JIANG Y,YANG Y,ZHANG X M.Review on the biodegradation and conversion mechanisms of typical polycyclic aromatic hydrocarbons[J].Acta Petrolei Sinica (Petroleum Processing Section),2014(6):1137-1150.
[36] GUO C L.Biodegradation ability and community structure of bacteria in mangrove sediments contaminated by polycyclic aromatic hydrocarbons(PAHs)[D].Hong Kong:City University of Hong Kong,2006.
[37] 张杰,刘永生,冯家勋,等.多环芳烃降解菌ZL5分离鉴定及其降解质粒[J].应用与环境生物学报,2003,9(4):433-435.
ZHANG J,LIU Y S,FENG J X,et al.Isolation and identification of PAHs-degrading strain ZL5 and its degradative plasmid[J].Chinese Journal of Applied & Environmental Biology,2003,9(4):433-435.
[38] PINYAKONG O,HABE H,SUPAKA N,et al.Identification of novel metabolites in the degradation of phenanthrene bySphingomonassp. strain P2[J].FEMS Microbiology Letters,2000,191(1):115-121.
[39] LUAN T G,YU K S H,ZHONG Y,et al.Study of metabolites from the degradation of polycyclic aromatic hydrocarbons(PAHs) by bacterial consortium enriched from mangrove sediments[J].Chemosphere,2006,65(11):2289-2296.
[40] 田雷.微生物降解菲的研究[D].上海:华东理工大学,2000.
[41] KIM Y H,FREEMAN J P,MOODY J D,et al.Effects of pH on the degradation of phenanthrene and pyrene byMycobacteriumvanbaalenii PYR-1[J].Applied Microbiology and Biotechnology,2005,67(2):275-285.
[42] MIHELCIC J R,LUTHY R G.Microbial degradation of acen-aphthene and naphthalene under denitrification conditions in soil-water systems[J].Applied and Environmental Microbiology,1988,54(5):1188-1198.
[43] RAMSAY J A,HAO L ,BROWN R S,et al.Naphthalene and anthracene mineralization linked to oxygen,nitrate,Fe(Ⅱ) and sulphate reduction in a mixed microbial population[J].Biodegradation,2003,14:321-329.
[44] BARBARO J R,BARKER J F.Controlled field study on the use of nitrate and oxygen for bioremediation of a gasoline source zone[J].Bioremediation Journal,2000,4:259-270.
[45] MCNALLY D L,MIHELCIC J R,LUEKING D R.Biodegradation of three-and four-ring polycyclic aromatic hydrocarbons under aerobic and denitrifying conditions[J].Environmental Science & Technology,1998,32:2633-2639.
[46] KRAIG J,SAMBHUNATH G.Feasibility of anaerobic biodegradation of PAHs in dredged river sediments[J].Water Science and Technology,1998,38(7):41-48.
[47] HAYES L A,NEVIN K P,LOVELY D R.Role of prior exposure on anaerobic degradation of naphthalene and phenanthrene in marine harbor sediments[J].Organic Geochemistry,1990,30:937-945.
[48] ROTHERMICH M M,HAYES L A,LOVELY D R.Anaerobic,sulfate-dependent degradation of polycyclic aromatic hydrocarbons in petroleum-contaminated harbor sediment[J].Environmental Science & Technology,2002,36:4811-4817.
[49] ZHANG X,SULLIVAN E R,YOUNG L.Evidence for aromatic ring reduction in the biodegradation pathwayof carboxylated naphthalene by a sulfate reducing consortium[J].Biodegradation,2000,11(23):117-124.
[50] RABUS R,WIDDEL F.Anaerobic degradation of ethylbenzene and other aromatic hydrocarbons by new denitrifying bacteria[J].Archives of Microbiology,1995,163(2):96-103.
[51] TSAI J C,KUMAR M,LIN J G.Anaerobic biotransformation of fluorene and phenanthrene by sulfate-reducing bacteria and identification of biotransformation pathway[J].Journal of Hazardous Materials,2009,164(2):847-855.
[52] ZHANG X,YOUNG L Y.Carboxylation as an initial reaction in the anaerobic metabolism of naphthalene and phenanthrene by sulfidogenic consortia[J].Applied and Environmental Microbiology,1998,63(12):4756-4764.
[53] KRAIG J.Anaerobic biodegradation of polycyclic aromatic hydrocarbons in dredged material[D].Utah:The University of Utah,2000.
[54] LANGENHOFF A A M,ZEHNDER A J B,SCHRAA G.Behaviour of toluene,benzene and napththalene under anaerobic conditions in sediment columns[J].Biodegradation,1996,7:267-274.
[55] GENTHNER B R S,TOWNSEND G T,LANTZ S E,et al.Persistence of polycyclic aromatic hydrocarbon components of creosote under anaerobic enrichment conditions[J].Archives of Environmental Contamination and Toxicology,1997,32:99-105.
[56] CHANG W,UM Y S,HOLOMAN T R P.Polycyclic aromatic hydrocarbon(PAH) degradation coupled to methanogenesis[J].Biotechnology Letters,2006,28:425-430.
[57] 谭文捷,李宗良,丁爱中,等.土壤和地下水中多环芳烃生物降解研究进展[J].生态环境,2007,16(4):1310-1317.
TAN W J,LI Z L,DING A Z,et al.Biodegradation of polycyclic aromatic hydrocarbons (PAHs) in soil and groundwater:a review[J].Ecology and Environment,2007,16(4):1310-1317.
[58] CHANG B V,SHIUNG L C,YUAN S Y.Anaerobic biodegradation of polycyclic aromatic hydrocarbon in soil[J].Chemosphere,2002,48:717-724.
[59] LI C H,WONG Y S,WANG H Y,et al.Anaerobic biodegradation of PAHs in mangrove sediment with amendment of NaHCO3[J].Journal of Environmental Sciences,2015,30:148-156. □
Research Progress of Biodegradation of Polycyclic Aromatic Hydrocarbons with Amendment of Different Electron Acceptors
HOU Xiaopeng1,2, LI Chunhua1, YE Chun1, XU Shihong2, ZHENG Xiangyong3
1.Chinese Research Academy of Environmental Sciences, Beijing 100012, China 2.School of Environmental Science and Engineering, Donghua University, Shanghai 201620, China 3.Zhejiang Provincial Key Lab for Water Environment and Marine Biological Resources Protection, Wenzhou 325035, China
As an essential material in microbial metabolism, the electron acceptors have a very important impact on the number of microorganisms of various types and their ability to biodegrade polycyclic aromatic hydrocarbons (PAHs). The impact of different electron acceptors on the microbial degradation of PAHs was analyzed. The microorganism types and degradation approaches of aerobic biodegradation, with oxygen as electron acceptor, were summarized. In terms of anaerobic biodegradation, a review of research progress was provided for different electron acceptors such as nitrate, sulfate, Fe(Ⅲ) or Mn(Ⅳ) and carbonate. The existing problems in the research on microbial degradation of PAHs were briefed and the prospects of future development provided.
polycyclic aromatic hydrocarbon; electron acceptor; biodegradation; degradation efficiency; degradation pathway
侯晓鹏,李春华,叶春,等.不同电子受体作用下微生物降解多环芳烃研究进展[J].环境工程技术学报,2016,6(1):78-84.
HOU X P, LI C H, YE C, et al.Research progress of biodegradation of polycyclic aromatic hydrocarbons with amendment of different electron acceptors [J].Journal of Environmental Engineering Technology,2016,6(1):78-84.
2015-07-09
国家自然科学基金项目(41101487);浙江省亚热带水环境与海洋生物资源保护重点实验室开放基金项目
侯晓鹏(1990—),男,硕士,主要从事水环境污染化学研究,hxp103@sina.cn
李春华(1977—),女,副研究员,博士,主要从事环境微生物、生态健康评价、水体生态修复研究,lich@craes.org.cn
X172
1674-991X(2016)01-0078-07
10.3969j.issn.1674-991X.2016.01.012

