新型荧光探针法检测食品中的亚硫酸盐含量
吕勇智 李宏达 邹 宁 张 硕 朱 昱(中国刑事警察学院 辽宁 沈阳 110035)
新型荧光探针法检测食品中的亚硫酸盐含量
吕勇智 李宏达 邹 宁 张 硕 朱 昱
(中国刑事警察学院 辽宁 沈阳 110035)
亚硫酸盐是常见的食品添加剂,然而对人体却有一定的毒性。通过设计、合成了一种新型的基于羟基半花菁染料的荧光探针(HHC),可以实现快速、准确、高效地检测食品检材中的亚硫酸氢根。探针分子具有较大的摩尔消光系数,可以实现可视化检测。另外,HHC探针荧光强度的变化量与浓度呈现良好的线性关系,并具有较低的极限检测浓度,可成功的应用于食品检材中浓度水平的监测。
荧光探针 亚硫酸盐检测 定量分析 食品检材
食品安全是一个重大的战略性问题,事关人民的身体健康和社会的和谐稳定。食品添加剂是食品中的必要成分,对食品添加剂的检验已日渐成为食品安全领域的一项重要工作[1]。亚硫酸盐(或)常作为食品和饮料中的添加剂,是一类很早就在世界范围内广泛使用的食品添加剂。然而亚硫酸盐具有一定毒性,大量的摄入可能导致皮肤过敏,呼吸道疾病(如哮喘),胃肠道疾病及脏器损伤等[2-3]。美国食品药物管理局(The United States Food and Drug Administration,FDA)规定食物中的亚硫酸盐的含量不得超过10μg/mL[4]。
目前,检测亚硫酸盐的方法有很多种,例如滴定法[5]、蒸馏法[6]、比色法[7]、离子色谱法[8]、分光光度法[9]、电化学法[10]、毛细管电泳法[11]、酶催化法[12]等。这些方法中或者由于前处理比较繁琐,需要借助大型分析仪器,检测时间较长,或者存在灵敏度低,选择性差等缺点,因而在食品检材中对于微量亚硫酸盐的检测受到一定限制。荧光探针法[13-21]具有灵敏度高、选择性好、操作简便、检测速度快等优点,引起了许多科学家的关注。本文设计合成了基于羟基半花菁染料的荧光探针HHC。该探针存在着非常强的分子内电荷转移(ICT),在长波长处产生非常强的红色荧光信号;当亚硫酸盐与探针HHC中的C=C作用后,阻碍了ICT作用,导致红色荧光信号发生猝灭,且测得的荧光信号变化量与加入的亚硫酸盐浓度之间呈现良好的线性关系。本文在优化反应条件的基础上,建立了检测食品检材中亚硫酸盐含量的新型荧光探针法。该方法具有操作简便,响应快速,灵敏度高等优点,存在着巨大的应用前景。探针HHC的合成路线及与HSO3-的作用机理如图1所示。
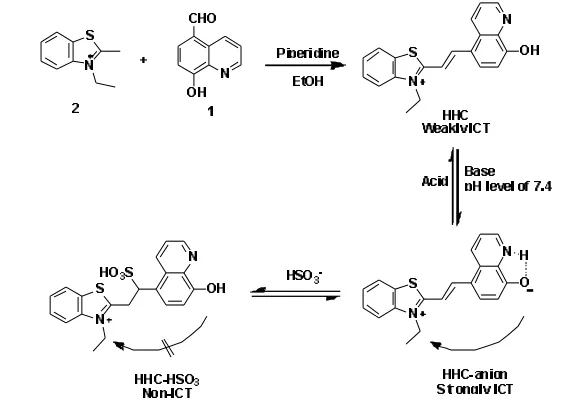
图1 探针HHC的合成路线及与的作用机理
1 实验仪器和材料
1.1 实验仪器
荧光和紫外分光光度计采用岛津公司的RF-5301PC和UV-2550进行测试,核磁共振仪采用Bruker AV-300进行测试,MALDI-TOF MS质谱仪采用岛津公司的AXIMA-CFRTM进行测试,HRMS (ESI-TOF)采用Bruker microTOF II focus进行测试。
1.2 实验材料
实验所用的原料样品及溶剂均来自国药控股有限公司,购买后未经处理直接使用。水,冰糖,红酒,白砂糖均采购于沈阳家乐福超市。层析硅胶采购于青岛海洋化工特种硅胶有限公司。
2 实验内容
2.1 荧光探针HHC的合成及表征
将200mg浓度为1.2mmol的碘化3-乙基-2-甲基-3-苯并噻唑(2)和354mg浓度为1.2mmol的8-羟基-5-喹啉甲醛(1)溶于5.0mL的无水乙醇中,然后添加2滴哌啶溶液作为反应的催化剂,在N2环境中,加热回流4小时,然后冷却至室温,加入适量的乙醚,将析出的晶体过滤,再用乙醇重结晶析出灰白色固体HHC (265.2mg)产率为48%。1H NMR(300MHz,DMSO-d6,ppm)δ:9.06(d,J=8.6Hz,1H,ArH),9.00(d,J=3.9Hz,1H,ArH),8.84(d,J=15.2Hz,1H,-CH=CH-Ar),8.64(d,J=8.3Hz,1H,ArH),8.45(d,J=8.1Hz,1H,ArH),8.31(d,J=8.4Hz,1H,ArH),8.05(d,J=15.3Hz,1H,-CH=CH-Ar),7.89(t,J=7.4Hz,1H,ArH),7.82-7.78(m,2H,ArH),7.33(d,J=8.4Hz,1H,ArH),5.00(q,J=6.8Hz,2H,-CH2-CH3),1.50(t,J=6.7Hz,3H,-CH2-CH3).13C NMR(75MHz,DMSO-d6,ppm)δ:162.2,147.3,141.7,140.6,136.1,132.4,131.0,128.2,125.2,125.1,124.9,124.7,123.1,122.3,114.1,113.8,112.8,95.0,44.3,13.0.MALDI-TOF Ms m/z:333.4 [M-I]+,HRMS(ESI-TOF)Calcd for C20H17N2OS+([M]+)333.1056.Found:333.1063。
用二甲基亚砜(DMSO)作为溶剂制备5× 10-4mol/L HHC储备液,并用磷酸盐缓冲液(10mmol/L,pH=7.4,2%DMSO)将其稀释到1×10-5mol/L。其他溶液用磷酸盐缓冲溶液(10mmol/L,pH=7.4,2%DMSO)溶解制备。在25℃下,采用10mm比色皿,吸收光谱扫描范围是200nm到700nm,找到HHC探针的最大吸收波长为568nm。然后配置不同浓度的溶液,往HHC探针溶液中滴加溶液,振荡摇匀并以568nm为激发波长,狭缝宽度5nm,扫描范围为550nm到800nm,测得与HHC探针混合液的荧光发射光谱图。
用去离子水作为溶剂制备浓度均为0.25g/mL的冰糖和白砂糖储备液,并用去离子水将红酒稀释100倍。然后将适量的(0,0.15或0.20μmol/L)样品储备液、HHC溶液(10μmol/L)加入3mL磷酸盐缓冲溶液(10mmol/L,pH7.4,2%DMSO)中,并在25℃条件下测定荧光强度。
2.4 检测限(LOD)
本实验的检测限用LOD=3δ/k表示,δ指10次空白测定结果的标准差,k指拟合曲线的斜率。
3 结果与讨论
3.1 光谱性质
由于大多数亚硫酸盐是添加在食物中,所以要求荧光探针在水介质中也可以进行测定。本文考察了不同pH浓度对荧光探针HHC测定的影响(如图2所示)。结果显示当溶液pH在7.4~9.0之间,在激发波长568nm测定下HHC的荧光强度最大,而当pH降到4,吸收带蓝移,最大吸收波长从568nm移动到431nm,紫红色溶液变为黄色(如图3所示)。由此可见,HHC在弱碱性溶液中去质子化,此时探针HHC的最大吸收波长为568nm,呈现紫红色,且最大发射波长为591nm(激发波长为568nm,如图6所示)。HHC与结合前,由于分子内电荷的转移(亚胺离子和酚羟基上氧负离子相互作用),使得HHC产生了强烈的荧光效应。而当(50mol/L)加入到HHC溶液中,在568nm和591nm处的最大吸收峰和最大发射峰消失,溶液颜色从紫红变为无色。由于反应前后产生明显的颜色变化,因此,HHC能够用于的可视化检测。另外,根据滴定曲线和Job拟合曲线可知,HHC和之间的化学计量比为1∶ 1(如图4所示),通过ESI-MS可知,[HHC-HSO3]+=415.51,也进一步证明了两者之间的化学计量比为1∶1,同时也印证了图1所示的反应机理。

图2 不同pH条件下探针HHC的荧光强度

图3 探针HHC(10μmol/L)在pH分别为4.0、7.4和9.0时的吸收谱图
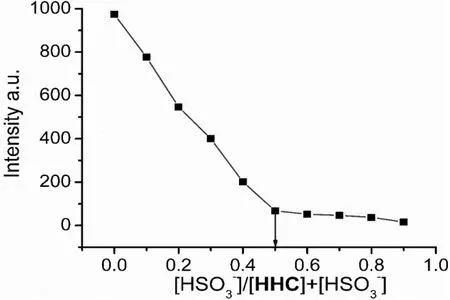
图4 探针HHC与作用的Job拟合曲线
在发射光谱中,我们可以看到在591nm处混合溶液的荧光强度随着浓度的增加而逐渐减弱,并且荧光强度的变化量与加入的浓度(0~10μmol/L)呈现很好的线性关系(R2=0.999,如图6所示),检测极限为6.8mol/L。

图5 探针HHC(10μmol/L)响应的吸收光谱图

图6 探针HHC(10μmol/L)响应的发射光谱图
在室温条件下,对探针HHC与类似分析物之间的相互作用进行了研究(分析物包含:阴离子、氧化剂和生物硫醇,如图7所示)。柱状图结果表明:仅有能够使探针HHC在591nm处的发射峰消失,其他分析物与HHC不发生作用,探针HHC与的相互作用不受其他分析物的干扰。因此,探针HHC可应用于复杂样品中的检测。

图7 探针HHC(10μmol/L)识别的选择性和干扰性柱状图
实验选取自来水、冰糖、稀释的红酒和白砂糖作为待测食品检材,利用探针HHC对待测检材进行分析。结果表明,探针HHC可以快速、准确、高效地识别食品检材中及加标样品中的,且都获得了非常理想的回收率(93.3%~101.4%,如表1所示)。此外,利用我们的检测方法和传统的滴定法对同一食品检材进行分析,获得了一个高度吻合的结果(如表2所示)。

Sample HSO3-level(μM) NaHSO3 added(μM) NaHSO3 founded by HHC(μM) Recovery% Tap water - - - -1 0.15 0.14±0.008 93.3 2 0.20 0.20±0.009 100.0 Crystal sugar 1.62 - - -1 0.15 1.76±0.012 99.4 2 0.20 1.81±0.022 99.5 Diluted Red wine 0.54 - - -1 0.15 0.70±0.015 101.4 2 0.20 0.73±0.012 98.6 Granualared sugar 2.22 - - -1 0.15 2.36±0.024 99.6 2 0.20 2.41±0.031 99.6
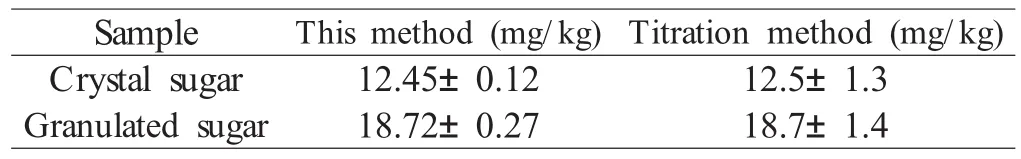
表2 传统滴定法与探针HHC比较分析结果
4 结论
本文成功合成了基于羟基半花菁染料的荧光探针HHC,并将其应用于复杂样品中的定性与定量分析。结果表明,探针HHC不仅能够快速、高灵敏度、高选择性地识别
,而且还可以实现可视化检测的目的。探针HHC的荧光强度变化量与加入的浓度(0~10μmol/L)呈现很好的线性关系,极限检测浓度为6.8nmol/L,可被成功地应用于食品检材中浓度水平监测。此外,这种新型荧光探针法的研究可以促进食品、环保等公共安全领域中无机毒性离子的检测与鉴定的发展。
[1]陈玉梅.亚硫酸盐类在食品中的应用及残留控制[J].检验检疫学刊,2010,3(3):22-24.
[2]党卫红.亚硫酸盐的毒性作用[J].河南预防医学杂志,2008,19(4):318-320.
[3]周志权,温韬,吴保壮.HACCP在亚硫酸法白砂糖生产中的应用[J].广西科学院学报,2008,24(1): 16-18.
[4]SYue,Z Dong,F Shanwei,et al.A Ratiometric Fluorescent Probefor Rapid Detection of Bisulfitethrough 1,4-Addition Reaction in Aqueous Solution[J].Journal of Agricultural&Food Chemistry,2014,62(15):3405-3409.
[5]王若燕,郁欣,周晓萍.直接碘量法测定银耳中的二氧化硫残留量[J].预防医学文献信息,2000,6(1):63.
[6]老倩群,梁志华.对蒸馏法测定亚硫酸盐的几点看法[J].广东卫生防疫,1998,24(3):11-12.
[7]张静,耿振新,吴建军.盐酸副玫瑰苯胺比色法测定食品中亚硫酸盐方法的要点及改进[J].职业与健康,2010,26(13):1483-1484.
[8]刘喆,刘克纳,宋强,等.离子排斥色谱法、脉冲安培检测器对食品中亚硫酸及其盐的分析与检测[J].食品与发酵工业,1997,23(4):19-20.
[9]SSM Hassan,MSA Ha mza,AHK Mohamed.A Novel Spectrophotometric Method for Batch and Flow Injection Determination ofSulfitein Beverages[J].Analytica ChimicaActa,2006,570(2):232-239.
[10]游京晶,李冬梅,戚苓,等.电位滴定法测定食品中的亚硫酸盐[J].食品与发酵工业,1992(3):60-66.
[11]G Jankovskiene,Z Daunoravicius,A Padarauskas.CapillaryElectrophoreticDeterminationofSulfiteUsingthe Zone-passing Technique ofin-capillary Derivatization [J].JournalofChromatographyA,2001,934(1-2):67-73.
[12]L He,W Lin,Q Xu,et al.A Unique Type of Pyrrole-Based Cyanine Fluorophores with Turn-on and Ratiometric Fluorescence Signalsat Different pH Regions for Sensing pH in Enzymesand Living Cells[J].ACS Appl.Mater.Interfaces,2014,6:22326-22333.
[13]王猛.LaF3:Eu,Tb荧光纳米粉末的制备及其在手印显现中的应用[J].中国刑警学院学报,2015(2): 56-58.
[14]张振宇,邹宁,齐宝坤,等.荧光光谱法检验车辆上的润滑油[J].中国刑警学院学报,2004(1):55-56.
[15]刘丽,李勇,金勇镒.荧光复合材料在手印显现中的应用研究[J].中国刑警学院学报,2012(4):27-28.
[16]谢涛,林添春,王猛.纳米发光材料在手印无损DNA显现中的研究[J].中国刑警学院学报,2015(3): 71-73.
[17]SYimin,Z Cheng,G Rui,et al.ARatiometric Fluorescent Chemodosimeter with Selective Recognition for Sulfite in Aqueous Solution [J].Journal of Organic Chemistry,2009,74(20):7943-7946.
[18]SYuan-qiang,W Pi,L Jing,et al.A fluorescent Turn-on Probe for Bisulfite Based on Hydrogen Bond-inhibited C=N isomerizationmechanism[J].Analyst,2012,137(15):3430-3433.
[19]J Chao,Y Zhang,H Wang,et al.Fluorescent Red GK asa Fluorescent Probe for Selective Detection of Bisulfite Anions [J].Sensors & Actuators B Chemical,2013,188(11):200 206.
[20]YChen,X Wang,XFYang,et al.Development of a Ratiometric Fluorescent Probe for Sulfite Based on a Coumarin-benzopyrylium Platform[J].Sensors&Actuators B:Chemical,2015(206):268-275.
[21]LJing,SYuan-qiang,H Yingying.Simultaneous Fluorescence Sensing of Cys and GSH from Different Emission Channels[J].Journal of the American Chemical Society,2014,136(2):574-577.
DF794.3
A
2095-7939(2016)01-0077-04
2015-11-25
2015年度辽宁省教育厅科技研究项目;2015年度中国刑事警察学院研究项目。
吕勇智(1990-),男,福建厦门人,中国刑事警察学院硕士研究生,主要从事刑事毒物、毒品分析检验研究。
孟凡骞)

