氧化还原反应在化学教学中的作用
氧化还原反应在化学教学中的作用
◇江苏陈瑞玉
氧化还原反应是重要而普遍的化学反应,提示了物质变化的本质和规律,是教学的重、难点,同时也是氧化还原反应高考的考点,应用十分广泛.如合成氨工业、硝酸工业、硫酸工业、氯碱工业、金属的腐蚀和防护等诸多方面都涉及氧化还原反应,因而其在学教学中占有重要的地位,对学生学好化学、用好化学起着重要作用.
1提高学生的认识水平
氧化反应和还原反应既对立统一又相互依存,通过教与学可培养学生辨证的思维方式,是提高学生认识能力的典型素材,并指导学生从宏观世界进入微观世界认识事物发展变化的本质.
例如:金属铁在氯气中燃烧,化学方程式为
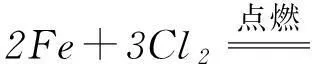
在上述反应中,每个Fe原子失去3个电子,每个Cl原子得到1个电子,可将上述反应拆分为2个半反应.
氧化反应:Fe-3e-=Fe3+,失电子,被氧化.
还原反应:Cl+e-=Cl-,得电子,被还原.
由此可见,在氧化还原反应中,化合价有升降,电子有得失,氧化反应和还原反应是同时进行的,相互对立又相互依存,不可分割,共存于同一化学反应中.
2帮助学生掌握物质变化的规律
氧化还原反应有其特殊的规律,掌握好其规律性,对元素及其化合物的学习有十分重要的意义.
1) 氧化剂具有氧化性,还原剂具有还原性规律.
2) 氧化剂越易得电子,氧化性就越强;还原剂越易失电子,还原性就越强,其阳离子氧化性就越弱;单质氧化性越强,其阴离子还原性就越弱.
3) 最低价态的元素只具有还原性,最高价态的元素只具有氧化性,价态处于中间的元素既有氧化性又具有还原性.
例如:H2S中-2价的硫元素只有还原性,H2SO4(浓)中+6价的硫元素只有氧化性,SO2中+4价的硫元素既有氧化性又有还原性.
4) 从具体的氧化还原反应判断强弱.
氧化性: 氧化剂大于氧化产物.
还原性: 还原剂大于还原产物.
5) 同种元素不同价态间的反应规律.
同种元素的不同价态之间的氧化还原反应,价态的变化“只靠拢,不相交”,相邻价态元素之间的物质不发生氧化还原反应.
利用氧化还原反应规律,可对物质的性质进行归类总结,在学习元素及其化合物性质时也能达到事半功倍的目的.
例: 推导归纳FeCl3的性质.
a) 具有盐的性质.
b)FeCl3属于铁的高价化合物,具有氧化性.
3促进学生学以致用
在教学过程中,要不断有效地拓展知识面,培养学生养成创造性学习的习惯.要做到所学知识来源于课本,又不拘泥于课本,结合实际,营造问题,能利用所学知识进行解疑,这才是教与学的宗旨.例如,凡能自发进行的氧化还原反应都可以设计原电池,根据这一点可让学生完成下列原电池的设计.

正极:2H2O+2e-=2OH-+H2.
总反应:2Al+2H2O+2OH-=2AlO2-+3H2↑.
金属镁的活泼性比铝强,但铝在浓硝酸中“钝化”,而金属性弱的铜和浓硝酸反应,因而铜为负极,铝为正极.
由以上事例可看出,在学好氧化还原反应原理基础之上,还应促进学生自主学习能力的运用,才能对所学知识进行发散式延伸,才能更好地应用.
总之,氧化还原反应的教学在中学阶段起着相当重要的作用,能够帮助学生学好化学,用好化学,让学生进入微观世界认识事物的本质.
(作者单位:江苏省宝应县画川高级中学)

