基于胶乳增强免疫比浊法的食物过敏原检测试剂盒方法学的建立及临床应用评价①
卢玲玲 郑国军 涂斐佩 吴海鸥 林晓琼
(瑞安市中医院检验科,瑞安325200)
基于胶乳增强免疫比浊法的食物过敏原检测试剂盒方法学的建立及临床应用评价①
卢玲玲郑国军②涂斐佩吴海鸥林晓琼
(瑞安市中医院检验科,瑞安325200)
[摘要]目的:建立基于胶乳增强免疫比浊法的食物过敏原检测试剂的方法并应用于临床。方法:采用胶乳增强免疫比浊法,对检测体系的标准曲线、最低检测量、稳定性、精密度、干扰实验等相关性能指标进行评价,通过检测健康体检人员及临床过敏人群血液标本并与目前应用于临床的较成熟的ELISA方法进行比对,评价胶乳增强免疫比浊法的食物过敏原检测试剂的临床应用可行性。结果:该方法的标准曲线Y=837.1x2-125.2x+10.036,线性范围:0~400 U/ml,相关系数为0.996,最低检测限为19.600 U/ml。批内、批间精密度均<10%。该方法的正常参考范围为<33.5 U/ml,敏感度89.61%,特异性65.22%,准确度84.00%,阳性预示值89.61%,阴性预示值65.22%,ROC的曲线下面积(AUC)为0.957,该方法与目前应用较广泛的ELISA法具有很强的相关性(r=0.890 2)。结论:胶乳增强免疫比浊法的食物过敏原检测试剂符合临床诊断的相关要求,可应用于临床食物过敏性患者的诊断及疾病监测。
[关键词]胶乳;免疫比浊;方法学;过敏原
过敏疾病为常见病、多发病,严重时可造成过敏性休克,甚至危及生命,约35%的过敏反应由食物诱发。其中我市近年来病史资料查询显示,蟹过敏人数较多,呈递增趋势。
本项目拟采用乳胶增强法进行国产化的蟹食物过敏原检测试剂盒的开发。替代现有食物过敏原ELISA检测试剂盒,此新型的产品可以用于迟发相食物过敏反应的临床诊断,检测食物过敏原,为预防和治疗过敏反应,排除类似过敏症状慢性疾病的误诊提供辅助诊断依据。并且在此项目建立的基础方法上我们将继续展开其他类型食物过敏原的检测项目。本项目的开展为加强食品安全检测提供技术支持,提升我国食品安全的发展具有非常重要的意义。
1材料与方法
1.1材料
1.1.1临床标本选取2013年6月至2015年6月在瑞安人民医院及瑞安市中医院蟹过敏患者100例,健康体检人员100例,采集他们的血清标本置-80℃冰箱保存备用。
1.1.2试剂和仪器主要试剂:浙江天科高新技术发展有限公司制备:蛋白缓冲液:25 mmol/L磷酸盐缓液(pH7.2~7.4),蟹蛋白过敏原致敏乳胶颗粒2.5 mg/ml;校准品人IgG(400 U/ml)购自杭州浙大迪迅生物基因工程有限公司[校准品溯源自 WHO International Stardard :Immunoglobulins G, A and M, human serum (67/086)];主要仪器:贝克曼库尔特IMMAGE 800特定蛋白分析:美国。
1.2分析性能评价
1.2.1试剂稳定性检测将标准品人IgG稀释成5个浓度(0、50、100、200、400 U/ml)来验证蟹蛋白过敏原致敏乳胶颗粒的稳定性。分别检测蛋白缓冲液与致敏乳胶颗粒在37℃/7 d、4℃/30 d、4℃/180 d的稳定性。
1.2.2标准曲线将人IgG标准蛋白稀释成0 U/ml(A)、6 U/ml(B)、30 U/ml(C)、150 U/ml(D)、400 U/ml(E)5个点,测试5次,由贝克曼库尔特IMMAGE 800特定蛋白分析自带软件绘制蟹蛋白的检测标准曲线。
1.2.3最低检测限与空白值空白检测限使用的是无蟹蛋白的血清标本;最低检测限采用无过敏性疾病的健康体检人员血清标本,稀释5倍后检测。最低检测限与空白检测标本均分为两个批次,连续5 d检测6次。本方法严格按照国际临床化学标准委员会(NCCLS)EP17-A进行。
1.2.4分析不精密度分别检测三个批次(标记为20150110、20150210和20150710)的试剂检测三种蛋白高、低两个浓度(200 U/ml,20 U/ml)各3次/d,连续20 d,分别计算批内及批间的变异系数。本方法严格按照国际临床化学标准委员会(NCCLS)EP5-A2进行。
1.2.5交叉反应分别选择鸡蛋、虾、牛奶的等食物IgG阳性、蟹IgG阴性的血清标本,与蟹蛋白过敏原致敏乳胶颗粒同时检测,照上述实验方法测定吸光度OD值,在同样条件下同时检测单一蟹IgG阳性的标本,作为基础样品测定值,计算与其他种类食物IgG的交叉反应情况。
1.2.6干扰实验将相当于甘油三酯浓度为2.00、3.00、4.00、5.00 mmol/L的橄榄油乳剂,血红蛋白含量为0.5、1.5、2.5、5 g/L的血红蛋白溶血液加到蟹IgG浓度为200 U/L的血清中,测定蟹IgG浓度,将实际测定值与理论预期值相比较,以误差大于10%为判断标准,观察脂血及溶血对该方法的影响。
1.2.7正常参考范围检测100份正常体检无明显临床疾病血清标本[男∶女=60∶40,年龄(39.03±15.98)岁],确定检测蟹食物蛋白的正常参考范围。
1.2.8方法学比较分别将100份蟹食物蛋白标本进行酶联免疫吸附实验(ELISA,仪器奥地利BioTek-Elx800,试剂批号:1505007)和PETIA(胶乳增强免疫比浊法)检测,检测结果进行线性回归计算其相关系数

2结果
2.1蟹蛋白过敏原致敏乳胶颗粒的稳定性检测试剂在37℃/7 d、4℃/30 d、4℃/180 d均保持稳定。结果见表1。
2.2最低检测限与空白值最低检测限(LoD)为19.600 U/ml,空白检测限(LoB)为13.241 U/ml;(计算公式:LoD: 13.241±2×3.844, LoD=LoB+2SD LoB:7.102 7±3.711 3, LoB=average+2SD)。所有检测数据均呈正态分布。
2.3检测范围与标准曲线以吸光度值OD为横坐标,以IgG的浓度为纵坐标,进行标准曲线拟合,其剂量-反应曲线见图1,标准曲线Y=837.1x2-125.2x+10.036相关系数为0.996,线性范围为0~400 U/ml。
表1试剂稳定性
Tab.1Stability of reagent

Proposedconcentration37℃OD7dconcentration(U/ml)4℃OD30dconcentration(U/ml)37℃OD180dconcentration(U/ml)A(0U/ml)0.0237.590.0316.960.0138.55B(50U/ml)0.29244.850.31955.280.32457.35C(100U/ml)0.39189.060.40596.640.38988.00D(200U/ml)0.562204.070.582220.720.549193.60E(400U/ml)0.765404.150.761399.540.785427.60
表2批内精密度
Tab.2Results of intra-assay precision

Proposedconcentration(U/ml)20150110IgG(U/ml)CV(%)20150210IgG(U/ml)CV(%)20150710IgG(U/ml)CV(%)20.022.52±1.787.925.35±2.289.018.79±1.548.2200212.08±18.678.8190.95±15.288.0219.06±15.557.1
表3批间的精密度(n=3×8)
Tab.3Results of inter-assay precision (n=3×8)

Additionalconcentration(U/ml)IgG(U/ml)CV(%)20.025.88±1.716.6200209.69±17.048.3
表4不同食物间交叉反应率
Tab.4Cross-reactivity rate of different kinds of food

Antigentypescross-reactionrate(%)EggShrimpMilkSoybeanBeefPorkCrab6.137.313.022.783.252.56
表5蟹IgG(200 U/ml)浓度中加入干扰物后预测值与实测值的比较
Tab.5Comparison of predicted values and measured values after Crab IgG(200 U/ml ) joining distractors

Crab-IgGconcentration(U/ml)Triglycerideconcentration(mmol/L)2345Hemoglobinconcentration(g/L)0.51.52.55Predictedvalue200200200200200200200200Measuredvalue195189193179192193188175Error2.55.53.510.54.03.56.012.5

图1 蟹蛋白过敏原胶乳免疫增强检测法标准曲线Fig.1 Crab protein standard curve of PETIA
2.4精密度交叉反应高低两个IgG浓度的变异系数(CV)分别为:批号20150110为7.9%和8.8%;批号20150210为9.0%和8.0%;批号20150710为8.2%,7.1%。批间变异系数分别为6.6%,8.3%;甘油三酯浓度在5.00 mmol/L以上,血红蛋白浓度在5g/L以上对蟹IgG检测浓度产生影响。见表2~5。
2.5参考范围所有检测数据均呈正态分布,其平均值为12.02 U/ml,标准差为10.753,得出胶乳免疫增强比浊法检测血清特异性蟹IgG的95%可信区间为<33.5 U/ml。将血清中蟹特异性IgG值大于33.5 U/ml的患者认定为阳性。见图2。

图2 蟹血清特异性IgG正态分布图Fig.2 Eyes crab serum specific IgG normal distribution
2.6ROC工作曲线收集100份蟹过敏性患者血清(男∶女=46∶54,年龄1~36岁)。结合临床,共有77名患者确诊为蟹过敏性疾病。胶乳免疫增强比浊法的敏感度89.61%,特异性65.22%,准确度84.00%,阳性预示值89.61%,阴性预示值65.22%(表6)。ROC的曲线下面积(AUC)为 0.957 (图3)。
2.7方法学比较收集100份患者血清,用PETIA法以及临床在用的ELISA法同时进行检测。回归方程为Y=1.264x+27.599(Y为ELISA法结果,x为PETIA法结果),相关系数为0.890 2(图4)。线性回归结果表明,两者具有良好的相关性,该结果表明我们新创的PETIA法可用于临床血清标本中蟹食物过敏原。
表6PETIA方法的敏感性和特异性
Tab.6Sensitivity and specificity of PETIA

ClinicaldiagnosisofallergiesTotal+-CrabIgG+69877-81523Total7723100
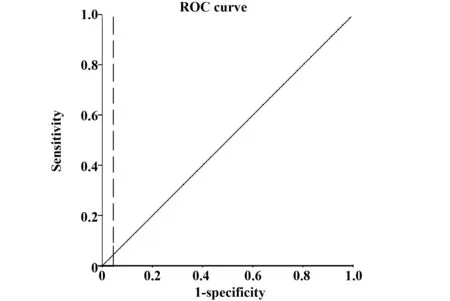
图3 PETIA ROC曲线Fig.3 ROC curve of PETIA

图4 ELISA和PETIA方法比较的线性回归图Fig.4 Comparison between ELISA and PETIA
3讨论
胶乳增强免疫比浊法(PETIA)是近年来出现的一种较为稳定、准确的体液蛋白均相免疫比浊检测方法[1-3]。是在高分子胶乳微球的表面交联抗体或抗原,当交联有抗体或抗原的微球与抗原或抗体结合后,在短时间内会迅速聚集在一起,改变了反应液的散光性能或透光性能。而且,反应液散光性能或透光性能(即吸光度)的改变与被测抗原或抗体的浓度有较强的相关性,在一定范围内可以反映被测物的浓度。PETIA法操作步骤的简化也相应地避免了许多人为操作因素和试剂、环境等外界因素的干扰,稳定性和重复性都较好,能较真实地反映被测物质的含量,从而能更好地帮助医生正确地诊断过敏原,并判定该过敏原的致敏反应程度。目前国外关于食物过敏原诊断试剂盒都生产企业主要有瑞典Pharmacia Diagnostis、英国GENESIS、美国BIOMERICA和德国MEDIWISS等公司,而国内主要是杭州浙大迪迅生物基因工程有限公司等公司。这些诊断试剂公司的食物过敏原诊断试剂盒都主要采用ELISA方法[3-12]。
该方法的标准曲线Y=837.1x2-125.2x+10.036,线性范围:0~400 U/ml,相关系数为0.996,本实验建立的蟹食物蛋白PETIA检测法,具有灵敏、特异、操作简单、快速、稳定且易自动化操作等优点,能够满足临床应用的要求:在表1我们看出,经4℃/7 d,37℃/30 d与半年时间检测,所得检测数据与曲线没有明显差异及偏移;方法灵敏,最低检测限(LoD)为19.600 U/ml。线性范围较宽:0~40 U/ml,相关系数为0.996,批内以及批间的变异系数均低于10%;在临床应用上,第一,我们获得参考范围95%可信区间为<33.5 U/ml。将血清中蟹IgG水平大于33.5 U/ml的患者认定为蟹食物过敏原阳性;第二,该方法的敏感度89.61%,特异性65.22%,准确度84.00%,阳性预示值89.61%,阴性预示值65.22%,甘油三酯浓度在5.00 mmol/L以下,血红蛋白浓度在5 g/L以下对蟹IgG检测浓度影响不大,ROC的曲线下面积(AUC)为0.957。第三,收集的100份患者血清,进行PETIA与ELISA法进行结果比对,显示回归方程为Y=1.264x+27.599(Y为ELISA法结果,x为PETIA法结果),相关系数为0.890 2,两者具有良好的相关性,由该结果可见我们新创的胶乳免疫增强比浊法可用于临床血清标本中蟹食物蛋白过敏原的检测,从而预示患者过敏状态的发生发展。所以我们建立的蟹食物蛋白过敏原胶乳免疫增强比浊法,符合2010版《中国药典》中有关体外诊断试剂的应用要求[13]。但也存在很多不足,如,我们改进了实验方法,但在检测范围上与其他检测方法相比并未改进;其次在临床评价上选取的标本例数100例,还需进一步检测,来提高方法的阴性预测值、阳性预测值以及方法的灵敏度与特异性。
参考文献:
[1] 郁新.乳胶增强免疫比浊法测定血清Lp(a)[J].江西医学检验,2007,25(5):433-434.
[2] 于德军,蒙凯.乳胶增强免疫比浊法测定血清胱抑素C[J].检验医学与临床,2011,8(10): 1159 -1160, 1163.
[3] 陈建文,张凡,刘玉侠,等.乳胶增强免疫比浊法测定血清肌钙蛋白I的实验探讨[J].中华全科医学,2013,11(11):1777-1778.
[4] 冯彦娟,袁娟丽,佟平,等.大豆过敏原的检测方法研究进展[J].食品科学,2012,33 (23):365-369.
[5] 廖万清,孟云芳.蛋白质过敏原与食物过敏[J].空军医学杂志,2013,29(1):5-7.
[6] 马超,王伟,吴玉红.慢性荨麻疹患者过敏原特异性IgE与特异性IgG分析[J].安徽医学,2014,35(2): 183-186.
[7] 周煌, 杨安树, 佟平,等.食物过敏原标准物质的研究进展[J].食品工业科技,2012,33 (23):438-443.
[8]闫飞, 廖志勇, 吴志华,等.食物过敏原蛋白的定量检测方法[J].食品科学,2010, 31(19): 426-429.
[9] 徐国强,倪海东,杨明,等.食物过敏原蛋白家族分类及其结构特点[J].检验检疫学刊,2012,22(5): 66-70,76.
[10]顾可飞,李春红,高美须,等.食物过敏原及检测技术的研究进展[J].食品科技,2006,(8):1-5.
[11] 陈颖,王玮.食物过敏原检测方法研究进展[J].检验检疫学刊,2011,21(3):4-7,19.
[12] 石良, 王锡昌, 刘源.食物过敏原免疫学检测技术研究进展[J].分析测试学报,2010, 29(9): 981-986.
[13]中国药物化学委员会.《中国药典》体外诊断试剂规程2010 版[J].北京:中国医药科技出版社,2010:1-200.
[收稿2015-07-16修回2015-11-25]
(编辑张晓舟)
Development and application of Latex enhanced immune turbidimetry for food allergen
LULing-Ling,ZHENGGuo-Jun,TUFei-Pei,WUHai-Ou,LIUXiao-Qiong.
RuianHospitalofTraditionalChineseMedicine,Ruian325200,China
[Abstract]Objective:To establish a method to detect food allergen based on Latex-enhanced immune turbidimetry (PETIA) and apply to clinic.Methods: The PETIA method was used for evaluating the detection system including standard curve, detection-limit,stability, intra-assay and inter-assay precision and cross-reactivity,clinical normal serum specimens and clinical allergic diseases serum specimens were measured to evaluated the perspective of the clinical application.Results: The standard curve :Y=837.1x2-125.2x+10.036, linear range: 0.0-400 U/ml,the correlation coefficient of the standard curve was 0.996,the intrabatch and interbatch precision was<10%.The normal reference range was≤33.5 U/ml,the AUC of ROC curve was 0.957,the sensitivity was 89.61%,The specificity was 65.22%,the accuracy was 84.00%, and the positive predicted value was 89.61%,the negative predicted value was 65.22%.the test results have strong correlation with ELISA (r=0.890 2).Conclusion: The PETIA method for detecting food allergen achieved corresponding clinical application standards and may be used for the diagnosis of food allergies.
[Key words]Latex;Immunonephelometry;Methodology;Allergen
中图分类号R383.2
文献标志码A
文章编号1000-484X(2016)03-0377-05
作者简介:卢玲玲(1984年-),女,硕士,主管检验师,主要从事临床诊断学研究。
doi:10.3969/j.issn.1000-484X.2016.03.018
①本文为瑞安市科技局项目(No.MS2015042)。
②瑞安市人民医院检验科,瑞安325200。

