天麻首乌片的HPLC指纹图谱研究*
苏文俏,彭艳梅,李跃辉,周润维,朱立华
(1.湖南省中医药研究院,长沙410013;2.湖南国华制药有限公司,长沙410013)
天麻首乌片的HPLC指纹图谱研究*
苏文俏1,彭艳梅1,李跃辉1,周润维1,朱立华2△
(1.湖南省中医药研究院,长沙410013;2.湖南国华制药有限公司,长沙410013)
目的:建立天麻首乌片的高效液相色谱指纹图谱。方法:采用Kromasil C18(250×4.6 mm,5 μm)色谱柱,以乙腈-0.3%磷酸水溶液为流动相进行梯度洗脱(0~18 min,5%~15%乙腈;18~32 min,15% ~26%乙腈;32~35 min,26% ~27%乙腈;35~48 min,27%~40%乙腈),检测波长230 nm,柱温30℃,进样量10 μL,分析时间48 min。结果:根据10批样品建立了天麻首乌片的高效液相色谱指纹图谱,确定了18个共有峰,其中包含天麻、何首乌等6味药的特征峰。结论:该法灵敏度高,稳定性和重复性良好,且分析速度较快,可用于天麻首乌片的质量评价。
天麻首乌片;高效液相色谱法;指纹图谱
天麻首乌片是由天麻、白芷、何首乌、熟地黄、丹参、川芎、墨旱莲、女贞子、白芍、黄精、甘草、当归、桑叶、蒺藜(炒)共14味药组成,具有滋阴补肾、养血息风的功能,用于肝肾阴虚所致的头晕目眩、头痛耳鸣、口苦咽干、腰膝酸软、脱发、白发;血管神经性头痛、脂溢性脱发见上述证候者,对治疗头痛、头晕、脱发、白发的效果较为明显。中药指纹图谱方法已广泛用于中药的质量控制,它能更为全面地反映中药中化学成分的相对关系,从而对其进行整体描述和评价[1-2]。本试验中采用 HPLC建立天麻首乌片特征图谱色谱条件,并通过与药材的比较对色谱峰进行定位归属,以期为天麻首乌片的质量控制及评价提供一种较全面的分析手段。
1 仪器与试药
1.1 仪器
LC-20AT型高效液相色谱仪(日本岛津),AL204型电子天平(梅特勒-托利多仪器(上海)有限公司),SHZ-D(Ⅲ)循环水式真空泵(巩义市予华仪器有限责任公司),HX-06型超声清洗器(武汉恒信世纪科技有限公司),HH型恒温水浴锅(江苏金坛市中天仪器厂)。
1.2 试药
对照品二苯乙烯苷(批号110844-201310,按94.9%计)、芍药苷(批号110736-201337,按94.9%计)、天麻素(批号110807-201507,按95.4%计)、没食子酸(批号110831-201204,按94.9%计)、甘草苷(批号111610-201106,按93.7%计)均购于中国食品药品检定研究院,特女贞苷(批号 MUST-11040402,纯度≥98%)购于成都曼斯特生物科技有限公司,甲醇(分析纯,湖南汇虹试剂有限公司),磷酸(分析纯,湖南汇虹试剂有限公司),乙腈(色谱纯,ACE),水为娃哈哈纯净水,天麻、白芷、何首乌、熟地黄、丹参、川芎、墨旱莲、女贞子、白芍、黄精、甘草、当归、桑叶、蒺藜(炒)均购自于长沙老百姓大药房,天麻首乌片(批号分别为20151102、20151104、20151106、20151114、20151123、20151205、20151217、20151222、20160110、20160113)由湖南国华制药股份有限公司提供。
2 方法
2.1 色谱条件
Kromasil C18(250×4.6 mm,5 μm)色谱柱,流动相乙腈(A)-0.3%磷酸水溶液(B)梯度洗脱,0~18 min,5% ~15%A,18~32 min,15% ~26%A,32~35 min,26%~27%A,35~48 min,27%~40% A。检测波长230 nm,流速1.0 mL·min-1,柱温30℃[3-5],分析时间48 min。精密吸取上述溶液10 μL注入高效液相色谱仪测定[6]。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取二苯乙烯苷、天麻素、芍药苷、没食子酸、甘草苷、特女贞苷对照品适量置于容量瓶,加甲醇溶解制成浓度分别为0.04408、1.000、0.06900、10.40、0.02040、0.4400 mg·mL-1对照品溶液。
2.2.2 供试品溶液的制备 取样品约0.5 g精密称定,置100 ml具塞锥形瓶中,精密加入甲醇25 ml,称定质量,加热回流提取30 min,取出放冷,再称定质量,用甲醇补足减失的质量,摇匀滤过,取续滤液即得。
2.2.3 药材溶液制备 称取天麻、何首乌、川芎对照药材各0.1 g,分别置于100 ml具塞锥形瓶中,精密加入甲醇25 ml,回流提取30 min滤过,取续滤液即得。
精密称取白芷、熟地黄、丹参、墨旱莲、女贞子、白芍、黄精、甘草、当归、桑叶、蒺藜(炒)对照药材各5 g,按工艺水煮后定容至100 ml,精密吸取25 ml蒸干,残渣加甲醇溶解并定容至25 ml,即得。
3 结果与讨论
3.1 复方的色谱指纹图谱研究
3.1.1 方法学考察 (1)精密度试验:取样品约0.5 g(批号20151102)精密称定,按2.2.2项下方法制备供试品溶液,重复进样6次,记录色谱图,以二苯乙烯苷为参照峰S,计算各色谱峰的相对保留时间和相对峰面积。结果显示,各特征峰相对保留时间RSD小于0.30%,相对峰面积RSD小于6.00%,表明方法精密度良好。
(2)重复性试验:取样品约 0.5 g(批号20151102)精密称定,平行6份按2.2.2项下方法平行制备6份供试液,在同一色谱条件下进样记录色谱图,以二苯乙烯苷为参照峰S,计算各色谱峰的相对保留时间和相对峰面积。结果显示,各特征峰相对保留时间RSD小于0.76%,相对峰面积RSD小于7.50%,表明方法重复性良好。
(3)稳定性试验:取供试品(批号20151102)溶液于0、1、2.5、5、10、20 h进样分析,以二苯乙烯苷为参照峰S,计算各色谱峰的相对保留时间和相对峰面积。结果显示,各特征峰相对保留时间RSD小于0.30%,相对峰面积RSD小于6.00%,表明方法在20 h内稳定性良好。
3.1.2 色谱指纹图谱的测定及相似性分析按2.2.2项下供试品溶液的制备方法处理10批供试品溶液,分别精密吸取10 μL,注入高效液相色谱仪,按2.1项下色谱条件进行测定,记录48 min的色谱图。
采用《中药色谱指纹图谱相似度评价系统(2.0版)》对10批样品的HPLC图进行多点校正、自动匹配(时间窗宽度为0.10),用中位数法生成对照图谱R(即共有模式图,见图1)并计算相似度,结果显示10批样品特征峰的相似度均在0.9以上。
根据图1中10批样品HPLC图给出的峰数、峰面积积分值及相对保留时间,选取其中18个共有峰作为特征指纹峰(见图2),并选择14号峰(二苯乙烯苷)作为参比峰(S峰),计算各色谱峰的保留时间和峰面积比值,得到相对保留时间和相对峰面积平均值(结果见表1)。
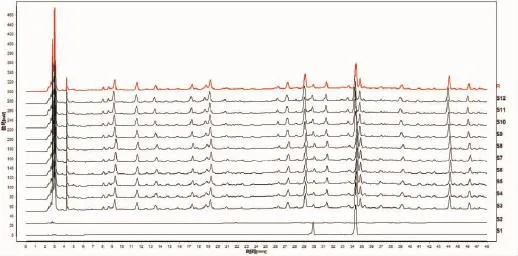
图1 10批天麻首乌片HPLC特征图谱注:S1.二苯乙烯苷对照品;S2.甲醇溶剂;S3~S12.10批样品;R.对照图谱
3.1.3 色谱峰归属分析 取天麻、白芷、何首 乌、熟地黄、丹参、川芎、墨旱莲、女贞子、白芍、黄精、甘草、当归、桑叶、蒺藜(炒)药材溶液,按上述色谱条件依次进样、测定,将样品与各单味药的HPLC色谱图进行比对(见图3)辨识与归属可知,1、8、12号峰为天麻的特征峰,14号峰为何首乌的特征峰,5、17号峰为丹参的特征峰,6、7、13、15号峰为女贞子的特征峰,10、11号峰为白芍的特征峰,2号峰为炒蒺藜的特征峰。其中1号峰为天麻素,3号峰为没食子酸,11号峰为芍药苷,13号峰为甘草苷,14号峰为二苯乙烯苷,15号峰为特女贞苷。
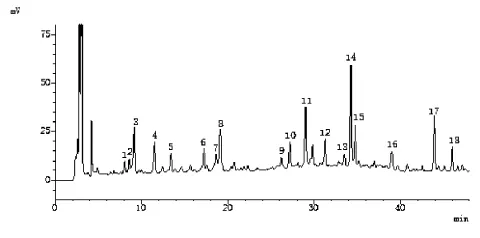
图2 天麻首乌片HPLC指纹图谱共有模式
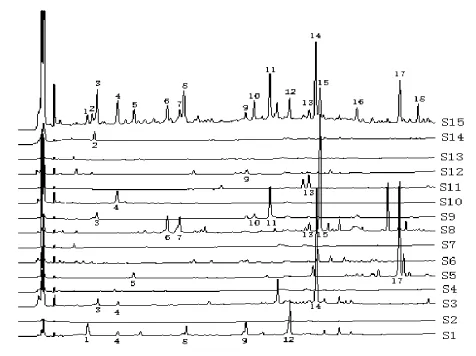
图3 天麻首乌片与单味药HPLC特征图谱的比较注:S1.天麻;S2.白芷;S3.何首乌;S4.熟地黄;S5.丹参;S6.川芎;S7.墨旱莲;S8.女贞子;S9.白芍; S10.黄精;S11.甘草;S12.当归;S13.桑叶;S14.炒蒺藜;S15.天麻首乌片

表1 HPLC指纹图谱特征峰相对保留时间、相对峰面积及归属
4 讨论
4.1 本试验中考察了多种流动相系统,如甲醇-水、乙腈-水、乙腈-0.2%磷酸溶液、乙腈-0.3%磷酸溶液、乙腈-0.4%磷酸溶液、乙腈-0.5%冰醋酸溶液。结果表明,以乙腈-0.3%磷酸溶液为流动相系统进行梯度洗脱时各个峰的分离效果较好,且基线相对平稳[7-8]。天麻首乌片药味多、成分复杂,以某单一成分的最大吸收波长为检测波长无法体现所有成分的特征,故对220 nm、230 nm、254 nm、280 nm、320 nm波长下的色谱图进行分析[9-11],结果显示220 nm、230 nm波长下色谱峰的个数最多,而220 nm接近甲醇溶剂的截止波长,故选择230 nm作为特征图谱的检测波长。
4.2 研究过程中,还考察了不同提取溶剂对样品的提取效果,以乙醇、70%乙醇、甲醇、70%甲醇作为提取溶剂提取样品。通过色谱图的比较发现,各方法对应色谱图中特征峰个数一致。但以甲醇为提取溶剂的样品所对应的色谱图峰形较好,故选择甲醇作为样品提取溶剂。
4.3 本实验进行了复方HPLC指纹图谱研究,标定了18个共有峰,对这18个共有峰进行了药味归属,初步阐明了共有峰的来源,其中天麻、何首乌、丹参、女贞子、白芍、炒蒺藜6味药在样品特征图谱上可对应到其特有的成分信息,通过与对照色谱图对比的方法,定性了部分色谱峰,另有2个色谱峰未能进行归属,有待进一步的研究。
[1]陈振华,刘苏珍,周斌,等.浅谈中药质量标准现状与几种质量评价方法[J].时珍国医国药,2016,27(3):694-696.
[2]李强,杜思邈,张忠亮,等.中药指纹图谱技术进展及未来发展方向展望[J].中草药,2013,11,44(22):3095-3104.
[3]马天成,崔思娇,张靓琦,等.川芎的UPLC指纹图谱研究[J].中国药房,2013,15:1389-1391.
[4]李帅锋,郑传柱,张丽,等.不同产地何首乌HPLC指纹图谱研究[J].中草药,2015,14:2149-2154.
[5]段华琴,张云天,徐以亮,等.天麻配方颗粒高效液相色谱指纹图谱研究[J].药物评价研究,2014,5:431-433.
[6]国家药典委员会.中国药典[M].北京:中国医药科技出版社,2015:176.
[7]胥爱丽,董玉娟,江洁怡,等.何首乌配方颗粒的UPLC指纹图谱及化学成分归属[J].中国实验方剂学杂志,2016,2:47-50.
[8]刘辉,张婧,樊光辉,等.HPLC法测定天麻素缓释片中天麻素的含量[J].中国药师,2013,6:825-827.
[9]周赛妮,刘明平,文艺,等.HPLC同时测定川芎-天麻药对中4种指标性成分的含量[J].中国实验方剂学杂志,2016,3:53-56.
[10]杨鑫,何华,王建新,等.何首乌特征图谱分析方法研究[J].贵州科学,2014,3:59-63.
[11]吕承恬,李心愿,徐仕奇,等.当归芍药胶囊高效液相色谱特征指纹图谱[J].中国医院药学杂志,2014,12:983-986.
Research on chromatographic fingerprints of Tianmashouwu Tablets by HPLC
SUN Wen-qiao1,PENG Yan-mei1,LI Yue-hui,ZHOU Run-wei1,ZHU Li-hua2△
(1.Traditional Chinese medicine research institute of hunnan province,Changsha,410013,China; 2.Hunan guohua pharmaceutical CO.,LTD.,Changsha,410013,China)
Objective To establish the HPLC chromatogram fingerprints of Tianmashouwu Tablets.Methods:The chromatographie fingerprints were obtained through Kromasil C18 column(4.6 mm×250 mm,5 μm)with the gradient elution solvent system composed of acetonitrile-0.2%phosphoric acid(0~18 min,5% ~15%acetonitrile;18~32 min,15%→26%acetonitrile;32~35 min,26% ~27%acetonitrile;35~48 min,27% ~40%acetonitrile).The detective wavelength was set at 230 nm;the flow rate was 1.0 m L/min;the column temperature was maintained at 30℃ and the injection volume was 10 μL;the analysis time was 120 min.Results The HPLC characteristic chromatogram was built on basis of 10 batches of Tianmashouwu Tablets,including 18 common peaks which contain the characteristic peaks of 6 Chinese herbal medicines,such as Gastrodia elata Bl,Fallopia multiflora(Thunb.)Harald.,etc.Conclusion:The established HPLC fingerprint has high is a reliable,available and quick method,which can be used in the quality evaluation of Tianmashouwu Tablets.
Tianmashouwu Tablets;HPLC;chromatogram fingerprints
R692.4
B
1006-3250(2016)11-1534-04
2016-04-27
苏文俏(1991-),女,在读硕士,从事中药学的临床与研究。
△通讯作者:朱立华(1964-),男,副研究员,从事企业管理与中药生产研究,Tel:13907312798,E-mail:380565887@qq.com。

