补脑软胶囊质量标准的研究
李喜香, 刘效栓, 毕映燕, 包 强, 李季文, 李妍怡, 潘从泽, 张亚会, 钱梦茹
(甘肃省中医院,甘肃兰州730050)
补脑软胶囊质量标准的研究
李喜香, 刘效栓, 毕映燕, 包 强, 李季文, 李妍怡, 潘从泽, 张亚会, 钱梦茹
(甘肃省中医院,甘肃兰州730050)
摘要:目的 建立补脑软胶囊(当归、川芎、黄芪、赤芍等)的质量标准。方法 TLC法鉴别胶囊中的当归、川芎和补骨脂,HPLC法对芍药苷、阿魏酸、毛蕊异黄酮葡萄糖苷的含有量进行测定。分析采用Waters C18色谱柱;流动相为乙腈-0.1%磷酸(16∶84);体积流量1.0 mL/min;检测波长230 nm;柱温室温。结果 当归、川芎和补骨脂可以被准确地鉴别。芍药苷、阿魏酸、毛蕊异黄酮葡萄糖苷分别在157.5~787.5 μg/mL(r=0.999 6)、10.9~54.5 μg/mL (r=0.999 6)、8.9~44.5 μg/mL(r=0.999 5)范围内线性关系良好,平均回收率分别98.87%、98.56、98.91% (RSD分别为1.7%、2.4%、2.5%,n =5)。结论 该方法操作简便,专属性强,重复性好,能有效控制补脑软胶囊的质量.
关键词:补脑软胶囊;芍药苷;阿魏酸;毛蕊异黄酮葡萄糖苷;TLC;HPLC
dol:10.3969/j.issn.1001-1528.2016.02.019
Quallty standard for Bunao Soft Capsules
LIXi-xiang, LIU Xiao-shuan, BIYing-yan, BAO Qiang, LIJi-wen, LIYan-yi, PAN Cong-ze,ZHANG Ya-hui, QIAN Meng-ru
(Gansu Provincial HosPital of TCM,Lanzhou 730050,China)
ABSTRACT: AIM To set uP a qua1ity standard for Bunao Soft CaPsu1es(Angelicae sinensis Radix,Liguszici Chuanxiong Radix,AstragaliMembranacei Radix,Paeoniae Rubrae Radix,etc.).METH0DS TLC was aPP1ied to detecting the existence of Angelica sinensis,Ligusticum chuanxiong and Psoralea corylifolia in the caPsu1es,whi1e HPLC was used for the quantity determination of Paeonif1orin,feru1ic acid and ca1ycosin-7-O-β-D-g1ycoside.The ana1ysiswas conducted on Waters C18co1umn(4.6 mm×250 mm,5 μm)at room temPerature,with acetonitri1e-0.1% PhosPhoric acid(16∶84)as themobi1e Phase at a f1ow rate of 1.0 mL/min and 230 nm for the detection wave1ength.RESULTS Angelica sinensis,Ligusticum chuanxiong and Psoralea corylifolia cou1d be sPecifica11y identified.Paeonif1orin,feru1ic acid and ca1ycosin-7-O-β-D-g1ycoside had good 1inear re1ationshiPs within the ranges of 157.5-787.5 μg/mL(r=0.999 6),10.9-54.5 μg/mL(r=0.999 6)and 8.9-44.5 μg/mL(r= 0.999 5),whose average recoveries were 98.87%,98.56% and 98.91% with the RSDs of 1.7%,2.4% and 2.5%(n =5),resPective1y.C0NCLUSI0N Besides the strong sPecificity and good reProducibi1ity,thismethod is easy to oPerate in terms of effective qua1ity survei11ance of Bunao Soft CaPsu1es.
KEYW 0RDS: Bunao Soft CaPsu1es;Paeonif1orin;feru1ic acid;ca1ycosin-7-O-β-D-g1ycoside;thin-1ayer chromatograPhy(TLC);high Performance 1iquid chromatograPhy(HPLC)
补脑膏是我院自制制剂(注册号甘药制字Z04000828),由夏勇潮医师在古方“佛手方(当归、川芎)”的基础上,合用黄芪、赤芍、补骨脂、枸杞、淫羊藿、龟板、水蛭、仙灵脾、益母草、仙茅、黄精、甘草制成(专利号ZL961222654,国际专利主分类号A61K35/78),具有益气养血、填精补髓、化瘀通络功效,用于脑外伤性神经损伤及后遗症,脑炎、脑膜炎后遗症,动脉硬化性脑损害,脑、脊髓变性性疾病,弱智儿童及脑性瘫痪等症的治疗[1],临床应用几十年,效果良好。在前期研究过程中,已将其剂型改进成软胶囊,为了更好地控制其质量,本实验采用薄层色谱(TLC)法,对川芎、当归、补骨脂药材进行定性鉴别,再采用高效液相色谱(HPLC)法,对方中赤芍主要成分芍药苷[2-5]、黄芪主要成分毛蕊异黄酮葡萄糖苷[6-8]、当归与川芎主要成分阿魏酸[9-14]同时进行测定,为该制剂的进一步开发研究提供技术支持。
1 仪器与试药
1.1 仪器 Waters高效液相色谱仪,包括Waters 1525泵、Waters 717进样器、Waters 2487双通道紫外检测器;HS6150超声波清洗仪(天津恒奥科技发展有限公司);Mett1er AE240电子天平(万分之一,德国赛多利斯公司);D6B/20-002A电热干燥箱;薄层板(自制)。
1.2 试药 当归、川芎、黄芪、赤芍等14味药材购自兰州安泰堂中药饮片有限公司,经甘肃省药品检验研究院宋平顺主任药师鉴定为正品。芍药苷(批号110736-200629)、毛蕊异黄酮葡萄糖苷(批号111920-201304)、阿魏酸(批号110773-200611)对照品(中国食品药品检定研究院)。乙腈、甲醇为色谱纯(天津光复精细化工研究所);其他试剂均为分析纯;水为自制超纯水。
2 方法与结果
2.1 当归、川芎的鉴别[15]取软胶囊内容物20粒,剪碎,精密称取4.0 g,加1%碳酸氢钠50 mL,超声20 min,取上清液,用盐酸调节PH至2~3,乙醚萃取2次,每次20 mL,合并萃取液,蒸干,残渣加甲醇1 mL溶解,作为供试品溶液。取阿魏酸对照品,加甲醇制成每1 mL含1 mg原料的溶液,作为对照品溶液。取缺当归、川芎药材的阴性制剂,同法制成阴性对照溶液。吸取上述溶液各10 μL,分别点于以CMC-Na为黏合剂的同一硅胶G薄层板上,以苯-乙酸乙酯-冰乙酸(5∶3∶0.1)为展开剂展开,取出,晾干,置紫外光灯(365 nm)下检视,结果见图1。由图可知,供试品色谱在与对照药材同一位置处显相同荧光斑点,而阴性样品不显示。
2.2 补脑软胶囊中补骨脂的鉴别[15]取软胶囊内容物20粒,剪碎,精密称取4.0 g,加乙酸乙酯20 mL,超声处理15 min,滤过,滤液蒸干,残渣加乙酸乙酯1 mL溶解,作为供试品溶液。取补骨脂0.36 g,同法制成对照药材溶液。再根据处方,制备缺补骨脂的阴性样品溶液。按照薄层色谱法(附录ⅥB),吸取上述3种溶液各10 μL,分别点于以CMC-Na为黏合剂的同一硅胶G薄层板上,以正己烷-乙酸乙酯(5∶1)为展开剂展开,取出,晾干,喷以10%氢氧化钾-甲醇溶液,置紫外光灯(365 nm)下检视,结果见图1。由图可知,供试品色谱在与对照药材相应的位置上显相同颜色的斑点,而阴性样品不显示。

A.3-阿魏酸 1、2、4-补脑软胶囊 5-阴性制剂 B.3-补骨脂 1、2、4-补脑软胶囊 5-阴性制剂A.3-feru1ic acid 1,2 and 4-Bunao Soft CaPsu1es 5-negative samP1e B.3-Psoralea corylifolia 1,2 and 4-Bunao Soft CaPsu1es 5-negative samP1e图1 当归、川芎、补骨脂T L C色谱图Flg.1 TLC chromatograms of Angelica sinensis,Ligusticum chuanxiong and Psoralea corylifolia
2.3 含有量测定
2.3.1 色谱条件与系统适应性试验 Waters Symmetry Shie1d-C18色谱柱(5 μm,4.6 mm×250 mm);流动相为乙腈(A)-0.1%磷酸(B)(16∶84);体积流量1.0 mL/min;检测波长230 nm;柱温室温;进样量10 μL。在该色谱条件下,供试品中其他成分与芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸均分离良好,阴性样品在对照品出峰处无干扰,表明专属性良好。结果见图2。

A.对照品 B.样品 C.阴性制剂A.reference substances B.samP1es C.negative samP1e1.芍药苷 2.毛蕊异黄酮葡萄糖苷 3.阿魏酸1.Paeonif1orin 2.ca1ycosin-7-O-β-D-g1ycoside 3.feru1ic acid图2 高效液相色谱图Flg.2 HPLC chromatogram s
2.3.2 溶液制备
2.3.2.1 对照品溶液的制备 精密称取芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸对照品适量,加甲醇溶解,稀释至刻度,制成每1 mL含芍药苷1.575 mg,毛蕊异黄酮葡萄糖苷1.09 mg,阿魏酸0.89 mg的储备液,即得。
2.3.2.2 供试品溶液的制备 精密称取补脑软胶囊内容物4.0 g,置于50 mL具塞锥形瓶中,加石油醚30 mL,超声(300 W、25 kHz)处理10 min,弃去石油醚液,残渣加甲醇30 mL,20℃超声(300 W、25 kHz)处理2次,每次30 min,过滤。合并滤液,减压回收甲醇,残渣用甲醇溶解,转移至10 mL量瓶中定容,摇匀,滤过,取续滤液,即得。
2.3.2.3 阴性样品制备 按补脑软胶囊的处方比例,称取除当归、川芎、黄芪、赤芍外的其余药味,根据制备工艺制得阴性样品,按“2.3.2.2”项下方法制得阴性对照液。
2.3.3 线性关系考察 取“2.3.2.1”项下对照品储备液适量,甲醇稀释后制得每1 mL含芍药苷157.5、315.0、472.5、630.0、787.5 μg,含毛蕊异黄酮葡萄糖苷10.9、21.8、32.7、43.6、54.5 μg,含阿魏酸8.9、17.8、26.7、35.6、44.5 μg的标样溶液,进样10 μL,每个质量浓度进样3次,在“2.3.1”项色谱条件下测定,以峰面积为纵坐标(Y),质量浓度为横坐标(X)绘制标准曲线,回归方程分别为Y=9.00×105X-5.01×105,r=0.999 6;Y=2.00×107X-1.46×107,r=0.999 6;Y=2.00×107X+2.04×107,r=0.999 5,表明芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸线性关系良好。
2.3.4 精密度试验 精密吸取混合对照品溶液10 μL,进样6次,测定峰面积。结果,芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸的RSD分别为0.9%、1.1%、0.8%,表明仪器精密度良好。
2.3.5 稳定性试验 精密吸取同一批号(140306)供试品溶液,分别在0、4、8、12、18、24 h进样10 μL,测定峰面积。结果,芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸的RSD分别为1.3%、0.9%、1.4%,表明样品在24 h内稳定性良好。
2.3.6 重复性试验 取同一批次(140306)样品,按“2.3.2.2”项下方法制备供试品溶液6份,精密吸取10 μL,测定峰面积。结果,芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸的RSD分别为1.6%、1.2%、1.7%,表明该方法重复性良好。
2.3.7 加样回收率试验 精密称取含有量已知的补脑软胶囊内容物2.0 g(芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸的含有量分别为1.75、0.048、0.079 mg/g),分别加入1.75、1.09、0.89 mg/mL的芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸对照品溶液1.8、0.080、0.2 mL,按“2.3.2”项下方法制备溶液,在“2.3.1”项色谱条件下进行测定,计算回收率。结果见表1。
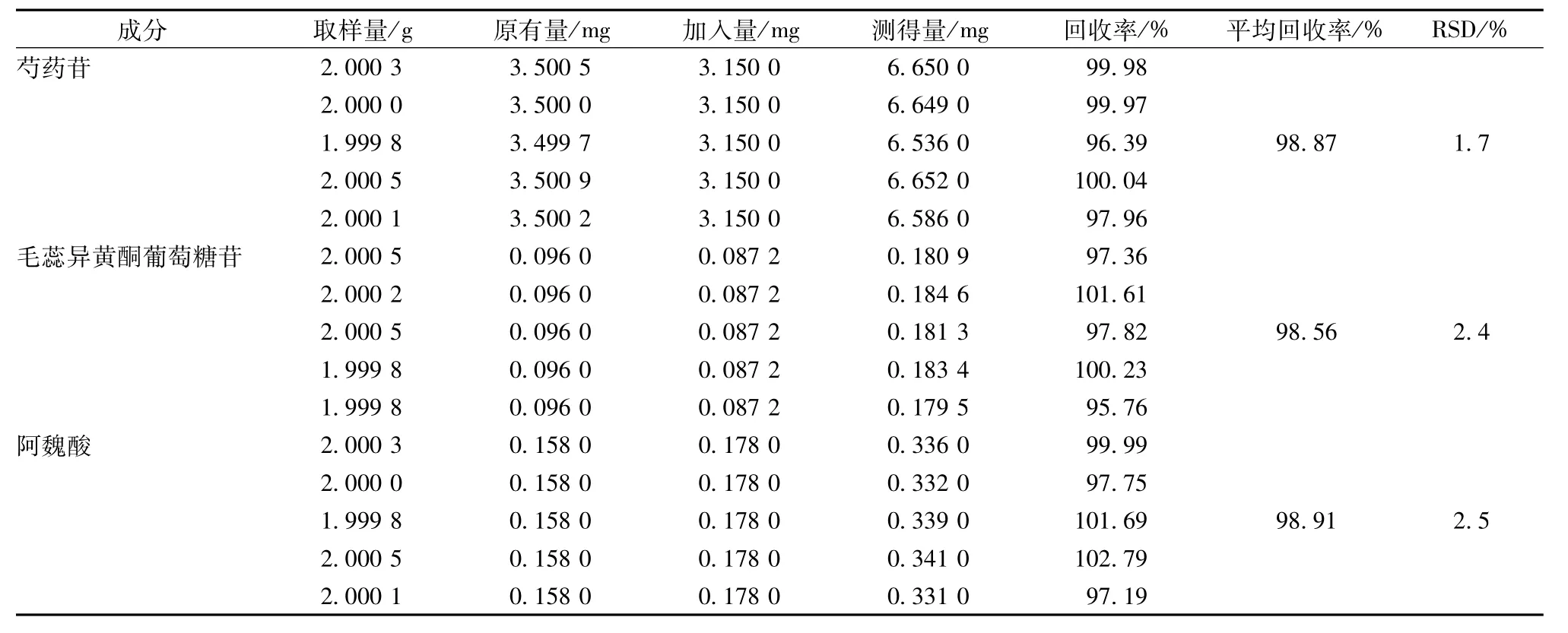
表1 加样回收率试验结果Tab.1 Results of recovery tests
2.3.8 样品测定 精密称取补脑软胶囊内容物(140306、140520、140617)4.0 g,按“2.3.2”项下方法制备供试品溶液,在“2.3.1”项色谱条件下进样测定,以“2.3.3”项下标准曲线计算各成分含有量。结果见表2。

表2 样品测定结果Tab.2 Determ lnatlon results of sam p les
3 讨论
在190~800 nm范围内,分别对芍药苷、毛蕊异黄酮葡萄糖苷、阿魏酸进行全波长扫描,发现其最大吸收波长分别为230、260、316 nm。其中在260 nm处,芍药苷、阿魏酸的吸收度均小于230 nm;在316 nm处,芍药苷、毛蕊异黄酮葡萄糖苷的吸收度均小于230、260 nm;在230 nm处,毛蕊异黄酮葡萄糖苷的吸收度与260 nm处基本一致,故在230 nm下对软胶囊中3种有效成分的含有量进行测定。另外,选取甲醇-酸、乙腈-酸流动相系统进行比较,发现阿魏酸为酸性物质,在乙腈-0.1%磷酸等度洗脱系统条件下,3个有效成分与相邻色谱峰均能完全分离,故选择乙腈-磷酸系统作为流动相[4]。
软胶囊内容物中含有蜂蜡、司盘-80、大豆油等脂溶性物质,如直接用甲醇超声处理提取后进样,样品在放置过程时,容器壁有脂溶性物质的析出,影响其测定。因此,先用石油醚将此类成分去除,再用甲醇超声提取。由于2种方法所测得3种有效成分的峰面积无差异,故选择先用石油醚处理,再用甲醇处理的样品制备方式。同时,对超声次数进行考察,发现超声提取2次与3次相比较,峰面积差异小于5%,故选择超声2次作为样品处理方式。
在当归、川芎薄层色谱鉴别方法中,本实验尝试环己烷-三氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.5)、甲苯-乙酸乙酯-冰乙酸(4∶1∶0.1)等展开系统,但均未将阿魏酸与相邻斑点分离,而在苯-乙酸乙酯-冰乙酸(5∶3∶0.1)展开系统下,阿魏酸薄层斑点清晰,而且专属性强。
参考文献:
[1] 李妍怡,窦友义,朱亚萍,等.补脑膏治疗小儿智力低下85例[J].中国中医药信息杂志,2005,12(5): 52.
[2] 陆小华,马 骁,王 建,等.赤芍的化学成分和药理作用研究进展[J].中草药,2015,46(4): 595-602.
[3] 刘 微,李冬冬,杨洪帅,等.超声辅助离子液体-反相液相色谱法测定赤芍中齐墩果酸和芍药苷的含量[J].中国中药杂志,2015,40(3): 443-449.
[4] 李喜香,毕映燕,李季文,等.正交试验优选补脑软胶囊水提乙醇沉降制备工艺[J].中成药,2014,36(12): 2625-2628.
[5] 李 琴,王晓玉,段贤春,等.紫参胶囊质量控制方法研究[J].中国中医药信息杂志,2013,20(3): 67-69.
[6] 刘德丽,包华音,刘 杨.近5年黄芪化学成分及药理作用研究进展[J].食品与药品,2014,17(1): 68-70.
[7] 王秀兰,奥·乌力吉,包晓华,等.HPLC法同时测定蒙古黄芪中6个有效成分的含量[J].药物分析杂志,2014,34 (4): 659-663.
[8] 刘 杨,包华音,王晓燕.不同产地黄芪药材中毛蕊异黄酮葡萄糖苷的定量分析[J].现代中药研究与实践,2014,28(3): 8-10.
[9] 周 鸿,黄含含,张静泽,等.川芎-当归药对研究进展[J].中成药,2015,37(1): 184-188.
[10] 刘晓坤,王 淼,王 一,等.HPLC法同时测定养血清脑胶囊中芍药苷和阿魏酸的含量[J].沈阳药科大学学报,2014,32(5): 375-378,383.
[11] 傅晓燕,黄巧玲.HPLC与UPLC法对比测定两种川芎药材中阿魏酸的含量[J].中药材,2011,34(7): 1070-1072.
[12] 刘小丽,石 丽,李 华.川芎药材HPLC指纹图谱及阿魏酸测定研究[J].中成药,2011,33(8): 1289-1292.
[13] 孔 铭,朱玲英,王佩娟,等.HPLC测定补肾活血颗粒中芍药苷,阿魏酸,淫羊藿苷的含量[J].中成药,2010,32(4): 600-603.
[14] 王漪檬,张晖芬,闫宝庆,等.HPLC法同时测定川芎药材中3种有效成分的含量[J].药物分析杂志,2009,29 (12): 2109-2112.
[15] 国家药典委员会.中华人民共和国药典: 2010年版一部[S].北京:中国医药科技出版社,2010: 174.
作者简介:李喜香(1968—),女,主任中药师,从事中药制剂研发工作。Te1: 15002550389,E-mai1: Lixixiang929@163.com
基金项目:兰州市科技计划项目(2012-2-78)
收稿日期:2015-06-12
中图分类号:R927.2
文献标志码:A
文章编号:1001-1528(2016)02-0321-05

