3,5-二甲基吡唑与锌(Ⅱ)配合物的合成、结构及光谱
朱兴城 黄超 张奇龙 朱必学*,
(1贵州大学大环及超分子化学重点实验室,贵阳550025)
(2遵义环境保护监测中心站,遵义563000)
(3贵州医科大学化学教研室,贵阳550004)
3,5-二甲基吡唑与锌(Ⅱ)配合物的合成、结构及光谱
朱兴城1,2黄超1张奇龙3朱必学*,1
(1贵州大学大环及超分子化学重点实验室,贵阳550025)
(2遵义环境保护监测中心站,遵义563000)
(3贵州医科大学化学教研室,贵阳550004)
采用3,5-二甲基吡唑(HL)与锌(Ⅱ)进行配位作用得到双核配合物[Zn2(HL)2(L)2Cl2](1)和四核配合物[Zn4(HL)4(L)4(OH)2](BF4)2(2)。通过元素分析、UV-Vis、红外光谱、荧光光谱及热分析等技术对化合物进行了表征,并采用X射线单晶衍射技术测定其晶体结构。晶体结构解析表明,配合物1和2都属三斜晶系,P1空间群。在两个配合物结构中,每个中心金属锌(Ⅱ)均具有扭曲的四面体配位构型。双核配合物1中2个金属锌(Ⅱ)由2个双齿配体(L)桥连,以双核配合物1作为次级配位单元,类似的2个次级配位单元中的金属锌(Ⅱ)进一步通过μ-O配位桥连形成四核配合物2。
3,5-二甲基吡唑;锌;晶体结构;荧光;热分析
吡唑及其衍生物属于有机含氮配体,具有良好的配位能力,与金属配位后能形成具有较高催化或生物活性的双金属配合物或多金属中心的配位聚合物,这些配合物在发光材料、磁性材料等领域均具有重要应用研究价值[1-2]。迄今,基于含吡唑结构单元的衍生配体及其金属配合物的合成与性质研究一直受到研究者的青睐[3-9]。同时,吡唑类衍生物是具有强烈的生理和药理活性的一类杂环化合物[10],在医药和农药的生产中有着重要用途。另一方面,金属锌离子普遍存在于动植物中,是生命必需的微量元素,在生命过程中起着重要作用。研究锌与含吡唑类有机配体间的配位作用与性质,对在生命体系中药物作用行为和作用机制的理解具有重要价值。
本文以3,5-二甲基吡唑配体(HL)和锌(Ⅱ)进行配位反应,得到未见报道的双核配合物[Zn2(HL)2(L)2Cl2] (1),进一步以1作为“次级配体”合成得到四核配合物[Zn4(HL)4(L)4(OH)2](BF4)2(2),并对化合物的荧光和热稳定性质进行考察。
1 实验部分
1.1 主要仪器与试剂
JEOL ECX 500 MHz核磁共振波谱仪;UV-256 FW型紫外-可见分光光度计;Bio-Rad型傅立叶红外光谱仪(4 000~400 cm-1);Vario ELⅢ型元素分析仪(德国);RF-540荧光分光光度计(日本岛津);晶体结构测定采用Bruker Smart Apex单晶衍射仪。3,5-二甲基吡唑,氯化锌,AgBF4(Alfa公司)及其它所用有机溶剂均为分析纯。
1.2 配合物的合成
双核配合物1的合成:在50 mL的圆底烧瓶中加入15 mL CHCl3和0.96 g配体3,5-二甲基吡唑(10 mmol),滴加含ZnCl2(0.68 g,5 mmol)的无水乙醇溶液20 mL。常温搅拌4 h,出现白色沉淀,抽滤、甲醇洗涤2~3次(每次用甲醇5 mL),空气干燥得1的产品0.88 g,产率60%。C20H30Cl2N8Zn2元素分析值(括号内为计算值,%):C 41.15(41.12),H 5.20(5.18), N 19.15(19.18).
四核配合物2的合成:在50 mL的圆底烧瓶中加入20 mL四氢呋喃和1.17 g双核配合物1(2 mmol),滴加含AgBF4(0.39 g,2 mmol)的乙腈溶液10 mL。常温搅拌2~3 h,出现白色沉淀,抽滤、甲醇洗涤2~3次(每次用甲醇5 mL),真空干燥得2的产品0.63 g,产率40%。C40H62N16O2Zn4B2F8元素分析值(括号内为计算值,%):C 38.95(38.92),H 5.08(5.06), N 18.13(18.16).
分别取少量上述配合物1和2的固体溶解在CHCl3和C2H5OH混合溶液中,常温放置3~4 d,即可得到适合于X射线衍射测定的红色块状晶体。
双核配合物1和四核配合物2的合成路线:
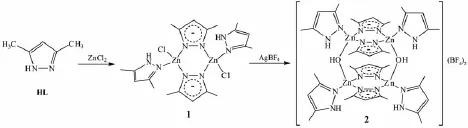
Scheme 1
1.3 单晶结构测定
选取大小合适的配合物晶体,用Bruker Smart Apex衍射仪收集数据。采用经石墨单色器单色化的Mo Kα射线(λ=0.071 073 nm),以φ-ω扫描方式在一定θ范围内,收集配合物衍射数据。强度进行了经验吸收校正、Lp校正。晶体结构由直接法解得。对全部非氢原子坐标极其各项异性热参数进行了全矩阵最小二乘法修正。所有计算用SHELX-97程序包完成[11],有关晶体学数据详见表1。
CCDC:825874,1;825875,2。

表1 配合物1和2的晶体学及结构精修数据Table 1Crystal data and structure refinement for the complexes 1 and 2
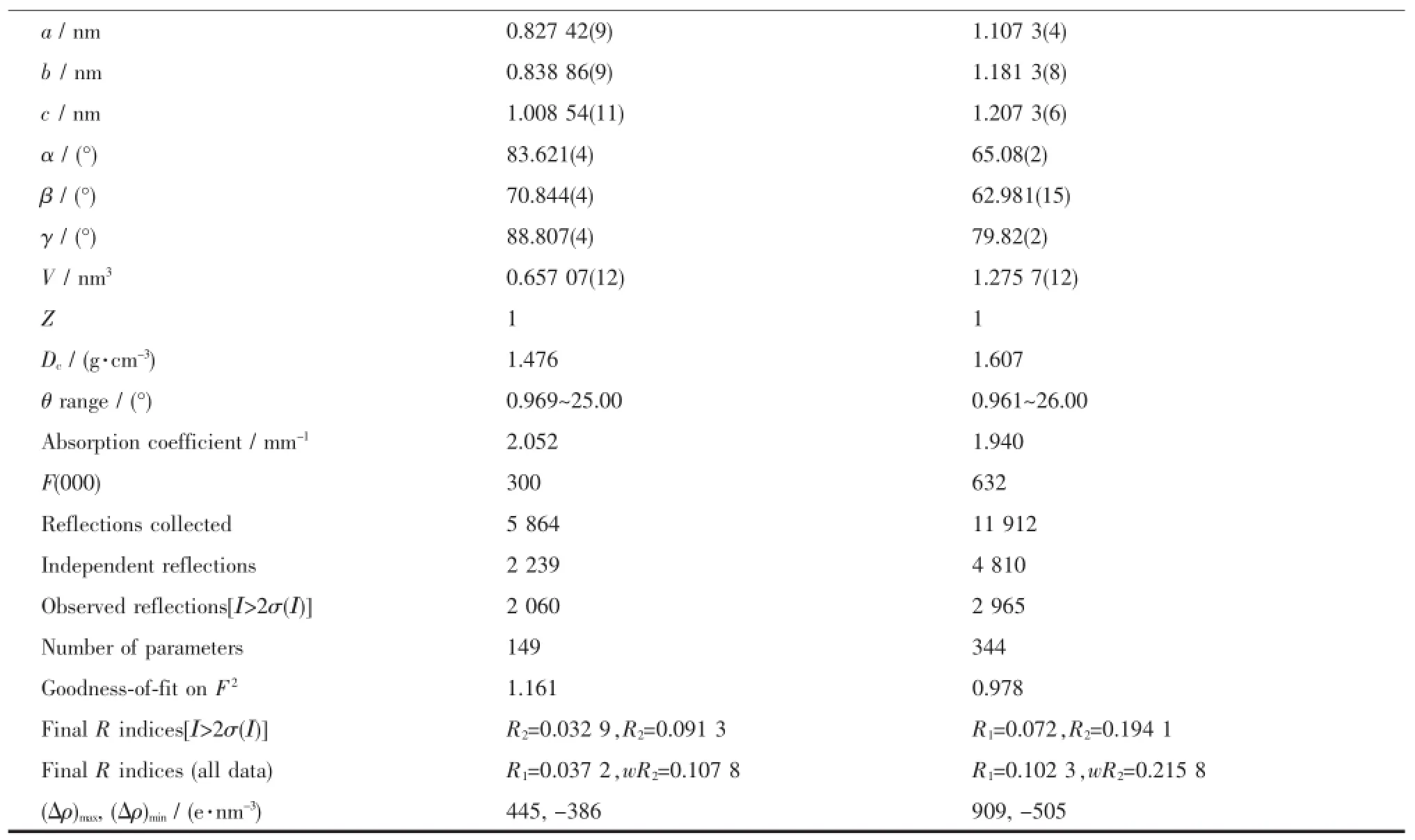
Continued Table 1
2 结果与讨论
2.1 配合物晶体结构描述
两个配合物1和2的主要键长和键角列于表2,分子结构分别见图1a和3a。在2个配合物分子中,配体3,5-二甲基吡唑与中心金属离子(Zn2+)配位分别采用2种配位形式(即电中性的HL和去质子化的L)同金属锌(Ⅱ)离子进行配位作用。作为单齿配体时,3,5-二甲基吡唑分子以其C=N中氮原子与金属锌(Ⅱ)进行配位作用;而作为双齿配体时,在配位过程中,3,5-二甲基吡唑分子的亚胺基先发生去质子化作用,形成带1个单位负电荷的有共轭体系的配体L,L以相邻的2个氮原子与同一中心金属离子(Zn2+)协同配位桥连。
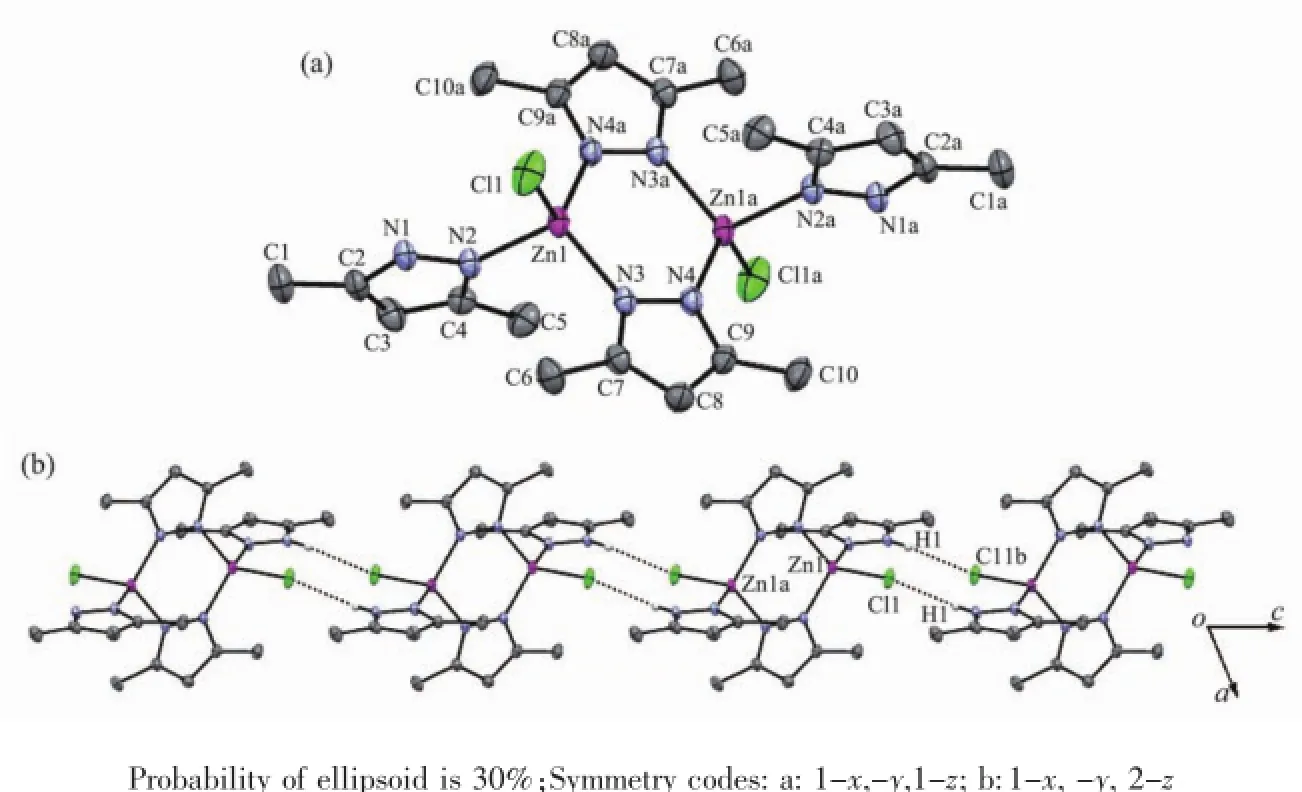
图1 (a)配合物1的分子结构;(b)配合物1通过分子间N1-H1…Cl1b氢键作用组装成一维链Fig.1(a)Molecular structure of the complex 1;(b)A section of the 1D chain structure of 1 via intramolecular N1-H1…Cl1b hydrogen bonding interactions
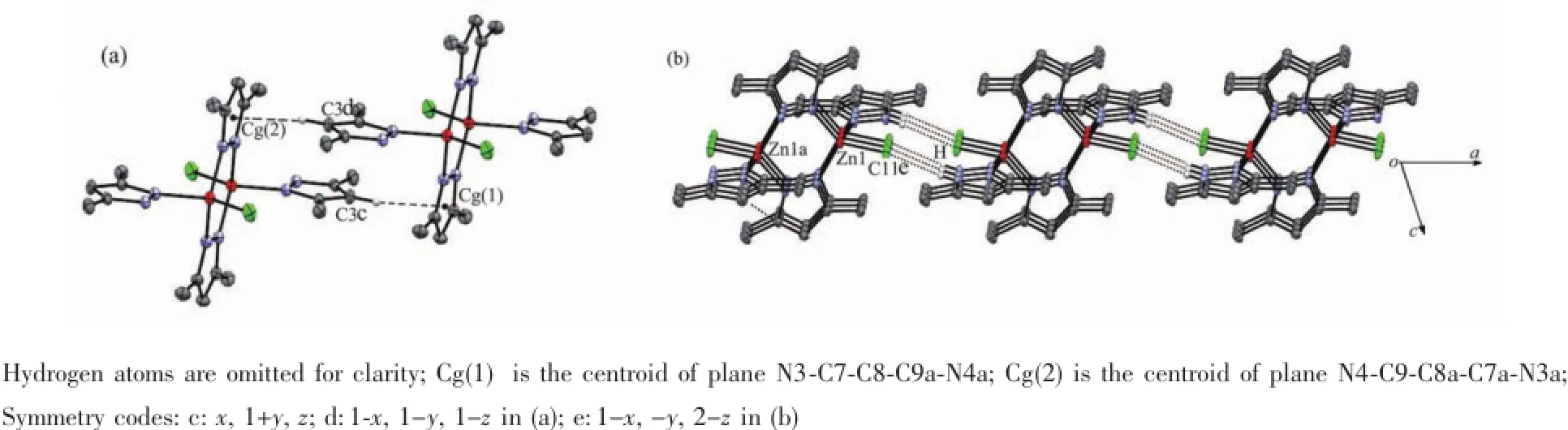
图2 (a)配合物1单元晶胞中2个不对称配合物分子间的C-H…π相互作用;(b)配合物1的层状结构Fig.2(a)C-H…π interactions between two asymmetric molecules in unit cell;(b)Non-interpenetrating layer-structure of 1
配合物1的单元晶胞中仅包含1个双核配合物分子,属于三斜晶系,P1空间群。中心离子锌(Ⅱ)具有四面体的几何构型,4个配位供体原子为1个氯和3个氮,其中2个氮原子分别来自于2个桥连双齿配体L,1个氮来自于单齿配体HL。围绕锌(Ⅱ)的Zn-N键长在0.198 3(3)~0.203 0(3)nm范围,Zn-Cl键长为0.223 7(11)nm,锌离子周围的N-Zn-N键角在104.94°~113.02°之间。2个锌中心通过一对桥连配体L连接形成双核配合物1。在双核配合物结构中,2个锌(Ⅱ)中心通过2个配体L桥连形成一个平面六元环,同六元环相连的2个桥连配体(L)的五元环与该六元环共平面,与锌配位的单齿配体HL和氯配体分别位于该平面的上方和下方,单齿配体HL的五元环和该平面六元环间几乎垂直,其间的二面角接近90°。
在双核配合物1的晶体结构中,双核配合物分子的2个氯配体与相邻分子的单齿配体(L)中亚胺质子形成分子间氢键,依靠这些分子间氢键作用将双核配合物分子组装形成一维链结构(图1b)。类似的1D链进一步通过相邻链中双核配合物分子间CH…π相互作用(图2a),沿晶体b轴方向平行扩展得到层状结构(图2b)。
我们以双核配合物1作为“次级配体”,原本拟通过AgBF4中银离子与次级配体配位键合作用达到具有多个异金属中心的超分子组装体构筑,但没有成功,而是得到了配合物2的结构。晶体结构解析表明,在配合物2的结构中,2个氢氧根(OH-)离子分别以氧原子同次级配体中的2个锌(Ⅱ)中心进行配位桥连形成四核配合物结构(图3a),在单元晶胞中,包含1个四核配合物和2个无序的抗衡阴离子(BF4-)。与次级配体1的结构相比,配合物2中每一个中心锌(Ⅱ)离子仍具有四面体的几何构型,围绕锌(Ⅱ)的Zn-N键长在0.194 4(6)~0.202 2(6)nm范围,2个双齿配体L与锌(Ⅱ)桥连形成六元环平面,2个双齿配体L的五元环与该六元环基本共面;与双核次级配体1不同,配合物2中2个单齿配体HL均位于该六元环平面的同侧,2个单齿配体的五元环和六元环平面间的二面角分别为94.3°和91.11°。立足于金属中心及其桥连原子的结构观察,四核配合物分子配位骨架表现为一个类似罐形的剖面结构(如图3b),在六元环结构中的2个锌(Ⅱ)距离为0.353 5 nm,经μ-O配位连接的2个锌(Ⅱ)距离为0.338 2 nm。

图3 (a)配合物2的分子结构;(b)配合物锌离子的主要配位骨架Fig.3(a)Molecular structure of the complex 2;(b)Principal structure of the coordination sphere of four zinc(Ⅱ)ions in 2
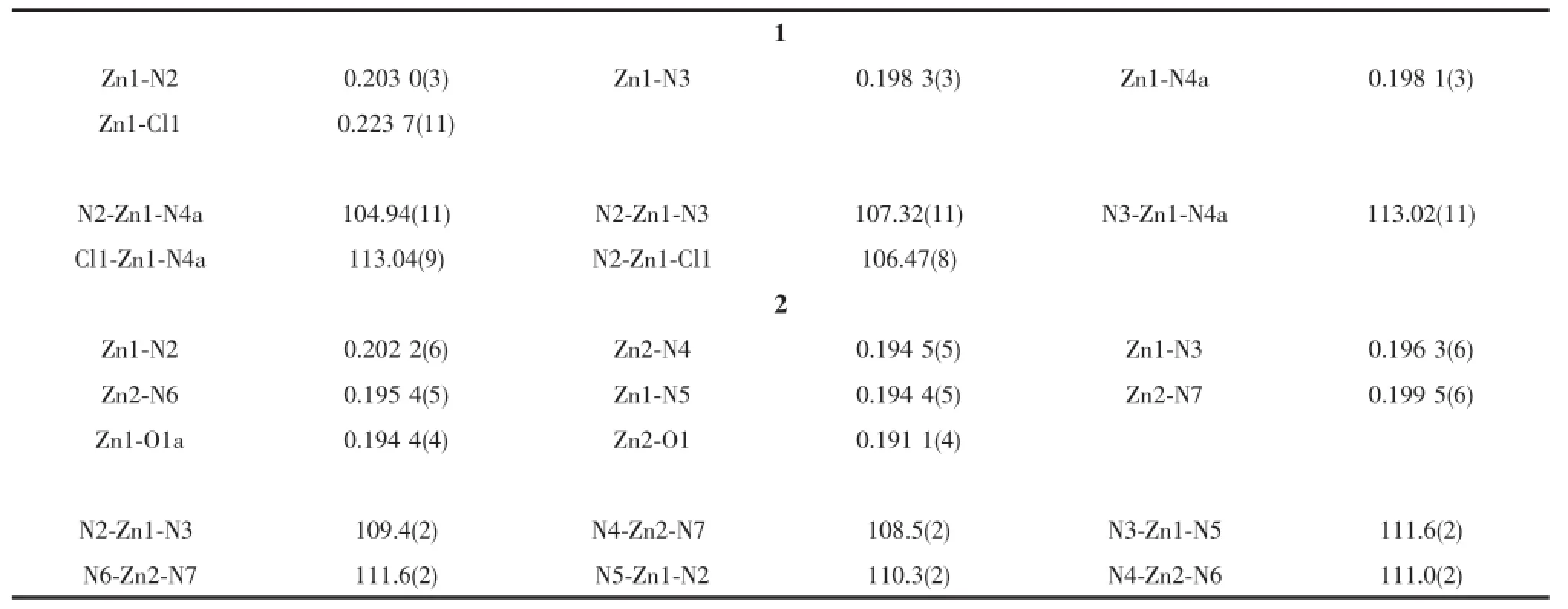
表2 配合物1和2的部分键长和键角Table 2Selected bond lengths(nm)and bond angles(°)for 1 and 2
2.2 UV-Vis和IR光谱
配体和配合物在四氢呋喃溶剂中的紫外吸收光谱测定表明,自由配体HL在242 nm处表现出一个强的吸收,在274 nm处呈现一个相对较弱的吸收;配合物1和2均出现2个吸收峰,即配合物1在242和325 nm两处,配合物2在242和357 nm两处。其中配体和配合物在242 nm附近的吸收由配体的π-π*跃迁所致[12],配体在274 nm处的吸收应由其C=N中氮原子上的孤对电子在共轭的键之间的n-π*跃迁产生,配合物1和2分别在325和 453 nm的吸收应归属为配体和中心金属离子间的荷迁移跃带(LMCT)[13];可见自由配体形成配合物后,因为C=N中氮原子上的孤对电子与中心金属离子配位,导致配合物中相应的n-π*跃迁产生的吸收消失。在配合物FTIR光谱中,配合物1和2中吡唑环上的νC=N伸缩振动峰分别出现在1 618和1 596 cm-1处,νN-H伸缩振动峰分别出现在3 449和3 445 cm-1处,同时配合物2在3 519 cm-1观察到尖的νO-H振动峰,这与氢氧根桥连2个锌(Ⅱ)中心形成的四核配合物结构相吻合。
2.3 荧光光谱
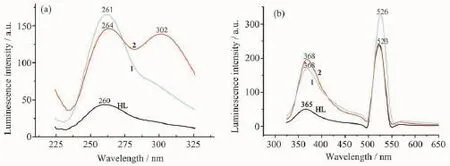
图4 (a)配体HL和配合物1、2的激发光谱;(b)配体HL和配合物1、2的发射光谱Fig.4(a)Excitation spectra of ligand and complexes;(b)Emission spectra of ligand and complexes
具有d10电子结构的简单金属配合物是不发光的,但与具有π共轭芳香类有机配体配位所形成的配合物能发射较强的荧光[14]。据此,对自由配体HL及其锌配合物1和2的荧光性质进行考察,激发光谱和发射光谱分别如图4所示。从激发光谱可见,双核配合物1与配体的最大激发波长λex接近,而四核配合物2分别在264和302 nm两处呈现2个强的激发峰(图4a)。发射光谱表明,自由配体HL和配合物1、2均有荧光效应(图4b),配体HL分别在365、523 nm附近各产生1个荧光发射峰,配合物1分别在368、523 nm附近各产生1个荧光发射峰。配合物2在368、526 nm处也有相似的发射峰,说明配合物的荧光发射是一种金属离子微扰的配体发光现象。与配体和配合物1相比,配合物2在526 nm的荧光发射峰(配体为523 nm)发生了部分红移,这可能是通过μ-O桥连2个双核Zn(Ⅱ)形成四核配合物后,整个分子结构的刚性增加所致[15]。
2.4 配合物2的热分解性质
在N2气氛下,以10℃·min-1的升温速度用示差扫描量热法(DSC)测定配合物2的热重(TG)曲线如图5。
从图5可见,配合物2热分解过程分为3步,在65~115℃出现第一个失重峰,对应于配合物固体粉末中所吸附的水分子失去(失重率约为4.88%);在温度较高的区域(158~219℃)出现第二个失重峰,总失重率约为2.58%,对应于桥连在双核锌(Ⅱ)配位亚单元之间的2个OH-离去(理论值2.76%)。在240~379℃区域DSC曲线表现出吸热效应,峰顶温度为306℃(失重率约为54.79%),对应于双核锌(Ⅱ)的配位亚单元进一步分解;在400℃以后失重曲线基本达到稳定状态,残余量为38.99%,推测剩余物为ZnO和Zn(BF4)2固体混合物(3ZnO+Zn(BF4)2),理论值为39.15%。
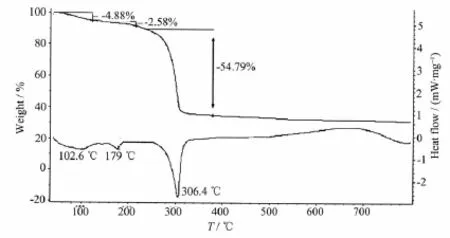
图5 配合物2的TG-DSC图Fig.5TG-DSC curves for the complex 2
[1]Dias H V R,Diyabalanage H V K,Eldabaja M G,et al.J. Am.Chem.Soc.,2005,127(20):7489-7501
[2]Reger D L,Pascui A E,Smith M D,et al.Inorg.Chem., 2012,51(21):11820-11836
[3]Müller H,Bauer-Siebenlist B,Csapo E,et al.Inorg.Chem., 2008,47(12):5278-5292
[4]Bouwman E,Driessen W L,De Graaff R A G,et al.Acta Crystallogr.,1984,C40:1562-1563
[5]Ehlert M K,Rettig S J,Storr A,et al.Can.J.Chem., 1990,68:1494-1498
[6]Reger D L,Foley E A,Smith M D.Inorg.Chem.,2009,48 (3):936-945
[7]Jin S W,Wang D Q.Inorg.Chim.Acta,2014,415:31-34
[8]Lin R B,Li F,Liu S Y,et al.Angew.Chem.Int.Ed., 2013,52:13429-13433
[9]Pérez J,Riera L.Eur.J.Inorg.Chem.,2009,33:4913-4925
[10]WANG Zhi-Hong(王志宏),WANG He(王贺),GUO Yan-Zhao(郭彦召),et al.Chinese J.Inorg.Chem.(无机化学学报),2012,28(9):1926-1934
[11]SheldrickGM.SHELX-97,UniversityofGöttingen, Germany,1997.
[12]ZHANG Rui(张瑞),XING Yong-Heng(邢永恒),TIAN Chun-Yan(田春燕),et al.Chinese J.Inorg.Chem.(无机化学学报),2014,30(2):264-270
[13]WANG Xin-Yu(王欣羽),LI Zhen(李桢),SUN Qiao(孙巧), et al.Chinese J.Inorg.Chem.(无机化学学报),2012,28(3): 483-490
[14]YANG Ying-Qun(杨颖群),LI Chang-Hong(李昶红),LI Wei(李薇),et al.Chem.J.Chinese Universities(高等学校化学学报),2008,29(3):449-452
[15]NIU Shu-Yun(牛淑云),CHI Yu-Xian(迟玉贤),JIN Jing (金晶),et al.Chem.J.Chinese Universities(高等学校化学学报),2004,25(10):1804-1806
Syntheses,Structures and Spectra of Complexes of Zinc(Ⅱ)with 3,5-Dimethylpyrazole
ZHU Xing-Cheng1,2HUANG Chao1ZHANG Qi-Long3ZHU Bi-Xue*,1
(1Key Laboratory of Macrocyclic and Supramolecular Chemistry,Guizhou University,Guiyang 550025,China)
(2Zunyi Environmental Monitoring Center,Zunyi,Guizhou 563000,China)
(3Department of Chemistry,Guizhou Medical College,Guiyang 550004,China)
The complexes[Zn2(HL)2(L)2Cl2](1)and[Zn4(HL)4(L)4(OH)2](BF4)2(2)were synthesized from the reaction of 3,5-Dimethylpyrazole(HL)with anhydrous ZnCl2sequentially and characterized by elemental analysis,UV-Vis, FTIR and fluorescence spectroscopy.The crystal structures of the complexes1and2were determined by X-ray diffraction analysis,and result reveals that each of the two complexes crystallizes in the triclinic system,space group P1,and the coordination environment around zinc(Ⅱ)is best described as distorted tetrahedral configuration in each case.Two zinc ions were bridged by two bidentate ligand(L)in dinuclear zinc(Ⅱ)complex1. Furthermore,the dinuclear complex is used as secondary ligand unit(sub unit),and the zinc ions of the same two sub units were bridged by two μ-O to give the tetranuclear zinc(Ⅱ)complex2.CCDC:825874,1;825875,2.
3,5-dimethylpyrazole;zinc ion;crystal structure;fluorescence;thermal analysis
O614.24+1
A
1001-4861(2016)06-1041-06
10.11862/CJIC.2016.128
2016-01-17。收修改稿日期:2016-04-20。
国家自然科学基金(No.21061003)和教育部“春晖计划”项目(No.Z2012054)资助。
*通信联系人。E-mail:sci.bxzhu@gzu.edu.cn

