阻塞性睡眠呼吸暂停低通气综合征对合并有哮喘患者肺通气功能的影响
许伟宁 李小娟 贾刚 牟照红 韩志强
【摘要】 目的 分析支气管哮喘(哮喘) 合并阻塞性睡眠呼吸暂停低通气综合征(OSAHS)患者的相关临床特点, 探讨阻塞性睡眠呼吸暂停低通气综合征对合并有哮喘患者肺通气功能的影响。方法 121例支气管哮喘患者检测出合并OSAHS患者87例, 随机分为组1(43例)和组2(44例), 不伴OSAHS的34例为组3。组1采用常规哮喘药物治疗的同时加用夜间持续正压通气(CPAP)治疗。组2、组3给予常规哮喘药物治疗。观察三组治疗前后症状、肺功能的变化。结果 治疗后组1、组3的哮喘症状控制程度及肺功能指标均高于组2(P<0.05)。组2各项肺通气功能指标在治疗后与治疗前比较差异无统计学意义(P>0.05)。组1第1秒用力呼气容积(FEV1)、最大呼气流量(PEF)及PEF变异率较组2明显改善, 差异有统计学意义(P<0.05或P<0.01), 治疗后组2、组3肺功能比较差异有统计学意义(P<0.05或P<0.01)。结论 支气管哮喘伴有OSAHS患者病情不易控制, 伴有OSAHS的哮喘患者常规治疗方案中加用夜间CPAP辅助治疗, 可显著改善患者的肺通气功能, 值得在临床推广。
【关键词】 阻塞性睡眠呼吸暂停低通气综合征;支气管哮喘;持续正压通气无创通气;肺功能
DOI:10.14163/j.cnki.11-5547/r.2016.07.065
哮喘是一种慢性气道炎症性疾病, 以发作性的咳喘、胸闷为主要症状, 多发于晨间及夜晚。OSAHS是以睡眠时反复呼吸暂停、严重打鼾、白天嗜睡为特征的慢性呼吸系统疾病, 哮喘和OSAHS 在全球的发病率有明显增高趋势。部分哮喘患者可能合并有OSAHS, 而OSAHS 也是哮喘急性发作的独立危险因素[1, 2]。本研究对合并OSAHS的支气管哮喘患者在给予常规抗哮喘治疗的基础上同时予夜间CPAP(经压力滴定后)治疗, 观察支气管哮喘伴OSAHS患者与支气管哮喘不伴OSAHS患者的哮喘好转程度的异同, 探讨OSAHS对支气管哮喘控制难易程度的影响, 观察夜间CPAP(经压力滴定后)治疗对合并OSAHS的哮喘患者哮喘控制测试(ACT)评分[3]、肺功能的影响。
1 资料与方法
1. 1 一般资料 选择2013年3月~2015年5月在本院就诊的121例支气管哮喘患者, 所有患者的诊断均依照中华医学会2003支气管哮喘防治指南的诊断标准[4]。按患者就诊先后顺序随机分组, 伴有OSAHS诊断[5]的支气管哮喘患者87例, 随机分为组1(43例)和组2(44例), 不伴有OSAHS的34例支气管哮喘患者为组3。患者及研究者均对分组情况不知情, 治疗药物由中心药房配给。组1男32例, 女11例, 平均年龄(41.6±4.9)岁;组2男33例, 女11例, 平均年龄(42.5±4.7)岁;组3男26例, 女8例, 平均年龄(41.9±4.6)岁。三组患者性别、年龄及治疗前的ACT评分、肺功能、气道反应性等一般资料比较差异无统计学意义(P>0.05), 具有可比性。
1. 2 方法 对所有受试者常规询问病史及体检, 参考支气管哮喘防治指南[4], 对三组患者根据哮喘病情控制分级制定常规治疗方案。组1同时给予夜间CPAP(经压力滴定后)治疗6 h/晚, 共8周, 组2、组3的常规抗哮喘治疗的药物的性状、用法用量、疗程与组1均一致。8周后对患者进行ACT评分。肺功能测定: 采用肺功能测定仪(德国 JAEJER公司MasterScreen Pneumo型电脑化肺功能仪) 测定每位患者的最大呼气流量、容积曲线和肺容量, FEV1、PEF及PEF变异率。
1. 3 统计学方法 使用SPSS13.0统计学软件对数据进行统计分析。计量资料以均数±标准差( x-±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验。P<0.05为差异具有统计学意义。
2 结果
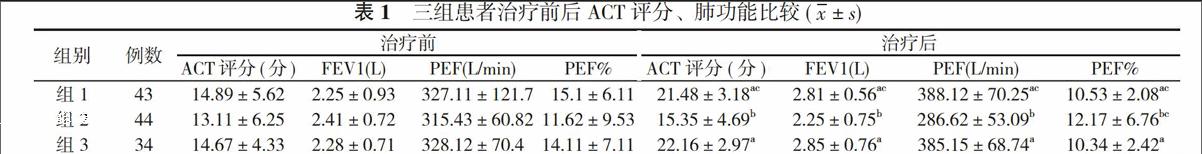
121例患者均完成本次试验, 无中间退出及失访情况。治疗后组1、组3的ACT评分及肺通气功能的各项指标均显著优于组2(P<0.05)。组2各项肺通气功能指标在治疗后与治疗前比较差异无统计学意义(P>0.05)。组1治疗前后ACT评分、肺功能与治疗前比较差异有统计学意义(P<0.05);治疗前组1、组2、组3的ACT评分、肺功能比较差异无统计学意义(P>0.05);治疗后组1、组2、组3肺功能比较差异有统计学意义(P<0.05)。见表1。
3 讨论
阻塞性睡眠呼吸暂停低通气综合征是哮喘急性发作的独立危险因素[1, 2], 同时也是导致支气管哮喘病情难以控制的因素之一, 本研究采用随机对照的试验方法, 观察夜间CPAP治疗对支气管哮喘合并OSAHS患者的疗效。结果显示, 在合并OSAHS的哮喘患者中进行夜间CPAP(经压力滴定后)治疗, 可改善患者ACT评分及肺功能指标(FEV1、PEF、PEF%), 分析OSAHS诱因及加重哮喘的可能机制:①哮喘合并OSAHS的患者多为体质量指数(BMI)超标的肥胖患者, 其过多的胸壁、腹壁脂肪组织造成呼吸系统顺应性的下降, 而这种顺应性下降又会导致肺容量的降低[6, 7];患者处于低肺容量状态下时, 上气道肺实质所形成的牵拽效应又将下降, 最终导致上气道塌陷性增加, 呼出气流的受限。②哮喘合并OSAHS患者可能存在呼吸模式的改变, 即潮气量降低和呼吸频率增加, 而该种呼吸模式改变也可能是气道狭窄的成因之一[8], 随着患者耗氧量的增加, 其心肺系统将处于过度疲劳状态, 肺扩张受限, 肺容量降低; 而且长期高负荷的运作可造成呼吸系统的功能性损伤, 易导致呼吸道黏膜慢性炎症发生, 可能导致哮喘急性发作不易控制。③胃食管反流是OSAHS主要并发症之一, 而且胃食管反流能够引起迷走神经高反应性调节异常, 造成食管下括约肌紧张度的下降, 导致食管下括约肌短暂性松弛现象[9], 误吸入呼吸道的反流物将直接刺激食管黏膜上的迷走神经受体, 导致支气管痉挛的发生[10, 11]。食管内酸性物质能激活支气管内神经的局部轴索反应, 而这种局部的神经反射所导致的炎性物质在黏膜释放的增加, 可以进一步造成气管黏膜水肿的加重。以上所述均与OSAHS相关, 针对OSAHS的夜间CPAP治疗可减少诱发气管黏膜炎症反应的相关因素。故本研究采用夜间CPAP(经压力滴定后)治疗6 h/晚, 共8周OSAHS的治疗方案, 组1患者OSAHS症状缓解明显, 哮喘症状控制较好。
综上所述, 支气管哮喘伴有阻塞性睡眠呼吸暂停低通气综合征患者病情较难控制, 阻塞性睡眠呼吸暂停低通气综合征对于支气管哮喘患者的肺功能具有显著影响, 故此在支气管哮喘患者日常诊疗工作中, 应注意患者是否合并OSAHS, 临床医生对哮喘合并OSAHS患者应进行早期监测和早期干预, 对合并OSAHS的患者进行及时有效的夜间CPAP治疗。
参考文献
[1] Alkhalil M, Schulmam E, Getsy J. Obstructive Sleep apnea syndrome and asthma:what are the links. J Clin Sleep Med, 2009, 5(1):71-78.
[2] Alkhalil M, Schulmam E, Getsy J. Obstructive Sleep apnea syndrome and asthma:the role of continuous positive airway pressure treatment. Ann Allergy Asthma Immunol, 2008, 101(1001):350-357.
[3] Nathan RA, Sorkness CA, Kosiniki M, et al. Development of the asthma control test:a survey for assessing asthma conrtol. J Allergy Clin Immunol, 2004, 113(1):59-65.
[4] 中华医学会呼吸病学分会哮喘学组.支气管哮喘防治指南(支气管哮喘的定义、诊断、治疗及教育和管理方案).中华结核和呼吸杂志, 2008, 3(13):177-185.
[5] 中华医学会呼吸病学分会睡眠呼吸障碍学组.阻塞性睡眠呼吸暂停低通气综合征诊治指南(2011年修订版) .中华结核和呼吸杂志, 2012, 35(1):9-12.
[6] Cotes JE, Chinn DJ, Reed JW. Body mass, fat percentage, and fat free mass as reference variables for lung function:effects on terms for age and sex. Thorax, 2001, 56(11):839-844.
[7] Wastson RA, Pride NB. Postural changes in lung volumes and respiratory resistance in subjects with obesity. J Appl Physiol(1985), 2005, 98(2):512-517.
[8] Campana LM, Malhotra A, Suki B, et al. The effect of lung stretch during sleep on airway mechanics in overweight and obese asthma. Respir Physiol Neurobiol, 2013, 185(2):304-312.
[9] 黄美君, 戴建国, 陈恩信. 反流性食管炎误诊67例原因分析.现代中西医结合杂志, 2010, 16(5):760-761.
[10] Castell DO, Schnatz PF. Gastroesophageal reflux disease and asthma. Reflux or reflex. Chest, 1995, 108(5):1186-1187.
[11] Theodoropoulos DS, Lockey RF, Boyce HW, et al. Gastroesophageal reflux and asthma:a review of pathogenesis, diagnosis, and therapy. Allergy, 1999, 5(47):651-661.
[收稿日期:2015-11-24]

