甲磺酸伊马替尼对慢性髓系白血病患者效果的相关因素研究
王良妥,张湘兰,司徒健瑜,黄远颖
(广东省阳江市人民医院血液科,广东 阳江 529500)
甲磺酸伊马替尼对慢性髓系白血病患者效果的相关因素研究
王良妥,张湘兰,司徒健瑜,黄远颖
(广东省阳江市人民医院血液科,广东 阳江529500)
摘要:目的研究甲磺酸伊马替尼对慢性髓系白血病(CML)患者效果的相关因素。方法2010年1月至2015年3月,该院接收70例慢性髓系白血病患者口服甲磺酸伊马替尼400~600 mg·d-1,其中慢性期患者(CP)55例(ECP30例,LCP25例),加速期(AP)15例,急变期(BC)9例。检测完全血液学反应(CHR)、完全细胞遗传学反应(CCyR)、主要细胞遗传学反应(MCyR)和完全分子学反应(CMoR)等指标,分析甲磺酸伊马替尼对慢性髓系白血病患者效果的相关因素。结果截至2015年3月,该院70例CML患者均能耐受伊马替尼。(1)70例CML患者中,初治组的CHR、CCyR、MCyR和CMoR分别为100%、71.9%、80.8%和74.9%,复治组分别为100%、45.8%、79.1%和53.9%,差异无统计学意义。(2)低危组的CHR、CCyR、MCyR和CMoR分别为100%、63.7%、78.9% 和56.3%;中危组分别为100%、76.1%、79.6%和47.9%;高危组分别为100%、49.8%、76.3%和46.8%,差异无统计学意义。(3)单因素分析表明,治疗前WBC数、Hb水平和外周血嗜碱粒细胞比率预示患者易于达到CHR、CCyR、MCyR或CMoR独立的有利因素,P值分别为0.032,0.024和0.0016。(4)CP(ECP30例,LCP25例):中位追踪为15个月,Logistic回归分析表明,患者获得的完全血液学反应(CHR)率为90.9%,完全细胞遗传学反应(CCyR)率为85.5%,主要细胞遗传学反应(MCyR)率为69.1%和完全分子学反应(CMoR)率为63.6%。其中ECP反应率分别为90%、83.3%、66.7%和63.3%;LCP反应率分别为92%、88%、72%和64%。AP和BC:中位追踪为15个月,获得的CHR、CCyR、MCyR和CMoR分别为55%、45%、30%和20%。结论伊马替尼可以使CML患者获得较高的CHR、CCyR、MCyR和CMoR。无论对于初治患者还是复治患者,伊马替尼均可以作为CML的首选分子靶向药物。
关键词:甲磺酸伊马替尼;慢性髓系白血病;相关因素
1资料与方法
1.1临床资料2010年1月至2015年3月,我院接受CML患者(按WHO2001诊断标准)70例,均口服伊马替尼,其中慢性期患者(CP)55例,早CP(病程<12个月)30例,晚CP(病程≥12个月)25例,加速期(AP)11例,急变期(BC)9例。
1.2治疗方法伊马替尼初始剂量400~600 mg·d-1, 大多数患者为400 mg·d-1, 持续口服。伊马替尼的副作用主要是血液毒性,在临床上根据血常规中白细胞数目、血红蛋白水平、外周血中性粒细胞数目及百分比作为评价其血液毒性的指标。病程≤6个月为初治组,共55例,病程>6个月为复治组, 共15例[1];根据Sokal积分将患者分为低危组 (36例)、中危组 (25例)和高危组 (9例)。
1.3观察指标观察本院70例患者的完全血液学反应(CHR)、完全细胞遗传学反应(CCyR)、主要细胞遗传学反应(MCyR)和完全分子学反应(CMoR)等指标,分析伊马替尼对CML患者效果的相关因素。
1.4统计学处理采用SPSS 15.0统计学软件进行数据处理,数据均以中位值(范围)表示。采用Logistic回归进行多因素分析,计数资料采用χ2检验。P<0.05为差异有统计学意义。
2结果
2.1伊马替尼治疗后初治组与复治组CHR、CCyR、MCyR和CMoR率的比较截至2015年3月,我院接收的70例CML患者均能耐受伊马替尼。所有CML患者的CHR均达到了100%,40例(71.9%的患者)达到了CCyR,44例(80.8%的患者)达到了MCyR,41例(74.9%的患者)达到了CMoR。初治组的CHR、CCyR、MCyR和CMoR分别为100%、71.9%、80.8%和74.9%,复治组分别为100%、45.8%、79.1%和53.9%(表1),差异无统计学意义。
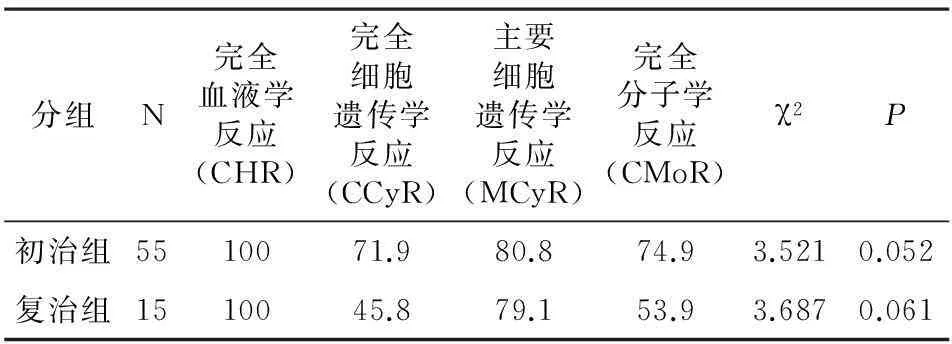
表1 伊马替尼治疗后初治组与复治组
2.2伊马替尼治疗后低危组、中危组和高危组 CHR、CCyR、MCyR和CMoR比较低危组的CHR、CCyR、MCyR和CMoR分别为100%、63.7%、78.9% 和56.3%;中危组分别为100%、76.1%、79.6%和47.9%;高危组分别为100%、49.8%、76.3%和46.8%(表2), 差异无统计学意义。
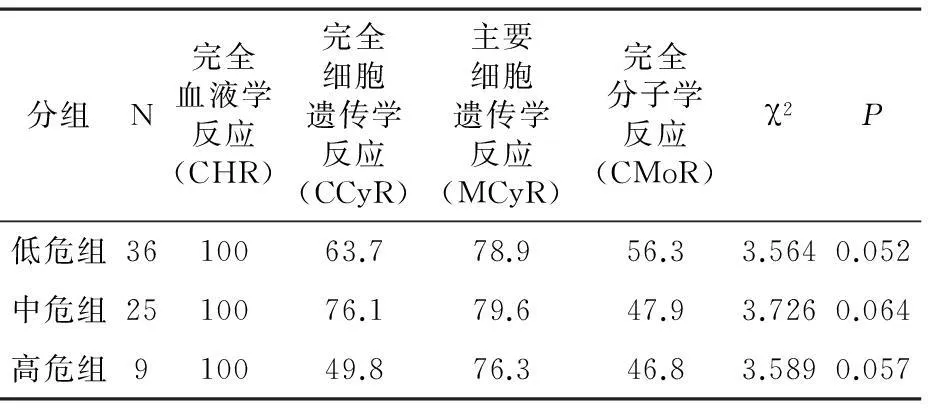
表2 伊马替尼治疗后低危组、中危组和高危组
2.3MCyR, CCyR和CMoR影响因素分析单因素分析表明,治疗前WBC数、Hb水平和外周血嗜碱粒细胞比率预示患者易于达到CHR、CCyR、MCyR或CMoR独立的有利因素,P值分别为0.032,0.024和0.0016(表 3)。伊马替尼治疗效果与CML患者的年龄、血小板数目、脾脏肿大程度、外周血和骨髓原始细胞细胞数目以及嗜酸性细胞数目无明显关系。
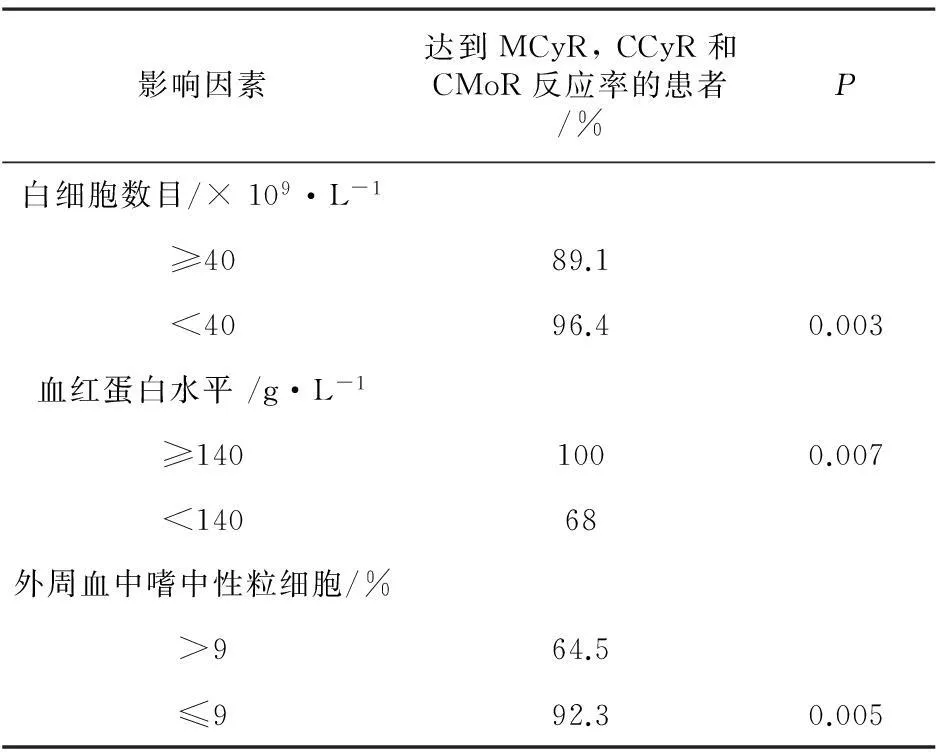
表3 MCyR, CCyR和CMoR影响因素分析
2.4甲磺酸伊马替尼对早CP、晚CP、AP和BC的疗效比较CML-CP患者中,ECP患者30例,LCP患者25例,中位追踪为15个月,采用Logistic回归分析发现,患者获得的完全血液学反应(CHR)率为90.9%,完全细胞遗传学反应(CCyR)率为85.5%,主要细胞遗传学反应(MCyR)率为69.1%和完全分子学反应(CMoR)率为63.6%。其中ECP反应率分别为90%、83.3%、66.7%和63.3%;LCP反应率分别为92%、88%、72%和64%。AP和BC:中位追踪为15个月,获得的CHR、CCyR、MCyR和CMoR分别为55%、45%、30%和20%(表 4)。
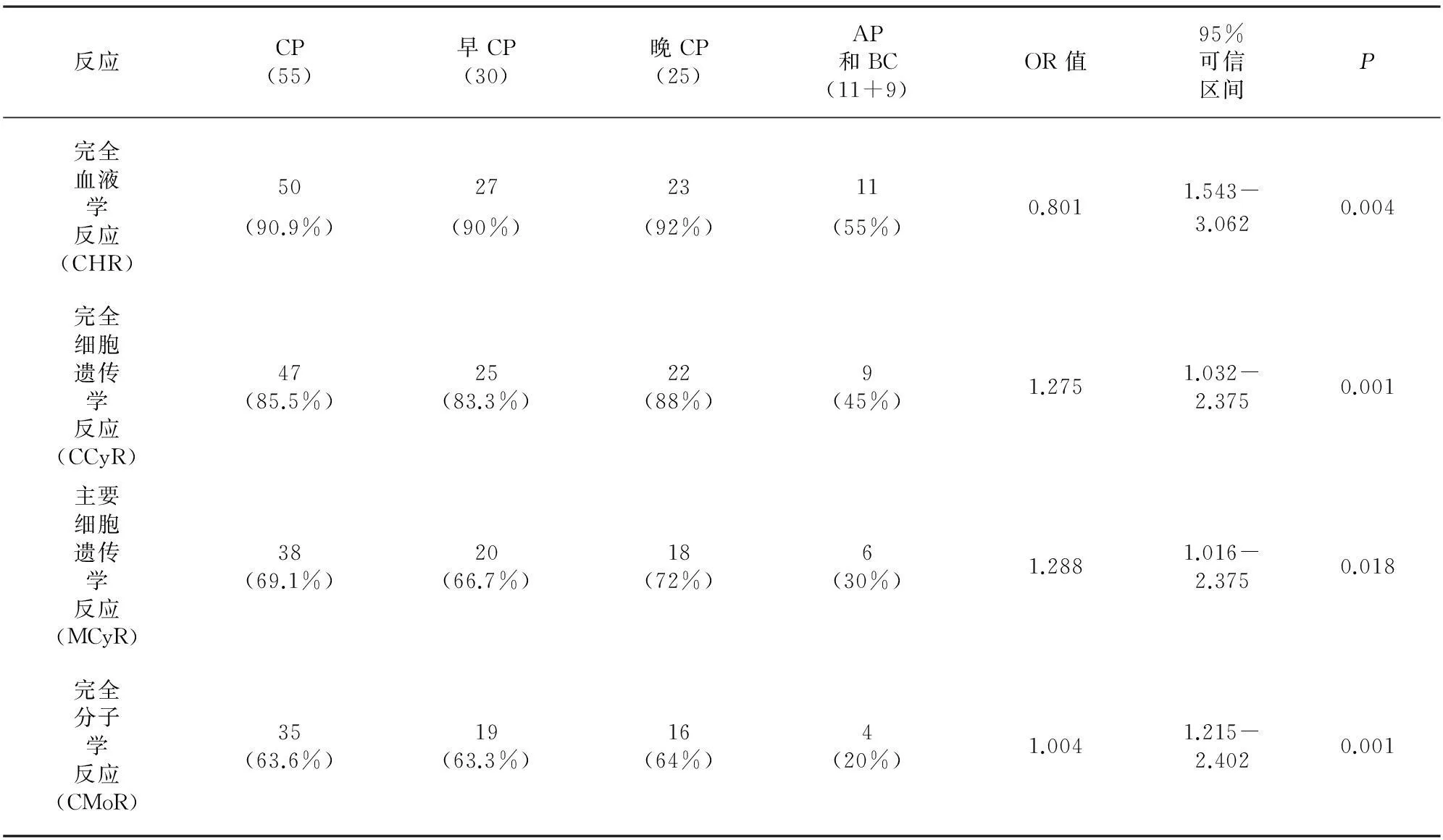
表4 甲磺酸伊马替尼对早CP、晚CP、AP和BC的疗效比较
3讨论
慢性粒细胞白血病( CML) 是一种起源于造血干细胞的血液系统恶性疾病,具有特征性的Ph 染色体,形成bcr /abl 融合基因,编码的蛋白P210 有很强的酪氨酸激酶活性,是其发病的基础。甲磺酸伊马替尼是酪氨酸激酶抑制剂,已被公认为目前治疗慢性粒细胞白血病的一线药物,能特异性阻断ATP 在abl 激酶上的结合位置,使酪氨酸残基不能磷酸化,从而阻止bcr /abl 阳性细胞的增殖[2]。研究发现: 以质粒介导的miR-203 真核表达载体通过下调bcr /abl 融合基因的表达从而效抑制K562 细胞增殖[3]。甲磺酸伊马替尼治疗CML的疗效显著,毒性低 ,已经成为目前国际上公认的CML首选分子靶向药物[4-5]。CML的诊断方式包括临床诊断、细胞遗传学诊断、分子生物学诊断等,TKI停药的前提是持续的完全分子反应(CMR)[6]。治愈CML不仅需要TKI靶向清除微小残留灶(MRD),更需要药物能够多角度清楚CML干细胞或祖细胞。伊马替尼早期临床疗效确切,可以观察到患者血象改善、脾脏缩小和临床症状改善[7-8]。
至2015年3月,我院接受70例CML患者,均口服伊马替尼,全部患者均达到了CHR,反应率为100%,中位达CHR时间为1个月,CHR、CCyR、MCyR和CMoR率分别为90.9%、85.5%、69.1%和63.6%。用药第3个月、6个月细胞遗传学反应显著,分子生物学反应良好。无患者因血液学毒性反应减量或停药,药物非血液学毒副反应较轻,未发现严重不良反应。采用Sokal评分将患者分为低、中、高危组患者,随访3个月结果提示药物早期疗效可靠,耐受性高,但临床医生也应关注药物不耐受导致剂量减低对疗效的影响。
近年来,很多学者将CML分为早CP(ECP)和晚CP(LCP),ECP指初次确诊的CP患者,LCP指曾经接受过治疗的CP患者。在本研究中,我们将病程≤6个月的患者定义为初治组,病程>6个月的患者定义为复治组。结果显示,患者获得的完全血液学反应(CHR)率为90.9%,完全细胞遗传学反应(CCyR)率为85.5%,主要细胞遗传学反应(MCyR)率为69.1%和完全分子学反应(CMoR)率为63.6%。其中ECP反应率分别为90%、83.3%、66.7%和63.3%;LCP反应率分别为92%、88%、72%和64%。AP和BC:中位追踪为15个月,获得的CHR、CCyR、MCyR和CMoR分别为55%、45%、30%和20%。初治组和复治组的CHR、CCyR、MCyR和CMoR并无统计学差异,说明伊马替尼可以作为ECP和LCP的首选靶向分子药物,对初治组和复治组均有效果。
本研究根据Sokal积分将患者分为:低危组(36例)、中危组(25例)和高危组(9例),这三组获得的CHR、CCyR、MCyR和CMoR并无显著差异。由于Sokal积分受很多因素的影响,尤其是需要大量的临床样本,限制了此方法在临床上的应用,要进一步阐述三组之间的差别,还需采用其他方法进行研究。
细胞遗传学和分子学的反应是CML患者长期生存的关键,因为伊马替尼成功抑制bcr/abl融合基因,使骨髓储备适量的造血干细胞祖细胞[9-10]。我们通过单因素分析发现,患者易于达到更好的CHR、CCyR、MCyR或CMoR反应。处于CML早期阶段的患者,白细胞数量较少,血红蛋白含量较高,骨髓中储备比较充足的正常造血干细胞祖细胞,这些患者接受伊马替尼治疗后,易于达到更好的细胞遗传学反应。CML患者外周血中含有较多的嗜碱性粒细胞,这些细胞分泌的炎性因子是CML患者不利于达到较好的CHR、CCyR、MCyR和CMoR反应的重要原因[11-12]。其他影响甲磺酸伊马替尼治疗效果的因素还有待进一步研究。
综上所述,甲磺酸伊马替尼可以使CML-CP患者获得极高的CHR、CCyR、MCyR和CMoR率,提高患者的生存时间,改善患者的生活质量,因此,甲磺酸伊马替尼是目前国际上公认的首选分子靶向药物。
参考文献:
[1]吴德沛.内科学[M].北京:人民卫生出版社, 2000, 610-611.
[2]Wang D,Zhang Q,Charles D,et al.Phase II Trial of neoadjuvant adjuvant imatinib mesylate for advanced primary and metastatic /recurrent operable gastrointestinal stromal tumors: long-term follow-up results of radiation therapy oncology group[J].Annals of Surgical Oncology,2012,19(4):1074-1080.
[3]何金花,黎毓光,谢杏仪,等.Hsa-miR-203 真核表达载体的构建及对K562 细胞增殖与凋亡的影响[J].临床检验杂志,2012,30(8):595-598.
[4]Wang Y.Clinical Efficacy of Dasatinib, Nilotinib and Imatinib in Newly Diagnosed Patients with Chronic-Phase Chronic Myeloid Leukemia: A Three-year Retrospective Analysis[J].Zhongguo Shi Yan Xue Ye Xue Za Zhi,2015,23(2):356-363.
[5]Castagnetti F,Palandri F,Amabile M,et al.Results of high-dose imatinib mesylate in intermediate Sokal risk chronic myeloid leukemia patients in early chronic phase: a phase 2 trial of the GIMEMA CML Working Party[J].Blood, 2009,113 (15): 3428-3434.
[6]Castagnetti F, Testoni N, Luatti S.Deletions of the derivative chromosome 9 do not influence the response and the outcome of chronic myeloid leukemia in early chronic phase treated with imatinib mesylate: GIMEMA CML Working Party analysis[J].Journal of clinical oncology,2010, 28(16):2748-2754.
[7]Jiang X,Forrest D,Nicolini F,et al.Properties of CD34+CML stem/progenitor cells that correlate with different clinical responses to imatinib mesylate[J].Blood,2010,116(12):2112-2121.
[8]Marcé S,Cortes M,Zamora L,et al.A Thirty-five Nucleotides BCR-ABL1 Insertion Mutation of Controversial Significance Confers Resistance to Imatinib in a Patient with Chronic Myeloid Leukemia (CML) [J].Exp Mol Pathol,2015,99(1):16-18.
[9]Dharmapuri G,Doneti R,Philip G,et al.Celecoxib sensitizes imatinib-resistant K562 cells to imatinib by inhibiting MRP1-5, ABCA2 and ABCG2 transporters via Wnt and Ras signaling pathways [J].Leuk Res,2015,39(7):696-701.
[10] Grimaudo S,Meli M,Di Cristina A,et al.The new iodoacetamidobenzofuran derivative TR120 decreases STAT5 expression and induces antitumor effects in imatinib-sensitive and imatinib-resistant BCR-ABL-expressing leukemia cells [J].Anticancer Drugs.2013,24(4):384-393.
[11] Levescot A,Flamant S,Basbpus S,et al.BCR-ABL-induced deregulation of the IL-33/ST2 pathway in CD34+ progenitors from chronic myeloid leukemia patients[J].Cancer Res,2014,74(10):2669-2676.
[12] Mashhadi M,Kaykhaei M,Mohammadi M,et al. Imatinib therapy in chronic myelogenous leukemia and thyroid function tests[J].Int J Hematol Oncol Stem Cell Res,2014, 8(3):20-23.
Analysis of related factors in 70 chronic myeloid leukemia patients
treated with imatinib mesylate
WANG Liang-tuo,ZHANG Xiang-lan,SITU Jian-yu,et al
(ThePeople’sHospitalofYangjiang,Guangdong529500,China)
Abstract:Objective The aim of this study was to investigate the related factors of imatinib mesylate on myeloid leukemia patients. Methods 70 CML patients received imatinib mesylate at a dose of 400~600 mg orally per day and we evaluated their complete hematologic response (CHR), complete cytogenetic response (CCyR), major cytogenetic response (MCyR) and complete molecular response (CMoR),etc.in patients of chronic phase (CP) (early chronic phase and chronic phase), accelerated phase (AP) and blast crisis (BC). And then analyzed the related factors of imatinib mesylate on chronic myeloid leukemia. ResultsUntil the February 2015 in our hospital, 55 cases of the 70 chronic myeloid leukemia patients are in chronic phase (CP) (30 cases of early chronic phase, 25 cases of late chronic phase); 11 cases are in accelerated phase (AP); 9 cases are in blast crisis (BC). (1)After a median follow up of 15 months, all the 70 cases of CML patients reached a 100% CHR. Among primary treated group, the CHR rate was 100%, CCyR rate 80.8%, MCyR rate 71.9% and CMoR 74.9%. And in retreated group, the CHR rate, CCyR, MCyR and CMoR were 100%, 45.8%, 79.1% and 53.9%, respectively, and there was no significant difference. (2)The CHR rate, CCyR, MCyR and CMoR in low-risk CML patients were 100%, 63.7%, 78.9% and 56.3%, respectively. The rates in intermediate risk CML patients were 100%, 76.1%, 79.6% and 47.9%, respectively. The rates in high-risk CML patients were 100%, 49.8%, 76.3% and 46.8%, respectively and there was no significant difference. (3)Before treatment, the WBC count was less than 100×109·L-1, the Hb level was much more than 130 g·L-1, and the rate of basophil count in peripheral blood was less than 0.05. This indicated that CML patients were susceptible to the beneficial rates of CHR, CCyR, MCyR or CMoR. (4)Chronic phase (30 patients of early chronic phase, 30 cases of late chronic phase) with a median follow-up of 15 months, overall CHR rate was 90.9%, CCyR rate 85.5%, MCyR rate 69.1%, and CMoR rate 63.6%. Among the total response rates, early chronic phase (<12 months) were 90%, 83.3%, 66.7% and 63.3%, respectively; that of late chronic phase (≥12 months) were 92%, 88%, 72% and 64%, respectively. AP and BC: with a median follow-up of 15 months, the rates of CHR, CCyR, MCyR and CMoR were 55%, 45%, 30% and 20%, respectively (Table 4). Conclusions The CML patients in chronic phase treated with imatinib mesylate can achieve a better CHR, CCyR, MCyR and CMoR and it should be considered that the imatinib mesylate is a drug of the optimal molecular-targeted medicine for primary treated and retreated CML patients.
Key words:chronic myelogenous leukemia; imatinib mesylate; related factors慢性髓系白血病(CML)是骨髓造血干细胞克隆性增殖形成的恶性肿瘤,绝大多数患者缓慢起病,bcr/abl融合基因是CML的主要病因,目前已经成为诊断CML的首要条件之一。甲磺酸伊马替尼是一种酪氨酸激酶抑制剂, 可以特异性抑制P210bcr-abl与P190bcr-abl酪氨酸激酶、干细胞生长因子受体(c-kit)和血小板衍化生长因子受体(PDGFR),是特异性治疗CML的首选分子靶向药物,迅速推动了CML治疗的新时代。我们分析了我院2010年1月至2015年3月70例CML患者应用伊马替尼的疗效,并初步探讨了伊马替尼对CML患者效果的相关因素。
收稿日期:(2015-07-08,修回日期:2015-10-21)
doi:10.3969/j.issn.1009-6469.2016.01.056

