HPLC法同时测定小儿复方呋喃西林滴鼻液中的盐酸麻黄碱与呋喃西林含量
湛 雯,景 霞,孙 芳,徐 进
(南京医科大学附属南京儿童医院药学部,江苏 南京 210008)
HPLC法同时测定小儿复方呋喃西林滴鼻液中的盐酸麻黄碱与呋喃西林含量
湛雯,景霞,孙芳,徐进
(南京医科大学附属南京儿童医院药学部,江苏 南京 210008)
摘要:目的建立同时测定小儿复方呋喃西林滴鼻液中盐酸麻黄碱和呋喃西林的含量测定方法。方法采用高效液相色谱法(HPLC)。色谱柱为Agilent Eclipse Plus-C18(4.6 mm× 250 mm, 5 μm)色谱柱;流动相,乙腈:水相(30 mmol·L-1Na2HPO4,0.1 %三乙胺,用50 %磷酸调节pH = 3.0 ± 0.03)= 18∶82;检测波长:210 nm,375 nm;柱温:25 ℃;流速:0.9 mL·min-1;进样体积:20 μL。结果盐酸麻黄碱测定质量浓度在0.08~0.40 g·L-1范围内与其相应峰面积积分值呈良好线性关系(r= 0.999 1);精密度、稳定性、重复性试验相对标准偏差(RSD)分别为0.58 %、0.67 %、0.82 %;平均回收率为100.56%,RSD为1.39 % (n= 9)。呋喃西林测定质量浓度在0.003 2~0.024g·L-1范围内与其相应峰面积积分值呈良好线性关系(r= 0.999 6);精密度、稳定性、重复性试验RSD分别为0.51 %、1.32 %、0.74 %;平均回收率为100.68 %,RSD为1.14 % (n= 9)。结论该方法专属性、重复性、准确性高,可用于小儿复方呋喃西林滴鼻液中盐酸麻黄碱和呋喃西林的含量测定。
关键词:小儿复方呋喃西林滴鼻液;盐酸麻黄碱;呋喃西林;高效液相色谱法;含量测定
小儿复方呋喃西林滴鼻液为我院自制制剂,成分为盐酸麻黄碱、呋喃西林、氯化钠、羟苯乙酯、纯化水。具有消炎、收缩血管作用,临床上用于鼻炎,鼻黏膜肿胀等疾病的治疗。
滴鼻液中盐酸麻黄碱和呋喃西林的处方量分别为5 g·L-1和0.2 g·L-1。原医院制剂标准[1]中采用旋光法检测盐酸麻黄碱的含量,采用紫外分光光度法检测呋喃西林的含量,但该两种检验方法专属性不是很强。为更有效的对小儿复方呋喃西林滴鼻液进行质量控制,加强儿童用药的安全性管理和精神药品的使用管理[2],本试验采用高效液相色谱(High Performance Liquid Chromatography ,HPLC)波长切换法[3-5],同时对其主要成分盐酸麻黄碱和呋喃西林进行含量测定方法研究,节约分析时间,提高分析灵敏度,为检测药品成分提供一种简单、准确的方法。
1仪器与材料
Agilent 1260 Infinity 高效液相色谱仪(G1312B二元泵,G1316A柱温箱,G4212B 二极管阵列检测器,十万分之一分析天平(瑞士Mettler Toledo,MS205DU)。
小儿复方呋喃西林滴鼻液为我院自制(批号:140723,141124,150104,150610),盐酸麻黄碱对照品购于中国食品药品检定研究院(批号:07149903),呋喃西林对照品购于中国食品药品检定研究院(批号:101167-201001),乙腈购于国药集团化学试剂有限公司,为色谱纯(批号:20141016),水为超纯水,其余试剂为分析纯。
2方法与结果
2.1色谱条件Agilent Eclipse Plus-C18(4.6 mm×250 mm, 5 μm)色谱柱;流动相,乙腈∶水相(30 mmol·L-1Na2HPO4,0.1 %三乙胺,用50 %磷酸调节pH = 3.0 ± 0.03)= 18∶82;检测波长:210 nm(0 ~ 7.5 min),375 nm(7.5 ~ 12 min);柱温: 25 ℃;流速:0.9 mL·min-1;进样体积:20 μL。
2.2溶液制备
2.2.1对照品贮备液取盐酸麻黄碱对照品约0.10 g,精密称定,至50 mL容量瓶中,加超纯水溶解并稀释至刻度,摇匀,即得。
取呋喃西林对照品约0.016 g,精密称定,至100 mL容量瓶中,加超纯水溶解并稀释至刻度,摇匀,即得。
2.2.2对照品溶液精密移取“2.2.1”项下盐酸麻黄碱储备液1.0 mL于10 mL量瓶中,以超纯水稀释并定容至刻度,摇匀,即得盐酸麻黄碱对照品溶液。
精密移取“2.2.1”项下呋喃西林储备液0.5 mL于10 mL量瓶中,以超纯水稀释并定容至刻度,摇匀,即得呋喃西林对照品溶液。
2.2.3供试品溶液取小儿复方呋喃西林滴鼻液一支,精密移取2.0 mL,以超纯水稀释并定容至50 mL,摇匀,过0.45 μm微孔滤膜,取续滤液,即得供试品溶液。
2.2.4阴性对照品溶液按小儿复方呋喃西林滴鼻液的处方工艺流程,分别制备不含盐酸麻黄碱或不含呋喃西林的空白制剂,按“2.2.3”项下方法进行处理,即得阴性对照品溶液。
2.3专属性试验按“2.1”项下色谱条件分别对对照品溶液,供试品溶液,阴性对照品溶液进行色谱分析,记录色谱图(图1)。由图1中看出,供试品溶液中盐酸麻黄碱和呋喃西林分别与对照品溶液中盐酸麻黄碱和呋喃西林色谱峰保留时间一致,且与相邻色谱峰分离度良好;阴性对照品溶液在盐酸麻黄碱或呋喃西林色谱峰位置无吸收峰。说明该测定方法专属性良好。
2.4线性关系考察精密吸取“2.2.1”项下对照品储备溶液适量,以流动性稀释,配制成浓度分别为0.08,0.16,0.20,0.24,0.30,0.40 g·L-1的盐酸麻黄碱溶液,及浓度分别为0.0032,0.0064,0.008,0.012,0.016,0.024 g·L-1的呋喃西林溶液。分别按2.1项下色谱条件进行分析,记录色谱峰面积。以各色谱峰面积积分值(Y)对样品中盐酸麻黄碱浓度或呋喃西林浓度(X, g·L-1)进行线性回归,得盐酸麻黄碱的回归方程:Y=42 591X+ 643.27,r= 0.9991;呋喃西林的线性回归方程:Y=103 676X-44.41,r= 0.999 6。结果表明,盐酸麻黄碱测试浓度在0.08~0.40 g·L-1范围内与其峰面积积分值呈良好线性关系;呋喃西林测试浓度在0.003 2 ~ 0.024 g·L-1范围内与其峰面积积分值呈良好线性关系。
2.5光谱鉴定分别吸取“2.2.2”、“2.2.3”项下的对照品溶液与供试品溶液进行色谱分析,采用二极管阵列检测器在210~ 400 nm波长范围内扫描,以对照品标准光谱图作为参考,对样品中盐酸麻黄碱和呋喃西林色谱峰进行光谱鉴定。结果显示,在色谱峰相同保留时间处,样品峰和对照品峰的吸收曲线相同,样品中盐酸麻黄碱和呋喃西林的色谱峰纯度均符合分析要求。
2.6精密度试验取“2.2.2”项下对照品溶液,按“2.1”项下色谱条件,连续进样6次,盐酸麻黄碱色谱峰面积的RSD为0.58 %,呋喃西林色谱峰面积的RSD为0.51 %,表明仪器精密度良好。
2.7稳定性试验取小儿复方呋喃西林滴鼻液一支(批号:150610)。按“2.2.3”项下方法制备供试品溶液。分别于室温放置0、1、2、4、8、12 h后,按2.1项下色谱条件进行测定。记录盐酸麻黄碱及呋喃西林色谱峰面积并计算RSD,结果分别为0.67% 和1.32%,表明供试品溶液中盐酸麻黄碱和呋喃西林在12 h内稳定。
2.8重复性试验取小儿复方呋喃西林滴鼻液一支(批号:150610)。按“2.2.3”项下方法制备6份供试品溶液。按“2.1”项下色谱条件测定6份供试品溶液中盐酸麻黄碱和呋喃西林的含量。结果盐酸麻黄碱和呋喃西林含量的RSD分别为0.82%和0.74%,表明该方法的重复性良好。
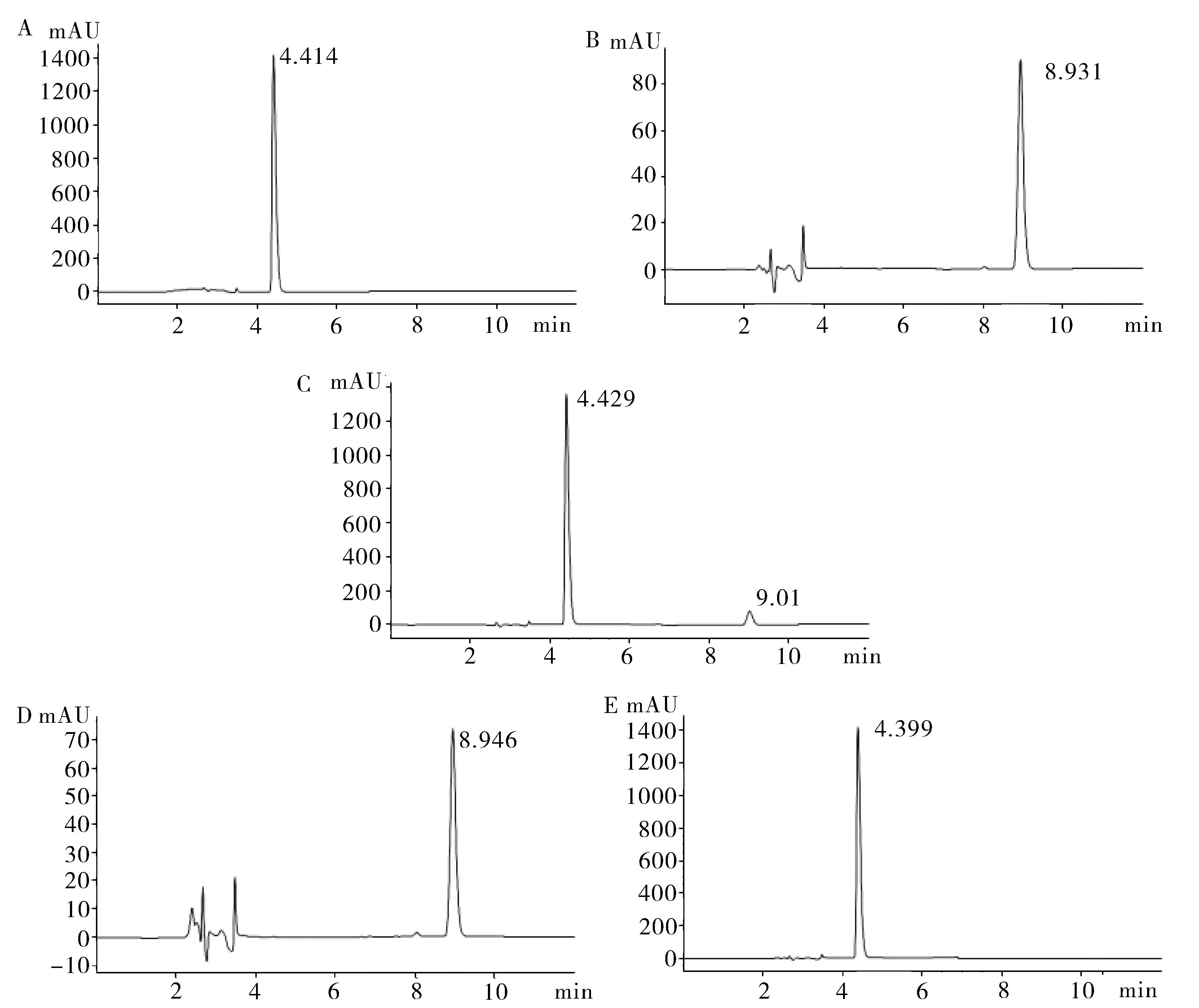
图1 HLPC图
盐酸麻黄碱注:(A)和呋喃西林(B)的对照品溶液色谱图,供试品溶液色谱图(C),盐酸麻黄碱阴性对照品溶液(D)和呋喃西林阴性对照品溶液(E)。
2.9回收率试验分别准确称取处方量80%、100%、120%的盐酸麻黄碱及呋喃西林对照品,并以处方比例加入空白辅料,按“2.2.3”项下方法处理,作为供试品溶液;另取盐酸麻黄碱及呋喃西林的对照品溶液,按“2.1”项下色谱条件测定盐酸麻黄碱及呋喃西林的峰面积,按外标法计算回收率,结果见表1。
2.10样品含量测定取小儿复方呋喃西林滴鼻液(批号:140723,141124,150104,150610),按2.2.3项下方法制备供试品溶液。按2.1项下色谱条件,分别取对照品溶液和供试品溶液进样,按外标法以峰面积计算样品中盐酸麻黄碱和呋喃西林的含量。另列出使用原医院制剂检测方法——旋光法和紫外分光光度法分别测得的盐酸麻黄碱和呋喃西林含量结果,见表2。
3讨论
3.1色谱条件的确定 本试验中,选择乙腈-磷酸盐水溶液作为流动相[6-8],流动相中加入适量三乙胺以改善色谱峰拖尾现象[9-11]。摸索了用乙腈和磷酸盐水相不同比例作为流动相,试验表明,当乙腈∶磷酸盐水相=18∶82时,盐酸麻黄碱和呋喃西林的色谱峰分离度良好,出峰时间适中。盐酸麻黄碱色谱峰理论塔板数大于8 000,呋喃西林色谱峰理论塔板数大于15 000。
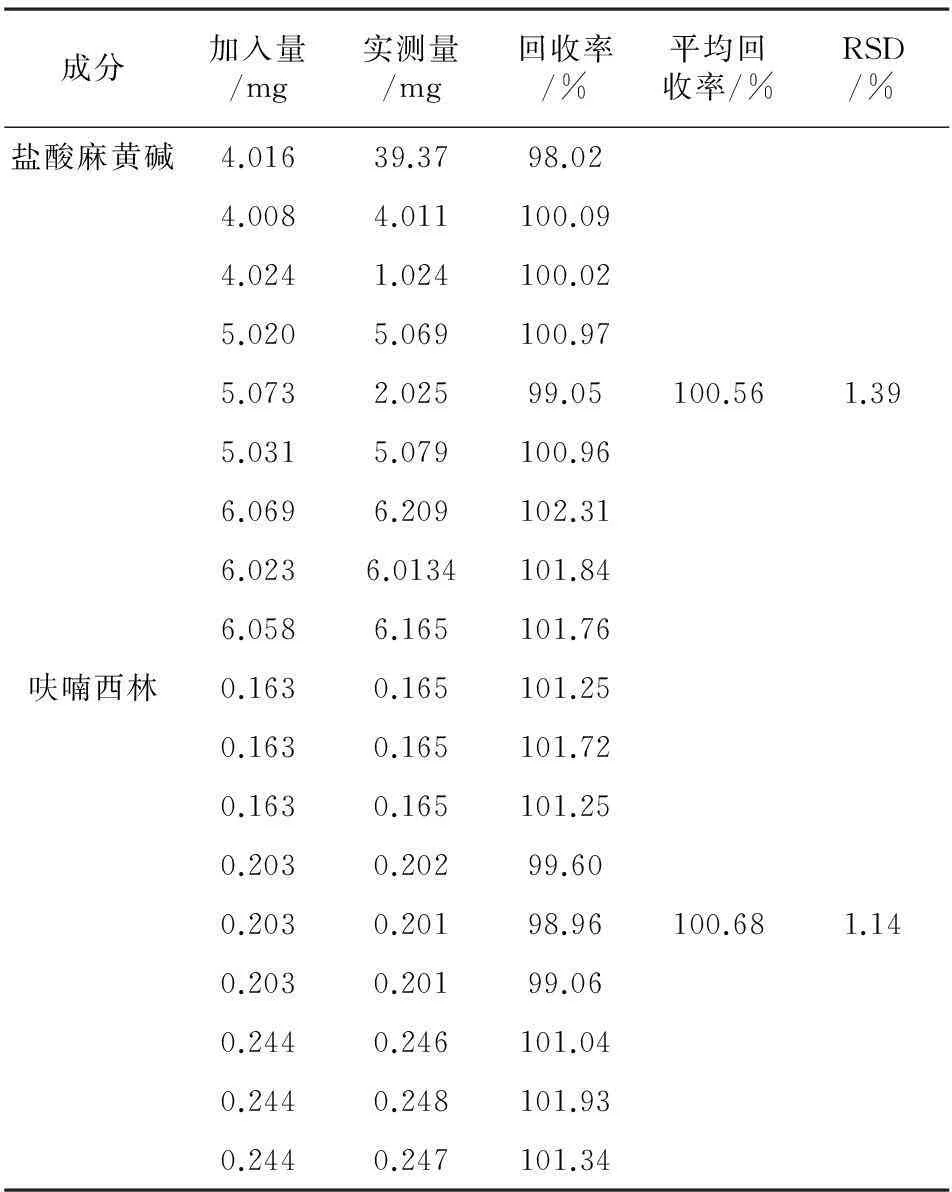
表1 回收率试验结果(n=9)
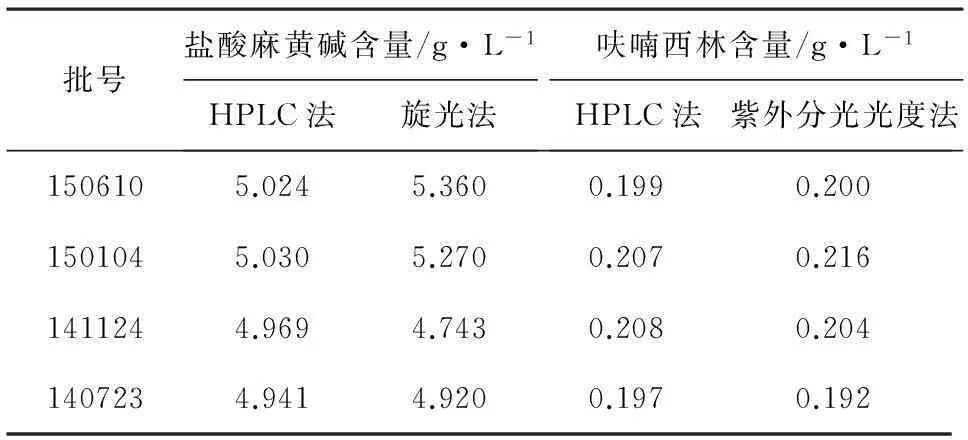
表2 小儿复方呋喃西林滴鼻液中盐酸麻黄碱和
3.2检测波长的选择用二极管阵列检测器在210~400 nm波长范围内扫描盐酸麻黄碱对照品溶液和呋喃西林对照品溶液,结果显示盐酸麻黄碱在210 nm波长处有末端最大吸收;呋喃西林在375 nm处吸收最强[12-14]。为保证两种成分均有最大吸收,本试验采用HPLC波长切换法,于210 nm波长处检测盐酸麻黄碱,375 nm波长处检测呋喃西林。
3.3样品前处理 从小儿复方呋喃西林滴鼻液的配方上可以看出,盐酸麻黄碱的含量为呋喃西林含量的25倍,需选择合适的进样浓度。本试验中将样品稀释25倍测定,同时满足盐酸麻黄碱和呋喃西林的定量测定要求。
3.4方法的稳定性本试验对方法的稳定性进行了考察,结果表明12 h内供试品溶液中盐酸麻黄碱和呋喃西林较稳定。但随着供试品放置时间的延长(24、48、72、96 h),呋喃西林色谱峰面积的RSD呈渐增大趋势,峰面积总体呈渐减小趋势。结合文献,呋喃西林易受光照、温度和放置时间的影响而渐发生降解[15]。因此,为保证含量测定准确性,建议供试品溶液现配现测。
本文使用二极管阵列检测器,采用HPLC法,同时检测了医院制剂小儿复方呋喃西林滴鼻液中盐酸麻黄碱和呋喃西林的含量,并进行方法学验证。将其测得的盐酸麻黄碱和呋喃西林含量同原医院制剂检测方法测得的盐酸麻黄碱和呋喃西林含量进行配对t检验分析,结果无统计学差异(P>0.05)。
本试验运用HPLC波长切换法检测盐酸麻黄碱和呋喃西林含量,灵敏度高,操作简单易行,线性关系良好,重现性好,精密度高,避免了重复制备,并提高样品检测的专属性,可用于小儿复方呋喃西林滴鼻液中盐酸麻黄碱和呋喃西林含量的测定,为儿童用药的安全性提供保障。
参考文献:
[1]潘学田 主编.中国医院制剂规范[M].2版.北京:中国医药科技出版社,1995:165-166.
[2]赵怀全,甄键存.麻黄碱及其药物制剂的监管法规与安全使用管理[J].中国药师,2010,13(1):149-150.
[3]王敏,张瑞麟,王逢春,等.高效液相色谱法单波长切换测定复方氯霉素醇溶液中水杨酸、氯霉素的含量[J].解放军医药杂志,2013,25(8):88-90.
[4]李桂本,王海波,李振国.HPLC波长切换同时测定知柏地黄丸中莫诺苷、马钱苷和丹皮酚的含量[J].中国实验方剂学杂志,2015,21(16):48-51.
[5]卢智玲.HPLC波长切换法同时测定清开灵胶囊中栀子苷和黄芩苷的含量[J].中国中医药科技,2014,21(1):46-47.
[6]李霞,李继,戴涌,等.高效液相色谱法测定复方甘草麻黄碱片中盐酸麻黄碱含量[J].中国药业,2015,24(1):43-44.
[7]张晓丹,蔡培培,金丽,等.苯海拉明麻黄碱滴鼻液的质量标准研究[J].解放军药学学报,2014,30(5):428-430.
[8]王逢春,王敏,张瑞麟.HPLC法测定复方呋喃西林滴鼻液中盐酸麻黄碱的含量[J].实用药物与临床,2014,17(1):71-73.
[9]杨金草.高效液相色谱法测定清肺平喘口服液中盐酸麻黄碱含量[J].甘肃医药,2009,28(3):184-185.
[10] 柯雪红,桂雪虹,张升,等.HPLC法测定呋喃西林冲洗液的含量及有关物质[J].药物分析杂志,2014,34(8):1509-1512.
[11] 邓芳,万莉,崔小平.高效液相色谱法测定呋喃西林溶液中呋喃西林含量[J].中国药业,2011,20(13):28-29.
[12] 张萍,吴敏,汤慧,等.基于HPLC-DAD方法建立的数字对照品库检索平台用于鸡蛋中四环素类药物残留的快速筛查[J].安徽医药,2015,19(2):252-255.
[13] 朱锐金,潘玮玮,蓝烨.紫外分光光度法测定呋喃西林炉甘石洗剂中呋喃西林的含量[J].轻工科技,2014(3):101-102.
[14] 金慧臻,郁丹红.呋喃西林滑石粉中呋喃西林的含量测定[J].北方药学,2014,11(12):25.
[15] 石嫱,庆格乐.呋喃西林溶液的制备方法改进及稳定性评价[J].中国药业,2013,22(23):45-46.
Simultaneous determination of ephedrine hydrochloride and furacilin in
pediatric compound furacilin nasal drops by HPLC
ZHAN Wen, JING Xia, SUN Fang,et al
(PharmaceuticalDepartment,NanjingChildren’sHospitalAffiliatedtoNanjingMedicalUniversity,
Nanjing210008,China)
Abstract:Objective To establish a method of quantitative determination of ephedrine hydrochloride and furacilin in Pediatric Compound Furacilin Nasal Drops.Methods The HPLC method was adopted with the Agilent Eclipse Plus-C18column (4.6 mm×250 mm, 5 μm) at room temperature (25℃) and acetonitrile 0.03 mol·L-1phosphoric acid solution (pH adjusted to 3.0 ± 0.03)(18/82) as the mobile phase at the flow rate of 0.9 mL·min-1. The detection wavelength for ephedrine hydrochloride and furacilin was 210 nm and 375 nm, respectively, and the injection volume was 20 μL.ResultsThe good linear relationship for ephedrine hydrochloride was in the range of 0.08 - 0.40 g·L-1(r= 0.999 1), while this for furacilin was in the range of 0.003 2~0.024 g·L-1(r= 0.999 6). RSDs of ephedrine hydrochloride for precision, stability and reproducibility tests were 0.58%, 0.67% and 0.82%, respectively. The average recovery of ephedrine hydrochloride was 100.56% (RSD =1.39%,n= 9). RSDs of furacilin for precision, stability and reproducibility tests were 0.51%, 1.32% and 0.74%, respectively. The average recovery of furacilin was 100.68% (RSD = 1.14%,n= 9). Conclusions This established method was specific, accurate and reproducible for the quantitative determination of ephedrine hydrochloride and furacilin in Pediatric Compound Furacilin Nasal Drops.
Key words:pediatric compound furacilin nasal drops;ephedrine hydrochloride;furacilin;HPLC;quantitative determination
收稿日期:(2015-08-22,修回日期:2015-10-19)
通信作者:徐进,男,副主任药师,研究方向:中药分析,E-mail:xujin_cn@163.com
doi:10.3969/j.issn.1009-6469.2016.01.014

