药 物 性 肝 损 伤 168 例 临 床 分 析
温祝杜 胡国信 郑 洁 杨 剑 陈智明
(1 广东省深圳市龙岗区第二人民医院社康中心,深圳市 518100,E-mail:dogmeat@163.com;2 广州医科大学研究生学院,广州市 510000;3 北京大学深圳医院感染科,深圳市 518100;4 北京大学深圳医院中医科,深圳市 518100)
临床创新
药 物 性 肝 损 伤 168 例 临 床 分 析
温祝杜1,2胡国信3郑 洁4杨 剑2陈智明2
(1 广东省深圳市龙岗区第二人民医院社康中心,深圳市 518100,E-mail:dogmeat@163.com;2 广州医科大学研究生学院,广州市 510000;3 北京大学深圳医院感染科,深圳市 518100;4 北京大学深圳医院中医科,深圳市 518100)
目的 探讨药物性肝损伤(DILI)的病因及临床特征和预后。方法 回顾性分析168例DILI患者的临床资料,采用RUCAM量表评价药物应用史与肝损伤的相关性,并总结肝损伤药物种类构成、DILI的临床特征及预后。结果 致肝损伤药物前3位为中草药90例(53.57%)、抗生素16例(9.52%)、解热镇痛药15例(8.93%)。男女性别比为1 ∶1.75。RUCAM分值以6~8分者居多,占75.00%,其次为>8分者,占16.67%。DILI临床表现多样,无特异性,以肝细胞损伤型居多,共87例(51.79%),胆汁淤积型50例(29.76%),混合型31例(18.45%)。经治疗,治愈及有效166例(98.81%);无效2例(1.19%)。结论 中草药是引起DILI最主要的原因,其次为抗生素和解热镇痛药;DILI的临床表现复杂多样,缺乏特异性;绝大多数DILI患者预后良好,停用一切可疑肝损药物是治疗关键。
药物性肝损伤;临床特征;预后;致病药物
以往有学者[1]认为,药物性肝损伤(drug-induced liver injury,DILI)发病率不高。近年,随着对DILI认识的不断深入,新药不断涌现及各类保健药物的应用,DILI的发病率明显增高。但DILI的临床表现复杂多样、实验室检查缺乏特异的标志物,易被误诊和漏诊,因此,选择一个可靠的诊断标准对临床DILI的诊治工作具有重要意义[2]。我们采用目前应用最广泛且被公认为相对可靠的Roussel Uclaf因果关系评价法(Roussel Uclaf Causality Assessment Method,RUCAM)量表,对DILI患者进行评分,评估致病药物与肝损伤的相关性,探讨DILI的致病因素、临床表现及预后特征。
1 资料与方法
1.1 临床资料 通过病案管理软件系统,搜索北京大学深圳医院和深圳市龙岗区第二人民医院2002年1月至2013年12月住院患者中含有“DILI”、“药物性肝炎”、“药物性肝衰竭”等诊断的病例。共有168例纳入本课题,中位年龄 47.5岁(18~89岁),<20岁4例(2.38%),≥20~<40岁56例(33.33%),≥41~<60岁88例(52.38%),≥60岁20例(11.90%)。男性61例(36.31%),女性107例(63.69%),男女比例为1 ∶1.75。
1.2 病例纳入和排除标准 (1)纳入标准:① 发病前1年内,特别是1~8周内有明确用药史;② 血清ALT≥5倍正常值上限,或ALT≥3倍正常值上限且同时总胆红素≥2倍正常值上限,和(或)碱性磷酸酶 ≥2倍正常值上限,和(或)有肝损伤病理学证据;③ 排除肝炎病毒感染、酗酒、脂肪肝、自身免疫等其他原因所致的肝脏生物化学异常;④ 偶然再次出现给药后又发生肝损害;⑤ 早期症状有发热、皮疹、瘙痒等;⑥ 血液嗜酸性粒细胞比例高于5%。凡具备第1、2条,加上第3~6条中的任何2条,即初步考虑DILI。进一步使用RUCAM量表再次评估。RUCAM量表分值>8分,非常可能为DILI;>6~≤8分,很可能为DILI;>3~≤5分,可能为DILI;>1~≤2分,不太可能为DILI;≤0,不是DILI。分值≥3分的病例纳入本研究。RUCAM评分实施方法:先培训3位感染科医师如何操作RUCAM量表,然后再由3位专科医师独立对这些病例进行评分;评分结果明显不一致的,由课题组集中讨论决定。(2)病例排除标准:① 甲、乙、丙、丁、戊型肝炎病毒标志物阳性;② 巨细胞抗体、EB病毒抗体阳性;③ 腹部B超监测结果提示肝脂肪浸润;④ 发病前2周内饮酒;⑤ 其他因素引起的肝损伤。
1.3 方法 记录168例患者的基本资料、临床表现、既往史、化验结果、服药史、治疗措施、疗效、预后等,分析致肝损伤药物的种类、RUCAM分值对应致病药物品种、临床分型、不同临床分型对应致病药物品种、临床症状发生情况及对应药物种类、DILI严重程度对应的致病药物种类。
1.4 临床分型 参照国际共识分为如下3型:(1)肝细胞损伤型:R>5;(2)胆汁淤积型:R<2;(3)混合型:R为2~5。R=(治疗前ALT实测值/ALT正常值上限)/(治疗前碱性磷酸酶实测值/碱性磷酸酶正常值上限)。1.5 临床严重程度分级 轻度DILI症状较轻或无自觉症状,总胆红素<34 μmol/L 且凝血酶原活动度>40%;中度DILI总胆红素34~171 μmol/L,凝血酶原活动度>40%;重度DILI症状重,总胆红素>171 μmol/L,凝血酶原活动度>40%;急性或亚急性肝衰竭型DILI症状更重,总胆红素>171 μmol/L,凝血酶原活动度<40%。
1.6 疗效判断 治愈:症状消失,肝功能恢复正常;有效:症状明显缓解,总胆红素或转氨酶下降>50%;无效:症状及肝功能无改善或逐渐加重,未达到有效标准而自动出院;死亡。
2 结 果
2.1 引起肝损伤的药物 可疑致肝损害药物包括中草药、抗感染药、解热镇痛药、抗肿瘤药、胃肠类药、降脂降压药、抗结核药等,比例最高前3类依次占53.57%、9.52%、8.93%,见表1。

表1 致肝损伤药物的种类及比例
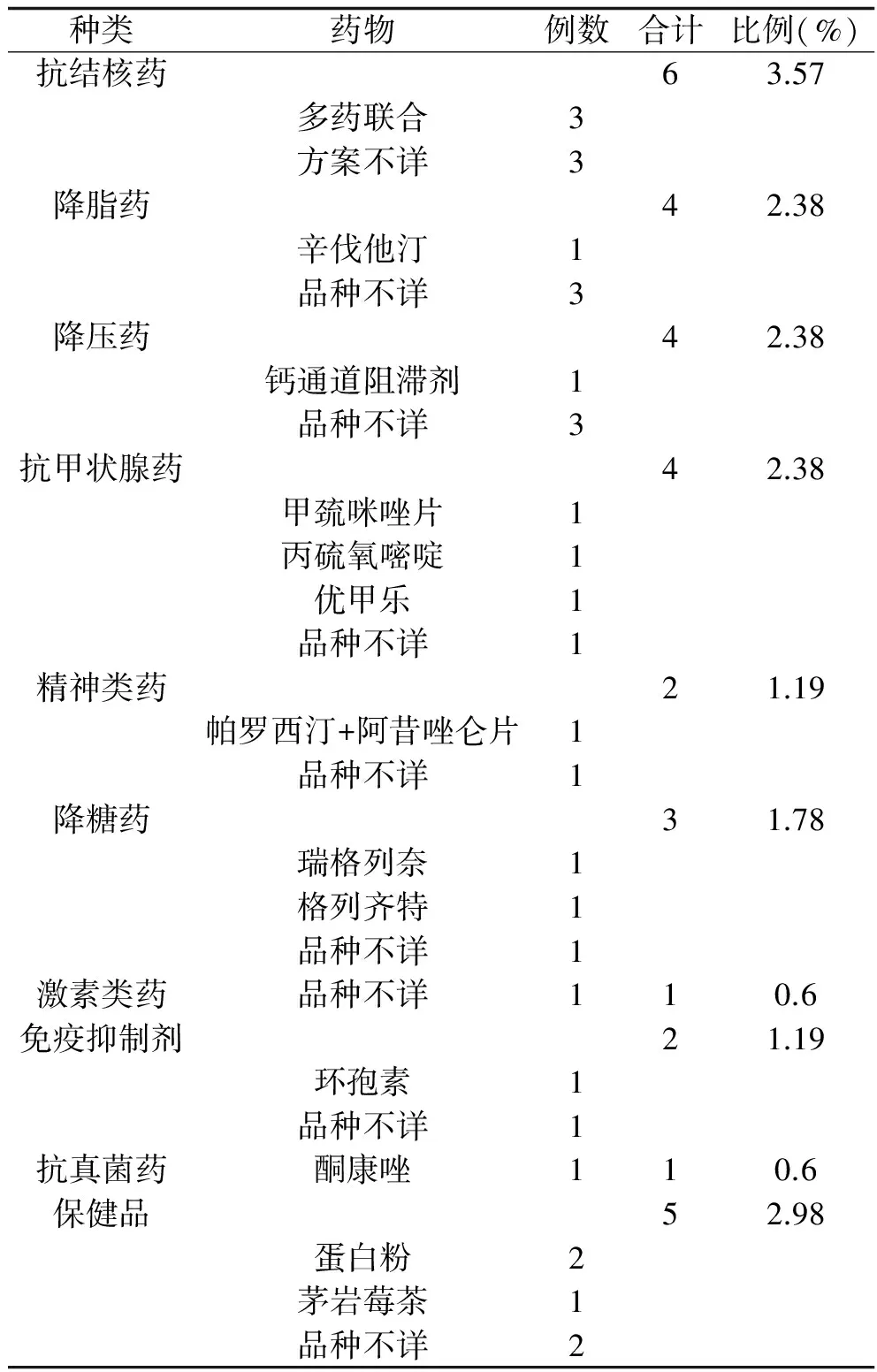
续表1
注:*含中草药、中成药及中药复合制剂;#含抗病毒药物。
2.2 RUCAM分值对应致病药物 RUCAM分值以6~8分者居多占75.00%,其次为>8分者,占16.67%。见表2。
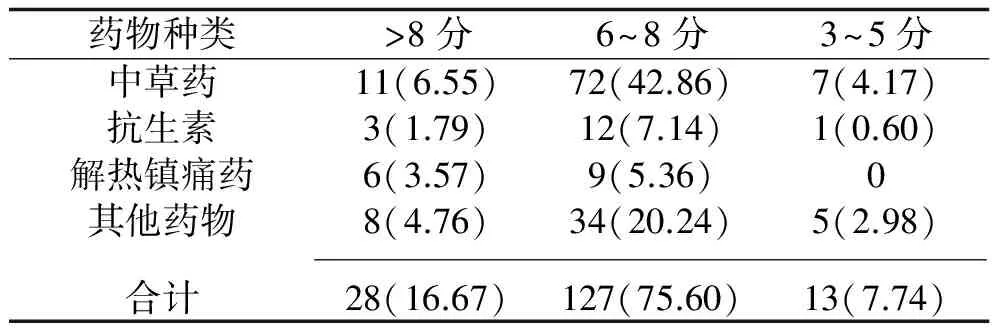
表2 168例DILI患者RUCAM分值对应致病药物种类(n,%)
2.3 DILI临床分型 肝细胞型DILI 87例(51.79%),胆汁淤积型DILI 50例(29.76%),混合型DILI 31例(18.45%)。肝细胞型DILI中位年龄46.5岁,胆汁淤积型DILI中位年龄54.0岁,混合型DILI中位年龄48.7岁。常见的中草药、抗生素、解热镇痛药DILI的临床分型见表3。
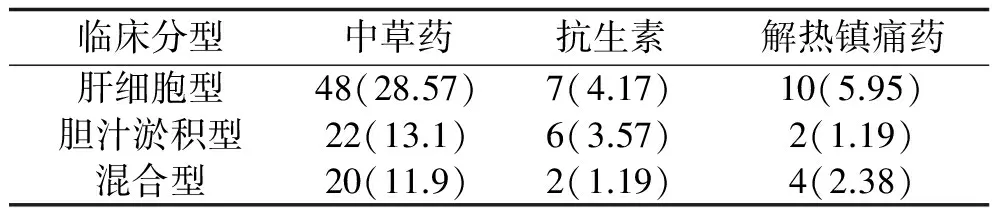
表3 不同临床分型对应致病药物品种(n,%)
2.4 临床参数分析
2.4.1 开始用药至出现肝损伤的时间:用药后≤2周出现肝损伤43例(25.60%),2<~≤4周40例(23.81%),4<~≤8周41例(24.40%),>8周以上44例(26.19%)。
2.4.2 实验室检查指标:治疗前血液嗜酸性粒细胞比例>5%者21例(12.50%)。治疗前血清ALT中位数462 IU/L(124~4 806 IU/L),总胆红素中位数58.5 μmol/L(7.4~473.1 μmol/L),碱性磷酸酶中位数171.3 IU/L(23.8~812 IU/L)。
2.4.3 DILI临床症状:中草药DILI症状最常见为发热33.33%(30/90),其次为皮疹3.33%(3/90),无症状者占24.44%(22/90);抗生素DILI者均无发热、皮疹症状;解热镇痛药DILI症状最常见为发热56.25%(9/16),其次为皮疹18.75%(3/16),无症状者占43.75%(7/16)。
2.4.4 临床严重程度分级: 多数DILI患者症状为轻度至中度(76.78%)。中草药致肝衰竭型DILI占62.50%(5/8)。见表4。

表4 DILI严重程度对应的致病药物种类(n,%)
2.5 预后 经治疗,治愈及有效166例(98.81%);无效2例(1.19%),均为肝衰竭,其中1例患者自动出院视为无效,另1例住院期间死亡,为肿瘤患者,死亡原因不能确定是否与肝损伤有直接关系。
3 讨 论
DILI是指药物本身或其代谢活性物质进入体内引起肝细胞毒性损伤或肝脏对药物及其代谢活性产物的过敏反应所导致的一类疾病的总称[3]。其发病机制目前尚不完全明确,主要有药物对肝脏的直接毒性损伤和肝脏对药物引发的特异质反应介导的损伤两类。前者与用药剂量有关,肝损伤程度与用药剂量、服药持续时间有关;后者与药物剂量无关,大多与药物代谢相关的酶缺乏、活性低下,或个体免疫应答异常等因素有关[4]。DILI的发病并不是按某个单一机制进行,而是由多个途径共同介导的。有研究发现,氧自由基相关通路介导的肝损伤在DILI的发病中起重要的作用[5]。
本组168例患者中,中草药、抗生素及解热镇痛药导致的DILI前3位分别占53.57%、9.52%、8.93%,表明我国中草药制剂仍然是引起DILI最主要的原因之一,与欧美等国家DILI主要致病药物为解热镇痛药和抗生素有所不同[6]。本研究所涉及的中草药品种较多,其中大多患者所使用的是中草药复合制剂或自制药方,故无法清楚具体组分。
近年来,中草药引起DILI的相关报告越来越多,原因有:(1)随着饮食结构及生活方式的改变,高血压、糖尿病、心脏病等慢性病不断增多,需要长期服药或短期治疗效果欠佳,很多慢性病患者误以为中草药无副作用或副作用很少,将治疗希望寄托于中草药;(2)快节奏的生活方式,使亚健康状态广泛存在,致使某些人(特别是中老年人)选择中草药保健品进行“调理”;(3)中草药在慢性皮肤病和肌肉、筋骨慢性损伤性疾病的治疗上具有一定的优势。中草药生物来源、化学物质、炮制方法、代谢途径及临床应用的多样性和不确定性,使其导致的DILI发病机制更加复杂[7],对此应加强中草药用药规范管理及相关知识常识普及。
本研究结果显示,抗肿瘤药、降糖调脂降压药、抗甲状腺药等导致的DILI病例越来越多。随着生活改善、膳食谱不断丰富,胃肠负担相应加重,胃肠道疾病也不断增多,以致胃肠类药物滥用及由此而产生的肝损伤也日益显现。抗结核药、精神类药、激素类、保健品等也可引起不同程度的肝损伤。本研究中抗结核药物引起的DILI病例较少,原因可能与本研究所收集病例的医院并非结核病定点收治单位及本市有专门的抗结核防治定点医院和规范的转诊制度等因素有关。
本组DILI患者年龄≥41~<60岁居多(52.38%),原因可能与中年人为社会及家庭支柱,身心常处于亚健康状态,以致倾向于选择中草药制剂和保健品进行调养有关。168例病例中,女性107例(63.69%),明显多于男性患者(36.31%),男女性别比为1 ∶1.75,原因可能与男女生理特性差异、女性因特有的生殖系统疾病应用中草药比例较大、女性更易迷信保健品和减肥药等因素有关。本文结果显示,肝细胞型DILI 87例(51.79%),胆汁淤积型DILI 50例(29.76%),混合型DILI 31例(18.45%),说明临床分型中肝细胞型较常见,该型预后较差,年龄高者出现胆汁淤积型DILI的可能性更大。
本文结果显示,用药后≤2周出现肝损伤43例(25.60%),2<~≤4周40例(23.81%),4<~≤8周41例(24.40%),>8周44例(26.19%)。说明开始服用药物至发生肝损伤的时间跨度及发生DILI后的持续时间相差较大,一方面提示DILI临床表现复杂多样,可表现为急性肝损伤,也可表现为慢性肝损伤[8],部分患者可无任何症状或症状不明显而未及时就诊,肝损伤出现时间及肝损伤程度跟服药间隔时间、剂量、合并用药等有关[9];另一方面提示,不同药物导致DILI的剂量依赖性和和超敏反应发生发展过程存在一定的差异。
本组168例经治疗后,治愈及有效166例(98.81%),无效2例(1.19%),提示大多DILI可治愈或好转,但伴有黄疸的患者治疗效果相对较差;出现肝衰竭的DILI是最危重型,预后最差。因此,早发现、早诊断、早治疗及停用一切肝损伤药物是临床治疗DILI的关键[10]。对出现黄疸的患者应给予足够的重视,及时处置,对出现肝衰竭的患者应给予严密的监护,并给予保肝药物及对症支持治疗。
总之,为有效减少DILI的发生,临床上使用可能导致肝损伤的药物时应该注意权衡药物给患者带来的利弊,尽量避免联合使用肝损伤药物,并加强肝功能监测,及早发现和治疗DILI[11]。
[1] Grant LM,Rockey DC.Drug-induced liver injury[J].Curr Opin Gastroenterol,2012,28(3):198-202.
[2] Teschke R,Frenzel C,Wolff A,et al.Drug induced liver injury:accuracy of diagnosis in published reports[J].Ann Hepatol,2014,13(2):248-255.
[3] David S,Hamilton JR.Drug-induced liver injury[J].US Gastroenterol Hepatol Rev,2010,6:73-80.
[4] Evans DC,Watt AP,Nicoll-Griffith DA,et al.Drug-protein adducts:an industry perspective on minimizing the potential for drug bioactivation in drug discovery and development[J].Chem Res Toxicol,2004,17(1):3-16.
[5] 李钦民,韩 真.药物性肝病发病机制的研究进展[J].实用肝脏病杂志,2005,8(2):124-126.
[6] Chalasani N,Fontana RJ,Bonkovsky HL,et al.Causes,clinical features,and outcomes from a prospective study of drug-induced liver injury in the United States[J].Gastroenterology,2008,135(6):1 924-1 934,1 934.e1-4.
[7] 华碧春,卢榜华.中草药的药物性肝损害[J].福建中医学院学报,2000,10(1):30-32.
[8] Giordano CM,Zervos XB.Clinical manifestations and treatment of drug-induced hepatotoxicity[J].Clin Liver Dis,2013,17(4):565-573,Ⅷ.
[9] Cárdenas A,Restrepo JC,Sierra F,et al.Acute hepatitis due to shen-min:a herbal product derived from Polygonum multiflorum[J].J Clin Gastroenterol,2006,40(7):629-632.
[10]Norris W,Paredes AH,Lewis JH.Drug-induced liver injury in 2007[J].Curr Opin Gastroenterol,2008,24(3):287-297.
[11]Chen M,Bisgin H,Tong L,et al.Toward predictive models for drug-induced liver injury in humans:are we there yet?[J].Biomark Med,2014,8(2):201-213.
温祝杜(1983~),男,在读硕士研究生,研究方向:药物性肝损伤、全科医学。
胡国信(1971~),男,博士,主任医师,副教授,研究方向:病毒性肝炎、肝纤维化、药物性肝损伤,E-mail:huguoxin8228@sina.com。
R 994.11
A
0253-4304(2016)04-0574-04
10.11675/j.issn.0253-4304.2016.04.39
2015-11-09
2016-02-10)

