密闭消解-光度法测定乙醇胺羟基铂中的铂含量
沙 娇,杨冬霞,徐 莲,黄 瑶,李 权,赵 力,毕向光,钱海富,赵云昆
(昆明贵研催化剂有限责任公司 贵金属催化技术与应用国家地方联合工程实验室,昆明 650106)
密闭消解-光度法测定乙醇胺羟基铂中的铂含量
沙 娇,杨冬霞,徐 莲,黄 瑶,李 权,赵 力,毕向光,钱海富,赵云昆*
(昆明贵研催化剂有限责任公司 贵金属催化技术与应用国家地方联合工程实验室,昆明 650106)
采用密闭法进行乙醇胺羟基铂的消解,用氯化亚锡光度法进行样品中铂的测定。实验表明,在160℃聚四氟乙烯密闭消解罐中,用12 mL HNO3-3 mL H2O2经6 h可消解3 mL样品;在盐酸介质中,Pt(IV)与SnCl2反应生成稳定的橙黄色络合物,在波长403 nm处进行分光光度法测定,铂量在0~20 mg /L范围内符合朗伯-比尔定律。对乙醇胺羟基铂样品中35.82~42.55 g/L 铂进行测定,相对标准偏差(RSD)和样品加标准回收率分别为0.072%~0.11%和99.3%~102.8%,与电流滴定法和氯铂酸铵重量法的测定结果吻合。
分析化学;乙醇胺羟基铂;铂;消解方法;分光光度法
铂类化合物在化工、医药、电子等领域中具有广泛的应用[1],乙醇胺羟基铂[(HOC2H4NH3)2Pt(OH)6]可作为前驱体,用于多种汽车催化剂的制备,在化工和催化剂行业有着重要的作用。铂是催化剂中的活性成分,准确测定乙醇胺羟基铂中的铂含量对催化剂产品质量的保证和生产工艺的控制具有重要意义。
乙醇胺羟基铂是金属有机化合物,具有很强的稳定性,故其的样品处理成为贵金属分析中费时和困难的一环[2-3]。其常规分解方法需反复加入H2SO4、HClO4,高温发烟破坏有机物,样品处理过程中消耗试剂量大,排放的气体对环境污染较大,且处理过程中随时需要有人照看[4-5]。文献[6]采用HNO3-H2O2密闭消解辛酸铑催化剂,样品分解完全、操作简便、消耗试剂量少和对环境污染小。
测定铂含量的方法较多,如适合于催化剂中微量和低含量铂的分光光度法(UV-Vis)[7]、原子吸收法(AAS)[8]、电感耦合等离子体原子发射光谱法(ICP-AES)[9]等,适合于化合物和合金中常量铂测定的高锰酸钾电流滴定法[10-11]、氯铂酸氨重量法[12]等。但针对组成单一的乙醇胺羟基铂,上述方法过程冗长,手续繁琐。而采用氯化亚锡水相分光光度法操作简便,铂的测定量大,已用于氯铂酸、硅铝载体催化剂中铂的测定[13-14]。
本文采用密闭酸消解法进行乙醇胺羟基铂的消解,以氯化亚锡水相分光光度法测定铂含量,比较了不同分解法对样品的分解影响。
1 实验部分
1.1 仪器和试剂
紫外-可见分光光度计(UV2450型,日本岛津);聚四氟乙烯压力溶样罐(30 mL);电热鼓风干燥箱(GZX-9246MBE型,上海博讯实业有限公司医疗设备厂)。
铂标准溶液(ρPt=100 µg/mL)。盐酸(HCl);硝酸(HNO3);高氯酸(HClO4);过氧化氢(H2O2,30%);氯化亚锡溶液(c(SnCl2)=1 mol/L,3.6 mol/L HCl介质),用时现配;NaCl溶液(ρNaCl=250 g/L)。所用试剂均为分析纯,水为纯水。
实验所用乙醇胺羟基铂为溶液样品,由昆明贵研催化剂有限责任公司提供。
1.2 实验方法
1.2.1 样品的消解
移取 2.00 mL样品于聚四氟乙烯压力溶样罐中,加入12 mL HNO3、3 mL H2O2,旋紧盖子,于160℃烘箱中消解6 h。取出,冷却,拧开盖子,将试液转移到300 mL烧杯中,加2 mL NaCl溶液,低温蒸发至湿盐状,并用盐酸赶除氮氧化物3次。加10 mL HCl,转入100 mL容量瓶中,用水稀释至刻度,混匀。
1.2.2 显色测定
取1.00 mL待测溶液于50 mL容量瓶中,加入12.5 mL HCl,加5 mL SnCl2溶液,用水稀释至刻度,混匀,静置1.5 h。转入10 mm比色皿中,以试剂空白为参比,在403 nm波长处,测定试液吸光度,从工作曲线上查得铂量。
2 结果与讨论
2.1 密闭消解条件的选择
2.1.1 试剂用量的选择
于一定温度、时间条件下,改变HNO3-H2O2的比例(1:1、2:1、3:1、4:1、5:1和1:2、1:3、1:4、1:5),对样品(ρPt=42.38 g/L)进行消解试验。结果表明,12 mL HNO3- 3 mL H2O2(4:1)至少可消解3 mL化合物;当消解温度为160℃、时间为6 h时样品消解完全,测得ρPt=42.35 g/L。选择消解试剂为12 mL HNO3-3 mL H2O2。
2.1.2 消解时间的选择
移取2.00 mL样品于聚四氟乙烯压力罐中,加入12 mL HNO3-3 mLH2O2,旋紧盖子,置于160℃烘箱中,消解4、6、8、12 h。测定结果表明,消解时间>4 h时,有机物消解完全,测得ρPt=42.35 g/L,选择消解时间为6 h。
2.2 密闭消解法与其它分解法的比较
将密闭消解法与其他湿法消解法消解效果进行对比,结果如表1所示。

表1 不同消解方法的比较Tab.1 Comparison of different decomposition methods
由表1可知,采用HNO3-HCl溶解法或HCl-H2O2消解法消解样品,处理样品量小,铂的测定结果明显偏低,且重现性差;采用H2SO4-HClO4溶解法,结果准确且重现性好,但方法处理样品量小,需经高温发烟和反复加入试剂处理,工作气氛差;而HNO3-H2O2密闭消解法处理样品量大,结果准确且重现性好,操作简单,所耗试剂量小,对环境污染小,适合作为乙醇胺羟基铂的消解方法。
2.3 测定Pt的条件
2.3.1 吸收光谱的选择
Pt(IV)-SnCl2为橙黄色络合物,实验所得Pt(IV)-SnCl2和试剂空白的紫外-可见吸收光谱如图1所示。
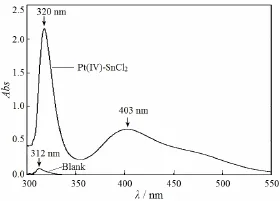
图1 Pt(IV)-SnCl2的紫外-可见吸收光谱Fig.1 UV-Vis absorption spectrometry of Pt(IV)-SnCl2
由图1可见,虽然在320 nm处有最大吸收峰,但此峰受到试剂空白光谱的干扰。为避免空白干扰,选择铂的测定波长为403 nm,表观摩尔吸光系数为4.59×104L·mol-1·cm-1。
2.3.2 盐酸浓度影响
实验表明,盐酸酸度对溶液吸光度有影响。当盐酸浓度为3~4 mol/L,吸光度值最大且稳定,测得样品铂含量为42.35 g/L。选择酸浓度为3~4 mol/L。
2.3.3 氯化亚锡溶液用量的影响
实验表明,显色剂氯化亚锡用量对溶液吸光度有影响。对50 mL试液,当氯化亚锡溶液加入量在4~8 mL时,溶液吸光度最大且恒定,测得样品铂含量为42.35 g/L。选择氯化亚锡溶液加入量为5 mL。
2.3.4 显色放置时间的选择
实验结果表明,Pt(IV)-SnCl2络合物的吸光度随时间延长而增大。加入显色剂氯化亚锡反应1 h后,测得吸光度最大且恒定,测得样品铂含量为 42.35 g/L。选择显色放置时间为1.5 h。
2.3.5 校准曲线
分别移取 0、2.00、4.00、6.00、8.00、10.00 mL铂标准溶液于50 mL容量瓶中,按1.2.2的操作测定标准溶液吸光度,以铂量为横坐标,相应的吸光度值为纵坐标,绘制校准曲线。结果表明,铂量在0~20 mg/L范围内服从比耳定律。
2.3.6 方法准确度实验
准确移取一定量乙醇胺羟基铂样品(ρPt=42.38 g/L),按1.2.1方法进行消解后,定容至100 mL容量瓶中,分取一定体积于50 mL容量瓶中,加入一定量铂标准溶液,按1.2.2进行测定,由表2结果可知,铂的加标回收率为99.3%~102.8%。

表2 加标回收试验Tab.2 Recovery of standard addition
2.4 实际样品分析及方法对比
按照实验方法对乙醇胺羟基铂样品中的铂含量进行测定,并与高锰酸钾电流滴定法、氯铂酸铵重量法结果进行对比,结果列于表3。

表3 样品铂含量分析结果及方法对照Tab.3 Analytical results of Pt content in samples with different methods
由表 3可知,样品分析结果的相对标准偏差 (RSD)≤0.11%,本法与精密电流滴定法和氯铂酸氨重量法测定结果吻合。
3 结论
本文采用密闭法进行乙醇胺羟基铂的消解,用氯化亚锡光度法进行样品中铂的测定。结果表明:
1) 在160℃聚四氟乙烯密闭消解罐中,用12 mL HNO3~3 mL H2O2经6 h可消解3 mL样品。
2) 在盐酸介质中,用氯化亚锡光度法于 403 nm处测定,铂量在0~20 mg /L范围内符合朗伯-比尔定律。
采用本法对乙醇胺羟基铂样品中 35.82~42.55 g/L的铂进行测定,相对标准偏差(RSD)和样品加标准回收率分别为0.072%~0.11%和99.3%~102.8%,与电流滴定法和氯铂酸铵重量法测定结果吻合。密闭消解-光度法测定试剂用量少、环境污染小,操作简便、快速,可满足生产分析的要求。
[1] 董守安. 现代贵金属分析[M]. 北京: 化学工业出版社, 2006: 49-53.
[2] 朱利亚, 胡秋芬, 刘云, 等. 微波消解技术在分析难处理贵金属及其物质中铑、铱、铂、钯的研究与应用[J]. 冶金分析, 2005, 25(5): 11-14. ZHU L Y, HU Q F, LIU Y, et al. Research and application of microwave- assisted digestion technique for analysis of Rh, Ir, Pt, Pd in difficultly decomposed precious metals and their materials[J]. Metallurgical analysis, 2005, 25(5): 11-14.
[3] MA Y H, PENG Y F, ZHU L Y, et al. Sold phase extraction and spectrophotometric determination of gold with 5-(2-hydroxy-4-nitrophenylazo)-rhodanine as chromogenicreagent[J]. South African journal of chemistry, 2005, 58: 116-119.
[4] 朱利亚, 杨光宇, 刘云, 等. 微波消解技术在难处理贵金属(铂)化合物分析中的应用[J]. 分析科学学报, 2005, 21(6): 627-629. ZHU L Y, YANG G Y, LIU Y, et al. Application of microwave-assisted digestion technique for platinum analysis in difficultly decomposed compounds of precious metals[J] Journal of analytical science, 2005, 21(6): 627-629.
[5] 李青. 炭载铂族金属催化剂中铂、钯、铑、钌的化学分析进展[J]. 贵金属, 2015, 36(4): 88-93. LI Q. Advances in chemical analysis of Pt, Pd, Rh and Ru in PGM catalysts supported on carbon[J]. Precious metals, 2015, 36(4): 88-93.
[6] 易秉智, 袁建良. 辛酸铑催化剂的消解及铑含量的测定[J]. 贵金属, 2013, 34(3): 66-68. YI B Z,YUAN J L. The digestion of rhodium octanoate dimer catalyst and determination of Rh[J]. Precious metals, 2013, 34(3): 66-68.
[7] 贵研铂业股份有限公司, 贵研催化剂有限公司. 贵金属催化剂化学分析方法 汽车尾气净化催化剂中铂、钯、铑量测定 分光光度法: GB/T23277-2009[S]. 北京:中国国家标准化管理委员会, 2009.
[8] 单玲, 李俊花, 刘树文, 等. 用原子吸收光谱法测定催化剂中的铂[J]. 石油大学学报, 2004, 28(6): 120-122. SHAN L, LI J H, LIU S W. et al. Determination of platinum in catalyst by atomic absorption spectrometry[J]. Journal of China university of petroleum, 2004, 28(6): 120-122.
[9] 杨红晓, 张林群. ICP-AES法测定活性炭负载型催化剂中铂镍的含量[J]. 应用化工, 2010, 39(11): 1778-1779. YANG H X, ZHANG L Q. Analysis Pt Ni content in active carbon support catalysts by ICP-AES[J]. Applied chemical industry, 2004, 28(6): 120-122.
[10] 贵研铂业股份有限公司. 贵金属合金化学分析方法金、铂、钯合金中铂量的测定 高锰酸钾电流滴定法: GB/T 15072.3-2008[S]. 北京: 中国标准出版社, 2008.
[11] 朱利亚, 陈云江, 赵辉. 微波消解和精密电流滴定法测定铂类化合物中的铂含量[J]. 贵金属, 2007, 28(3): 51-55. ZHU L Y, CHEN Y J, ZHAO H, et al. Determination of platinum content in platinum compounds using microwave digestion and micro electricity titration methos[J]. Precious metals, 2007,28(3): 51-55.
[12] 国家首饰质量监督检验中心. 铂合金首饰 铂钯含量的测定 氯铂酸铵重量法和丁二酮肟重量法: GB/T 19720.3-2005[S]. 北京: 中国标准出版社, 2005.
[13] 王敏, 凌凤香. Pt/SiO2-Al2O3催化剂中铂含量测定的方法[J]. 理化检验-化学分册, 2008, 44(1): 17-19. WANG M, LING F X. Determination of platinum in Pt/SiO2-Al2O3catalyst[J]. Physical testing and chemical analysis part B: chemical analysis, 2008, 44(1): 17-19.
[14] 金珊, 吕娟, 谢莉. 分光光度法测定铂-铼催化剂中铼含量[J]. 分析实验室, 1999, 18(6): 42-45. JIN S, LÜ J, XIE L. Spectrophotometric determination of rhenium in Pt-Re catalysts[J] Analytical laboratory, 1999, 18(6): 42-45.
Determination of the Content of Platinum in Ethanol Amine Hydroxyl Platinum by Sealed Digestion and Spectrophotometry
SHA Jiao, YANG Dongxia, XU Lian, HUANG Yao, LI Quan,
ZHAO Li, BI Xiangguang, QIAN Haifu, ZHAO Yunkun*
(State-Local Joint Engineer Laboratory of Precious Catalytic Technology and Application,
Kunming Sino-Platinum Metals Catalyst Co. Ltd., Kunming 650106, China)
Using the sealed digestion method of ethanolamine hydroxyl platinum, and content of platinum in sample was determined by SnCl2spectrophotometry. The results showed that 3 mL ptoctanoate tlimer sample could be digested completely with 12 mL HNO3and 3 mL H2O2at 160℃ in a PTFE Jar for 6h. In hydrochloric acid medium, Pt(IV)-SnCl2forms a orange stable complex with stannous chloride. The platinum sample was determined by spectrophotometry at the wavelength of 403 nm, the result shows Beer’s Law is obeyed in the range of 0~20 mg/L. The samples of hydroxyl ethanolamine platinum were determined for Pt content from 35.8~42.55 g/L, the relative standard deviations (RSD) and the recoveries of standard addtion are 0.072%~0.11% and 99.3%~102.8%, respectively. The result is coincided with that of the amperometric titration and ammonium chloroplatinate gravimetry.
analytical chemistry; ethanolamin ehydroxyl platinum; platinum; digestion methods; spectrophotometry
O657.32,O652.4
:A
:1004-0676(2016)01-0047-04
2015-06-25
沙 娇,女,工程师,研究方向:贵金属分析研究。E-mail:shajiaoli@163.com
*通讯作者:赵云昆,男,博士,研究员,研究方向:贵金属技术研究。E-mail:yunkunzhao@163.com
——庆祝中国共产党成立一百周年贵金属纪念币展

