19种扩增试剂盒的确证试验
张庆霞,刘小芳,路志勇,王顺霞
(1. 北京市公安司法鉴定中心,北京 100192;2. 北京市昌平区公安司法鉴定中心,北京 102200)
19种扩增试剂盒的确证试验
张庆霞1,刘小芳2,路志勇1,王顺霞1
(1. 北京市公安司法鉴定中心,北京 100192;2. 北京市昌平区公安司法鉴定中心,北京 102200)
目的测试11种国产试剂盒(包含DNATyperTM15、Goldeneye16A、Goldeneye16BT、Goldeneye16C、Goldeneye20A、Goldeneye BASIC、AGCU17+1、AGCU Expressmarker16、AGCU Expressmarker22、AGCU Expressmarker20、STRtyper-21G)和8种进口试剂盒(包含Identifler、ID-Direct、ID-Plus、Sinofler、PowerPlex16、PowerPTheselex16HS、PowerPlex18D、PowerPlex21)的技术性能指标,评估其法医学应用能力,并对各种试剂盒进行分析比较。方法制定测试方案,从方法学、准确性、均衡性、灵敏度、批次间试剂的稳定性、耐受性、适应性与一致性、种属特异性、混合样本、不同反应体系的适应性等10个方面进行测试。结果阳性DNA样本分型正确,内标和等位基因分型标准物符合要求;等位基因间、同一荧光标记基因座间及不同标记物间的均衡性较好;试剂盒使用说明书中推荐的最小DNA模板量的阳性DNA样本均能检出全部STR基因座分型;不同批次间和反复冻融后试剂盒测试可以获得正确分型;对降解检材和混有抑制剂的样本等具有一定的耐受性;能对案件中多种检材进行分型且分型结果一致;各种试剂盒均具有种属特异性和混合DNA样本检测的能力;各种试剂盒在扩增体系为25 μL、10 μL时均可以得到完整的DNA分型。结论所检测试剂盒在上述性能指标等方面已经达到国际同类产品的技术水平,可用于法庭科学的实际检案与建库。
法医物证学;扩增试剂盒;确证试验;短串联重复序列
本检测中心受中国安全技术防范认证中心的委托,承担法庭科学产品自愿性认证检测工作。自2009年6月至今共检测19种扩增试剂盒:为了保证这19种试剂盒的检测质量,确保DNA检测与比对的准确性,北京市公安局测试组参照国际DNA分析方法科学工作组制定的确证指南(Revised Validation Guidelines, 2004)[1],同时依据行业标准《法庭科学人类荧光标记STR复合扩增检测试剂质量基本要求》(GA/T 815-2009),从方法学、准确性、峰值均衡性、灵敏度、批次间试剂的稳定性测试、耐受性、不同检材的适应性与一致性、种属特异性、混合样本[2]、不同反应体系的适应性等10个方面制定了测试方案。现将结果报道如下。
1 材料及方法
1.1 主要仪器及试剂
9700型PCR热循环仪(美国AB公司);3500XL测序仪(美国AB公司);7500定量仪(美国AB公司);19种试剂盒,具体为:公安部物证鉴定中心的DNATyperTM15,北京基点认知技术有限 公 司 的Goldeneye16A、Goldeneye16BT、Goldeneye16C、Goldeneye20A、Goldeneye BASIC,中德美 联AGCU17+1、AGCU Expressmarker16、AGCU Expressmarker22、AGCU Expressmarker20,宁波海尔施基因科技STRtyper-21G,美国AB公司的Identifler、ID-Direct、ID-Plus、Sinofler,Promega公司的 PowerPlex16、PowerPlex16HS、PowerPlex18D、PowerPlex21;Qiagen试剂盒;Chelex-100。
1.2 检测项目与样本
1.2.1 阳性DNA对照样本的制备
9947A(10 ng/μ L,Promega,美国)和9948(10 ng/μL,Promega,美国);阳性DNA对照样本的定量及制备:用AB 7500进行定量检测,使9947A终浓度分别为1.0,0.5,0.25,0.125,0.0625 ng/μ L,分别编号为A1~A5;9948终浓度为1.0 ng/μ L,编号为A6。
1.2.2 准确性检测
取阳性DNA对照样本A1和A6分别用各种试剂盒进行检验并重复1次,判断分型结果与说明书上的描述是否一致。
1.2.3 峰值均衡性检测
分析阳性DNA对照样本的检测结果,等位基因间的峰值均衡性是否大于70 %,同一荧光标记基因座间的均衡性是否大于50 %,不同标记物间的均衡性是否大于30 %。
1.2.4 灵敏度检测
取A1~A5样品各1 μL,分别用各种试剂盒对样品DNA进行检验并重复试验1次。
1.2.5 批次间试剂的稳定性检测
从各种试剂盒(均在保质期内)中分别抽取不同批次(标注不同生产日期和不同批次)的试剂盒进行测试;将各试剂盒中的试剂进行反复冻融1~10次后进行检验,并重复1次。
1.2.6 制备、检测混合样品
将浓度为1.0 ng/μ L的阳性DNA对照样本9947A和 9948按 19∶1、18∶2、16∶4、12∶8、10∶10、8∶12、4∶16、2∶18、1∶19的比例进行混合,依次编为B1~B9号,4 ℃放置备用。
1.2.7 种属特异性检测
猪、牛、马、狗、鸡、鸭、羊、鼠、兔、猫、鱼及大肠杆菌的DNA样品均稀释为1.0 ng/μ L,分别编号为C1~C12,4 ℃放置备用。
1.2.8 不同检材适应性及一致性
取已知分型的血斑、精斑、唾液斑、脱落细胞、肌肉组织、带毛囊的毛发、软骨、牙齿各两份,分别编为D1~D16,分别用《法庭科学DNA实验室检验规范》(GA/T 383-2014)中Chelex-100法和磁珠法提取DNA,用AB 7500定量至1.0 ng/μL,4 ℃放置备用。取其中血斑、精斑、唾液斑、肌肉组织和软骨DNA,分别由不同检测人员,在不同扩增仪和测序仪上进行扩增和电泳,分析结果的一致性。
1.2.9 耐受性检测
降解样本制备:取1.2.1中浓度为1.0 ng/μ L的9947A 17 μ L与1 μ L Alu I DNA内切酶、3 μ L酶切缓冲液、2 μL BSA混合,37 ℃水浴放置60 min,再加1 μL HaeⅢ DNA内切酶,两种酶切缓冲剂各2 μL混合,37 ℃水浴放置60 min[2]。用Qiagen试剂盒纯化,浓缩至2 μ L,编号为E1。
含抑制因素的样品:0.1 %靛蓝1 μ L与1.2.1中浓度为1.0 ng/μ L的9947A样品10 μ L混合,编号为E2;在1.0 ng/μ L的9947A中,分别加入血红素,使其终浓度分别为5、10、20、40 μ mol/L,编号为E3-1、E3-2、E3-3、E3-4。
1.2.10 不同反应体系的适应性检测
将各试剂盒中反应混合液的各组分按照比例缩小,使扩增体系分别为25、10、5 μL体系进行扩增,分析是否可以得到完整的DNA分型。
备注:除ID-Direct、PowerPlex18D两个直扩试剂盒外,其他试剂盒均检测上述每个项目;IDDirect、PowerPlex18D主要检测的项目包括对血液样本的直接扩增,种属特异性、分型准确性、灵敏度、一致性、峰值均衡性、稳定性、批次差等8个方面。
2 结果与讨论
2.1 方法学验证及分型准确性
阳性对照样本9947A和9948进行扩增得到与这19种试剂盒提供的基因分型一致的结果,未出现等位基因丢失的情况,峰值在800~5000相对荧光单位(RFU)之间。
所检测的各种试剂盒的等位基因分型标准物的各等位基因分型与其描述的完全一致,每个等位基因分型的峰高大于200 RFU。经软件分析,等位基因分型标准物和阳性DNA对照样本产生的误差均在0.5个碱基的容差区间内波动,表明所检测的试剂盒均能够准确判定基因分型[3]。
2.2 峰值均衡性检测
对阳性DNA对照样本进行检测,当模板量为试剂推荐的最佳用量时,根据DNA检测分型的峰高,所检测的各种试剂盒杂合等位基因间的均衡性均不小于72.62 %,同一荧光标记基因座间的均衡性均不小于50.65 %,不同标记物间的均衡性均不小于45.46 %。峰值均衡,表明19种试剂盒能够检测出样品的所有等位基因。
2.3 灵敏度测试
根据试剂盒使用说明书中均推荐的DNA模板量范围,对19种试剂盒进行灵敏度测试。在加入阳性DNA对照样本量低至试剂盒推荐的最小DNA模板量时,所检测的19种试剂盒均能检出全部STR基因座分型,能够解决法医实践中微量检材的DNA检验。其中试剂盒Identifler、ID-Plus在阳性DNA对照样本量低至0.0625 ng/μ L时,均能检出全部STR基因座分型,且灵敏度较高。
2.4 批次间试剂的稳定性测试
不同批次的19种试剂盒的重复检验中,结果稳定,无明显差异。19种试剂盒经过10次反复冻融后,检验结果无明显变化,说明该试剂盒可以长期保存,检测结果稳定。
2.5 耐受性检测
除ID-Direct、PowerPlex18D直扩试剂盒未进行该项目的检测外,其他所检测的17种试剂盒对内切酶处理的降解样本有一定的检测能力,对现场检材常见影响PCR的抑制剂如靛蓝和血红素等[2]采用该17种试剂盒进行检测,靛蓝<240 mmol/L、血红素<20 μmol/L均得到清晰的分型结果。说明该17种试剂盒对不同条件下的检材具有一定的耐受性。
2.6 不同检材适应性及一致性检测
采用Chelex-100、磁珠法等方法提取各类案件常见检材D1~D16,用所检测试剂盒进行扩增,得到完整的分型结果,未检见等位基因丢失现象。
不同检验人员在不同检测设备的条件下,对同一样本进行重复性检验,其分型结果一致;对已知分型的同一批样本检验时,19种扩增试剂盒分型结果与已知分型无显著差异。
2.7 种属特异性测试
C1~C12采用上述19种试剂盒检测未发现特异分型,说明所检测试剂盒能够用于种属鉴定,区分人和非人。
2.8 混合样本测试
9947A、9948两者混合比例为19:1、18:2、16:4、12:8、10:10、8:12、4:16、2:18、1:19时, 除ID-Direct、PowerPlex18D等直扩试剂盒未进行该项目的检测外,其他所检测的17种试剂盒均可以准确判断两个DNA样本每个等位基因的分型。
通过两个不同样本不同比例混合检测,说明该17种试剂盒能够对混合样本具有检测能力。
2.9 不同反应体系的适应性
采用各试剂盒推荐的扩增体系进行扩增,分型结果均良好,Identifler、ID-Plus两种试剂盒缩体系至 5μL仍可以得到完整的DNA分型。
3 结论
3.1 基因座数量、名称方面的差异
在本试验中,采用19种试剂盒共检测了除性别基因座外的22个STR基因座(D21S11、D8S1179、D7S820、D3S1358、CSF1PO、D16S539、D13S317、 vWA、D18S51、D5S818、FGA、D2S1338、D19S433、TH01、TPOX、PentaE、 D6S1043、PentaD、D12S391、D1S1656、D2S441、D10S1248等)。另外,Goldeneye16BT试剂盒加入了ABO基因分型引物,可对个体进行ABO血型的基因分型。各试剂盒包含基因座的情况见表1。
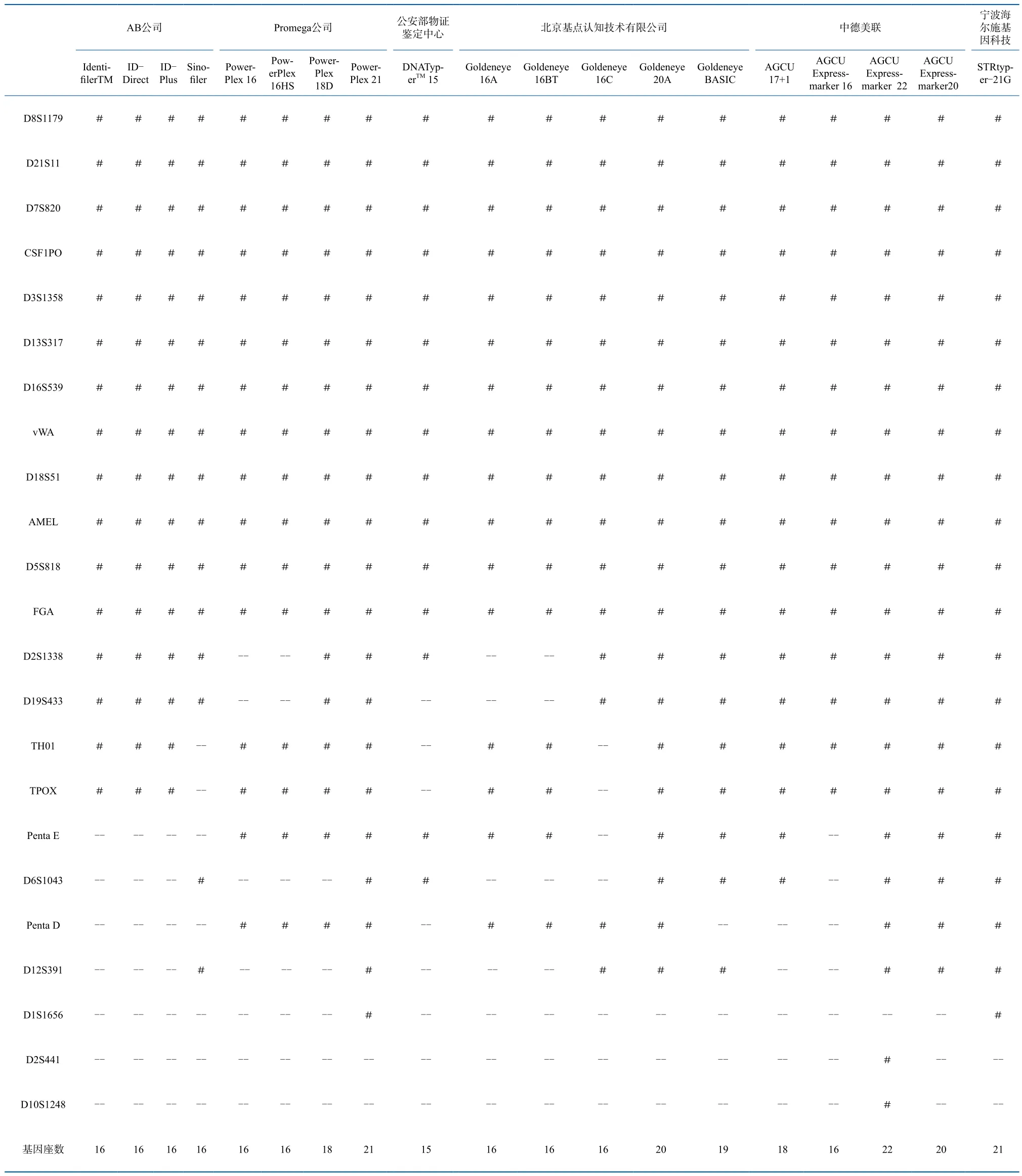
表 1 不同试剂盒基因座统计表Table 1 The STR loci to be tested in the different kits
3.2 可直接扩增试剂盒
可用于直接扩增DNA样本的试剂盒包括:AB公司生产的ID-Direct、ID-Plus;Promega公司生产的 PowerPlex 18D、PowerPlex 21;中德美联公司生产的AGCU 17+1、AGCU Expressmarker 22;北京基点认知技术有限公司生产的Goldeneye 20A。直扩试剂盒可简化检验流程、缩短检验时间,尤其在DNA数据库的样本检验中有较好应用。
3.3 可快速扩增试剂盒
中德美联公司生产的AGCU Expressmarker 16、AGCU Expressmarker 22、Promega公司生产的PowerPlex 18直扩试剂盒,扩增时间短,可80 min完成扩增。
3.4 适用于微量检材、含抑制因素检材的扩增
对降解、含有抑制因素的DNA样本,所检测试剂盒均能保持其相应的稳定性,其中ID-Plus试剂盒对微量或降解检材的扩增效果较佳。
3.5 灵敏度差异
在本次确证试验中,对该19种试剂盒灵敏度进行测试,阳性DNA对照样本量低至0.125 ng时均能检出全部STR基因座分型,其中试剂盒Identifler、ID-Plus在样本量低至0.0625 ng/μ L时,均能检出全部STR基因座分型,且灵敏度较高,能够解决法医实践中微量检材的DNA检验。
通过对4个公司11种国产试剂盒和2个公司8种进口试剂盒的10个方面进行测试,峰值均衡,检验结果稳定,具有较高的检测灵敏度,不同批次的试剂盒分型准确,对不同检材有很好的适应性,对降解、含有抑制因素的DNA样本具有较强的耐受性,能够区分人与非人,并能够对混合样本DNA进行正确分型,对不同反应体系的适应性较好。说明该19种试剂盒在上述性能指标等方面已经达到了GA/T 815-2009的技术要求,可用于法庭科学的检案与建库。
[1] Scientifc Working Group on DNA Analysis Methods (SWGDAM). Revised Validation Guidelines[EB/OL]. (2014-04-21). http://www.fbi.gov/about-us/lab/forensicscience-communications/fsc/july2000/codispre.htm/codis2a.htm.
[2] 王洁,黄艳梅,张庆霞,等. 国产GoldeneyeTM 20A 试剂盒性能指标验证[J]. 中国法医学杂志,2012,27(1):12-15.
[3] 姜成涛,叶健,赵兴春,等. DNATyperTM15试剂盒的确证试验[J]. 中国法医学杂志,2008,23(2):73-76,81
Validation of 19 Kits for PCR Amplifcation
ZHANG Qingxia, LIU Xiaofang, LU Zhiyong, WANG Shunxia
(1. Judicial Identifcation Center of Beijing Public Security Bureau, Beijing, 100192, China; 2. Forensic Science Service of Changping Branch of Beijing Public Security Bureau, 102200, China)
ObjectiveThe performance of 11 homemade PCR amplification kits (DNATyperTM15, Goldeneye16A, Goldeneye16BT, Goldeneye16C, Goldeneye20A, Goldeneye BASIC, AGCU17+1, AGCU Expressmarker16, AGCU Expressmarker22, AGCU Expressmarker20, STRtyper-21G) was to test and their forensic applicability evaluated together with the 8 foreign counterparts (Identifiler, ID-Direct, ID-Plus, Sinofiler, PowerPlex16, PowerPlex16HS, PowerPlex18D, PowerPlex21) in this paper.MethodsValidation protocols were designed to comply with the guidelines issued by the Scientifc Working Group on DNA AnalysisMethods(SWGDM). The evaluation of the 19 kits for PCR amplifcation was carried out in terms of genotyping method, precision and accuracy, peak height balance, sensitivity, stability, survivability, adaptability and consistency for various samples, species specifcity, mixed samples, and the suitability into different reaction systems.ResultsThe DNA genotyping results from all the 19 kits were accurate with the positive control sample while the requirements were met by their internal standard and ladder. The 19 kits for PCR amplifcation were able to be amplifed successfully and to genotype clearly and efficiently, meanwhile there was no peak height imbalances leveling at high sensitivity obtained. Genotyping results were correct among different batches of the same kits even subjected to repeated freezing/melting. The 19kits were also capable of being used in some degraded and/or inhibitory DNA samples, and well performed with revealing the consistent genotypes for the DNA from various sources. These kits were highly specifc for human DNA and able to genotype for mixed samples. For different amplifying reaction setting-ups, the 19 kits were capable of getting the consistent genotypes.ConclusionAll the 19 kits for PCR amplifcation are suitable for both the routine casework and DNA database construction in forensic practice.
forensic biological evidence; PCR amplifcation kits; validation test; short tandem repeat (STR)
DF795.2
B
1008-3650(2016)06-0507-05
2015-11-30
格式:张庆霞,刘小芳,路志勇,等. 19种扩增试剂盒的确证试验[J]. 刑事技术,2016,41(6):507-511.
10.16467/j.1008-3650.2016.06.019
张庆霞(1978—),女,河南淮阳人,硕士,副主任法医师,研究方向为法医遗传学。E-mail: qingxiazhang@sina.com

