利用兽药典方法对青霉素钾工业盐和原料药的检测比较
徐嫄,于丽娜,韩宁宁,龚旭昊,王静文,郝利华,赵晖
(中国兽医药品监察所,北京100081)
利用兽药典方法对青霉素钾工业盐和原料药的检测比较
徐嫄,于丽娜,韩宁宁,龚旭昊,王静文,郝利华,赵晖*
(中国兽医药品监察所,北京100081)
为了辨别青霉素钾工业盐和青霉素钾原料药,依据《中国兽药典》中青霉素钾的质量标准,对四家青霉素原料药生产企业提供的4批青霉素钾工业盐和4批青霉素钾原料药进行了检测,项目包括性状、鉴别、吸光度、结晶性、溶液澄清度与颜色、青霉素聚合物、干燥失重、不溶性微粒、酸碱度、有关物质、细菌内毒素、可见异物、无菌和含量测定。结果表明,8批样品均符合现行兽药典青霉素钾标准中各项规定,但结果无法用以区分青霉素钾工业盐和青霉素钾原料药,提示青霉素钾的质量标准需进一步完善,以提高对成品药——注射用青霉素钾的质量控制。
青霉素钾;工业盐;原料药;中国兽药典
青霉素是β-内酰胺类抗生素,被广泛应用于畜禽细菌感染疾病的防治。青霉素工业盐是青霉素和各种半合成抗生素药品生产过程中的药用中间体。青霉素的生产需要经过多次萃取、过滤、结晶、脱色、洗涤和干燥等复杂的工艺过程,最终由青霉素工业盐得到青霉素钾原料药,无菌分装后得到符合国家药典标准的产品[1-2]。由此可知,生产过程中药用中间体及原料药的质量控制对成品药的质量至关重要。
国内兽药市场中曾有直接利用青霉素工业盐代替青霉素原料药分装成注射用青霉素产品的违法现象,并且产品质量参差不齐[3-4]。本实验以《中国兽药典》(2010年版)[5]为依据,对四家青霉素原料药生产企业提供的青霉素钾原料药和青霉素钾工业盐进行比较,以期对两者进行辨别,为兽医行政管理部门执法检查打击制售假劣兽药的非法行为提供技术依据。
1 材料与方法
1.1 标准品与样品 青霉素对照品,含量93.1%,中国食品药品检定研究院(130437-201306);青霉素系统适用性对照品,中国食品药品检定研究院(130606-201202)。青霉素钾原料药:企业A(批号:1021301009),企业B(批号:20081202033),企业C(批号:101211004),企业D(批号:120421)。青霉素钾工业盐:企业A(批号:1205139-3),企业B(批号:280113012096),企业C(批号:231301215),企业D(批号:1221305141)。
1.2 主要仪器及试剂 Waters 2695高效液相色谱仪,2487紫外检测器,Waters公司;AX205分析天平,梅特勒公司;Milli Q超纯水仪,美国Millipore公司;TU-1901紫外可见分光光度计,北京普析通用仪器有限公司;FT-IR550傅立叶变换红外光谱仪,美国NICOLET公司;MET-50智能恒温加热仪,天大天发科技公司;CX41RF显微镜,OLYMPUS;CS101-2电热鼓风干燥箱,重庆四达公司;SPX-250B-Z生化培养箱,上海博迅实业公司;GWF-8JA微粒分析仪,天津天河分析仪器公司;HTY-601集菌仪,集菌培养器,杭州泰林生物技术设备公司;YB-2型澄明度检测仪,天津大学精密仪器厂。甲醇(Merck公司,色谱纯);磷酸二氢钾,冰醋酸(国药集团,分析纯);液状石蜡(国药集团,化学纯);青霉素酶,细菌内毒素工作标准品,鲎试剂,细菌内毒素检查用水(中国食品药品检定研究院)。
1.3 方法 依据《中国兽药典》(2010年版)中青霉素钾质量标准,对8批样品进行检测。
2 结果
2.1 性状 8批样品均为白色结晶性粉末,符合兽药典规定。实验中发现,在白炽灯下肉眼可见企业A和D生产的青霉素钾原料药和工业盐均为细腻的结晶性粉末,但原料药的亮度比工业盐更高。企业B和C的工业盐和原料药颜色基本一致,但工业盐中的大颗粒更多。2.2 鉴别 依兽药典鉴别项下(1)和(2)两个检验项目对8批样品的检测结果表明:(1)8批样品在含量测定项下记录的色谱图中,主峰的保留时间均与对照品溶液主峰的保留时间一致;(2)8批样品的红外吸收测定结果均符合兽药典规定。
2.3 检查 对8批样品进行吸光度、结晶性、溶液澄清度与颜色、青霉素聚合物、干燥失重、不溶性微粒、酸碱度、有关物质、细菌内毒素、可见异物与无菌共10个项目的检测,均符合兽药典规定,且无明显差异。具体结果如下:2.3.1 青霉素聚合物、干燥失重、不溶性微粒、酸碱度、有关物质检测 结果均符合标准规定,见表1。其中,青霉素聚合物的测定结果均在限度范围内,但同一企业工业盐的数值均高于原料药。不溶性微粒检测结果显示,企业A、B和C的工业盐中10 μm及10 μm以上微粒数含量均高于原料药。

表1 青霉素聚合物、干燥失重、不溶性微粒、酸碱度、有关物质检测结果
2.3.2 吸光度测定 在280~325 nm的波长处测定吸光度,吸光度均不大于0.10,在264 nm的波长处均有最大吸收,4批工业盐测定值均大于4批原料药,但吸光度值均在0.8~0.88规定范围内(表2),以企业A提供样品为例,其紫外吸收结果见图1。2.3.3 结晶性检查 采用偏光显微镜法,实验中称取适量样品,分别加1mL液状石蜡使晶粒浸没其中,由于晶体具有光学各向异性,在偏光显微镜下观察呈现双折射和消光位的晶体光学性质。通过显微镜放大观察,四家企业的工业盐中长度在200 μm以上的晶体颗粒均多于原料药。结果见图2。

表2 吸光度测定264 nm处最大吸收值

图1 企业A样品的紫外吸光度测定
2.4 含量测定 标准规定青霉素钾含量按干燥品计算,不得少于96.0%。利用高效液相色谱法测定
8批供试品含量,经计算含量均符合规定,结果见表3。

图2 结晶性检查结果
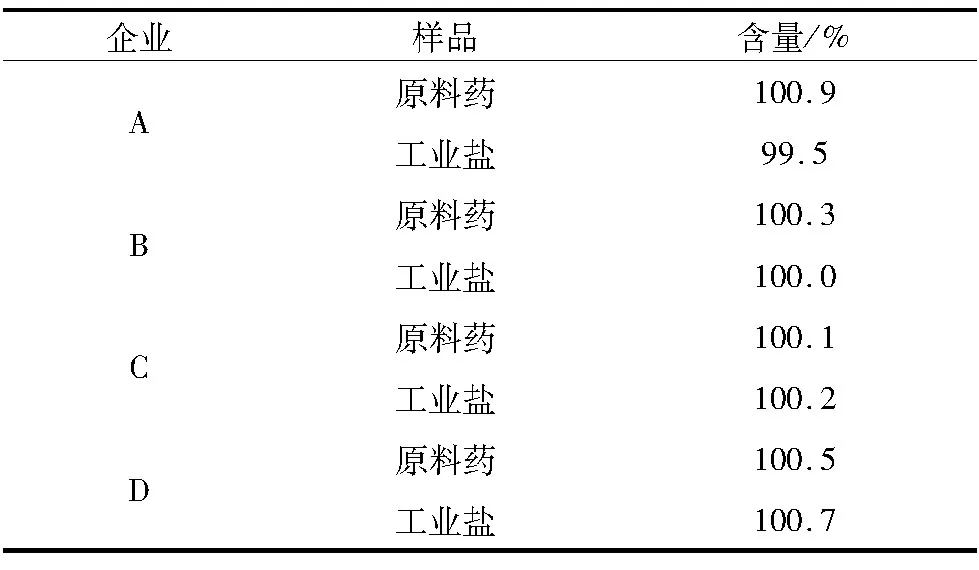
企业样品含量/%A原料药100.9工业盐99.5B原料药100.3工业盐100.0C原料药100.1工业盐100.2D原料药100.5工业盐100.7
3 讨论
依据《中国兽药典》(2010年版)中青霉素钾的质量标准对四家青霉素原料药生产企业提供的青霉素钾工业盐和青霉素钾原料药进行检测,结果均符合规定;但检测结果无法用以区分青霉素钾工业盐和青霉素钾原料药。钱志平[3]在1995年曾指出青霉素工业盐的性状、杂质含量、无菌、澄明度等控制项目无法达到药用青霉素标准。但是,随着生产技术水平的提高,青霉素聚合物、含量、有关物质、无菌、细菌内毒素等质量控制关键项目,依照现有标准和限度已无法对青霉素钾工业盐和原料药加以区分。
工业盐作为药用中间体,不同企业在生产中,质量控制标准可能略有差异。在青霉素生产过程中,脱色和洗涤等工艺可以提高产品透明度、降低杂质含量,且脱色中活性炭的粒度大小和滤速控制均会对产品外观性质产生影响[6]。本实验的上述发现说明青霉素钾工业盐和原料药在性状、颗粒大小、不溶性微粒、聚合物及吸光度等方面存在差异,但由于样品数量有限、企业之间生产工艺及不同批次产品之间可能存在不同,需要检测更多样品才能核实、确认两者的“差异点”;另外,可根据药物的性质和生产工艺特点,寻找其他方法对两者进行鉴别。张秀英等[7]曾利用色差计对注射用青霉素溶液进行比较;曹艳玲[8]和杨井兰[9]等应用气相色谱法分别测定了青霉素钾和青霉素钠中正丁醇、乙酸乙酯和乙酸丁酯等残留溶媒;刘广桢等[10]应用X射线衍射分析方法对注射用青霉素钠进行分析鉴别。因此,为保证成品药的质量安全,建议对现行控制标准和限度进行修订或制定新的控制项目,以区分青霉素钾工业盐和原料药。
[1] 吴国员,查舜行. 青霉素生产概述[J]. 上海医药情报研究,1997,45(2):26-33.
[2] 张翼飞. 青霉素提炼新工艺在青霉素G生产过程中的应用[J]. 科技视界,2010,8,37-38.
[3] 钱志平. 浅谈青霉素工业盐的辨别[J]. 中国兽药杂志,1995,29(1):37-38.
[4] 侯及波,包温奎. 兽医注射用青霉素钾质量检测[J]. 青海畜牧兽医杂志,2001,31(3):25.
[5] 中国兽药典委员会. 中华人民共和国兽药典[S]. 二〇一〇年版. 北京:中国农业出版社,2011:121-122.
[6] 赵素霞,刘建辉,纪爱民,等.青霉素生产中活性炭粒度与滤速的关系探讨[J]. 河北化工,2011,34(6):25-28.
[7] 张秀英,陆连寿. 色差计在注射用青霉素溶液颜色判定中的应用[J]. 中国兽药杂志,2010,44(2):29-30.
[8] 曹艳玲,刘学良. 顶空气象色谱法测定注射用青霉素钠中残留溶媒[J]. 黑龙江医药,2007,20(4):302-303.
[9] 杨井兰,李新华. 气相色谱法测定青霉素钾盐残留溶媒[J]. 黑龙江医药,2005,18(2):34-35.
[10]刘广桢,胡文红,杨娜. 注射用青霉素钠的X射线衍射分析[J]. 中国现代应用药学,2011,28(1):76-78.
(编辑:李文平)
Tests Comparing of Benzylpenicillin Potassium Industry Salt and Benzylpenicillin Potassium Active Pharmaceutical Ingredient by Methods in Chinese Veterinary Pharmacopoeia
XU Yuan,YU Li-na,HAN Ning-ning,GONG Xu-hao,WANG Jing-wen,HAO Li-hua,ZHAO Hui*
(ChinaInstituteofVeterinaryDrugControl,Beijing100081,China)
In order to distinguish between benzylpenicillin potassium industry salt and benzylpenicillin potassium active pharmaceutical ingredient, 4 bathes of industry salt samples and 4 bathes of active pharmaceutical ingredient samples offered by 4 different veterinary drug manufacturers respectively were identified according to quality standards in Chinese Veterinary Pharmacopoeia 2010 version. Results of those 8 batches of samples were all in compliance with the standards, however, finding no distinguish differences between industry salt and active pharmaceutical ingredient, which might indicate that quality standard of benzylpenicillin potassium need to be improved in order to enhance quality control of the finished drug-benzylpeninicillin potassium for injection.
benzylpenicillin potassium;industry salt;active pharmaceutical ingredient;Chinese Veterinary Pharmacopoeia
徐嫄,硕士,从事抗生素检验及检测方面工作。
2015-11-14
A
1002-1280 (2016) 01-0056-05
S859.79

