生物反馈治疗卒中后焦虑抑郁状态伴失眠的研究
杜晓霞,徐舒,宋鲁平
卒中后睡眠障碍(post-stroke sleep disorders,PSSD)发病率高。不同国家不同研究的报道中,其发病率在44%~95%[1-4]。卒中后睡眠障碍的类型包括失眠、睡眠增多、睡眠结构紊乱、异态睡眠、鼾症等[5-6]。卒中后焦虑和抑郁是卒中常见的并发症之一[7]。卒中所致的认知功能障碍、焦虑和抑郁还可能诱发和加重失眠。
失眠导致患者康复训练时注意力不集中,主动配合性差,延缓患者的康复,影响预后[8]。目前,失眠治疗主要有药物治疗和非药物治疗(包括心理行为治疗、物理因子治疗等)[9]。多导睡眠监测(polysomnography,PSG)排除阻塞性睡眠呼吸暂停(obstructive sleep apnea,OSA)后,失眠的治疗重点是良好的睡眠卫生习惯,并使用认知行为技术,包括睡眠限制、刺激控制和渐进式放松疗法等[10]。本项研究拟观察生物反馈疗法治疗卒中后焦虑抑郁状态伴失眠的有效性。
1 对象与方法
1.1 研究对象 2015年4月-2016年2月中国康复研究中心北京博爱医院康复科治疗的成年卒中患者。入组标准:①年龄≥18岁;②脑出血和脑梗死,病程在1个月以上,符合全国第4届脑血管病学术会议制定的脑血管病诊断标准[11];③符合焦虑、抑郁及失眠的诊断标准;④患者的焦虑、抑郁情绪及失眠状态出现在卒中后;⑤意识清楚、查体合作,患者及家属签署知情同意书。
排除标准:①短暂性脑缺血发作;②卒中前有睡眠障碍及抑郁等精神疾病史;③智力障碍及明显失语者;④重症患者无法配合康复治疗者。
焦虑、抑郁诊断参考《美国精神障碍诊断统计手册》(第四版)标准[12]:汉密尔顿焦虑量表(Hamilton Anxiety Scale,HAMA)≥7分:可能有焦虑,≥14分:肯定有焦虑(轻度),≥21分:肯定有明显焦虑(中度),≥29分严重焦虑(重度)。汉密尔顿抑郁量表(Hamilton Depression Scale,HAMD)(21项)≥7分:轻度抑郁,≥17分:中度抑郁,≥24分:重度抑郁。
卒中后抑郁和焦虑的诊断另外需要符合以下条件:①患者有卒中病史及卒中后相应的神经功能缺损;②抑郁和焦虑的出现和卒中的发生有明显的关系,通常在卒中后数天就可出现;③非短暂性,通常要持续2周以上;④抑郁和焦虑影响了患者的社会功能,尤其影响了患者积极参与神经功能的恢复;⑤除外其他原因导致的抑郁,如兴奋药物过量、催眠镇静药物或抗焦虑药物的戒断反应。
失眠诊断参考《中国精神障碍分类与诊断标准(第3版)》中继发性失眠症的诊断标准[13]和《中国成人失眠诊断与治疗指南》标准[14]。失眠发生在卒中后,卒中后出现睡眠数量的减少和睡眠质量的下降,总睡眠时间小于6 h和日间功能障碍。
以上心理量表的评估由心理科医师完成。
1.2 研究方法 评估后纳入符合入组条件的卒中后焦虑抑郁伴失眠患者32例,所有纳入研究的患者均给予生物反馈治疗。全部患者常规治疗原发病并进行康复训练。
生物反馈治疗仪器采用中科心桥(北京)心理医学研究院心率变异性(heart rate variability,HRV)检测及训练系统,给予每周5次,每次30 min的催眠钟摆、荷花、心灵家园进行放松、缓解情绪康复训练。催眠钟摆是通过脑部计算机接口(brain computer interface,BCI)技术将人的脑电波信号转换为数字信号,传送给电脑系统,电脑编制一个摆动的钟摆的画面。当人的大脑放松、思维抑制时钟摆的摆动就会变慢,反之钟摆变快。患者通过形象地控制钟摆的摆动速度来控制大脑,从而有利于入睡。荷花和心灵家园的训练是采用中科心桥(北京)心理医学研究院提供的“最佳心理状态检测与训练系统”,用于检测与训练自主神经系统的功能。当患者的自主神经平衡时电脑画面的荷花就会逐渐长大并盛开,心灵家园会逐步建立起来。相反,当患者交感神经或副交感神经过度活跃时,荷花就会慢慢变小,心灵家园也会慢慢拆除。患者通过控制画面的呈现以及治疗师的训练提示,不断变化自己的状态,逐步找到自主神经平衡的调节方法。生物反馈训练时间定于晚餐后进行。
全部患者在治疗前及治疗后4周采用HAMA和HAMD进行焦虑抑郁测评,匹兹堡睡眠质量指数量表(Pittsburgh Sleep Quality Index,PSQI)和患者健康问卷-9(Patient Health Questionnaire 9,PHQ-9)在治疗前后进行分析评定,同时统计患者每夜实际睡眠时间治疗前后的变化,生物反馈治疗前和治疗4周后简易精神状态检查表(Mini-mental State Examination,MMSE)、Fugle-Meyer肢体功能评分(Fugle-Meyer Scale,FMS)、美国国立卫生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)、Barthel指数(Barthel Index,BI)变化。
2 结果
2.1 一般资料 研究共纳入32例患者,研究过程中,1例患者因为注意力不集中退出训练,另外1例患者因为出现症状性癫痫退出训练。完成训练和治疗的30例患者中男性26例,女性4例,脑出血患者14例,脑梗死患者16例,年龄34~75岁,平均(49.33±11.09)岁。
2.2 治疗后HAMA、HAMD和睡眠时间变化治疗后患者睡眠时间较治疗前显著增加[(4.81±1.58)hvs(7.30±1.34)h,P<0.001]。HAMA[(17.50±8.41)vs(9.00±7.01)]和HAMD[(19.53±7.82)vs(9.23±4.42)] 评分均有显著改善(均P<0.001)。
2.3 治疗后PSQI和PHQ-9变化 患者经过生物反馈治疗后较治疗前PSQI[7(5.5,11)vs18(15,23)]和PHQ9[10(9,14)vs18(14.5,27)]评分无显著差异。
2.4 训练后MMSE、FMS、NIHSS及BI的变化患者训练后其MMSE、FMS及BI的评分没有显著变化,但NIHSS评分显著降低(表1)。
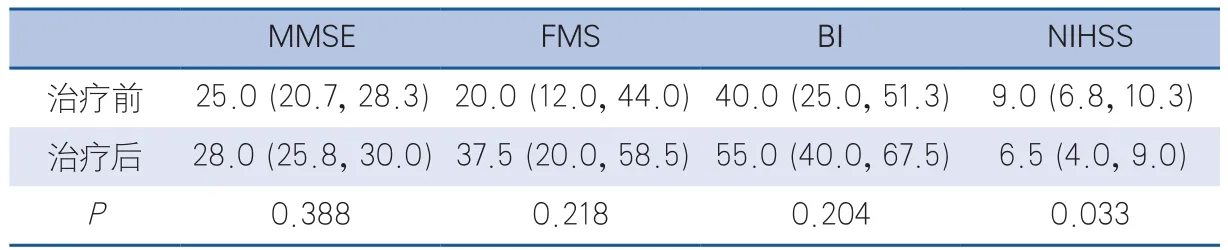
表1 生物反馈训练后患者认知功能、运动功能及生活自理能力变化
3 讨论
生物反馈又称自主神经学习法,是在行为疗法的基础上发展起来的一种心理治疗技术,被认为是继医学传统治疗、药物和物理治疗之外的一种新的治疗和预防疾病的方法,是操作性条件反射的范例。通过反馈的图像及音乐信号自我调节,并转化为易于患者掌握和调控的信号,患者可以通过信号反馈提供的信息,调节呼吸节律,降低自主神经的兴奋性[15-16]。目前,生物反馈技术用于临床相对较少[17]。我们的研究发现入组的30例患者治疗前后HAMA、HAMD、夜间睡眠时间评分情况均有改善,差异有显著性,说明随着生物反馈治疗可以改善卒中患者的焦虑抑郁情绪,而且随着焦虑抑郁情绪的改善,睡眠时间也有增加。本研究中训练4周前后患者的PSQI和PHQ-9均有改善,虽无统计学意义,但能看到功能改善的趋势。康复治疗4周后虽然MMSE评分、FMS分数和BI指数的改善没有达到统计学意义,但标记卒中严重性的NIHSS评分显著降低,表明生物反馈治疗有利于神经功能的恢复。
卒中后睡眠障碍有不同表现,本研究的入选病例均为失眠伴焦虑抑郁患者,需要与其他原因引起的卒中后睡眠障碍患者鉴别[18]。常见的呼吸相关性睡眠障碍,如睡眠呼吸暂停并不适合生物反馈训练。相对于其他治疗,生物反馈治疗要求患者有一定的认知能力,能够集中精力配合训练,故本研究所选入组患者认知功能障碍相对较轻。
卒中后患者多要经历震惊期、否认期、抑郁期、反对独立期、适应期等心理康复过程。康复需要患者主动参与以取得更好的效果,卒中后焦虑抑郁和失眠严重影响患者的康复速度。生物反馈技术用于治疗失眠已有数十年[19],能避免使用镇静催眠药物导致的不良反应和成瘾倾向,消除患者的心理负担,对于卒中后失眠患者,如能配合训练,能够改善情绪和睡眠[20]。在临床中可以扩大应用病例数并推广至其他脑损伤患者的失眠康复治疗中,但要注意分析患者睡眠障碍的类型和患者认知功能的筛查。
本研究存在不足之处,由于入组条件的限制,病例来源可能存在偏倚;研究样本量偏少,由于样本量的关系,没有分层比较轻中重度焦虑抑郁患者对生物反馈治疗的疗效差异,在以后的研究中会进一步改善。
1 Marquez-Romero JM,Morales-Ramirez M,Arauz A.Non-breathing-related sleep disorders following stroke[J].Neurologia,2014,29:511-516.
2 王娇,梅丽,孟会红,等.脑卒中后睡眠障碍的临床相关因素研究[J].脑与神经疾病杂志,2013,4:281-285.
3 孟会红,梅风君.多导睡眠图对卒中后睡眠障碍的评价意义[J].现代电生理学杂志,2012,4:226-230.
4 Wallace DM,Ramos AR,Rundek T.Sleep disorders and stroke[J].Int J Stroke,2012,7:231-242.
5 白莹,张宁,王春雪.卒中后睡眠障碍研究进展[J].中国卒中杂志,2013,8:407-411.
6 Pasic Z,Smajlovic D,Dostovic Z,et al.Incidence and types of sleep disorders in patients with stroke[J].Med Arh,2011,65:225-227.
7 王伊龙,张宁,张彤,等.神经内科患者伴发抑郁状况与用药情况的横断面调查[J].中国卒中杂志,2010,4:798-800.
8 Wang L,Tao Y,Chen Y,et al.Association of post stroke depression with social factors,insomnia,and neurological status in Chinese elderly population[J].Neurol Sci,2016,37:1305-1310.
9 刘珂,屈云.失眠的物理因子治疗[J].华西医学,2010,11:2121-2123.
10 Im K B,Strader S,Dyken ME.Management of sleep disorders in stroke[J].Curr Treat Options Neurol,2010,12:379-395.
11 中华神经科学会.各类脑血管病诊断要点[J].中华神经科杂志,1996,29:379-380.
12 刘新民,伍汉文.临床急症[M].沈阳:辽宁科学技术出版社,2006:163-165.
13 中华医学会精神科分会.CCMD-3中国精神障碍分类与诊断标准[M].3版.济南:山东科学技术出版社,2001:118-122.
14 张鹏,赵忠新.《中国成人失眠诊断与治疗指南》解读[J].中国现代神经疾病杂志,2013,5:363-367.
15 姜乾金.医学心理学[M].北京:人民卫生出版社,2002:146-148.
16 郑延平.生物反馈的临床实践[M].北京:高等教育出版社,2003:111.
17 陆雪松,姜亚军,顾迅,等.肌电生物反馈治疗脑卒中患者的临床研究[J].中华物理医学与康复杂志,2003,7:56-57.
18 Ferre A,Ribo M,Rodriguez-Luna D,et al.Strokes and their relationship with sleep and sleep disorders[J].Neurologia,2013,28:103-118.
19 Cortoos A,Verstraeten E,Cluydts R.Neurophysiological aspects of primary insomnia:implications for its treatment[J].Sleep Med Rev,2006,10:255-266.
20 李鸥,冯晓梅,郭知学.生物反馈治疗卒中后失眠症的临床研究[J].现代中西医结合杂志,2012,17:1870-1871.

