高考电化学试题的命题解读和教学策略浅析
张晋

摘要:基于高中生电化学认识模型,解读了高考电化学试题特点,并分析其命题趋向,提出“建立解决高考电化学试题的系统的审题、解题模式”、“利用真实情景讨论知识”、“加强问题驱动、任务解决的复习课教学”的教学策略,以期帮助学生优化知识结构,形成解决电化学问题的系统思维,从而提高学生解决化学实际问题的能力。
关键词:电化学试题;命题解读;教学策略;中学化学教学
文章编号:1005-6629(2016)1-0081-07 中图分类号:G633.8 文献标识码:B
1.问题的提出
追求能力和综合素质的提高是当今高考改革的趋势。早在1999年,教育部就在《关于进一步深化普通高等学校招生考试制度改革的意见》中指出,“高考试题命制要从知识立意向能力立意转换,考查学生的基础知识和创新能力”。随后在2001年开始了以全面提高学生科学素养为核心的新课程改革。2009年,《国家中长期教育改革和发展规划纲要(2010-2020)》中提出“德育为先、能力为重、全面发展”的教育改革发展战略,并指出要“深化考试内容和形式改革,着重考查综合素质和能力”。可见注重学生综合能力的培养,一直是我国基础教育改革与发展的重要目标。
高考试题的命题思路与新课程的教学理念正好吻合、统一,是培养学生解决化学实际问题能力的极好切入点。基于此,教师应该怎样解读和分析高考电化学真题,才能充分利用此习题资源,以加深学生对电化学知识的理解,提高学生解决化学实际问题的能力呢?
1.1解析高考电化学试题的已有研究
对高考电化学试题解析方式的已有研究多以高考大纲为背景,以高考试题为典型例题进行解析,基本形式是:高考电化学知识考点归纳-典型高考电化学真题-分析解题思路。其中,柴勇通过对电化学基础知识进行梳理,以及电化学热点问题的分析提出了高考命题趋向与应试策略;柴勇还对高考电化学试题进行了分类总结。薄晓军对高考命题进行了分析,对重点知识进行了梳理并对高考热点题型进行了例析。这种分析方式虽有利于学生把握高考的考点,但忽略了对学生解决实际问题能力发展的需要,缺少对学生系统分析电化学类试题能力的培养,具体表现在学生面对简单的任务类型时尚且能自主解决,但是面对高考试题中综合复杂的任务类型时,学生解题思路不系统,导致题海战术成为学生提高应试能力的主要路径之一。因此,需要能真正体现电化学学科本体知识以及发展学生学科能力的新的解题方式。
1.2电化学教学的已有研究
文献中已报道的电化学认识模型不仅体现了电化学问题的知识结构,还揭示了学科教学的内涵。其中,王磊等对其进行了系列研究,蒋涛在其硕士论文中对原电池的教学进行了自上而下的系统研究,通过对不同学段教材中与原电池相关的内容进行梳理,建立了原电池认知结构,同时根据布鲁姆的教育目标分类理论,从理解、分析、应用三个维度对原电池教学内容进行了能力水平划允进而将认识角度与能力水平组合,提出了原电池的认识发展层级模型。王维臻等从电化学的本体维度、认识维度和问题维度出发,构建并提出了高中阶段的电化学认识模型,并在高三原电池复习教学中进行应用的基础上,分析和概括了基于电化学认识模型建构的原电池复习教学有效策略。丁晓新借鉴蒋涛的基于电化学学科本体知识的研究成果进行了研究,同时在其硕士论文中进一步发展和完善了王维臻等建构的电化学认识模型,并在高一“化学能与电能”的新授课教学中进行应用的基础上,提出了促进学生认识发展的教学策略。
1.3本研究的目的和任务
综上所述,电化学认识模型在新授课和复习课教学研究中起到了很好的教学效果,但还未涉及如何利用高考试题作为教学资源以培养学生能力的研究。基于此,确定了本研究的主要任务:(1)基于“高中生电化学认识模型”解读电化学高考试题特点,并就近几年高考电化学试题分析其命题趋向。(2)提出电化学教学策略,以期帮助学生优化知识结构,形成解决电化学问题的系统思维,提高学生解决化学实际问题的能力。
2.基于“高中生电化学认识模型”,解读和分析高考电化学试题
2.1对“高中生电化学认识模型”的理解
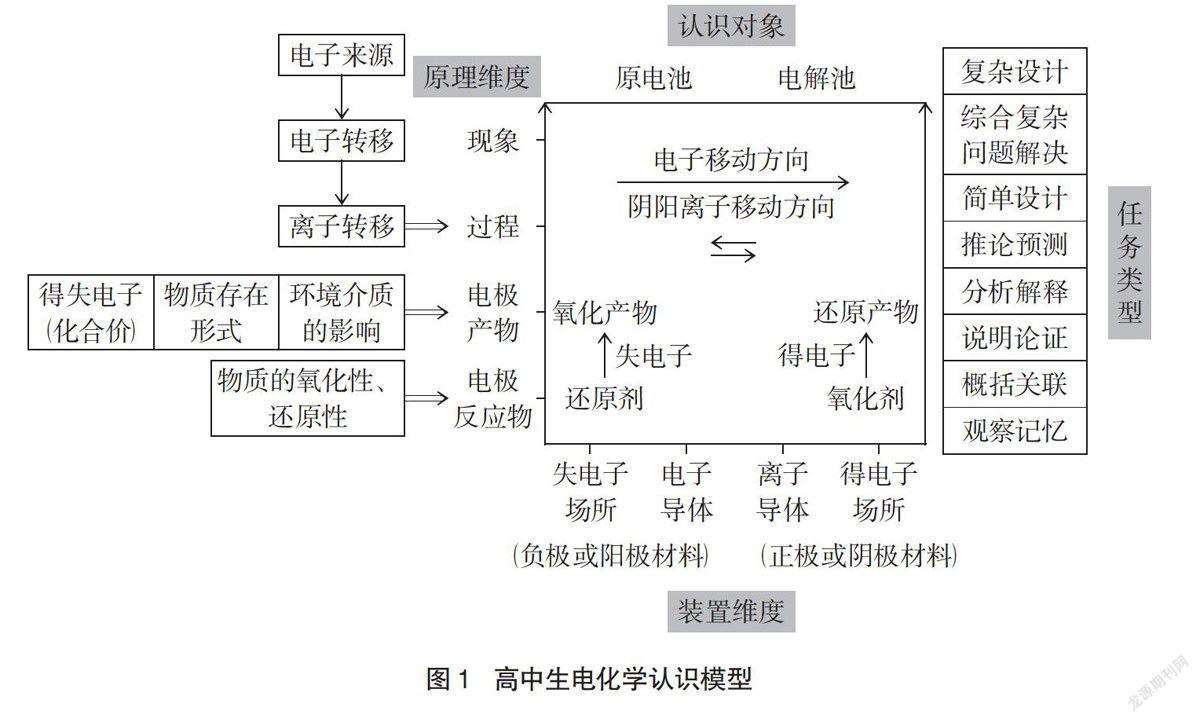
王磊、丁晓新等建构的“高中生电化学认识模型”如图1所示。共由4个维度组成,其中认识对象维度包括原电池和电解池,其共同点在于2大核心要素:电势差和闭合回路,其不同点在于能量的转化方向不同。装置维度包括原电池或电解池里面的所有装置要素,即失电子场所(负极材料或阳极材料)、电子导体(导线)、离子导体(电解质溶液或盐桥、膜等)、得电子场所(正极材料或阴极材料);原理维度以氧化还原反应为基础,包括电极反应物、电极产物、工作过程、反应现象;任务类型维度包括观察记忆、概括关联、说明论证、分析解释、推论预测、简单设计、综合复杂问题解决、复杂设计8类。丁晓新还依据“高中生电化学认识模型”提取出原电池4个核心认识角度,包括电极反应物、电极材料、离子导体、电子导体。
从结构上看,“高中生电化学认识模型”纵向满足电化学认识层级模型,横向满足学科本体知识的需求,并且增加了认识对象、认识路径以及认识能力对应的任务类型的关系。从功能上看,高中生电化学认识模型不仅体现了电化学知识结构即各个角度之间存在的动态推理关系,而且体现了对学生能力的要求。因此,高中生电化学认识模型为解读和分析高考电化学试题提供了一定的理论依据。
2.2基于“高中生电化学认识模型”,解读高考电化学试题特点
基于“高中生电化学认识模型”对高考试题的解读,不难发现电化学作为高考试题中考查学生学科知识和学科能力重要的组成部分之一有其必要性。对电化学知识内容的考查,不仅是对氧化还原反应、化学反应中的能量变化、水溶液、离子反应、金属活动性顺序等知识的综合运用,同时它还蕴含着跨学科的知识,涉及对化学中电化学与物理学中电学知识的综合理解和运用;对电化学试题的素材的选择,注重与生产生活中的化学问题相联系,注重挖掘教材中联系实际的内容,意在考查学生解决电化学实际问题的能力,包括分析电池的能力和设计电池的能力。将其具体到不同水平层次的任务,分析电池要求学生不仅具备对原型电池进行分析的能力,还要有对实际生产生活中复杂电池进行分析的能力;设计电池要求学生不仅具备设计简单电池的能力,还要具备创新性设计电池的能力。根据高考试题分梯度、多角度考查学生能力的特点,具体到学科内容又可将能力梯度由低到高划分为三个不同的水平,A水平即学习理解能力包括A1观察记忆、A2概括关联、A3说明论证;B水平即应用实践能力包括B1分析解释、B2推论预测、B3简单设计;C水平即探究创新能力包括C1综合复杂问题的解决、C2复杂设计。
2.3基于“高中生电化学认识模型”,分析高考电化学试题的命题趋向
在解读电化学高考试题特点的基础上,笔者基于“高中生电化学认识模型”对近5年高考电化学试题的命题趋向作了进一步的分析,并从中提出电化学的教学策略。
2.3.1考查学生学习理解能力水平的试题,单独设题的比例较小
A水平学习理解能力的题中,A1水平要求学生具备观察记忆的能力,即要求学生能记住典型原电池原型及能分析出原电池基本构成要素;A2水平概括关联的能力,即要求学生能自主判断氧化还原反应与原电池的关系,能宏观地说明生活中的一些简单的电化学现象。当指定认识角度时,能建立起原电池装置要素和化学原理的对应关系;A3水平说明论证的能力,即要求学生能根据物质性质说明和论证一些与生活相关的简单的电化学现象。高考试题中,A1、A2水平的试题无法区分学生的能力水平,所以在高考中,几乎不单独设题。A3水平的试题一般以选择题的形式进行考查,单独设题比例较小。典型的高考试题展示如下例1。
例1 (2014北京理综,8)如表1,电池工作时,O2在正极放电的是( )
[审题]
本题给定的认识角度是正极反应物(O2)、正极电极材料,其他认识角度不在考查范围中,要求学生具备A3水平说明论证的能力,即要求学生能论证生产生活中常见电池的放电情况。
[解题]
根据“高中生电化学认识模型”,从原理维度分析。B项,氢氧燃料电池中,电极反应物是氢气和氧气,氢气具有还原性,氧气具有氧化性,所以氧气是正极反应物,在正极放电,正确。其他,A项,锌锰电池,电极反应物是zn和MnO2;C项,铅蓄电池电极反应物是Pb和PbO2;D项,镍铬电池,电极反应物是Cd和NiOOH,都没有氧气参与反应,所以B项正确。
2.3.2考查学生应用实践能力水平的试题,所占比例相对较大,多以选择题的形式单独设题
B水平应用实践能力的试题中,B1水平要求学生具备分析解释的能力,即要求学生能自主运用不同认识角度分析真实电池的工作过程及其在生活中的作用;B2水平推论预测的能力,即要求学生能预测简单电池装置可能发生的电化学现象(不需要系统分析);B3水平简单设计电池的能力,即要求学生能设计简单的电池装置解决生活中电化学问题,如自主应用电化学防腐、电镀、电解的知识设计电池装置。高考中B1、B2水平的题能均衡高考试题的难度,所以在高考试题中占据一定的比例。但B3水平的试题,由于开放性大、没有封闭答案等特点,所以目前高考试题中涉及的比较少。近五年高考试题中仅在2014广东理综32(5)题中出现,该题要求学生对自然水体中铜件的电化学防腐进行一个简单电池的设计。考虑到发展学生解决实际化学问题能力要求,设计型题目的比例在未来高考中应该会呈一定比例的增长。典型高考试题展示如下例2。
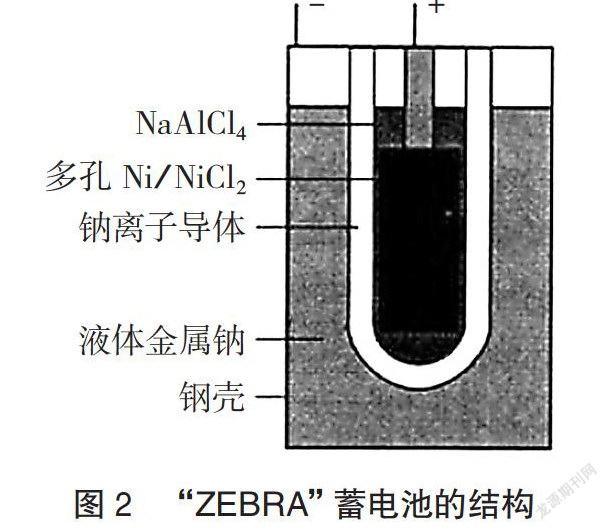
例2 (2013课标Ⅱ,11)“ZEBRA'’蓄电池的结构如图2所示,电极材料多孔Ni/NiCl和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三个铝离子
C.正极反应为:NiCl2+2e-=Ni+2Cl-
D.钠离子通过钠离子导体在两电极间移动
[审题]
本题给定显性的认识角度是正极电极材料(多孔Ni/NiCl)、负极电极材料(金属钠),隐性的认识角度为离子导体(钠离子)和电子导体,未知的认识角度是电极反应物。结合选项知考查的是电极反应式和总反应式的书写,离子导体的运动方向的判断。要求学生具备B1水平分析解释的能力,即要求学生能自主调用给定的认识角度确立电极反应物并根据相关知识分析“ZEBRA”蓄电池的工作过程。
【解题】
根据“高中生电化学认识模型”,将装置维度和原理维度关联进行分析。
首先,根据物质氧化性还原性(化合价的变化)确定电极反应物。负极材料周围除Na外没有其他物质,且Na具有还原性,所以Na是负极反应物。其次,分析物质得失电子(化合价的变化),然后考虑该化合价都有哪些物质存在形式,Na失电子化合价要升高生成Na+,因为电子导体是钠离子,Na+不受环境介质的影响,所以确定负极产物为Na+;同理正极反应物化合价要降低,所以正极反应物只能是NiCl,NiCl中Ni+得电子生成Ni,所以正极产物为Ni。
最后,进行原电池过程及现象分析。负极№失电子生成Na+,负极反应式为:Na-e-=Na+,正极NiCl中Ni+得电子生成Ni,正极反应式为:NiCl2+2e-=Ni+2C1-(C项正确),故电池的总反应式为:2Na+NiCl2=2NaCl+Ni,所以电池反应有NaCl生成(A项正确、B项错误)。负极产生的Na+由于静电吸引移向正极(D项正确)。
所以答案选B。
2.3.3考查学生探究创新能力水平的试题,所占比例最大,考题形式多样
考查学生C探究创新能力水平的试题中,C1水平要求学生具备解决综合、复杂问题的能力,即要求学生面对复杂、陌生的电化学情境时,能够自主调用认识角度对生产生活中新型的电池装置进行分析;能通过书写陌生、复杂电池的电极反应式(涉及酸碱性介质),并对复杂电化学过程进行系统分析(分析任务涉及电极反应、电解质溶液的变化、带电微粒的定向移动等),熟识有关电池发展的前沿动态;C2水平设计复杂电池的能力,即要求学生能创造性设计复杂的原电池装置。这种试题难度较大,通常是将A、B水平的试题综合起来考查学生的能力,这与高考试题作为高校选拔具有较高科学素养和学科能力的人才相吻合,所以这种试题在高考中所占比例最大,而且考查形式多样。典型高考试题展示如下例3。
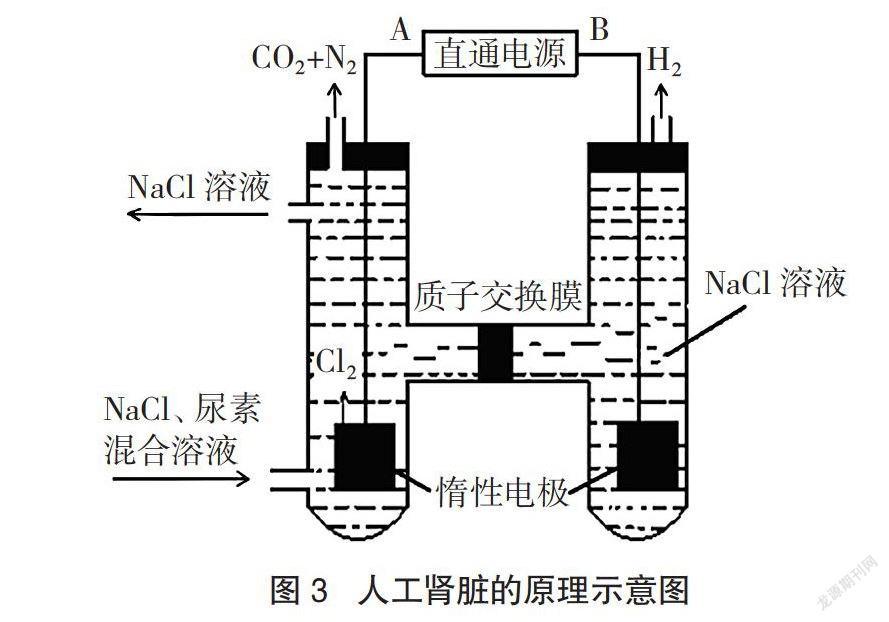
例3[2012重庆理综,29(3)]人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],其原理如图3所示。
①电源的负极为 (填A或B)。
②阳极室中发生的反应为 、 。
③电解结束后,阴极室溶液pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解度)。
[审题]
本题给定隐性的认识角度是电极材料(惰性电极)、电极反应物[NaCl和CO(NH2)2的混合溶液1、离子导体(质子交换膜)和电子导体(电源、导线),还可以从装置中找到电极产物是C12和H2。由题目可知,①考查电极材料阴阳极的确定;②正负电极反应物的确定以及电极方程式的书写;③电解过程的分析和现象的预测,另外还有代谢产物的计算。要求学生具备C1水平解决综合、复杂问题的能力,即面对人工肾脏这一新型的电池装置,能自主地调用给定认识角度及其相关知识解决综合、复杂的电化学问题,并通过原理维度的分析,知道人工肾脏是如何采用间接电化学方法除去代谢产物中尿素[CO(NH2)2]的。
[解题]
根据“高中生电化学认识模型”,将装置维度和原理维度关联进行分析。
已知电极产物,所以可根据电极产物逆推电极反应物。首先,分析电极产物化合价的变化,然后考虑该化合价都有哪些物质存在形式,最后考虑环境介质的影响,从而确定电极反应物。从题目中给出的装置可知,电源B极周围的电极产物是H2,其化合价只能升高,升高后应为H+,所以H+为B极的电极反应物;H+具有还原性,所以H+是阴极电极反应物,因此可确定B极所连的惰性电极是阴极材料,应连接电源的负极即B极。由此,也可以确定A极是电源正极,A极所连接的惰性电极是阳极材料,阳极上电极产物C12化合价降低为C1-,C1-是阳极反应物。电极产物C12会和环境介质中的尿素进一步发生反应生成N2、CO2和Cl-。
其次,进行原电池过程及现象分析,该电池工作时,阳极室C1-失电子生成C12,C12与环境介质中的尿素发生氧化还原反应生成N2、CO2和Cl-,所以阳极室中发生的反应是:2Cl-2e-=C12,CO(NH2)2+3C12+H2O=N2+CO2+6HCl;阴极室H+得到电子生成H2,其电极反应式为2H++2e-=H2↑,由于中间的质子交换膜只允许H+通过,在静电引力的作用下,阳极室生成的H+移向阴极室,补充阴极室由于H+得电子生成H2时失去的H+,所以阴极室溶液的pH不变。
通过上述分析可知,每生成3mol C12会生成3mol的H2,每消耗3mol C12会消耗1molCO(NH2)2,同时生成各1mol的N2和CO2,所以每消耗1mol CO(NH2)2,阴阳极室共生成5mol的气体。所以当两极共收集到气体13.44L(标准状况)即0.6mol时,会消耗0.12mol的CO(NH2)2即7.2g。
所以答案为:①B;
②2CF--2e-=Cl2,CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl;
③不变,0.12mol。
综上,电化学高考试题与实际生产生活联系紧密,其在提供具体的问题情境的同时还能体现化学这门自然科学的社会功能。学生在解答这些问题的过程中,是否能全面地、系统地思考问题,实际上也体现了学生解决实际化学问题的能力高低。从高考整个大背景来看,进入高考复习之初的学生基本具备了对电化学问题的学习理解能力,中等以上水平的学生基本具备了实践应用的能力,而只有少部分学优生具备解决综合、复杂问题的能力,而对综合、复杂问题的解决能力的考查是近几年高考的重点,因此在电化学专题复习中,如何将学生学习理解的能力转化为实践应用的能力,进而发展成解决综合、复杂问题的能力,这是教师教学的重点,也是难点。因此,笔者提出如下改进电化学教学的策略。
3.电化学教学策略
3.1建立解决高考电化学试题的系统的审题、解题模式
之所以学生欠缺解决综合、复杂问题的能力,究其根本原因是学生对真实情境下的电池进行分析时,没有建立起分析电池问题的认识角度,没有形成解决电池问题系统的思维。
3.1.1高考电化学试题的审题模式
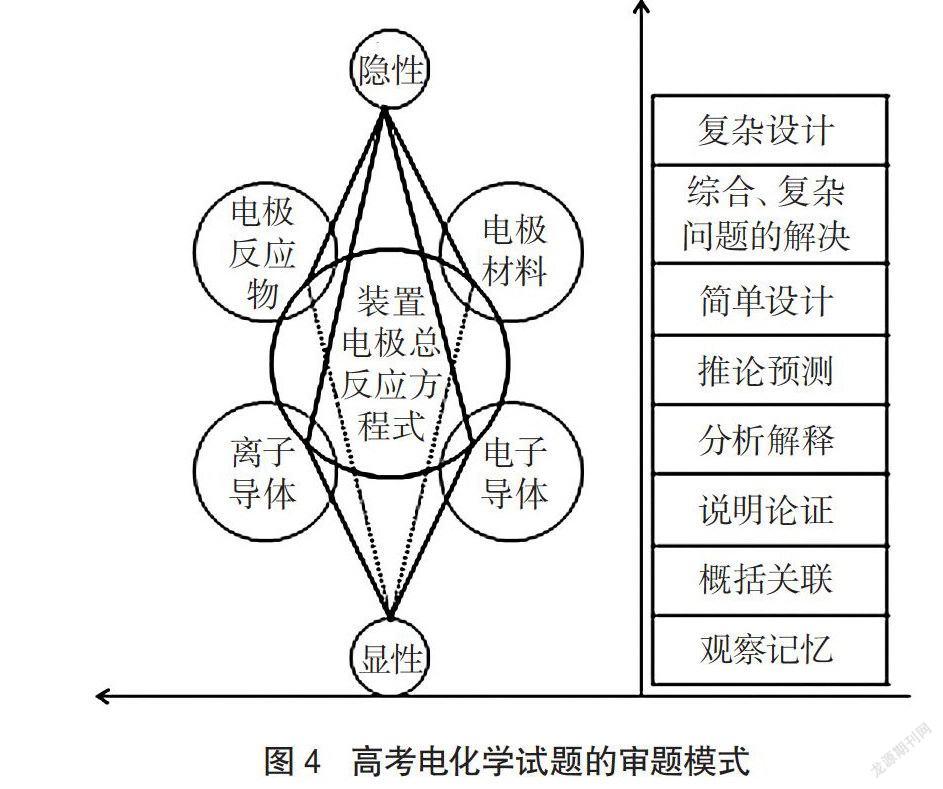
笔者发现电化学高考试题中,已知条件的设置主要包括两种情况:一是给定电池装置,二是给定电池总反应方程式;未知条件的设置主要是对电池工作原理的考查。这些已知点和未知点都是从电极反应物、电极材料、离子导体、电子导体这4个基本的认识角度设置的。设置的方式是通过调控已知条件中给定角度的多少以及这些角度的显、隐性变化来改变各个认识角度间由此及彼的推理关系,从而使学生感受到解答试题时的难易程度。所以进行审题时,我们需要关注这四个基本认识角度,明确题目的已知条件中给定了哪些角度,这些给定角度的显、隐性情况,即题目是否明确告知电池装置的正负(阴阳)电极反应物是什么,正负(阴阳)电极材料是什么,离子导体是什么及其中阴阳离子的移动方向,电子导体中电子的移动方向等,若明确告知是显性,反之则是隐性。最后结合试题明确试题考查点。高考电化学试题的审题模式如图4所示。
3.1.2高考电化学试题的解题模式
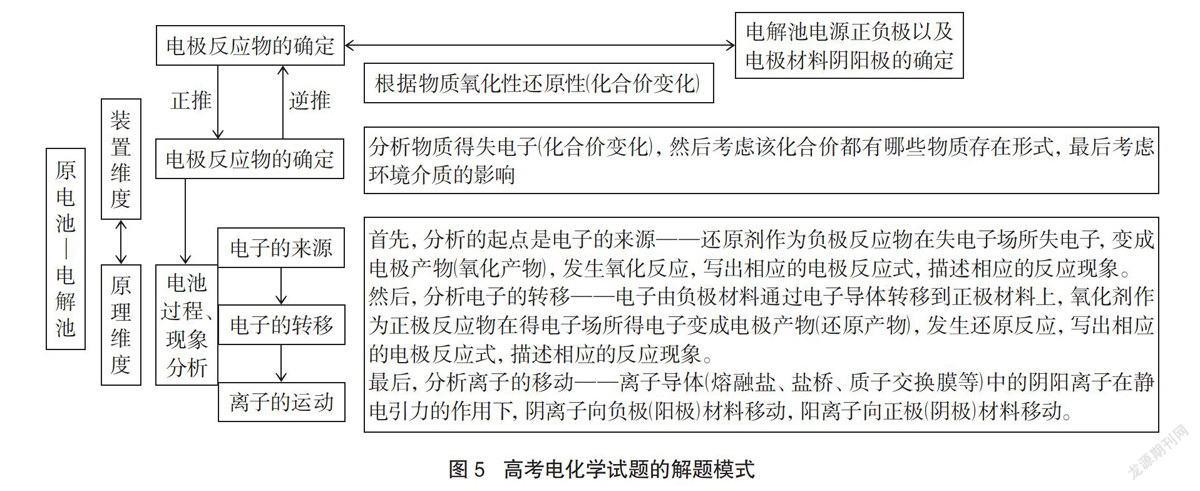
笔者还发现在考查学生分析真实生产生活中电池能力的习题时,其所承载的不论是原电池、电解池还是电化学腐蚀等方面的知识,学生都可以依据模型找到2个维度即原理维度和装置维度,明确2个维度下的重要的认识角度。所以进行解题时,我们联系电化学试题的审题模式,根据“高中生电化学认识模型”,将装置维度和原理维度关联进行分析。首先,根据物质氧化性还原性(化合价的变化)确定电极反应物;其次,通过分析物质得失电子(化合价的变化)考虑该化合价都有哪些物质存在形式;然后考虑环境介质的影响确定电极反应物。确定了电极反应物可以正推出电极产物,同样确定了电极产物也可以逆推出电极反应物。如果确定了电解池的电极反应物可以进而判断出电源的正负极以及电极材料的阴阳极;最后,依据确定好的电极反应物和电极产物进行电池过程、现象的分析。高考电化学试题的解题模式如图5所示。
这样的审题、解题模式并非要求学生一蹴而就,而是有一个由易到难的建构过程。
3.2利用真实的生活情境讨论知识
在教学中,教师可在基本实验、化工生产、日常生活等广泛背景中讲解电化学基础知识和基本技能,同时引导学生提炼分析解决问题的思路,培养学生应用电化学知识解决实际问题的能力。教师还可充分利用教材,设置实用或有趣的情境,刺激学生进行思考、对比和总结,这会比教师简单重复地讲解更有效。在习题课教学中,也可以借鉴梁德娟、蔡红悦教师提出的“问题表征多样化、问题情境生动化、应用深广素养化、科学品质潜默化、能力培养多元化”等教学策略来推进我国新课程教学改革。
3.3加强问题解决、任务驱动式的复习课教学
问题解决、任务驱动式的复习课教学要求教师关注知识的使用情境,在联系实际的背景下提出问题,帮助学生体验知识的形成过程、发展方向,领会知识之间的贯通联系。当教师提出的问题是生产生活中需要解决的实际问题时,不仅可以避免由于知识梳理和习题讲练的单一复习课教学模式引起学生的枯燥感,还能够引导学生将实际问题转化成化学学科问题,然后利用相应的解题思路、结合适当的实验手段,寻找问题解决的方式和结果,使学生在问题解决的过程中领会所学知识的内涵和应用价值。

