浅析苯磺酸左氨氯地平片的制备工艺和质量标准
袁 静
(江苏省南通卫生高等职业技术学校 江苏 南通 226000)
苯磺酸左氨氯地平(Levoamlodipine Besylate)是二氢吡啶类钙拮抗剂。此药可用于治疗高血压、心绞痛,具有安全性好、不良反应的发生率低且程度较轻等特点,是临床上治疗高血压的首选药物之一。为了降低此药的成本,减轻患者的经济负担,更好的服务于高血压患者,我们对苯磺酸左氨氯地平片的制备工艺和质量标准进行研究,并进行了筛选和优化。
1 仪器与试药
1.1 仪器
本次研究使用的仪器有:①梅特勒-托利多仪器有限公司生产的AB265-S型电子精密天平。②台湾KSON公司生产的THS-DOC-100型恒温恒湿实验机。③美国安捷伦公司生产的Agilent 1100高效液相色谱仪。④梅特勒-托利多仪器有限公司生产的HG-63型水分测定仪。⑤上海天凡药机制造厂生产的旋转式压片机。⑥天津大学无线电厂生产的ZRS-8G型智能溶出试验仪。⑦日本岛津公司生产的Shimadzu U2550型紫外-可见分光光度计。⑧德国西门子公司生产的MP1型流化床。
1.2 试药
本次研究选用的药品有:苯磺酸左氨氯地平(由上海海尼药业有限公司新品部合成,批号:07041601),淀粉(由海盐六和淀粉化工有限公司生产,批号:20070511),乳糖(由上海运宏化工制剂辅料技术有限公司生产,批号:20071207),微晶纤维素(由山东聊城阿华制药有限公司生产,批号:20070814),磷酸氢钙(由湖州展望药业有限公司生产,批号:20070921),羧甲基淀粉钠(由湖州展望药业有限公司生产,批号:20071106),硬脂酸镁(由湖州展望药业有限公司生产,批号:20070429)。
2 方法与结果
2.1 辅料相容性研究
2.1.1 研究方法 将用量较大的辅料(如稀释剂等)与主药以5:1的比例混合,将用量较小的辅料(如润滑剂,崩解剂等)与主药以20:1的比例混合,按照药物影响因素实验方法进行实验。将配制样品分别置于60℃的恒温箱中,于当天、第5天、第10天考察其有关物质的变化[1]。
2.1.2 实验结果 结果表明,乳糖和苯磺酸左氨氯地平混合后,在当天无明显变化,在60℃的恒温箱中放置第5天、第10天时,在6.4 min峰,11.5 min峰时出现杂质峰,且随着时间延长,其4.0 min峰的峰面积增大。可见乳糖和苯磺酸左氨氯地平不能配伍使用。淀粉、微晶纤维素、磷酸氢钙、羧甲淀粉钠和硬脂酸镁与苯磺酸左氨氯地平混合后,在第0天、第5天、第10天时主药峰面积均无明显变化,且无其他未知峰出现。因此,苯磺酸左氨氯地平片可选用淀粉、微晶纤维素和磷酸氢钙作为填充剂,选用羧甲淀粉钠作为崩解剂,选用硬脂酸镁作为润滑剂。详情见表1。
2.2 制备工艺的研究
2.2.1 制备方法 精密称取3.47g苯磺酸左氨氯地平(相当于左氨氯地平2.5g),与崩解剂羧甲基淀粉钠混合后过100目筛、备用。加入微晶纤维素、磷酸氢钙混合后再过100目筛。然后加入适量的浓度为2%的淀粉浆制成软材,过30目筛制粒。在60℃的环境下进行干燥,直至药粒的水分含量为2%~4%。再加入硬脂酸镁,混合均匀、压制成片(制成1000片)。
2.2.2 溶出度测定 取苯磺酸左氨氯地平片,根据溶出度测定法(中国药典2010年版二部附录XC第三法),以200 ml浓度为0.1mol/l的盐酸溶液为溶剂,进行离心处理时的转速为每分钟50转,依法操作,30分钟后,取适量溶液,滤过,取续滤液作为供试品溶液。另取17 mg苯磺酸左氨氯地平作为对照品,将其置于100 ml的容量瓶中,加入2 ml的甲醇进行溶解后,加入浓度为0.1 mol/l的盐酸进行稀释、摇匀。精密量取5 ml的此溶液,将其置于50 ml的容量瓶中,加入浓度为0.1 mol/l的盐酸溶液进行稀释、摇匀,作为对照品溶液。取上述两种溶液,根据紫外——可见分光光度法(中国药典2005年版二部附录ⅣA),在238 nm的波长处分别测定其吸光度。计算出每片苯磺酸左氨氯地平的溶出量。

2.2.3 处方筛选 经研究发现,影响苯磺酸左氨氯地平片质量的因素为微晶纤维素(A)、磷酸氢钙(B)、羧甲基淀粉钠(C)和硬脂酸镁(D)的用量。选用L 9(34)正交表进行正交试验,其中每种因素各取3个水平,以溶出度为评定标准,正交设计因素水平见表1,试验结果见表2。

表1 正交设计因素水平
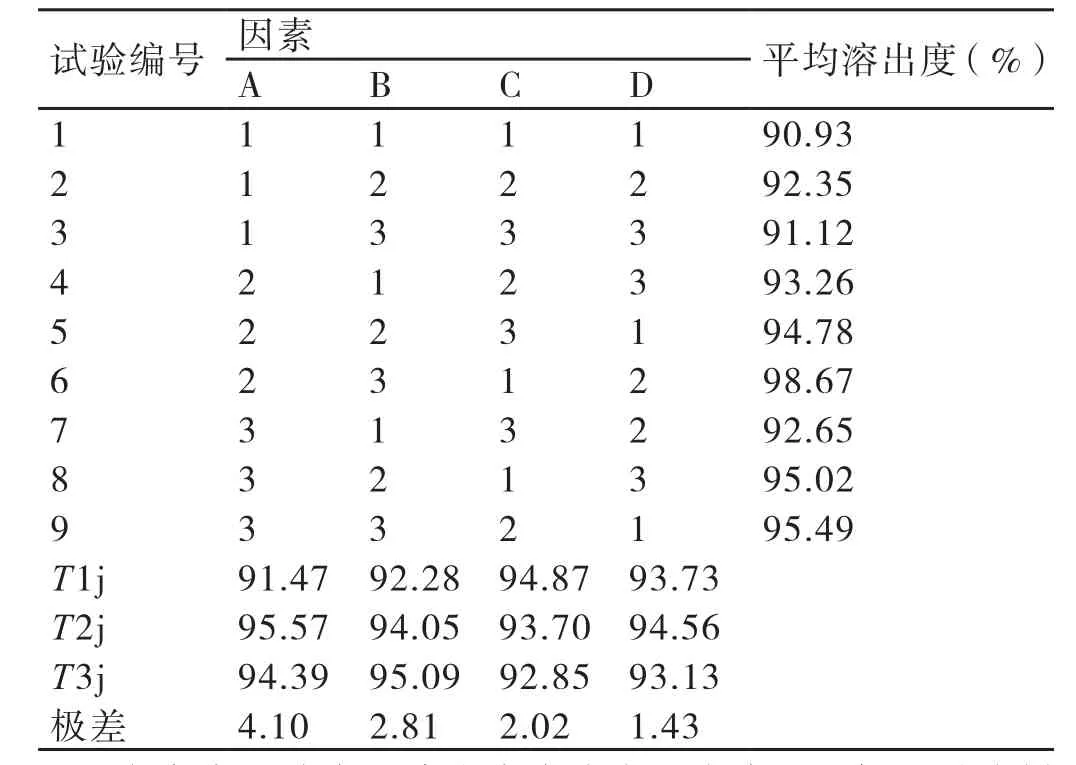
表2 正交试验结果
在本次试验中以溶出度大为宜。由表2可知,对片剂的溶出度影响最大的是因素A(A2>A3>A1),其次是因素B(B3>B2>B1)和 C(C1>C2>C3),对片剂的溶出度影响最小的是D(D2>D1>D3)。因此,最佳制备工艺应为A2B3C1D2。参考表1,即微晶纤维素50克,磷酸氢钙40克,羧甲基淀粉钠2克,硬脂酸镁1克。
2.3 对工艺放大及工艺重现性的研究
根据正交试验的结果,按照同等比例放大处方量至10000片,采用流化床工艺试制三批(批号:08050901,08050902,08050903)苯磺酸左氨氯地平片,以验证正交试验结果。
2.3.1 工艺流程 ①将苯磺酸左氨氯地平片粉碎后过100目筛备用。②采用冲浆法配制浓度为2%的淀粉浆备用。③根据正交试验结果得出的处方量称取适量的苯磺酸左氨氯地平、微晶纤维素、磷酸氢钙、羧甲基淀粉钠,将它们一起加入流化床中混合10分钟,保证混合均匀。④向混合粉中喷入适量的浓度为2%的淀粉浆,用流化床制成湿颗粒。控制物料的温度为20℃~35℃、进风的温度为40℃~70℃、出风的温度为20℃~35℃、进风量为800~1200m3/小时,喷雾压力为1.5~4bar(1bar=0.1MPa)、流速为50~80转/分钟。⑤将湿颗粒用流化床进行干燥,控制物料的温度为20℃~60℃、进风的温度为40℃~80℃、出风的温度为20℃~60℃、进风量为800~1200m3/小时、烘干至水分为2.0%~4.0%。⑥将烘好的颗粒用干式整粒机进行整粒,过24目筛网。⑦将整粒后的颗粒加入处方量的硬脂酯镁,混合均匀,测定其中间颗粒的含量。⑧按照中间颗粒的含量计算理论片重,采用直径为7 mm的浅弧冲模压片,控制片重差异在±7.5%之间。⑨按质量标准进行检验。⑩将检验合格的苯磺酸左氨氯地平片用铝塑泡罩进行包装。
2.3.2 工艺重现性结果 按照试验项“2.3.1”中的方法测定三批样品苯磺酸左氨氯地平片的溶出度,与正交试验编号6(批号:08041201)的溶出度进行比较。结果显示,苯磺酸左氨氯地平片的处方采用流化床工艺重现性良好。三批样品的试验结果与小试结果相似。详情见表3。
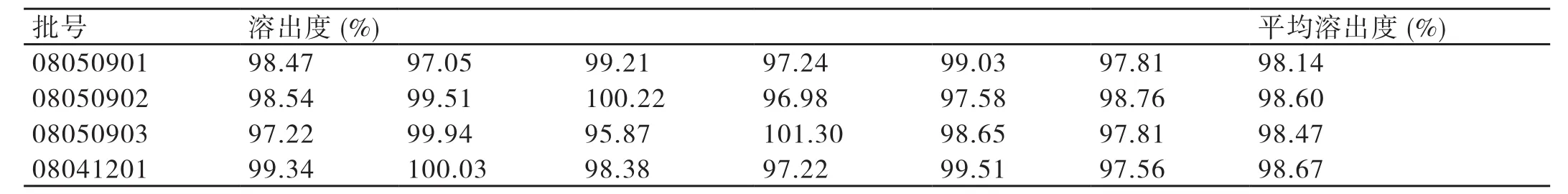
表3 工艺重现性三批样品溶出度的比较
3 讨论
3.1 开发新处方首先要进行辅料相容性的筛选[2],再进行模型处方的设计[3]和稳定性测试(制成相应剂型),最后确定最佳处方。若不筛选辅料而仅对辅料进行稳定性的研究,则耗时长、费用高,进行辅料筛选可节省时间、人力和资金[4]。在苯磺酸左氨氯地平辅料相容性的研究中发现,乳糖与苯磺酸左氨氯地平具有配伍禁忌。其原因是乳糖中含有不定量的5-羟甲基糠醛等杂质,这些杂质能与胺类药物如异烟肼、苯丙胺等生成棕黄色的加成物。处方中若同时含有酒石酸盐或醋酸盐,或在碱性润滑剂的影响下,能加速变色反应。苯磺酸左氨氯地平为胺类药物,有可能与乳糖中的5-羟甲基糠醛等杂质发生加成反应,因而导致苯磺酸左氨氯地平与乳糖具有配伍禁忌。而另外几种辅料(淀粉、微晶纤维素、磷酸氢钙、羧甲淀粉钠和硬脂酸镁)则无明显干扰。
3.2 进行正交试验设计表明,微晶纤维素对片剂溶出度的影响最大,但并不是用量越多越好。研究中尝试使用60克或70克的微晶纤维素(以制成1000片计量),但片剂的溶出度并无明显提高。崩解剂羧甲淀粉钠对片剂的溶出度也有较大的影响。研究结果显示,本试验崩解剂的最佳用量为2克。试验过程中我们尝试采用内加、外加的方法,按1:1或2:1的内外加比例来制粒、压片,结果片剂的溶出度无明显改变。考虑到内加工艺简单便捷,因此本次研究全部采用内加工的方法进行制备。一般情况下,淀粉浆的浓度越高,则粘度越大,越有利于压片。但如果淀粉浆浓度过高,造成粘度过大,则不利于喷浆。因此,选用浓度为2%的淀粉浆作粘合剂粘度适中,既保证了硬度要求又适合于工业化生产。
3.3 工艺放大是进行工艺研究的重要内容,是实验室制备技术向工业化生产转移的必要阶段,是药品工业化生产的重要基础,同时也是制备工艺进一步完善和优化的过程。在进行工艺放大的中试阶段,采用的是流化床一步制粒,不同于小试时的湿法制粒。由于中试所采用的原辅料大都预先经过粉碎处理,且流化床制粒比较均匀,因此没有另外将原辅料过筛。由连续三批样品的溶出度测定结果可知,本处方工艺的重现性良好,保证了制剂质量的一致性。
综上所述,苯磺酸左氨氯地平片的处方设计合理,测定方法操作简便,制备工艺简单、稳定,可用于大规模生产。
[1] 化学药物研究技术指导原则(药学部分05年版).
[2] TAMBWEKAR KR,KAKARIYA RB,GARG S.A validated highpe rformance liquid chromatographic method for analysis of nicotine in pure form and from formulations[J].J Pharm Biomed Anal,2003,32(3):441-450.
[3] SIMS JL,CARREIRA JA,CARRIER DJ,et a1.A new approa ch to accelerated Drug-excipient compatibility testing[J] Pharm Dev Technol,2003,8(2):119-126.
[4] 王弘,王东晓,王波.固体稳定性和辅料相容性的研究进展[J].中国新药杂志,2006,15(16):1337-1341.

