偶氮杯芳烃Li+印迹聚合物的制备及其性能研究
郑小三,裘俊红
(浙江工业大学化学工程学院,浙江 杭州 310014)
锂及其化合物有着“工业味精”的美誉,在航天和能源方面有着重要的战略意义。在化学电源方面,锂离子电池已成为世界范围的研究热潮[1-2],预测它在未来将取代传统燃料作为大型设备的动力能源,所以又有“21世纪新能源的美誉”。锂及其化合物在玻璃、陶瓷、润滑剂、制冷剂、冶金、制药和化学试剂等行业也应用广泛。相对于传统的卤水、矿石提锂,海水中锂资源更加丰富。
不同于分子筛技术提锂,本文运用了离子印迹技术,制备了有选择性的、环保且循环利用的锂离子印迹聚合物来提取海水中的锂。离子印迹技术作为分子印迹技术发展的一个新方向,应用于海水提锂过程,开辟了一条除分子筛提锂技术的又一条新道路。在离子印迹中,模板离子与功能单体通过螯合作用结合,两者间的配位作用相对于非共价键有足够的稳定性,同时又能通过改变环境来控制配位键的结合与断裂速度。
1 实验部分
1.1 仪器和药品
仪器:台式恒温振荡器 (THZ-C)、超声波清洗仪(KQ-50E)、pH计 (pHS-2F)、电子天平 (精度0.001g)、紫外可见分光光度计 (TU-1810)、电子扫描电镜(HITACHI S4700)、傅里叶变换红外光谱仪 (NEXU 470)。
药品 (分析纯):叔丁基苯酚、甲醛、对氨基苯甲酸、间氨基苯甲酸、碳酸钠、亚硝酸钠、盐酸、乙酸钠。
1.2 聚合物的制备
在三口烧瓶中,依次加入对氨基苯甲酸0.45g,水3.0mL,15%Na2CO3溶液0.8mL,浓盐酸0.88g,有白色固体析出,用冰浴降温[3]。滴加2.11g 10% 的NaNO2溶液,反应物变为橘黄色较澄清的液体。用30.0mL DMF-甲醇混合溶剂溶解杯[4]芳烃0.30g,加入到三口烧瓶中,继续搅拌,用20%乙酸钠溶液调节pH值为6~7,偶合反应2h后,加入少许浓盐酸,调节pH值小于1,加入30.0mL水,搅拌30min,静置一定时间后抽滤,得到产物a 0.54g。
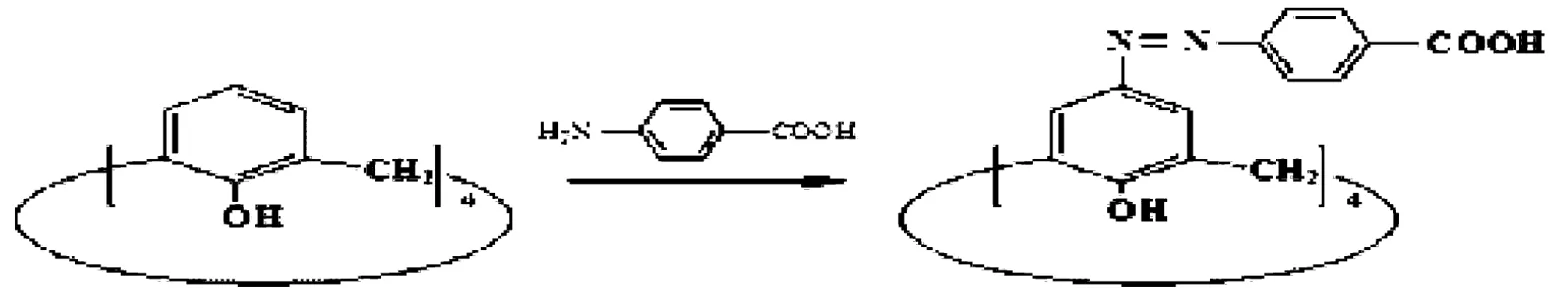
图1 对羧基苯基—偶氮基杯四芳烃的制备图
采用同样的制备方法,用间氨基苯甲酸代替对氨基苯甲酸得到产物b。
取4.00g钛酸丁酯加入锥形瓶,依次加入11.0mL无水乙醇、6.0mL蒸馏水、5.0mL冰乙酸。超声振荡3h,再加入适量的盐酸酸化,并调节pH为2~3,静置待用[4]。取0.50g偶氮基杯[4]芳烃溶于30.0ml无水乙醇,加入1.00g LiCl2,充分溶解后,放入恒温振荡箱螯合4h后加入备用的钛酸丁酯溶液,将上述混合液放入超声波振荡仪中,然后用蒸馏水洗涤未反应的残留物,用1mol/L的盐酸洗脱,得到印迹聚合物。
2 结果与讨论
2.1 红外光谱分析
图2是对羧基苯基—偶氮基杯四芳烃印迹聚合物的傅里叶变换红外表征图,傅里叶变换红外分析的波长范围在4000.0~400.0cm-1。图2中在3167.7cm-1附近的峰值证明酚羟基的存在,在1603.0cm-1附近出现的峰值表明印迹聚合物中偶氮基的存在,而1523.9cm-1附近的峰值是对苯甲酸基的吸收峰[5]。图3是间羧基苯基—偶氮基杯四芳烃印迹聚合物的傅里叶变换红外表征图。图3中在1591.8cm-1峰值附近出现的峰值证明偶氮基团的存在,在3400.0cm-1峰值附近出现的峰值证明酚羟基的存在,而在1543.9cm-1附近的峰值则证明了间苯甲酸基团的存在。
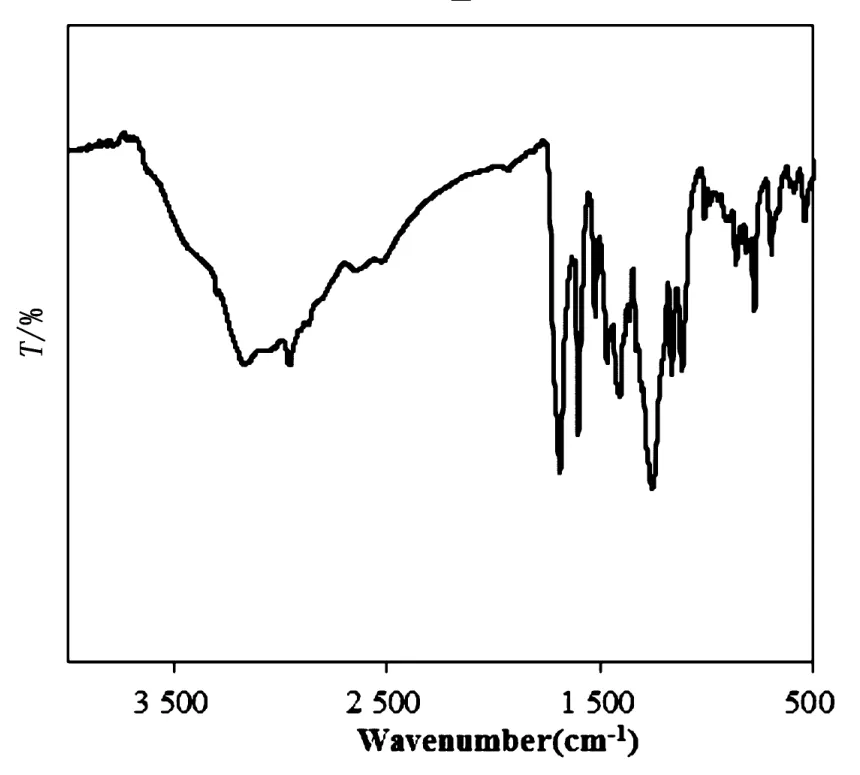
图2 印迹聚合物a的红外光谱图
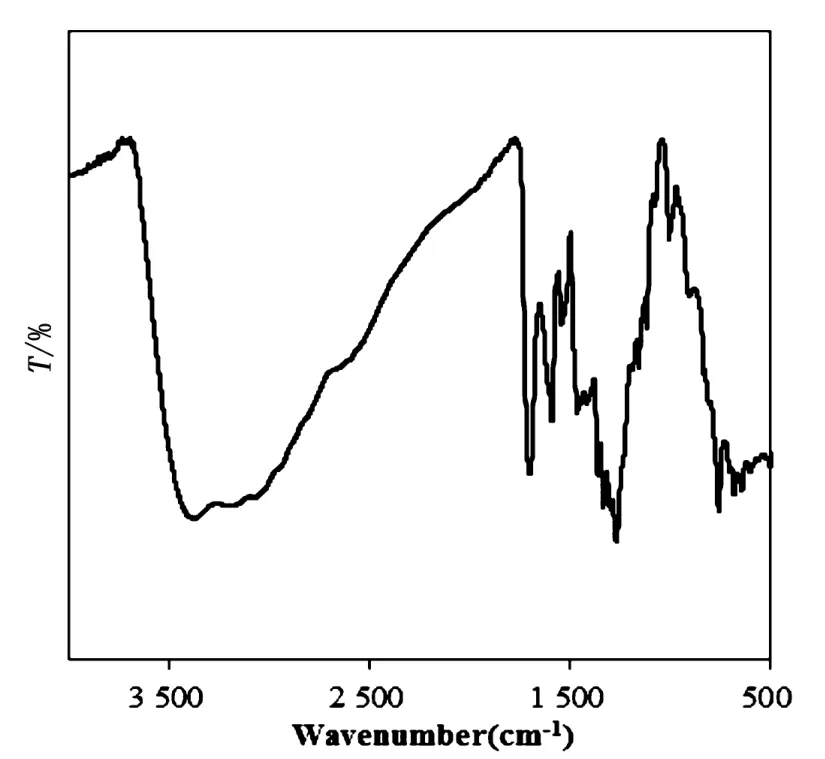
图3 印迹聚合物b的红外光谱图
2.2 扫描电镜分析
图4中是印迹聚合物a在不同放大倍数下的扫描电镜图。从图4中可以看出,检测过程中的物理碾压使印迹聚合物呈现的是不规则的几何状,在不断的放大过程中可以看出印迹聚合物表面分布着细小的晶体状的小颗粒,经过分析,这种小颗粒可能是交联剂残留在印迹聚合物的表面所形成的。图5是印迹聚合物b在不同的放大倍数下的扫描电镜图,与图4中的印迹聚合物a比较,在形状和外观上基本相似,均呈不规则的几何状,但是在经过物理碾压之后与印迹聚合物a相比大小比较均匀。

图4 印迹聚合物a的扫描电镜图

图5 印迹聚合物b的扫描电镜图
2.3 吸附性能测定
称取0.3g印迹聚合物a、b和0.3g非印迹聚合物a、b分别放入2支锥形瓶中,分别加入50.0mL 0.5g/L的氯化锂溶液,调节pH=4后,将其放入温度为20℃ 的真空震荡箱内,每2h取上清液测其吸光度。图6、7分别是印迹聚合物a、非印迹聚合物a在吸附过程中Li+浓度随时间的变化图;图8、9分别是印迹聚合物b、非印迹聚合物b在吸附过程中Li+浓度随时间的变化图。

图6 Li+浓度与吸附时间的关系图 (印迹聚合物a)
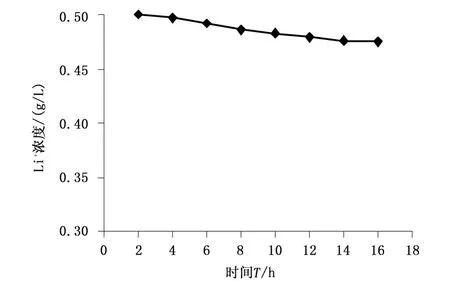
图7 Li+浓度与吸附时间的关系图 (非印迹聚合物a)
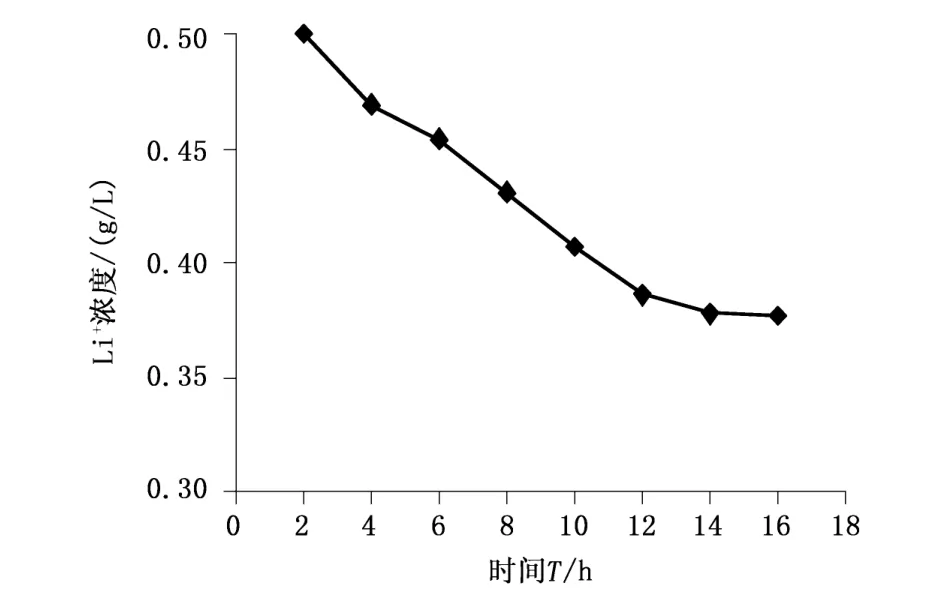
图8 Li+浓度与吸附时间的关系图 (印迹聚合物b)

图9 Li+浓度与吸附时间的关系图 (非印迹聚合物b)
由图6可以计算出印迹聚合物a的吸附量是20.43mg/g,图7中非印迹聚合物a对锂离子的吸附量是4.17mg/g;由图8可以计算出印迹聚合物b的吸附量是20.39mg/g,图9中非印迹聚合物 b对锂离子的吸附量是4.15mg/g。
3 结语
印迹聚合物a的吸附量比钟辉[6]合成的偏钛酸锂的交换容量 29.15mg/g低,比 Hideki Koyanak[7]的 17.0mg/g高。印迹聚合物b的吸附量为20.39mg/g,与印迹聚合物a的吸附量基本一致。非印迹聚合物对锂离子的吸附量是印迹聚合物的1/5。此外,印迹聚合物的制作成本较金属分子筛低,且可循环利用,更加符合可持续发展的科学目标。
[1] Dilic,Mkilb,Kholl,et a1.Recent progress in rechargeable nickel metal hydride and lithium ion miniature rechargeable batteries[J].Journal of Power Sources,1999,80(1-2):112-115.
[2]温贤勇,裘俊红.杯[4]芳烃衍生物与Li+络合研究和海水提锂的新展望 [J].浙江水利科技,2014,193(3):8-12.
[3]韩广甸,赵瑞新,李述文,等.有机制备化学手册 (中)[M].北京:化学工业出社,1980:38-50.
[4]雷家珩,弓巧侠,尚建华,等.锂离子筛前驱体正尖晶石结构LiMn2O4的合成及其特性的研究[J].武汉大学学报:理学版,2001,47(6):707-711.
[5]谢英娜,王正德.对溴苯基偶氮基杯[4]芳烃的合成及表征[J].内蒙古科技大学学报,2010,29(3):257-259.
[6]钟辉.偏钛酸型锂离子交换剂的交换性质及从气田卤水中提锂[J].应用化学,2000,17(3):307-309.
[7] Hideki Koyanaka,Osamu Matsubaya,Yoshio Koyanaka,et al.Quantitative correlation between Li absorption and H content in manganese oxide spinel-MnO2[J].Journal of Electroanalytical chemistry,2003,559(11):77-81.
- 浙江水利科技的其它文章
- 浅谈 “温州模式”下的水环境整治——以龙湾区为例

