齐拉西酮联用奥氮平对精神分裂症疗效及糖化血红蛋白的影响
周勇,黄汉津,唐建良
(1.温州医科大学附属第二医院 神经内科,浙江 温州 325027;2.嘉兴市康慈医院 精神科,浙江嘉兴 314500;3.桐乡市第一人民医院,浙江 嘉兴 314500)
·临 床 经 验·
齐拉西酮联用奥氮平对精神分裂症疗效及糖化血红蛋白的影响
周勇1,2,黄汉津1,唐建良3
(1.温州医科大学附属第二医院 神经内科,浙江 温州 325027;2.嘉兴市康慈医院 精神科,浙江嘉兴 314500;3.桐乡市第一人民医院,浙江 嘉兴 314500)
目的:探讨齐拉西酮早期联用奥氮平治疗精神分裂症的疗效以及对血糖和糖化血红蛋白的影响。方法:选择自2013年1月至2014年1月期间7家精神卫生医院确诊精神分裂症患者197例作为观察对象,随机分为单药组(齐拉西酮99例)和联用组(齐拉西酮联用奥氮平98例),2组治疗起始5周均以齐拉西酮联用奥氮平,5周后单药组渐停奥氮平,联用组继续联用奥氮平治疗,均持续12周时间。比较2组在治疗前及治疗后1、5、7、9、12周末PANSS量表评定结果,以及空腹血糖及糖化血红蛋白数值。结果:2组治疗后的PANSS评分均有显著下降,差异有统计学意义(P<0.05);各时点2组间的PANSS量表评分差异无统计学意义(P>0.05)。而空腹血糖在第9、第12周末时,联用组血糖升高更明显,两者差异有统计学意义(P<0.05);糖化血红蛋白在各时点的变化,差异无统计学意义(P>0.05)。结论:单用齐拉西酮与齐拉西酮联用奥氮平的疗效相当,后期以齐拉西酮单药维持有利于血糖的控制,而且病情相对稳定。
精神分裂症;齐拉西酮;奥氮平;代谢综合征;糖化血红蛋白
精神分裂症作为一种临床常见的精神疾病具有复发率高的特点,而目前降低复发率的有效措施之一就是长期服药维持治疗,随着精神药理学的发展,非典型抗精神病药物在精神分裂症的治疗中广泛应用[1],但是近年来发现非典型抗精神病药物可导致患者糖、脂代谢紊乱,增加心血管疾病、高血压、糖尿病等疾病风险[2]。随着研究的深入,有关新型抗精神病药物对代谢影响的报道越来越多[3-4]。为进一步探讨非典型抗精神病药物长期维持治疗所带来的代谢相关问题,本研究采取多中心(浙江省立同德医院、嘉兴市康慈医院、杭州市第七医院、湖州市第三医院、金华市第二医院、衢州市第三医院、建德市第四医院)联合的方式选取精神分裂症患者作为研究对象,探讨齐拉西酮联用奥氮平治疗精神分裂症患者的疗效以及维持期以齐拉西酮单药巩固治疗对代谢方面的影响。
1 资料和方法
1.1 一般资料 共收集7家医院自2013年1月至2014年1月期间门诊或住院的精神分裂症患者,完成本研究的共197例,所有入组病例均完成为期12周的研究。入组患者均经主治医师以上的高年资精神科医师确诊。将所有患者按数字表法随机分成单药组(齐拉西酮,思贝格胶囊,江苏恩华产,20 mg)及联用组(齐拉西酮联用奥氮平,欧来宁片剂,江苏豪森产,5 mg/片),单药组99例,年龄(38.14±11.78)岁,病程(9.27±7.80)年,住院次数(3.12±3.08)次,男女比例0.74∶1;联用组98例,年龄(36.43±13.45)岁,病程(9.16±9.15)年,住院次数(4.05±5.86)次,男女比例0.66∶1。入组标准:①符合《中国精神疾病分类和诊断标准》(第3版)(CCMD-3)或《疾病和有关健康问题的国际统计分类》(ICD-10)标准;②PANSS总分>60分;③年龄在18~60岁间;④无脑器质性疾病及由此引起的躁狂表现;⑤无物质依赖以及由此引起的精神障碍;⑥排除激素引起的疾病发作;⑦知情同意;⑧经医院伦理委员会讨论后通过。排除标准:①妊娠或哺乳期妇女,或计划妊娠者;②患有下列疾病:癫痫、心肌梗死、不稳定性心绞痛、充血性心衰、严重肝硬化、急慢性肾功能衰竭、严重糖尿病、再生障碍性贫血、其他严重神经系统、心、肝、肾、内分泌、血液系统等躯体疾病或可能干扰试验评估的疾病,如窄角型青光眼;③符合CCMD-3/ICD-10酒、药物依赖诊断标准的患者;④入选前1周内使用过抗精神病药物、抗抑郁药、抗躁狂药及抗抽搐药或入选前2周内使用过长效抗精神病药制剂者;⑤入选前1个月使用过氯氮平≥200 mg·d-1;⑥患有或曾患有药源恶性症状群,严重锥体外系反应(EPS)、明显的迟发性运动障碍者,具有严重自杀企图者,或有严重冲动兴奋且不能进行药物清洗的患者;⑦正接受二种或二种以上其他抗精神病药物治疗者;⑧最近30 d内曾参加过其他药物临床试验者;⑨不愿或不能完成临床研究者;⑩近期发生过心肌梗死者。脱落标准:①严重威胁生命的不良反应,如急性肝坏死或心脏疾病或肾功能衰竭;②在2周内症状几乎没有改善或改善率<10%,需要添加非研究允许药物者;③一般药物反应,经过处理患者依然无法耐受;④患者自动退出;⑤门诊患者失访。2组性别构成比、年龄、住院次数及病程等基线资料差异无统计学意义(P>0.05),见表1。
表1 2组一般人口学资料比较()

表1 2组一般人口学资料比较()
1.2 方法
1.2.1 分组方法:197例符合入组对象患者随机分成单药组99例及联用组98例后,前5周均服用齐拉西酮联合奥氮平。5周后单药组渐停奥氮平,而联用组继续服用齐拉西酮联用奥氮平。治疗前、治疗后第1、第5、第7、第9、第12周末,评定PANSS量表以及记录所测量的空腹血糖及糖化血红蛋白的数值。观察时间为12周,所有患者均统一饮食及住院生活方式。
1.2.2 给药和血样检测方法:奥氮平用法用量:7 d加至15 mg/d;思贝格用法用量:7 d加至120 mg/d,正餐时服用,第7天以后调整至120~160 mg/d。第5周后单药组渐减奥氮平至停。若患者在原药减量过程中出现症状轻度复燃,可能是撤药反应。可肌注或口服氯硝西泮,每次1~2 mg,每日总量不超过6 mg;如患者存在严重睡眠障碍,可于晚间短期间歇性使用苯二氮卓类药物;其他常见的不良反应可对症处理;稳定的躯体疾病的药物治疗可以继续服用。研究期间出现的一般躯体性疾病可对症治疗,如病情严重则需中止试验。入组患者于治疗开始时、治疗第1、第5、第7、第9、第12周末分别空腹采血1次。采血前禁食12 h,抽静脉血5 mL后肝素抗凝。采用全自动生化仪分析检测空腹血糖及糖化血红蛋白。
1.3 统计学处理方法 采用SPSS 13.0统计软件进行统计学分析。计数资料采用表示,治疗开始时组间比较用独立样本t检验,各时点组间比较用协方差分析,各指标变化趋势组间比较用重复测量方差分析。P<0.05为差异有统计学意义。
2 结果
2.1 2组间各时点PANSS量表评分的比较 2组PANSS评分治疗后均较治疗前明显降低,第5周末与治疗前比较PANSS评分总分上单药组及联用组差异均有统计学意义(P<0.05)。第5周末后单药组逐渐停用奥氮平,单药组和联用组比较12周末与治疗前PANSS评分总分上差异有统计学意义(P<0.05)。2组各时点PANSS评分比较,差异无统计学意义(P>0.05)。见图1和表2。
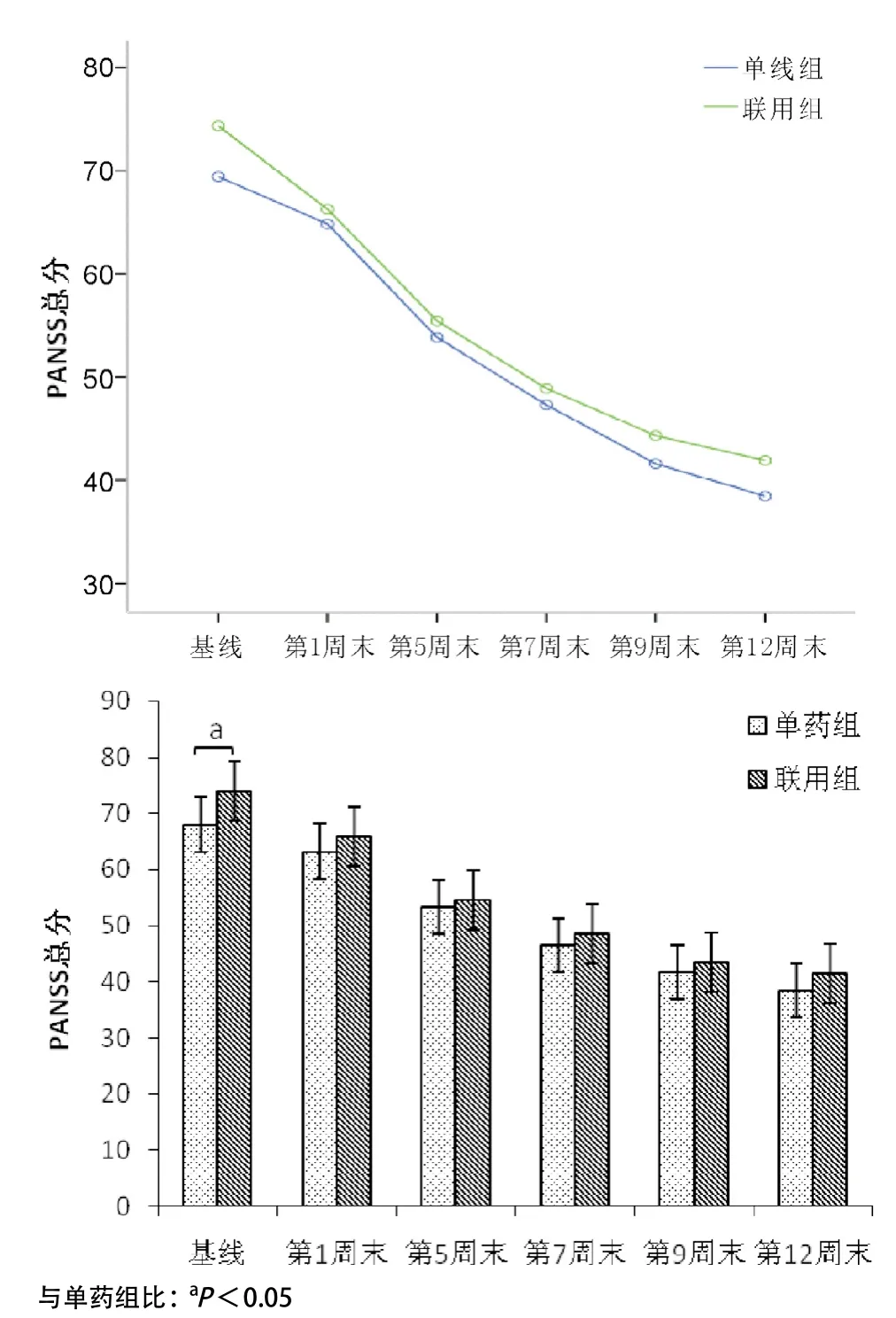
图1 2组间PANSS总分变化趋势和比较
2.2 2组间各时间点空腹血糖的比较 单药组第5周末与治疗前比,空腹血糖值差异无统计学意义(P>0.05);单药组第5周末与第12周末比,空腹血糖数值差异无统计学意义(P>0.05)。联用组第5周末与治疗前比,空腹血糖数值差异无统计学意义(P>0.05);联用组第12周末与第5周末比空腹血糖数值明显升高,差异有统计学意义(P<0.05)。2组间空腹血糖在治疗开始时第1、第5、第7周末比较差异无统计学意义(P>0.05);而在第9、第12周末血糖均在正常范围内,但联用组空腹血糖升高大于单药组,差异有统计学意义(P<0.05),见图2和表3。
表2 2组间各时点PANSS总分比较()

表2 2组间各时点PANSS总分比较()
时间单药组联用组t/FP基线67.97±17.7373.99±14.74-2.590.01第1周末63.18±16.9965.83±12.57 2.410.12第5周末53.28±13.5154.44±12.99 0.950.33第7周末46.51±13.5348.50±11.62 0.050.82第9周末41.64±10.3443.33±12.49 0.000.96第12周末38.47±10.5241.45±11.32 0.850.36
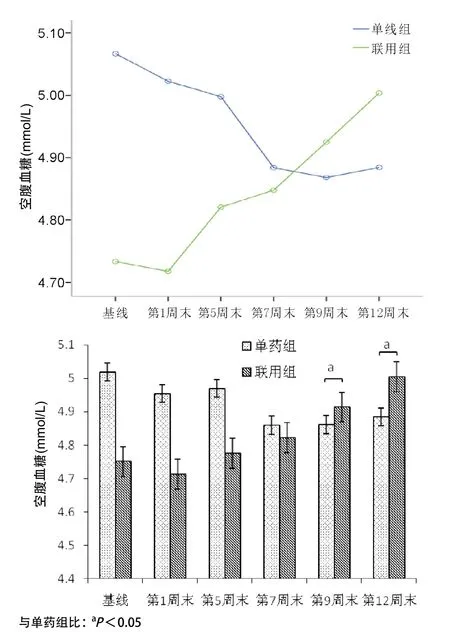
图2 2组间各时间点血糖变化趋势和比较
2.3 2组间各时间点糖化血红蛋白比较 单药组在第12周末较第5周末糖化血红蛋白数值明显降低,差异有统计学意义(P<0.05);联用组在第12周末与第5周末糖化血红蛋白,差异无统计学意义(P>0.05)。2组间糖化血红蛋白在各时点比较,差异无统计学意义(P>0.05),见图3和表4。
表3 2组间各时间点血糖比较()
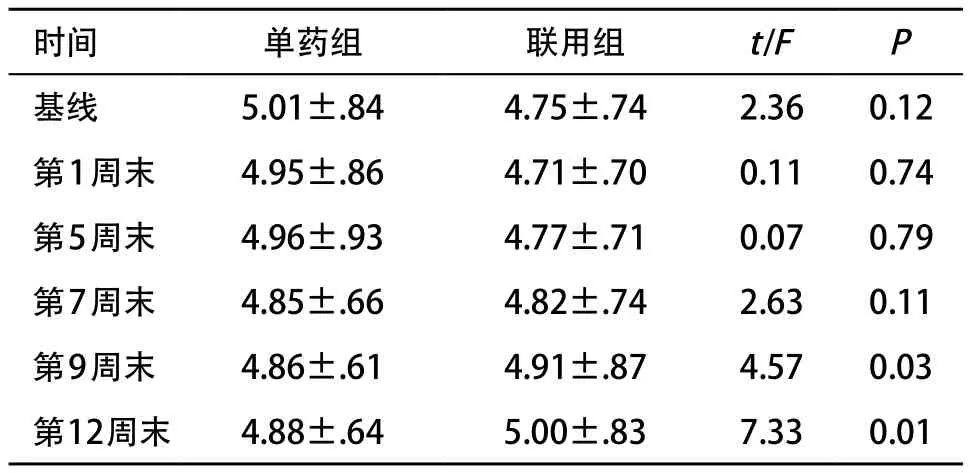
表3 2组间各时间点血糖比较()
时间单药组联用组t/FP基线5.01±.844.75±.742.360.12第1周末4.95±.864.71±.700.110.74第5周末4.96±.934.77±.710.070.79第7周末4.85±.664.82±.742.630.11第9周末4.86±.614.91±.874.570.03第12周末4.88±.645.00±.837.330.01

图3 2组间各时间点糖化血红蛋白变化趋势和比较
表4 2组各时点糖化血红蛋白组间比较()
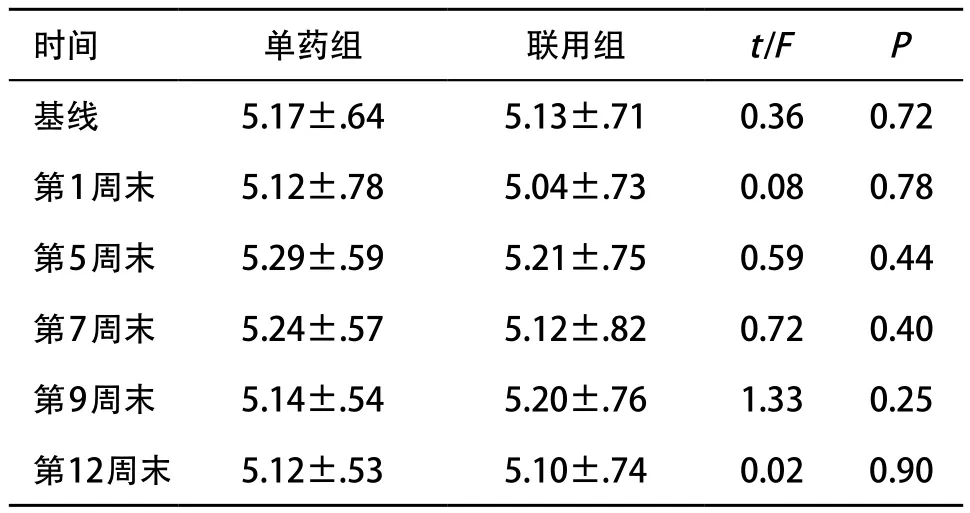
表4 2组各时点糖化血红蛋白组间比较()
时间单药组联用组t/FP基线5.17±.645.13±.710.360.72第1周末5.12±.785.04±.730.080.78第5周末5.29±.595.21±.750.590.44第7周末5.24±.575.12±.820.720.40第9周末5.14±.545.20±.761.330.25第12周末5.12±.535.10±.740.020.90
2.4 2组各时间点不良反应的比较 2组治疗前、第1、第5、第9周末不良反应量表(treatment emergent symptom scale,TESS)评分比较,差异无统计学意义;但在第7周末及第12周末TESS评分单药组相比较联用组明显降低,差异有统计学意义(P<0.05),见图4和表5。
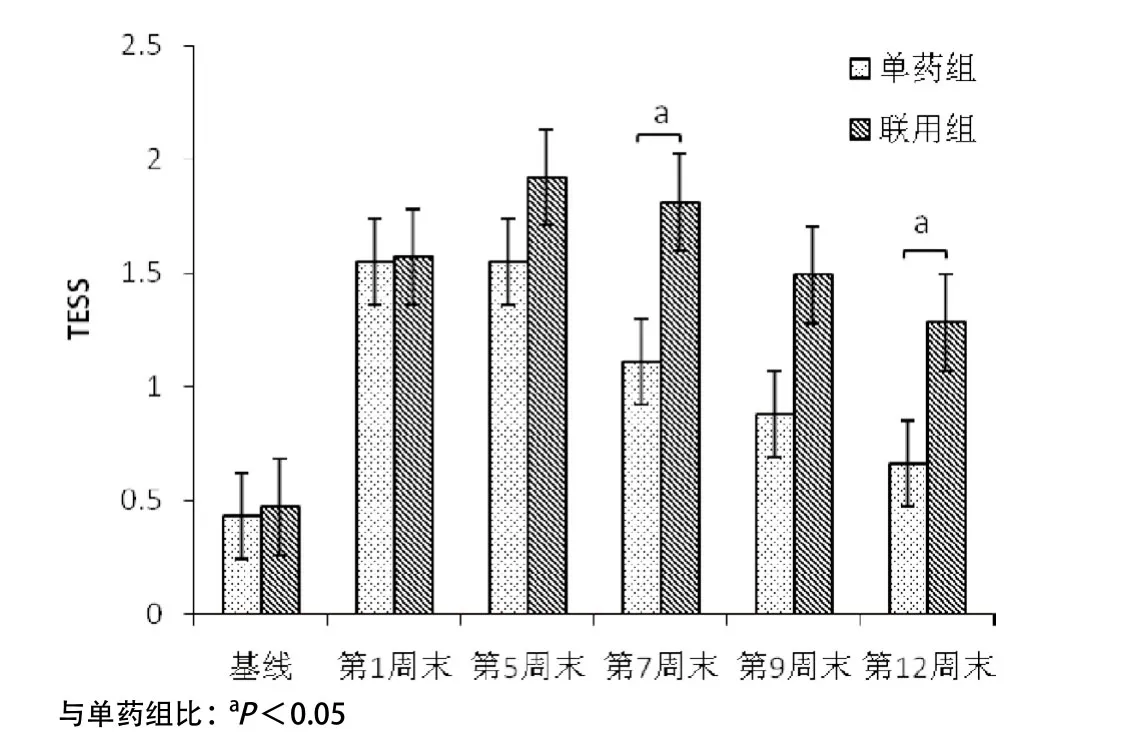
图4 2组间各时间点TESS评分比较
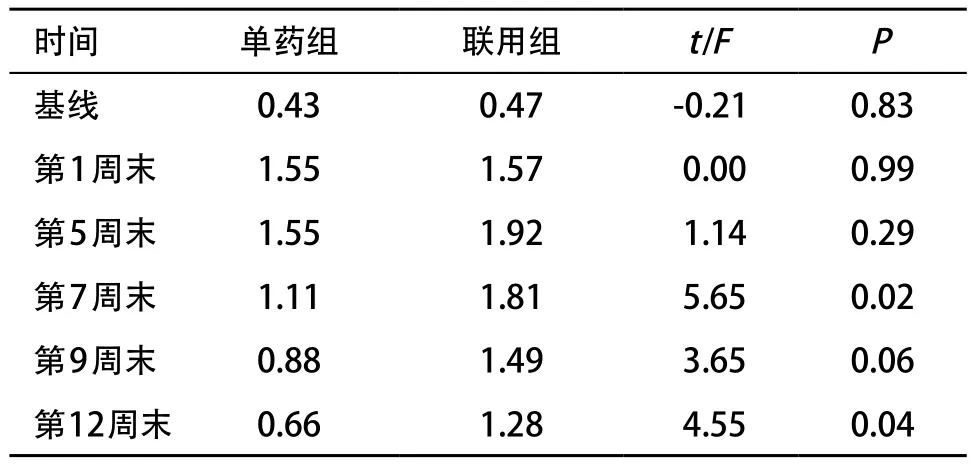
表5 2组各时间点TESS评分比较
3 讨论
随着人们对精神分裂症治疗研究的进一步深入,抗精神病药物所带来的对代谢方面的影响越来越受到人们的重视。精神分裂症代谢综合征(metabolic syndrome,MS)是一种多系统代谢紊乱的复杂疾病,如中心性肥胖(腹型肥胖)、高血糖、高血压及血脂异常等临床综合征将严重影响人类健康。尽管不同抗精神病药物对血糖水平的影响程度并不平衡,但药物引起血糖的升高趋势毋庸置疑[5-6]。徐爱良等[7]认为:如果排除住院生活方式、饮食等影响因素,可以认为抗精神病药物治疗是精神分裂症患者血脂异常的主要危险因素。因此,我们希望能找到一种既能在早期快速地控制精神病性症状,又能巩固及维持期保证疾病的稳定,同时减少药物对代谢方面(如血糖等)影响的治疗方法,从而改善患者的生活质量,减轻患者的相关风险,提高患者的服药依从性,更好地恢复患者的社会功能。
Simpson等[8]的研究中,比较了齐拉西酮和奥氮平治疗急性住院精神分裂症和分裂样精神障碍的疗效和安全性,结果显示两药的疗效相当。齐拉西酮作为新型的非典型抗精神病药物,其特点是长期服用对代谢的影响较小。但其在低剂量(40~80 mg/d)时可拮抗5HT2A受体,但不足以拮抗D2受体,其可能导致激活现象,患者在临床上可能出现激越、焦虑的表现[9-10]。奥氮平是一类多受体阻抗药物,其5HT2>D2受体占据的机制及对H1受体的拮抗作用表明其与氯氮平一样对兴奋、激越的患者有较为确切的作用;与本研究结果相似,在治疗起始5周PANSS评分显著下降,早期的联用对精神病性症状能起到快速有效的控制。临床研究[11]证实,糖化血红蛋白的寿命与红细胞的寿命相近,并且在正常生理条件下,人体内糖化血红蛋白浓度始终保持在一个相对稳定状态。糖化血红蛋白的检测能够在一定程度上反映患者检测前近8~12周血糖的控制情况,而空腹血糖反映的是当前患者的代谢状况。较多的研究也提示在非典型抗精神病药物中,奥氮平和氯氮平对血糖等代谢相关方面的影响较大,其次是喹硫平和利培酮,而齐拉西酮、阿立哌唑和氨磺必利的风险最低[12]。故本研究设计单药组在5周后渐停奥氮平,以齐拉西酮单药巩固治疗,同时2组患者的饮食及运动量状况统一,门诊患者加强告知定期复诊。2组患者的PANSS评分在第7、第9、第12周末的比较差异无统计学意义;组内比较显示,第5周末单药组逐步停止联用奥氮平后,患者并没有因单用齐拉西酮维持治疗而发生病情的反复。组内比较单药组在逐步停用奥氮平后,空腹血糖的数值有所下降,但前后差异没有统计学意义;而联用组继续联用奥氮平治疗,空腹血糖明显升高,前后比较差异有统计学意义。2组间空腹血糖在第9、第12周末的比较差异有统计学意义,联用组高于单药组。说明在病情控制后继续联用奥氮平将会使血糖明显升高,影响患者的代谢,引起一系列的代谢问题。糖化血红蛋白在第12周末相比第5周末单用组有明显降低,差异有统计学意义;联用组差异无统计学意义,组间在各时间点的比较差异无统计学意义,这与以往的研究[13]结果基本一致。由上结果分析可以看得出治疗5周后,逐步地将奥氮平减少并停止并没有对患者已经控制的病情产生很大的影响,而之后以齐拉西酮单药治疗下,维持患者病情稳定的同时对患者代谢方面(如血糖等)影响较小,是相对理想的巩固、维持治疗的手段之一,有利于患者长期维持治疗。
早期齐拉西酮联用奥氮平治疗可以较好地控制精神病性症状,巩固期渐停奥氮平,不会对患者的病情产生明显的影响,同时可以减轻药物对血糖等代谢方面的影响,减少了患者罹患代谢综合征的风险。
[1] Chwieduk CM, Keating GM. Paliperidone extended release: A review of its use in the management of schizophrenia[J]. Drugs, 2010, 70(10): 1295-1317.
[2] 方泽忠, 连国民. 五种非典型抗精神病药物对血糖及血脂水平影响的对照研究[J]. 浙江临床医学, 2008, 10(3): 319-320.
[3] Wirshing DA, Spellberg BJ, Erhart SM, et al. Novel antipsychotics and new onset diabetes[J]. Biol Psychiatry, 1998, 44(8): 778-783.
[4] 罗诚, 杨俊伟, 任继平. 奥氮平对精神分裂症患者血脂、体质量的影响研究[J]. 精神医学杂志, 2008, 21(1): 46-47.
[5] Karayal ON, Glue P, Bachinsky M, et al. Switching from quetiapine to ziprasidone: a sixteen-week, open-label, multicenter study evaluating the effectiveness and safety of ziprasidone in outpatient subjects with schizophrenia or schizoaffective disorder[J]. J Psychiatr Pract, 2011, 17(2): 100-109.
[6] Baptista T, Serrano A, Uzcátegui E, et al. The metabolic syndrome and its constituting variables in atypical antipsychotic-treated subjects: comparison with other drug treatments, drug-free psychiatric patients, frst-degree relatives and the general population in Venezuela[J]. Schizophr Res, 2011, 126(1-3): 93-102.
[7] 徐爱良, 金燕君, 蔡文治. 精神分裂症患者药物治疗后血糖、血脂和尿酸代谢变化及相关因素分析[J]. 温州医学院学报, 2013, 43(5): 340-342.
[8] Simpson GM, Glick ID, Weiden PJ, et al. Randomized, controlled, double-blind muhicenter comparison ot the effcacy and tolerability of ziprasidone and olanzapine in acutely ill in patients with schizophrenia or schizoaffective disorder[J]. Am J Psychiatry, 2004, 161(10): 1837-1847.
[9] Stahl SM, Shayegan DK. The psychopharmacology of ziprasidone: receptor-binding propreties and real-world psychiatric practice[J]. J Clin Psychiatry, 2003, 64 Suppl 19: 6-12.
[10] Caley CF, Cooper CK.Ziprasidone: the fifth atypical antipsychotic[J]. Ann Phannacother, 2002, 36(5): 839-851.
[11] 刘洁, 张卫星. 糖化血红蛋白检测在2型糖尿病患者中的应用与分析[J].中国医药指南, 2014, 12(1): 22-23.
[12] Scheen AJ, De Hert MA. Abnormal glucose metabolism in patients treated with antipsychotics[J]. Diabetes Metab, 2007, 33 (3): 169-175.
[13] Zhang Y, Dai G. Effcacy and metabolic infuence of paliperi done ER, aripiprazole and ziprasidone to patients with frstepisode schizophrenia through 52 weeks follow-up in China [J]. Hum Psychopharmacol, 2012, 27(6): 605-614.
(本文编辑:吴彬)
Efficacy of ziprasidone and olanzapine in treating patients with schizophrenia and their influences onblood glucose and glycosylated hemoglobin at early stage of course of treatment
ZHOU Yong1,2, HUANG Hanjin2, TANG Jianliang3. 1.Department of Neurology, the Second Affiliated Hospital of Wenzhou Medical University, Wenzhou, 325027; 2.Department of Geriatrics, Kangci Hospital of Jiaxing, Jiaxing, 314500; 3.The First Hospital of Tongxiang, Jiaxing, 314500
Objective: To explore the effcacy of ziprasidone and olanzapine in treating patients with schizophrenia and their infuences on blood glucose and glycosylated hemoglobin at early stage of course of treatment. Methods: 197 cases of schizophrenia patients were randomly divided into experimantal group (99 cases administered only with ziprasidone) and control group (98 cases administered with ziprasidone and olanzapin). All the patients were selected from 7 different psychiatric hospital who were diagnosed from 2013.1-2014.1. Both groups were administered with olanzapin and olanzapine at the frst 5 weeks. Then olanzapine was abandoned gradually in experimental group, while the control group went on its original treatment both groups were treated for 12 weeks. Scores of PANSS, level of blood glucose and glycosylated hemoglobin were compared between the two groups before treatment and the 1st, 5st, 7st, 9st, 12stweekend after treatment. Results: Both groups showed signifcant decrease after the treatment (P<0.05), but there’s no statistical difference at every time point (P>0.05). The level of limosis blood glucose in control group was higher than that in experimental group at the 9thand 12thweekend (P<0.05). There’s no statistical difference at the level of glycosylated hemoglobin in both groups by every time point (P>0.05). Conclusion: The effcacy of single ziprasidone and combination treatment is similar, but single ziprasidone at later stage shows more beneft for blood glucose control and meanwhile shows relatively reliable effcacy.
schizophrenia; ziprasidone; olanzapine; metabolic syndrome; glycosylated hemoglobin
R749.3
B
10.3969/j.issn.2095-9400.2015.09.011
2015-03-05
嘉兴市科技计划项目(2014AY21064)。
周勇(1979-),男,安徽淮南人,副主任医师,在职硕士生。
黄汉津,主任医师,硕士生导师,Email:hhj@wmu. edu.cn。

