羟考酮复合舒芬太尼用于腹腔镜下结直肠癌根治术术后镇痛的效果
钞海莲,杨晓平,李 荣,张新侠,赵会利,齐炜红,雷晓鸣(西安交通大学第二附属医院麻醉手术科,西安 70004;西安交通大学第二附属医院胸外科;通讯作者,E-mail:leixiaoming007@63.com)
腹腔镜下结直肠癌根治术是目前广泛开展的手术方式,具有创伤小、恢复快的优点,但术后常伴有切口痛、内脏痛,处理不当可能会转为慢性疼痛。舒芬太尼是高选择性μ受体激动药,已广泛应用于术后镇痛,但难以完全消除内脏痛,剂量过大会引起呼吸抑制、恶心呕吐等副作用。研究证实κ受体在内脏痛中起着重要的作用[1]。羟考酮是μ、κ受体双重激动剂,对κ受体具有较强的激动作用,对内脏痛有着更好的镇痛效果。本研究拟观察羟考酮和舒芬太尼联合使用对腹腔镜结直肠癌根治术的镇痛效果,为此类手术患者寻求安全有效的术后镇痛方法。
1 资料与方法
1.1 一般资料
选择我院2013-06~2014-12全麻下择期行腹腔镜结直肠癌根治术90例,ASAⅠ-Ⅱ级,年龄41-76岁,体重45-78 kg,男68例,女22例,体质量指数18-28 kg/m2。经西安交通大学第二附属医院伦理委员会通过,患者及家属知情同意并签署知情同意书。排除标准:①阿片类药物滥用史;②长期使用阿片类药物治疗慢性疼痛史;③肝肾功能不全;④有精神疾病史或长期应用精神类药物;⑤术中改为开腹手术者。采用随机数字表法随机分为三组,每组 30 例:S1 组(舒芬太尼 2.0 μg/kg)、S2 组(舒芬太尼 1.0 μg/kg)、S+O 组(舒芬太尼 1.0 μg/kg+羟考酮0.2 mg/kg)。
1.2 麻醉方法
患者入室后开放上肢静脉,输注复方氯化钠液。常规监测 SBP、DBP、HR、ECG、SpO2;监测脑电双频谱指数(bispectral index,BIS)和四个连串刺激(train of four,TOF)。麻醉诱导:咪达唑仑 0.05 mg/kg,丙泊酚 2 mg/kg,舒芬太尼 0.5 μg/kg,眼睑反射消失后,静脉注射顺阿曲库铵0.15 mg/kg,BIS <50、TOF值<0.25时行气管插管。连接麻醉机行机械通气,潮气量8 ml/kg,呼吸频率12次/min,吸呼比1∶2,吸入氧浓度50%,PETCO2维持在35-45 mmHg。麻醉维持靶控输注丙泊酚,血浆靶浓度3-4 μg/ml,瑞芬太尼血浆靶浓度4-8 ng/ml,顺阿曲库铵0.15 mg/(kg·h)。维持BIS 40-50。人工气腹压维持在12 mmHg。手术结束前20 min停止顺阿曲库铵输注,解除气腹时停止丙泊酚和瑞芬太尼输注,TOF>0.8,BIS>80时拔除气管导管,送苏醒室观察30 min后送返病房。
1.3 镇痛方法
三组解除气腹时给予舒芬太尼0.1 μg/kg,连接镇痛泵,S1组术后镇痛采用舒芬太尼2.0 μg/kg+托烷司琼10 mg/100 ml,S2组采用舒芬太尼1.0 μg/kg+ 托烷司琼 10 mg/100 ml,S+O 组采用舒芬太尼 1.0 μg/kg+ 羟考酮 0.2 mg/kg+ 托烷司琼10 mg/100 ml,三组镇痛泵均用生理盐水稀释,背景剂量2 ml,每次自控给药量2 ml,锁定时间15 min。VAS评分 >6分追加哌替啶 50-100 mg肌注。
1.4 观察指标
三组术毕(T1)及术后6 h(T2)、12 h(T3)、24 h(T4)与48 h(T5)VAS评分、Ramsey镇静评分以及呼吸频率;术后48 h PCA有效按压次数;上腹部不适等不良反应发生情况。
1.5 统计学分析
2 结果
2.1 一般情况
三组患者性别、年龄、身高、体重、ASA分级以及手术时间的差异无统计学意义(P>0.05,见表1)。
2.2 术后VAS评分和Ramsey镇静评分比较
三组术后各时点疼痛VAS评分均<4分,T2-T4时S2组疼痛VAS评分明显高于S1、S+O组(P<0.05);S1组Ramsey镇静评分高于S2、S+O组(P<0.05,见表2)。
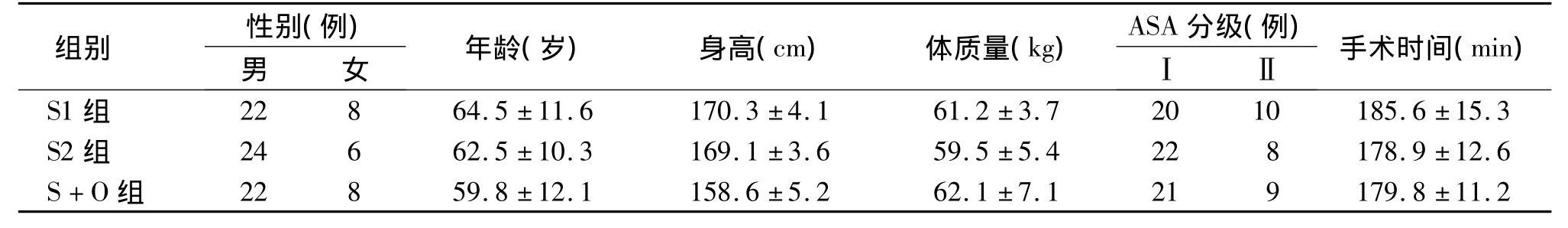
表1 三组患者一般资料的比较 (n=30)Table 1 General clinical data of the patients in three groups (n=30)
表2 三组患者术后各时点VAS和Ramsay评分的比较(±s,n=30)Table 2 Comparison of VAS and Ramsay scores at different postoperative time among three groups(±s,n=30)

表2 三组患者术后各时点VAS和Ramsay评分的比较(±s,n=30)Table 2 Comparison of VAS and Ramsay scores at different postoperative time among three groups(±s,n=30)
与 S1、S+O 组相比,#P <0.05;与 S2、S+O 组相比,★P <0.05
指标 组别 T1 T2 T3 T4 T5 VAS S1组2.5 ±1.1 2.0 ±1.4 1.9 ±1.0 1.7 ±0.7 1.1 ±0.6 S2 组 2.6 ±1.4 3.1 ±1.0# 2.9 ±0.8# 2.0 ±0.4# 1.2 ±0.5 S+O 组 2.4 ±0.8 1.9 ±1.2 1.8 ±0.6 1.8 ±0.7 1.2 ±0.8 Ramsay S1 组 3.3 ±0.8 3.2 ±1.2★ 2.9 ±0.6★ 2.8 ±0.7★ 2.0 ±0.4 S2 组 3.6 ±1.0 2.8 ±0.9 2.5 ±0.4 2.2 ±0.2 1.9 ±0.4 S+O组3.4 ±1.0 2.7 ±0.7 2.4 ± o.7 2.1 ±0.4 2.0 ±0.5
2.3 三组自控镇痛按压次数比较
三组自控镇痛按压次数比较。48 h内S+O组自控镇痛按压次数明显低于S1、S2组(2.1±0.6 vs 4.6 ±1.2,6.5 ±2.6,P <0.05)。
2.4 不良反应
三组均未发生低血压和呼吸抑制等不良反应。与S2、S+O组比较,S1组恶心、呕吐、头晕、嗜睡发生率明显升高(P<0.05)。与S1、S2组比较,S+O组下腹部疼痛不适的发生率明显降低(P<0.05,见表3)。

表3 三组患者术后不良反应的比较 [n=30,例(%)]Table 3 The incidences of adverse reactions in three groups [n=30,cases(%)]
3 讨论
腹腔镜结直肠癌根治术创伤小、视野清楚、恢复快,已成为临床常见的手术方式,但术后也常伴有切口痛、内脏痛以及背部疼痛等,原因主要有CO2气体的残留,胃肠道的牵拉,肠道血流阻断,手术伤口的创伤、感染,腹腔内炎性渗出物的刺激,精神因素等。其中以内脏痛为甚,主要表现为下腹部的胀痛。内脏痛所涉及的病理生理机制尚不完全清楚,目前认为位于内脏神经中的κ受体起着重要的作用。
阿片类药物是目前最常用的术后镇痛药。舒芬太尼选择性激动μ阿片受体,脂溶性强,镇痛效应是芬太尼的5-10倍,已广泛应用于术后镇痛[2]。舒芬太尼用于静脉镇痛的作用机制是直接作用于脊髓、延髓和中脑等痛觉传导区μ阿片受体,并与之相结合,从而产生确切的镇痛效果[3]。临床应用时因参数设定的差异可出现术后镇痛不全或增加不良反应,背景剂量过大可出现明显的呼吸抑制、镇静过度、恶心、呕吐、头晕和嗜睡等,严重者出现低血压和心动过缓,背景输注速率过低可出现镇痛不全[4]。
本研究结果显示,当舒芬太尼采用1.0 μg/kg时,患者术后6,12,24 h的VAS分明显高于其他两组,48 h内自控镇痛按压次数及下腹部疼痛不适的发生率亦明显高于其余两组,说明采用此背景剂量镇痛不足。当舒芬太尼增加至2 μg/kg时,患者术后6-24 h时VAS评分下降,但自控镇痛按压次数和术后下腹部不适发生率依然高于S+O组,同时恶心呕吐、头晕和嗜睡不良反应的发生率明显升高,说明单纯增加镇痛泵里舒芬太尼的剂量来减轻术后疼痛并非完善的方法。也验证了腹腔镜结直肠癌根治术后疼痛主要来源于内脏痛。同时我们发现S1组患者术后6,12,24 h Ramsay评分升高,说明舒芬太尼可以产生镇静作用,与刘礼胜等的研究结果[5]一致。三组患者均未出现呼吸抑制,亦与 Conti等[6]研究发现的舒芬太尼并不引起显著的呼吸动力、分钟通气量和呼吸频率的改变等研究结果一致。但老年患者阿片受体对阿片类药更加敏感,提示我们在应用于老年患者时应注意镇静过度和呼吸抑制的风险。
羟考酮是μ、κ阿片受体激动剂,其药理作用包括镇痛、抗焦虑、止咳和降低平滑肌张力等,其镇痛无封顶效应[7]。由于其κ受体激动作用,因此对内脏痛较单纯μ受体激动剂有更好的镇痛效果[8]。本研究结果显示舒芬太尼和羟考酮联合使用后术后VAS评分与S1组患者无明显不同,48 h内自控镇痛按压次数较S1组明显减少,下腹部疼痛不适发生率较S1、S2两组明显下降,说明其能够有效缓解腹腔镜结直肠癌根治术患者的术后疼痛。有研究表明使用羟考酮的术后恶心呕吐发生率低于吗啡[9]。本研究结果显示S+O组患者联合使用舒芬太尼和羟考酮恶心呕吐、头晕和嗜睡的发生率明显较S1组减少,与以往研究结果一致[10,11]。
综上所述,羟考酮和舒芬太尼联合应用于腹腔镜下行结直肠癌根治术患者的术后镇痛效果优于单纯使用舒芬太尼,能够有效缓解术后疼痛,降低不良反应的发生率,是一种安全有效的镇痛方法,但两者联用的最佳剂量尚需进一步研究。
[1]Riviere PJ.Peripheral kappa-opioid agonists for visceral pain[J].Br J Pharmacol,2004,141(8):1331-1334.
[2]Zhao Y,Duan JL,Wu XM,et al.Two-stage analysis of pharmacokinetics of sufentanil administered by target-controlled infusion in Chinese patients[J].Chin Med J(Engl),2009,122(17):1979-1984.
[3]De Brito Cancado TO,Omais M,Ashmawi HA,et al.Chronic pain after cesarean section.Influence of anesthetic/surgical technique and postoperative analgesia[J].Rev Bras Anestesiol,2012,62(6):762-774.
[4]Draisci G,Frassanito L,Pinto R,et al.Safety and effectiveness of coadministration of intrathecal sufentanil and morphine in hyperbaric bupivacaine-based spinal anesthesia for cesarean section[J].J Opioid Manag,2009,5(4):197-202.
[5]刘礼胜,张兴安,邵伟栋,等.麻醉诱导期间靶控输注舒芬太尼对丙泊酚镇静作用的影响[J].中国药房,2010,21(16):1469-1472.
[6]Conti G,Arcangeli A,Antonelli M,et al.Sedation with sufentanil in patients receiving pressure support ventilation has no effects on respiration:a pilot study[J].Can J Anaesth,2004,51(5):494-499.
[7] 徐建国.疼痛药物治疗学[M].北京:人民卫生出版社,2007:93-117.
[8]Koch S,Ahlburg P,Spangsberg N,et al.Oxycodone vs Fentanyl in the treatment of early post-operative pain after laparoscopic cholecystectomy:a randomized double-blind study[J].Acta Anaesthesiol Scand,2008,52(6):845-850.
[9]许幸,吴新民,薛张纲,等.盐酸羟考酮注射液用于全麻患者术后镇痛的有效性和安全性:前瞻性、随机、盲法、多中心、阳性对照临床研究[J].中华麻醉学杂志,2013,33(3):269-274.
[10]申红兰,玄光日.羟考酮不同给药方式治疗晚期癌性疼痛的疗效观察[J].医学理论与实践,2014,27(16):2178-2179.
[11]张庆梅,夏晓琼,王炎,等.羟考酮联合帕瑞昔布钠对胃癌根治术术后镇痛的影响[J].临床麻醉学杂志,2014,30(10):989-991.

