碳纳米点为还原剂的纳米金制备及其催化性能研究
杨瑞桥,张友玉
(1.湖南幼儿师范高等专科学校,中国常德 415000;2.湖南师范大学化学化工学院,中国长沙 410081)
金纳米(AuNPs)由于其独特的物理和化学性质受到研究者们的广泛关注,在传感器[1]、电子[2]、光学[3]、检测[4]和催化领域[5]展现出良好的应用前景.比如,研究者们利用诱导AuNPs 聚集引起的颜色变化,构建了一系列的比色传感器用于Hg2+[6]、葡萄糖[7]和DNA[8]等的检测;基于AuNPs 可以降低电化学反应的超电势和维持氧化还原的可逆性,构建了基于AuNPs 的电催化和电化学传感器[9-10];同时AuNPs 还广泛地应用于催化领域,如作为醇氧化的催化剂[11].
目前,AuNPs 制备通常是利用还原剂还原氯金酸,需加入一定量的钝化剂或保护剂,以避免AuNPs 的聚集[12-14].合成过程中必须使用还原剂,如硼氢化钠、柠檬酸钠等.硼氢化钠作为一种高活性的化学物质具有潜在的环境危害;而以柠檬酸钠为还原剂则整个反应过程需要在沸水中进行,消耗能量.因此,发展一种环境友好与条件温和的AuNPs 制备方法具有非常重要的意义.
本文发展了一种以荧光碳纳米点(C-dots)为还原剂和稳定剂合成AuNPs 的方法,合成的纳米金具有优异的催化性能,可将水中的对硝基酚催化还原成对氨基酚,并研究了其催化反应动力学,该结果对处理废水中的酚类化合物具有参考价值.
1 实验部分
1.1 仪器与试剂
试剂:氯金酸、乙二醇、氢氧化钠、盐酸、对硝基酚和硼氢化钠购自国药集团化学试剂有限公司.所有试剂均为分析纯.水为实验室自制双重蒸馏水.
仪器:PL303 电子天平(梅特勒-托利多上海有限公司),ZNCL-G 磁力搅拌器(巩义市予华仪器有限公司),JEOL-1230 型透射电镜(JEOL,日本),UV-2450 型分光光度计(Shimazu,日本),F-4500 荧光光谱仪器(Hitachi,日本).
1.2 AuNPs 的合成
以乙二醇为原料通过电化学方法制备了C-dots,并将所得到的C-dots 作为还原剂和稳定剂合成了AuNPs.具体方法如下:以98 mL 乙二醇溶液和2 mL 0.5 g·mL-1的NaOH 溶液的混合液为电解液,铂片为阴极和阳极,以20 V 的直流电电解1 h,得到C-dots 粗溶液.将粗溶液酸化后,经MW 1000 的透析膜透析2天得到C-dots 溶液.在室温下,往0.1 mg·mL-1的C-dots 溶液中,加入0.2 mmol·L-1HAuCl4溶液,摇匀,静置25 min,即制备得到AuNPs 溶液.
1.3 AuNPs 催化对硝基酚的还原
反应在150 mL 烧杯中进行.向烧杯中加入90 mL 浓度为7.6×10-5mol·L-1对硝基酚溶液和10 mL 浓度为7.2×10-1mol·L-1硼氢化钠溶液,充分混匀,随后加入0.052 mL 浓度为4.2×10-8mol·L-1的金纳米粒子溶液.此时对硝基酚和硼氢化钠的最终浓度分别为6.8×10-5mol·L-1和7×10-2mol·L-1.每两分钟记录一次反应体系的紫外-可见吸收光谱,并记录其400 nm 处的吸光度.
2 结果与讨论
2.1 合成的C-dots 与AuNPs 的表征
通过透射电镜,紫外-可见光谱和荧光光谱对合成的C-dots 和纳米金进行了表征.图1 为C-dots 的电镜图(TEM)和高分辨电镜图(HRTEM).可以看出C-dots 近球形,分布均匀,尺寸分布范围为2~6 nm.HRTEM 显示其具有晶格结构,其相应的晶格间距为0.20 nm,与石墨化的碳(111)面的晶格常数相同(JCPDS 26-1076).
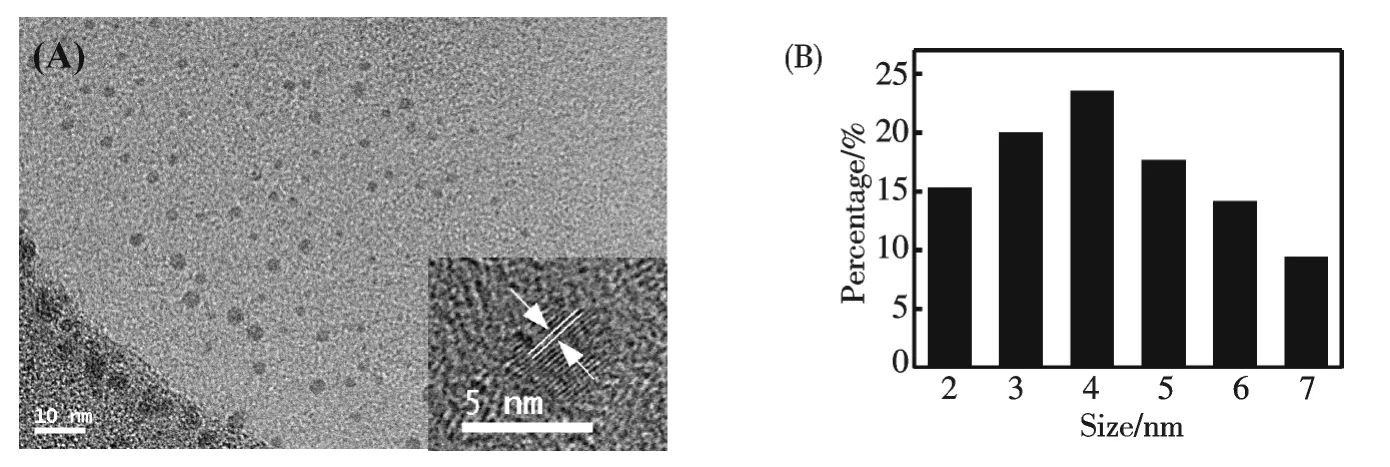
图1 荧光碳纳米点TEM 图(A)和尺寸分布图(B).插图为单个荧光碳纳米点的HRTEM 图Fig.1 (A)Typical TEM image of as-synthesized C-dots,inset:HRTEM image of single C-dots;(B)Size distribution of C-dots
C-dots 的紫外-可见光谱图如图2(A)所示,由图可见在262 nm 处有一个强的吸收峰,归属于π→π*跃迁.图2(B)为C-dots 的荧光光谱图,其最大激发波长为356 nm,相应的最大发射波长为453 nm,并且显示出激发依赖的荧光性质.
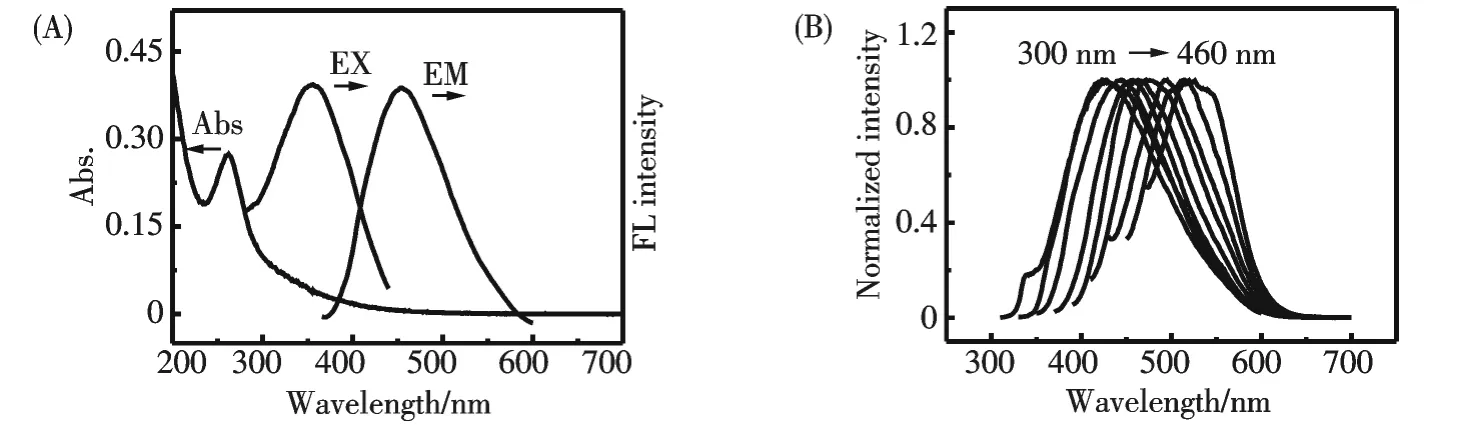
图2 (A)所制得的荧光碳纳米点的紫外-可见和荧光激发、发射光谱图;(B)在不同激发光激发下的归一化的荧光发射光谱图Fig.2 (A)UV-vis spectra and FL spectra of as-synthesized C-dots.(B)Normalized FL emission spectra of C-dots at different excitation wavelengths
合成得到的AuNPs 表征结果如图3所示.从图3 中可以看出AuNPs 成球形,尺寸在14~18 nm 之间;HRTEM 结果揭示AuNPs 晶格间距为0.24 nm,与金(111)面晶格间距相符(JCPDS 04-0784);其紫外-可见光谱如图4所示,在526 nm 处有一个明显的吸收峰,对应于AuNPs 的特征表面等离子共振峰.由于乙二醇的羟基具有还原性,作者推测在以乙二醇为原料合成的C-dots 表面的仍保留有部分高活性的羟基,这部分羟基作为还原基团,将氯金酸还原成AuNPs.

图3 (A)AuNPs 的TEM 图和(B)相应的尺寸分布图.插图为单个AuNPs 的HRTEM 图Fig.3 (A)Typical TEM image of as-synthesized AuNPs,inset:HRTEM image of single AuNPs.(B)Size distribution of AuNPs

图4 所制得的AuNPs 的紫外-可见光谱图Fig.4 UV-vis spectra of as-synthesized AuNPs
2.2 AuNPs 的催化性能
AuNPs 的比表面积大,具有很强的活性,可用作优良的催化剂.作者研究了AuNPs 催化硼氢化钠还原对硝基酚的反应.通过考察其紫外-可见光谱随时间的变化计算求得AuNPs 对催化硼氢化钠还原对硝基酚的反应速率常数,并在同样的条件下,以传统的柠檬酸钠为还原剂制备的AuNPs 做对照,考察两种方法制备的AuNPs 的催化活性.图5A 为对硝基酚水溶液的紫外-可见光谱图,对硝基酚的原始吸收峰位于317 nm 处,当加入硼氢化钠后,生成对硝基酚盐,其吸收峰红移到400 nm 处,相应的颜色也由亮黄色变为黄绿色.尽管硼氢化钠还原对硝基酚在热力学上是可行的[15],但是在没有催化剂的存在下这个反应却很难进行.如图5B所示,当反应体系中没有加入AuNPs 时,吸收峰位移没有明显变化,说明在该实验条件下无AuNPs 催化时对硝基酚不能被硼氢化钠还原.当加入AuNPs 溶液后,反应体系即出现褪色,表明对硝基酚已经开始被硼氢化钠还原,通过记录反应体系的紫外-可见光谱随时间的变化情况可以发现(图6A),反应体系在400 nm 处的吸光度随反应时间的延长逐渐降低,而在300 nm 处出现了一个新的吸收峰,为对硝基苯胺的特征吸收峰,表明AuNPs 成功地催化了硼氢化钠还原对硝基酚.以柠檬酸钠还原制备的AuNPs 替代荧光碳纳米点还原制备的AuNPs,也达到了同样的效果(图6B),在实验中,对硝基酚和硼氢化钠的最终浓度分别为6.8×10-5mol·L-1和7×10-2mol·L-1,后者在反应中大大过量,因此可以近似认为硼氢化钠在反应体系中的浓度不变,反应速率只与对硝基酚的浓度有关,反应为准一级反应.根据朗伯-比尔定律,反应体系在400 nm 处的吸光度值与溶液中对硝基酚的浓度成正比,因此对硝基酚在反应时间t 时400 nm 处的吸光度值At与未加入金纳米粒子催化剂前400 nm 处的空白值A0的比值即为对硝基酚的浓度的比值Ct/C0.图7A 为Ct/C0比值随时间的变化曲线,从图中可以看出,随着时间的延长,Ct/C0的比值不断减小.以ln(Ct/C0)与t 作图(图7B),得到的斜率即为AuNPs 催化硼氢化钠还原对硝基酚反应的反应速率常数.经计算得到以C-dots 为还原剂和柠檬酸钠为还原剂制得的AuNPs 催化硼氢化钠还原对硝基酚反应的反应速率常数分别为0.13 min-1,0.15 min-1.结果表明,以C-dots 为还原剂所制备的AuNPs 与传统方法柠檬酸钠还原法制备的AuNPs 相比,其催化性能相近.
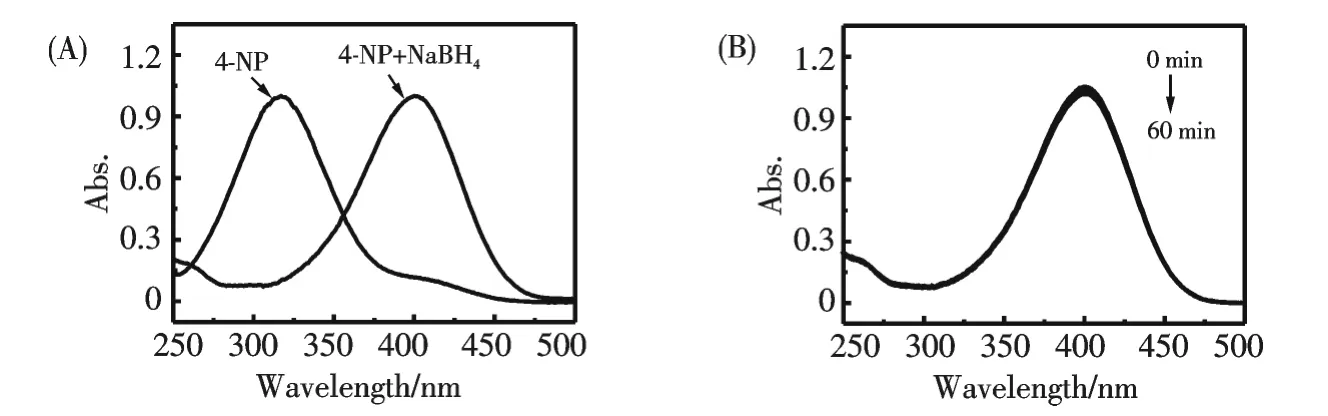
图5 (A)对硝基酚与硼氢化钠混合前后的紫外-可见光谱,(B)无催化剂AuNPs 存在下对硝基酚与硼氢化钠混合溶液的紫外光谱Fig.5 (A)UV-vis spectra of 4-NP in the absence and presence of NaBH4.(B)Normalized absorption spectra of 4-NP and NaBH4 mixture in the absence AuNPs as catalyst

图6 不同时间下AuNPs 催化硼氢化钠还原对硝基酚的紫外-可见光谱图.(A)用C-dots 还原的AuNPs,(B)用柠檬酸钠还原的AuNPsFig.6 UV-vis spectra for the reduction reaction of 4-NP.AuNPs synthesized by(A)C-dots and(B)sodium citrate.

图7 对硝基酚的还原反应动力学曲线.A:C/C0~t,B:ln(C/C0)~t.(曲线a 代表荧光碳纳米点合成的AuNPs 为催化剂,曲线b 代表柠檬酸钠合成的AuNPs 为催化剂)Fig.7 (A)Concentration of 4-NP versus reaction time for the reduction of 4-NP catalyzed by AuNPs synthesized by C-dots(a)and synthesized by sodium citrate(b),respectively.(B)The corresponding kinetic curves for the reduction of 4-NP catalyzed by AuNPs synthesized by C-dots(a)and synthesized by sodium citrate(b)
3 结论
以乙二醇为起始原料,经电化学方法成功地制得了荧光碳纳米点,产物荧光碳纳米点具有很强的还原性,能在无任何其他化学试剂和能量供给的情况下还原氯金酸制备AuNPs,制备的AuNPs 具有强的催化活性,能在温和条件下催化硼氢化钠还原对硝基酚的反应.
[1]SU J,ZHOU W,XIANG Y,et al.Target-induced charge reduction of aptamers for visual detection of lysozyme based on positively charged gold nanoparticles[J].Chem Commun,2013,49(69):7659-7661.
[2]LEE C H,QIN S,SAVAIKAR M A,et al.Room-temperature tunneling behavior of boron nitride nanotubes functionalized with gold quantum dots[J].Adv Mater,2013,25(33):4544-4548.
[3]SHIMADA T,IMURA K,OKAMOTO H,et al.Spatial distribution of enhanced optical fields in one-dimensional linear arrays of gold nanoparticles studied by scanning near-field optical microscopy[J].Phys Chem Chem Phys,2013,15(12):4265-4269.
[4]WANG J,WANG L,LIU X,et al.A gold nanoparticle-based aptamer target binding readout for ATP assay[J].Adv Mater,2007,19(22):3943-3946.
[5]LU Y M,ZHU H Z,LI W G,et al.Size-controllable palladium nanoparticles immobilized on carbon nanospheres for nitroaromatic hydrogenation[J].J Mater Chem A,2013,1(11):3783-3788.
[6]LIU D,QU W,CHEN W,et al.Highly sensitive,colorimetric detection of mercury(II)in aqueous media by quaternary ammonium group-capped gold nanoparticles at room temperature[J].Anal Chem,2010,82(23):9606-9610.
[7]JIANG Y,ZHAO H,LIN Y,et al.Colorimetric detection of glucose in rat brain using gold nanoparticles[J].Angew Chem,2010,122(28):4910-4914.
[8]LIU P,YANG X,SUN S,et al.Enzyme-free colorimetric detection of DNA by using gold nanoparticles and hybridization chain reaction amplification[J].Anal Chem,2013,85(16):7689-7695.
[9]SHAN C,YANG H,HAN D,et al.Graphene/AuNPs/chitosan nanocomposites film for glucose biosensing[J].Biosens Bioelectron,2010,25(5):1070-1074.
[10]LIU M,CHEN Q,LAI C,et al.A double signal amplification platform for ultrasensitive and simultaneous detection of ascorbic acid,dopamine,uric acid and acetaminophen based on a nanocomposite of ferrocene thiolate stabilized Fe3O4@Au nanoparticles with graphene sheet[J].Biosens Bioelectron,2013,48(1):75-81.
[11]ZHANG P I,QIAO Z A,JIANG X,et al.Nanoporous ionic organic networks:stabilizing and supporting gold nanoparticles for catalysis[J].Nano Lett,2015,15(2):823-828.
[12]ZHANG J,WANG L,PAN D,et al.Visual cocaine detection with gold nanoparticles and rationally engineered aptamer structures[J].Small,2008,4(8):1196-1200.
[13]YANG D,MA J,ZHANG Q,et al.Polyelectrolyte-coated gold magnetic nanoparticles for immunoassay development:toward point of care diagnostics for syphilis screening[J].Anal Chem,2013,85(14):6688-6695.
[14]TSUNOYAMA H,SAKURAI H,NEGISHI Y,et al.Size-specific catalytic activity of polymer-stabilized gold nanoclusters for aerobic alcohol oxidation in water[J].J Am Chem Soc,2005,127(26):9374-9375.
[15]JIN R,XING Y,YU X,et al.Facile synthesis of well-dispersed silver nanoparticles on hierarchical flower-like Ni3Si2O5(OH)4with a high catalytic activity towards 4-nitrophenol reduction[J].Chem Asian J,2012,7(12):2955-2961

