高效液相色谱–电感耦合等离子体质谱联用法测定海水中的烷基汞*
陈念念,刘小骐,李艳苹,潘献辉
(国家海洋局天津海水淡化与综合利用研究所,天津 300192)
目前,海产品中的重金属富集现象越来越严重,其中以汞元素最为显著。汞具有多种形态,如单质汞、无机汞、甲基汞、乙基汞及其它有机汞化合物[1]。在所有汞的形态中,有机汞比无机汞的毒性强,其中甲基汞是最具毒性的汞形态[2]。在水体环境中,无机汞可以通过微生物作用转化为甲基汞,进一步被水生动植物吸收、富集,并通过食物链被放大,进而威胁人体健康[3]。
汞元素的形态分析方法大多基于不同的分离和检测联用系统[4–11],如将高效液相色谱(HPLC)、气相色谱(GC)、毛细管电泳(CE)、离子色谱(IC)等与原子吸收光谱(AAS)、原子荧光光谱(AFS)、电感耦合等离子发射光谱(ICP–AES)或质谱(ICP–MS)等检测方法相结合而进行测定的分析方法[12]。其中HPLC–ICP-MS具有较高的分辨率和灵敏度,更宽的线性范围,相对少的基体干扰,因而成为目前汞形态分析中首选的联用方法。此外,该方法还具有接口简单、应用范围广、前处理过程简便而有利于保持待测样品原始形态不变等优点[8],在汞形态分析中已有不少应用[4,9–10]。
一般公海海域中,海水中汞的含量约为1~20 ng/L,近海海水由于人为排放等因素,汞的质量浓度可达100 ng/L以上[13]。通常海水中盐分较高,如含有较高浓度的Na+,K+,Ca2+,Mg2+,Cl–。相对于淡水水域,海水中汞形态分析方法通常较为复杂,针对这一难点,目前文献报道的海水中汞形态的检测方法主要基于样品的浓缩富集,如液–液微萃取(liquid–liquid microextraction,LLME)[14],浊 点 萃取(cloud point extraction,CPE)[15]、沉浸液滴微萃取(immersed single drop microextraction,SDME)[16]、固相微萃取(solid phase extraction,SPE)[17],在线阳离子交换树脂上吸附洗脱富集等[2,18]。这些方法能实现较高的检测灵敏度,但存在着样品处理过程复杂、耗时,检测精度与准确度无法保证等问题。
笔者建立了HPLC–ICP–MS联用方法,对海水中的甲基汞、乙基汞进行测定,该方法无需样品前处理,简便、快速、稳定,测量精密度、准确度满足要求。
1 实验部分
1.1 主要仪器与试剂
ICP–MS仪:iCAP Qc型,美国赛默飞世尔科技(中国)有限公司;
超声波清洗仪:KQ3200B型,昆山超声仪器有限公司;
纯水仪:Milli-Q型,密理博(中国)有限公司;
甲基汞标准溶液:编号为GBW 08675,国家标准物质信息中心;
乙基汞标准溶液:编号为GBW(E)081524,国家标准物质信息中心;
乙酸铵:分析纯,国药集团化学试剂有限公司;
甲醇:HPLC级,美国赛默飞世尔科技(中国)有限公司;
张良俊[24]等根据实验数据分析了热力膨胀阀在空气源热泵热水器中的稳定特性,提出了其在空气源热泵热水器全年运行工况中存在的局限性,并指出只有同时把握好热力膨胀阀开度和制冷剂充注量,才能保障系统的安全稳定运行。
L-半胱氨酸:纯度为98%,英国阿尔埃莎公司;
硝酸、氨水:优级纯。
1.2 仪器工作条件
1.2.1 HPLC仪
色谱柱:Acclaim C18柱(50 mm×4 mm,5 μm);柱温:25℃;流动相:60 mmol/L乙酸铵溶液–5%甲醇–10 mmol/L L-半胱氨酸,pH 7.5,流量为1.0 mL/min;进样体积:50 μL。
1.2.2 ICP-MS仪
RF功率:1 550 W;冷却气流量:14 L/min;辅助气流量:0.79 L/min;雾化气流量:1.05 L/min;采样深度:5.0 mm;待测质量数:202Hg;数据采集模式:Transient TRA;驻留时间:200 ms;定量方式:FullQuant;Start/Stop模式:Auto Trigger。
1.3 样品采集和处理
采样器皿为聚四氟乙烯材料,所有容器在使用前均于浓HNO3中浸泡至少24 h。海水样品在分析前采用0.45 μm微孔纤维滤膜过滤,若不能即刻分析,则需密封冷冻。
2 结果与讨论
2.1 色谱条件的选择
在汞形态分析中,常用反相高效液相色谱作为分离方法,且大多使用C18色谱柱。在反相键合色谱中,固定相的极性小于流动相的极性,适合于分离非极性、极性和离子型化合物[4]。本法采用Acclaim C18分析柱,选择适当的络合剂与汞化合物反应,生成非极性化合物在反相柱上进行分离。
2.1.1 络合剂
常见的络合剂多为含硫化合物,如吡咯烷二硫代氨基甲酸(APDC)、L-半胱氨酸(L-Cys)、2-巯基乙醇(2-ME)等。与2-巯基乙醇相比较,L-半胱氨酸绿色环保,安全无毒。L-半胱氨酸的等电点PI值为5.2,当流动相pH值大于PI值时,L-半胱氨酸带负电,可以与MeHg(+)、EtHg(+)形成非极性化合物。各种汞络合物在C18柱上保留较弱,可缩短检测时间,同时可以较好地消除汞的记忆效应,因此选择L-半胱氨酸作为络合剂[4]。实验发现,随着L-半胱氨酸浓度的增加,汞化合物的色谱峰形越来越尖锐,保留时间变短,尤其是乙基汞的保留时间明显缩短,灵敏度大幅提高。当L-半胱氨酸浓度增加到一定值后,色谱峰形、保留时间和灵敏度都不再有明显变化。考虑到L-半胱氨酸浓度过高会损害色谱柱[11],采用10 mmol/L L-半胱氨酸作为汞形态分析的络合剂。
2.1.2 流动相
在流动相中加入少量有机改性剂和缓冲盐,可以更好地改善色谱峰峰形,从而使各种形态的汞在反相柱上得到很好的分离。本实验向流动相中添加5%甲醇及60 mmol/L乙酸铵。
在不同的pH条件下,不同形态的汞不仅质谱检测的灵敏度有较大差异,而且色谱分离度、色谱峰高、拖尾因子、柱效也有很大程度的区别。在pH条件优化过程中,选择10%氨水和硝酸对混合标准溶液(5 μg/L的甲基汞和乙基汞)的pH 值进行调节,结果表明,当pH值在6.5~8.5范围内变化时,EtHg的保留时间以近线性式增加,而MeHg的保留时间则在pH 7.5之后变化显著。从缩短分离时间和控制良好的分离度考虑,pH值宜控制在7.5左右。
当流动相流量在0.4~1.2 mL/min范围内变化时,MeHg和EtHg的保留时间随着流动相流量的增加而缩短,其中EtHg的变化趋势尤为显著。为了缩短分离时间,应选择较大的流动相流量,但流量过大时,带入的盐类不仅容易在ICP-MS 的截取锥锥口沉积,同时对色谱柱的损伤也较为严重。综合考虑,选择流动相流量为1.0 mL/min。
综合上述实验优化结果,流动相组成为60 mmol/L乙酸铵–5%甲醇–10 mmol/L L-半胱氨酸(pH 7.5),流动相流量为1.0 mL/min。
2.2 标准曲线和检出限
以流动相逐级稀释汞形态标准溶液,分别配制0.0,0.1,0.5,1.0,2.0,5.0 μg/L的MeHg和EtHg的混合标准溶液,在上述优化的检测条件下,以峰面积(Y)对标准溶液浓度(X)进行线性回归,计算得线性方程。平行测定7次样品空白溶液,以测定结果标准偏差的3倍作为该方法的检出限。线性范围、回归方程和检出限见表1。

表1 MeHg 和EtHg的线性方程、线性范围、相关系数及检出限
由表1可知,在最优化条件下,MeHg和EtHg的方法检出限分别为5 ng/L和3 ng/L,满足痕量汞形态的检测要求。5.0 μg/L 的混合标准溶液的色谱图见图1。由图1可知,MeHg和EtHg的保留时间分别为77.0,176.3 s,两种汞形态能在5 min内分离并被测定。
2.3 精密度与加标回收试验
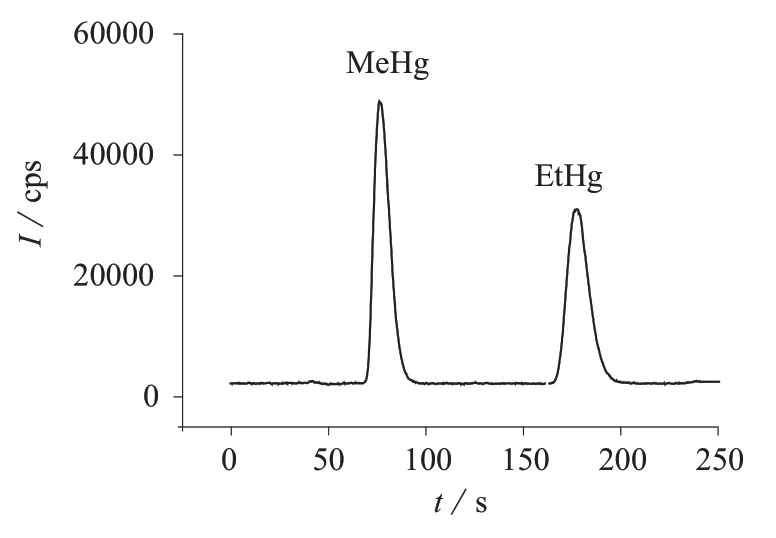
图1 5.0 μg/L 甲基汞和乙基汞混合标准溶液的色谱图
在优化的色谱条件下,对来自天津和唐山的两份海水样品进行测定,并添加0.5 μg/L的混合标准溶液,进行加标回收试验,平行测定7次,加标海水样品的色谱图见图2,加标回收率及其相对标准偏差见表2。由图2可知,海水中的MeHg和EtHg分离良好。由表2可知,两种海水样品中均未检测出MeHg和EtHg,在添加了0.5 μg/L混合标准溶液后,计算得其加标回收率在84%~94%之间,且相对标准偏差不大于4.9%,说明该方法能有效消除海水高盐基体的干扰,且精密度良好。
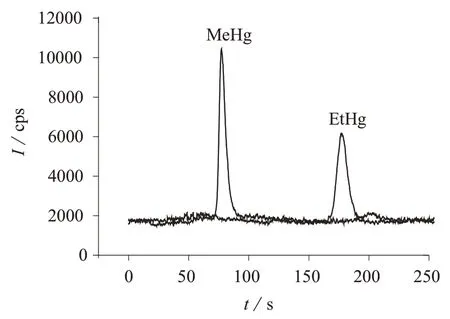
图2 加标(0.5μg/L)海水样品1的色谱图
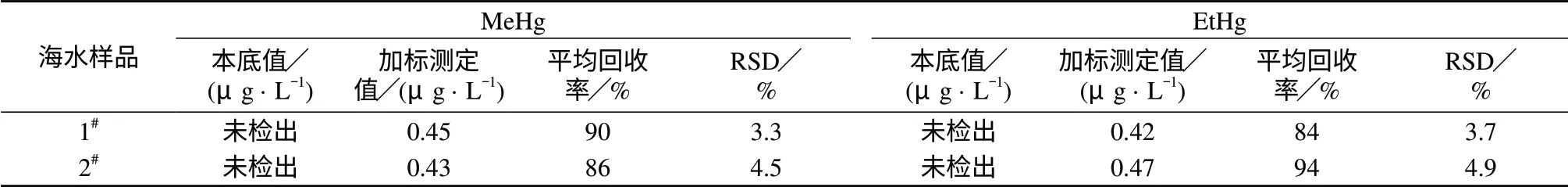
表2 海水样品中汞形态分析测定结果(n=7)
3 结语
通过对色谱和质谱的仪器条件进行优化,采用HPLC–ICP-MS联用法测定海水中的甲基汞和乙基汞,该方法样品处理操作简单,溶剂用量少且绿色环保,耗时短,两种汞形态可以在5 min内分离并检测,且灵敏度高,稳定性好。该方法可用于海水及浓盐水中汞形态的快速分离和检测。
[1]Chen J,Yu X P,Guo Y F,et al. Speciation analysis of mercury in natural water [J]. Rock and Mineral Analysis,2012,31(6): 939–944.
[2]Jia X,Gong D,Han Y,et al. Fast speciation of mercury in seawater by short-column high-performance liquid chromatography hyphenated to inductively coupled plasma spectrometry after online cation exchange column preconcentration[J]. Talanta,2012,88: 724–729.
[3]Driscoll CT,Mason R P,Chan H M,et al. Mercury as a global pollutant:sources,pathways,and effects[J]. Environ Sci Technol,2013,47(10): 4 967–4 983.
[4]梁立娜,江桂斌.高效液相色谱及其联用技术在汞形态分析中的应用[J].分析科学学报,2002,18(4): 338–343.
[5]陈邵鹏,顾海东,秦宏兵.高效液相色谱–氢化物发生–原子荧光光谱联用技术测定水中烷基汞[J].中国环境监测,2012,28(5): 78–82.
[6]江桂斌,顾晓梅,倪哲明,等.毛细管气相色谱–原子吸收法测定生物样品中的有机汞化合物[J].色谱,1991,9(6): 350–352.
[7]陈雪昌,梅光明,张小军,等.高效液相色谱–原子荧光法测定水产品中甲基汞含量[J].食品科学,2012,33(4): 234–237.
[8]李妍,刘书娟,江冬青,等.气相色谱–电感耦合等离子体质谱联用技术应用于水产品中汞形态分析[J].分析化学,2008,36(6): 793–798.
[9]高尔乐,何滨,江桂斌,等.酸浸提–HPLC–ICP-MS 系统测定土壤与底泥样品中的甲基汞、乙基汞[J].环境化学,2008,27(5): 698–700.
[10]陈玉红,米健秋,张兰.高效液相色谱–电感耦合等离子体质谱联用测定环境水样中的二价汞、甲基汞、乙基汞与苯基汞[J].环境化学,2011,30(4): 893–896.
[11]林立,王琳琳,孙海波,等.离子色谱–电感耦合等离子体质谱法测定乳粉的汞形态[J].岩矿测试,2014,33(3): 390–396.
[12]黄志勇,吴熙鸿,胡广林,等.高效液相色谱/电感耦合等离子体质谱联用技术用于元素形态分析的研究进展[J].分析化学,2002,30(11): 1 387–1 393.
[13]Cairns W R L,Ranaldo M,Hennebelle R,et al. Speciation analysis of mercury in seawater from the lagoon of Venice by online pre-concentration HPLC–ICP–MS[J]. Anal Chim Acta,2008,622(1–2): 62–69.
[14]Jia X Y,Han Y,Wei C,et al. Speciation of mercury in liquid cosmetic samples by ionic liquid based dispersive liquidliquid microextration combined with high-performance liquid chromatography inductively coupled plasma mass spectrometry [J]. J Anal Atom Spectrom,2011,26(7): 1 380–1 386.
[15]Chen J G,Chen H W,Jin X Z,et al. Determination of ultratrace amount methyl,phenyl and inorganic mercury in environmental and biological samples by liquid chromatography with inductively coupled plasma mass spectrometry after cloud point extraction concentration[J]. Talanta,2009,77(4): 1 381–1 387.
[16]Pena-Pereira F,Lavilla I,Bendicho C,et al. Speciation of mercury by ionic liquid-based single-drop microextraction combined with high-performance liquid chromatographyphotodiode array detection[J]. Talanta,2009,78(2): 537–541.
[17]Yin Y G,Chen M,Peng J F,et al. Dithizone-functionalized solid phase extraction-displacement elution-high performance liquid chromatography-inductively coupled plasma mass spectrometry for mercury speciation in water samples[J]. Talanta,2010,81(4–5): 1 788–1 792.
[18]Chen X P,Chao H,Cheng H Y,et al. Rapid speciation analysis of mercury in seawater and marine fish by cation exchange chromatography hyphenated with inductively coupled plasma mass spectrometry[J]. J Chromatogr A,2013,1314: 86–93.

