高速熔融搅拌法制备双氯芬酸钾缓释微丸的处方工艺考察
刘春憬
(青岛科技大学 药学院,山东 青岛 266042)
双氯芬酸钾(DP)为新一代强效非甾体抗炎药,其半衰期较短(约为1 h),口服吸收迅速,可很快达到较高的血药浓度,呈现明显的峰谷现象[1-2]。同时,与其它非甾体抗炎药一样,双氯芬酸钾对胃肠道也有刺激性。因此,制成缓释制剂可提供稳定的血药浓度,克服其口服剂量小、半衰期短而不易达到预期治疗效果、胃肠道刺激大等缺点,方便病人用药,提高治疗效果。
高速熔融搅拌法制微丸出现在20 世纪90 年代末[3],该法是在一个高速搅拌制粒锅中,在操作温度高于粘合剂熔点的条件下,将熔融的粘合剂与固体药物粉末进行搅拌、粘合而成颗粒或微丸。用该方法制备的微丸表面光滑,圆整度高,粒度分布均匀。与其他方法相比,具有节能节时、工艺简单、产率高、重复性好的优点[4-5]。
1 实验部分
1.1 原料与仪器
双氯芬酸钾原料(批号:100880-200601,纯度99.7%);固体石蜡、预胶化淀粉、柠檬酸均为化学纯;硫酸钙(含量≥99.0%)。
高速熔融搅拌制粒机,自制;FA1204B 电子天平;UV-1000 紫外分光光度计;ZRS-12G 型溶出仪。
1.2 双氯芬酸钾微丸的制备
将蜡质辅料于粉碎机中粉碎,过20 目筛,其他辅料过80 目筛,主药过100 目筛,分别取其筛下细粉备用。按处方量称取主药及各辅料,混合均匀后,置于已经预热的制粒机内,初始水浴温度为55 ℃,控制升温速率为1 ℃/4 min,直到温度升高至60 ℃。加入物料的同时启动搅桨,控制搅桨转速初始时为300 r/min,待粘合剂开始熔融时,将转速调整至800 r/min。物料边加热边搅动,持续10 min左右,即可制得微丸。待微丸成型后,停止加热,继续搅动约2 min 后取出,冷却至室温,筛分,取16 ~40 目的微丸,装囊,即为所得产品。
1.3 体外分析方法的建立[6-7]
1.3.1 测定波长的选择 称取干燥恒重的双氯芬酸钾适量,以pH=6.8 的磷酸盐缓冲液(人工肠液)溶解,稀释到适宜的浓度,以同样的浓度溶剂做空白,在λ=200 ~400 nm 的波段内扫描,得到最大吸收波长为274 nm。按处方比例取各辅料适量,同法在274 nm 波长处测定吸收度。结果表明辅料在该波长无吸收,故选择检测波长为274 nm。
1.3.2 标准曲线的建立 精密称量干燥恒重的双氯芬酸钾100 mg,加入到250 mL 的容量瓶中,以pH=6.8 的磷酸盐缓冲液定容,作为储备液,于冰箱中5 ℃储存。分别移取1.0,1.2,1.5,1.7,2.0,2.5,3.0 mL储备液至50 mL 容量瓶中,以pH=6.8 的磷酸盐缓冲液定容,得到浓度梯度为8.0,9.6,12.0,13.6,16.0,20.0,24.0 μg/mL 的溶液。在紫外分光光度计上λ=274 nm 处测定其吸收度,将浓度与对应的吸收度进行线性回归,得到回归方程为:C =33.42A+0.139 4,r =0.999 9(n =7),说明双氯芬酸钾在8.0 ~24.0 μg/mL 范围内,线性关系良好。1.3.3 稳定性实验 取浓度为12.0 μg/mL 供试品溶液,37 ℃放置,分别于0,1,2,3,4,6,8,12,24 h取样,测定峰面积,求得RSD 为0.88%,表明供试液在24 h 内基本稳定。
1.3. 4 回收率实验 按处方量的80%,100%,120%分别称取主药及辅料,配制供试溶液各3 份(适当超声使溶解),求得平均回收率分别为99.7%,100. 21%,99. 2%,RSD 分 别 为2. 6%,1.4%,3.1%,表明本方法回收率良好。
1.4 释放度的测定
参照《中国药典》(2010 年版,二部)附录XC 第一法装置(转篮法),按照附录XD 第一法进行体外释放实验,称取微丸400 mg 装囊,置于转篮中,量取药物释放介质(pH =6.8 的磷酸盐缓冲液)900 mL于溶出杯中,保持温度在(37 ± 0. 5)℃,转速100 r/min,转篮开启时开始计时,定时取样5 mL,并补充等量的释放介质,样液用0.8 μm 的微孔滤膜过滤,精密移取2 mL 的续滤液加6 mL 的释放介质稀释,以释放介质作对照,于λ=274 nm 处测定吸收度,按1.3.2 节所得标准曲线计算累积释放度。
2 结果与讨论
2.1 影响药物释放的工艺考察
2.1.1 粒径对药物释放的影响 按照处方制备微丸,分别取16 ~20 目,20 ~40 目微丸,装囊,测定药物释放度,药物释放曲线见图1。

图1 粒径对药物释放的影响Fig.1 Effect of pellet size on drug release
由图1 可知,微丸大小在16 ~40 目,粒径对药物释放无显著影响,故选择粒径在16 ~40 目之间的微丸。
2.1.2 温度对药物释放的影响 分别在50,55,60 ℃下制备微丸,测定药物释放度,药物释放曲线见图2。

图2 不同温度对累积释放度的影响Fig.2 Effect of different temperature on release degree
由图2 可知,温度越高,药物释放越慢。但温度较高时微丸易出现团块,温度过低,黏合剂不能完全熔融,造成辅料不能充分黏结,故选择在制备过程中采用先预热至熔点下限[8],再按一定速率升温至熔点上限,然后降温的温度控制方法。
2.1.3 搅拌桨转速对药物释放度的影响 分别在500,800,1 200 r/min 3 个不同的转速下制备微丸,测定药物释放度,药物释放曲线见图3。
由图3 可知,转速越高,微丸成粒越快;转速越低,微丸的粒径越小,内部结构疏松,药物的释放快。故最终选择的搅拌桨转速为800 r/min。
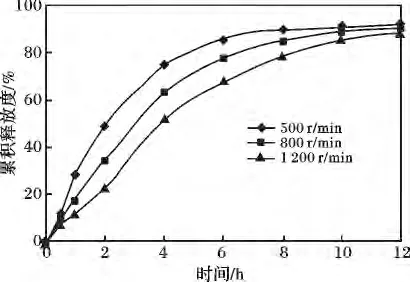
图3 搅桨转速对药物释放的影响Fig.3 Effect of the agitator’rotating speed on drug release
2.2 处方的确定
经前期预实验,确定以固体石蜡为粘合剂,以预胶化淀粉和柠檬酸为释放调节剂,采用3 因素3 水平正交实验考察粘合剂及调节剂的用量对药物释放度及释放速率的影响,见表1。其中保持药物含量和片重不变,依照释放度测定方法测定缓释微丸在2,4,6,8,10,12 h 的释放度。
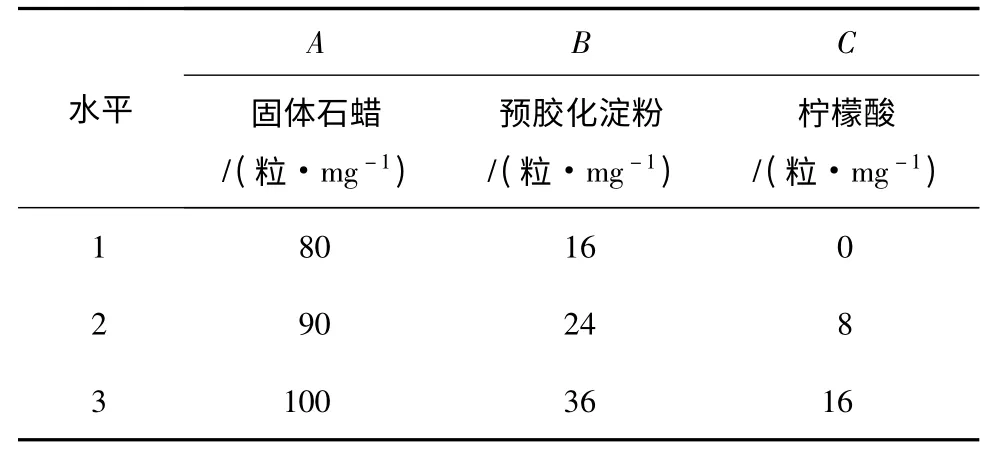
表1 正交实验因素与水平Table 1 Factors and levels for orthogonal test
为了更加准确的反映各因素水平对药物释放的影响,采用综合平衡法对正交设计的实验结果进行分析,以选出各因素最优水平的组合。即以国外同类产品的释放度作为参考标准,确定6 个评价指标,分别为2,4,6,8,10,12 h 的累积释放度分别是10%,30%,50%,70%,90%,100%,各指标的权重系数均为1,得到计算公式为:L =︱T2-10%︱+︱T4-30%︱+︱T6-50%︱+︱T8-70%︱+︱T10-90%︱+︱T12-100%︱。对各处方6 个点的累积释放度进行计算,L 值越小,说明因素的水平数越佳,结果见表2,方差分析见表3。
由表2 可知,各因素对药物释放影响的大小顺序为:A >B >C,又根据方差分析,其中因素A、B 有显著性影响,因素C 没有显著性影响,故得到各因素的最佳组合是:A3B1C2,即每粒胶囊含有主药60 mg,固体石蜡100 mg,预胶化淀粉16 mg,柠檬酸8 mg 及硫酸钙适量。
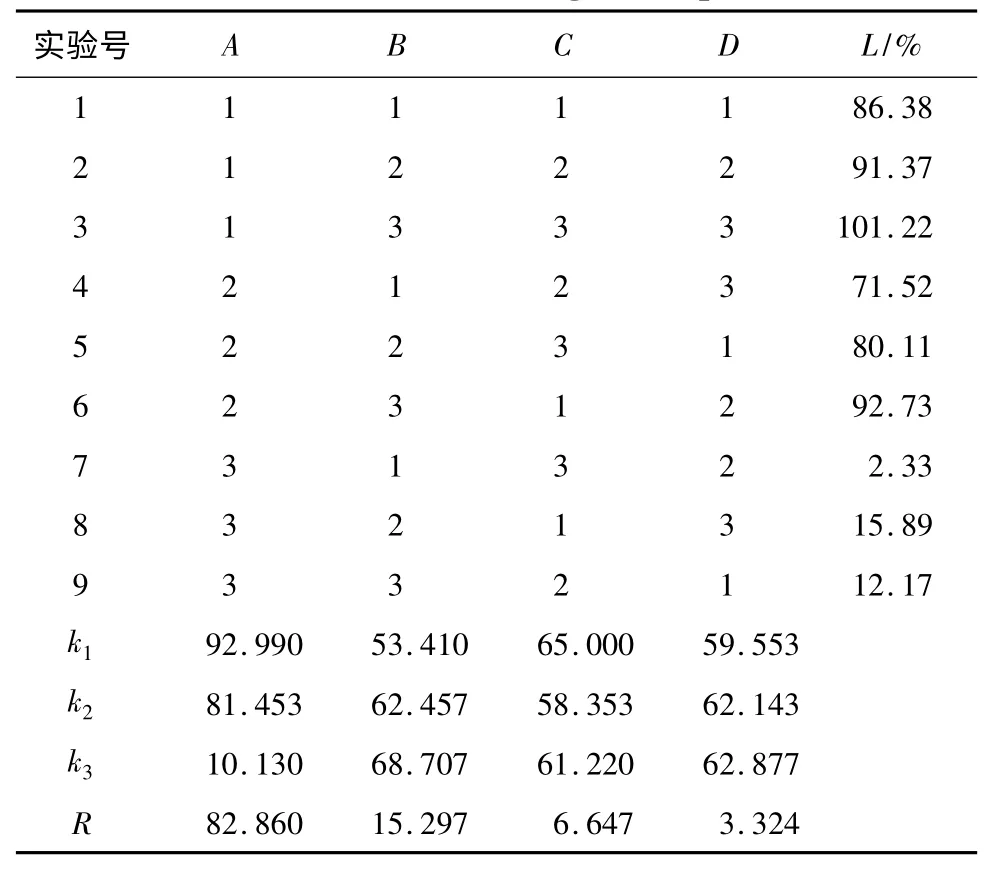
表2 正交实验测定结果(粒/mg)Table 2 Results of orthogonal experiment

表3 方差分析结果Table 3 Variance analysis result
注:F0.05(2,2)=19。
2.3 微丸缓释机制的研究
将双氯芬酸钾微丸的体外释放曲线按照以下几种数学模型进行拟合[9],结果表明,Higuchi 模型要优于一级和零级模型,拟合结果见表4。

表4 双氯芬酸钾缓释微丸各模型拟合结果Table 4 Model-fitting parameters for the release of captopril from pellets
3 结论
采用高速熔融搅拌法制备了双氯芬酸钾缓释微丸,并对影响药物释放的工艺因素进行考察,并对处方进行筛选,最终得到最佳的处方及工艺条件。
实验中发现,固体石蜡为一有效控制双氯芬酸钾释放的骨架材料,随着固体石蜡量的增加,药物的释放明显减慢,但其用量增至一较大值后,若再继续增加,则对药物释放的阻滞作用不再有明显加强。预胶化淀粉对药物释放前期的释放速率有明显作用,但后期的药物释放速率并不随着预胶化淀粉的加入有明显改变,这是因为在药物释放初期预胶化淀粉溶解,缓释骨架溶蚀较快,药物释放也较快,当预胶化淀粉全部溶解后,缓释骨架溶蚀缓慢,致使后期的药物释放速率较慢。双氯芬酸钾为一强碱弱酸性药物,其溶解度随着pH 值的变化有较大的改变,在pH 较低时,它可形成双氯芬酸,溶解度很低,在pH 较高时,溶解度较高,处方中加入柠檬酸,可使微丸内部形成酸性环境,双氯芬酸钾的溶解度降低,药物释放慢,随着药物释放时间的延长,柠檬酸全部溶出,药物处在碱性环境中,溶解度升高,释放加快。
[1] 吴妍,黄萍,韩敏,等. 双氯芬酸钾胶囊人体药代动力学与相对生物利用度研究[J]. 临床药学,2001,12(3):158-159.
[2] 潘洁,黄仲义,黄毅慧,等.双氯芬酸钾胶囊的人体生物等效性研究[J].中国药房,2005,16(15):1157-1159.
[3] 于少云,王洪光,刘璐,等.微丸的进展[J]. 中国新药杂志,1999,8(12):802-805.
[4] 黄文天,徐群为,郝钦.双氯芬酸钾缓释微丸的初步研制[J].广西药学,2000,22(4):704-706.
[5] 尔艳,王洪光,杯晓.熔融高速搅拌法制备氢氯噻嗪缓释微丸[J].沈阳药科大学学报,2001,18(4):247-250.
[6] 马福家.双氯芬酸钾HPMC 骨架片体外释药影响因素研究[J].上海医药,2005,26(6):271-272.
[7] 胡晓,吴瑞,宗莉,等. 双氯芬酸钾延迟缓释微丸的制备及体外释放[J]. 中国药科大学学报,2010,41(2):135-140.
[8] Badawy S I,Lee T J,Menning M M. Effect of drug substance particle size on the characteristics of granulation manufactured in a high shear mixer[J].AAPS Pharm Sci Tech,2000,1(4):E33.
[9] 孟祥磊,王洪光,刘会芹,等. 高速熔融搅拌法制备卡托普利缓释微丸及体外释放度[J]. 中国医院药学杂志,2010,30(6):475-477.

