伊立替康联合洛铂或顺铂二线治疗复发或转移广泛期小细胞肺癌的对比观察*
石 磊,柏玉举,李 宁,杨卫兵,李 列,邢时云,岳国军,罗 伟,张廷友
(遵义医学院附属肿瘤医院胸部肿瘤科,贵州遵义 563099)
临床经验交流
伊立替康联合洛铂或顺铂二线治疗复发或转移广泛期小细胞肺癌的对比观察*
石 磊,柏玉举,李 宁,杨卫兵,李 列,邢时云,岳国军,罗 伟,张廷友
(遵义医学院附属肿瘤医院胸部肿瘤科,贵州遵义 563099)
目的比较伊立替康(CPT-11)联合洛铂或顺铂(DDP)二线治疗经治后6个月内复发或转移的晚期小细胞肺癌,观察近期疗效和毒副反应。方法收集41例经治复发及进展的广泛期小细胞肺癌病例,以抽签方式随机分为实验组和对照组。实验组21例,采用洛铂(LBP)30mg/m2,d1,伊立替康(CPT-11)65mg/m2,d1、8,21d为1周期;对照组20例,采用CPT-11 65mg/m2,d 1、8,DDP 25mg/m2,d1~3,21d为1周期。病例至少完成2周期化疗。结果两组间客观缓解率、疾病控制率、生存时间无差异(P>0.05);实验组平均无进展生存时间有所延长(P=0.04);毒副反应中,实验组治疗后Ⅲ~Ⅳ度血小板减少发生率38.1%,对照组为20%,差异具有统计学意义(P=0.03);实验组治疗后Ⅲ~Ⅳ度恶心呕吐发生率为9.5%,对照组为35%,差异也具有统计学意义(P=0.049)。结论CPT-11联合LBP方案二线治疗复发或转移小细胞肺癌(SCLC)在控制肿瘤进展方面较CPT-11联合DDP方案有一定优势,而且毒副反应可耐受。
小细胞肺癌;伊立替康;洛铂;化疗;复发
小细胞肺癌(SCLC)占全部肺癌患者的13%[1],其恶性程度高,虽然对化疗、放疗较敏感,但预后仍比较差。由于SCLC具有独特的生物学特性,70%~80%局限期患者及几乎所有的广泛期患者在治疗后数月内即发生复发或疾病进展[2]。有资料表明,小细胞肺癌的自然中位生存期仅数月[3]。SCLC广泛期初治者对一线化疗敏感,但常短期发生获得性耐药而出现肿瘤复发或转移[4]。临床上对于6个月内复发或进展的小细胞肺癌如何选择有效且可耐受的方案解救患者,是亟待解决的问题。我们对2010年7月至2011年9月的41例复发或进展的小细胞肺癌广泛期患者按随机对照原则进行分组,一组选用二线方案伊立替康(CPT-11)联合顺铂(DDP)方案进行化疗,另一组选用伊立替康(CPT-11)联合洛铂(LBP)治疗,观察对比两者的疗效、毒副反应。并为临床提供更多可借鉴的经验。现将治疗经过报告如下。
1 资料与方法
1.1 入组标准 所有入组病人符合小细胞肺癌诊断的金标准;原发及远处转移病灶必须符合影像学阳性诊断标准,必须是广泛期小细胞肺癌;KPS评分≥60分;曾接受过一线的抗肿瘤治疗(化疗也包括放疗),均要达到临床缓解,化疗方案为EP方案(依托泊昔联合DDP)或CE方案(依托泊昔联合卡铂)并在放、化疗后6个月内病灶复发或进展。1.2 排除标准 有各类化疗禁忌;药物过敏;重要器官功能损害;无法被履行告知义务的患者;满足任何不能入组条件的情况。
1.3 一般资料 自2010年7月至2011年9月,共入组SCLC病人41例,其各项病例特征,包括病例数、性别、年龄、疗程分布相近(P>0.05)。采用抽签的方式随机分组,A组进入实验组,B组进入对照组。实验组21人,对照组20人。
1.4 治疗方法 实验组:洛铂30 mg/m2稀释于5%葡萄糖500 mL中,静脉滴注2 h,第1天;伊立替康65mg/m2稀释于0.9%氯化钠注射液250 mL中,静脉滴注1.5 h,第1、8天,21 d为1周期。对照组:伊立替康65 mg/m2稀释于0.9%氯化钠注射液250 mL中,静脉滴注1.5 h,第1、8天;顺铂25 mg/m2稀释于0.9%氯化钠溶液500 mL中静脉滴注,第1~3天,21 d为1周期。
1.5 评价标准 各组化疗前及化疗2周期后进行CT检查,评价病灶变化情况。根据实体肿瘤的疗效评价标准(RECIST1.1),分完全缓解(CR)、部分缓解(PR)、稳定(SD)、病情进展(PD)、无进展生存期(PFS)、中位生存时间(OS),以CR+PR计算客观缓解率(0RR),以CR+PR+SD计算疾病控制率(DCR)。毒副反应评价,依照NCI-CTC 3.0标准进行。随访时间均满1年,期间无失访。
1.6 统计学处理 采用SPSS 19.0统计软件包进行分析。分类资料采用χ2检验;连续型变量采用T检验;两组生存时间趋势比较采用生存分析中的Log Rank分析。P<0.05为有统计学意义。
2 结果
2.1 疗效 所有入组病人完成超过2个疗程的治疗,平均为3.3个治疗周期,满足疗效评估标准。实验组客观缓解率为42.9%,对照组为30.1%,组内比较无统计差异(χ2=0.73,P=0.39);实验组疾病控制率61.9%,对照组45%,组内也无统计差异(χ2=1.18,P=0.28);两组平均无进展生存时间采用t检验,方差齐,经比较有统计差异(t= 2.130,P=0.04);两组中位生存时间采用Log Rank检验,无统计差异χ2=0.014,P=0.905(见表1~2,图1)。

表1 两组近期疗效比较

表2 平均无进展生存期及中位生存时间比较
2.2 毒副反应 两个试验组中所有指标在治疗前都是0度正常。按照病情轻重程度,将0~Ⅱ级划为非重度,Ⅲ~Ⅳ度为重度,作为二分类变量来用χ2检验比较实验组与对照组重度发生率是否不同。血液毒性:重度白细胞下降发生率无统计学差异(χ2=0.672,P=0.41);两组重度血小板减少症发生率有统计学差异(χ2=4.63,P=0.03)。两组重度恶心呕吐发生率有统计学差异(χ2=3.88,P =0.049);两组重度延迟性腹泻发生率无差异(χ2=0.75,P=0.39)。其它毒性反应均无差异(见表3)。
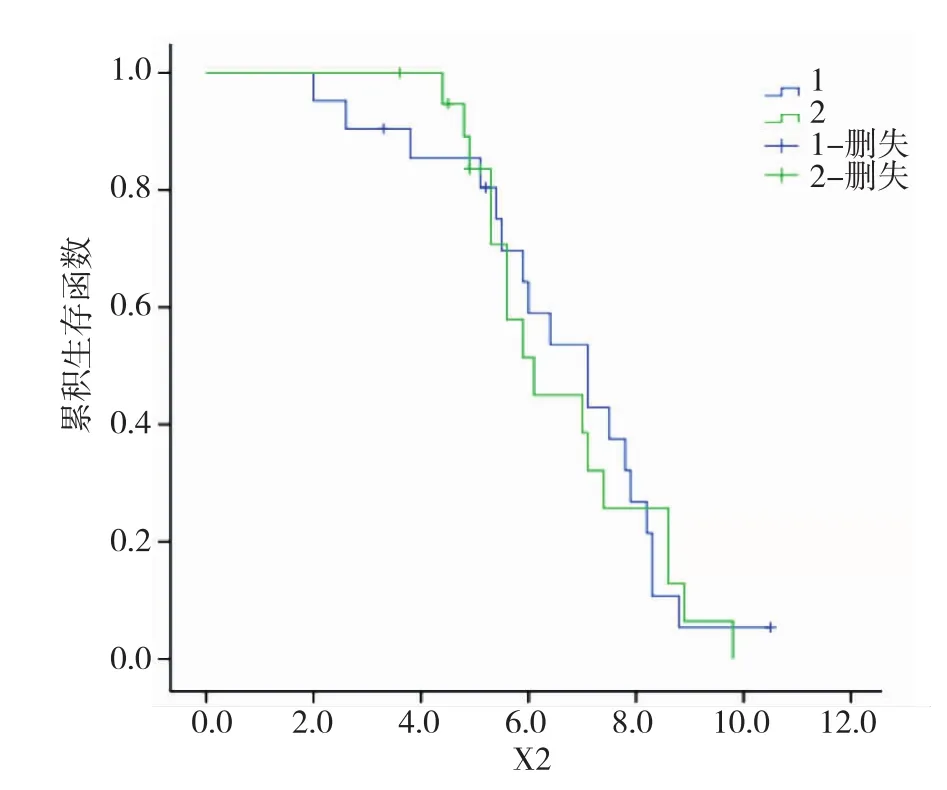
图1 两组生存函数曲线
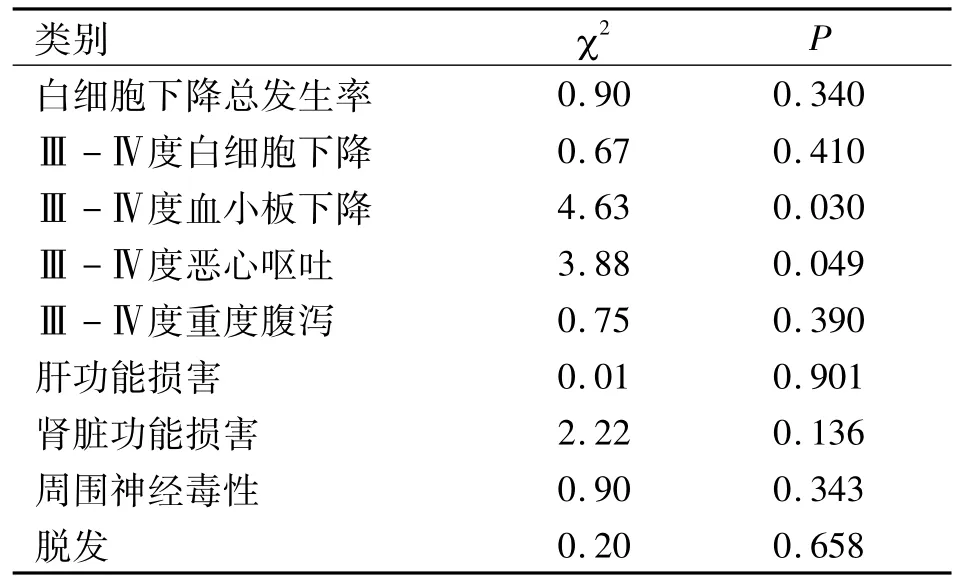
表3 两组各种毒副反应程度比较
3 讨论
临床中IP方案是经EP方案治疗有效后复发或转移广泛期小细胞肺癌的常用二线化疗方案,而其有效率常常较低。经研究发现,小细胞肺癌二线化疗失败的众多因素中,顺铂产生耐药性是其主要原因之一。顺铂耐药的常见类型有凋亡信号传导异常、DNA损伤修复基因表达异常[5]、体内干细胞的还原性谷胱甘肽(GSH)发挥保护细胞免受顺铂损伤的作用等[6]。病理学研究逐渐抓住了原发性耐药的实质,原因是小细胞肺癌治疗后复发的患者约有35%转型,成为NSCLC或混有NSCLC成分的类型,因此发生对化疗药物的耐药。洛铂药物的发明和临床应用,拓展了小细胞肺癌二线化疗的领域。洛铂是第3代铂类抗癌药物,其疗效与顺铂(PDD)和卡铂(CBP)类似,而毒副作用仅与卡铂[7]相当,并且最被推崇的是避免了与DDP的交叉耐药性发生。药理学研究显示,洛铂还具有毒副反应小、起效时间短、药效持续久和肿瘤组织中浓度高而血浆低的特点,因此药物有高选择性特点。在LBP获准进入中国的注册性临床研究中,小细胞肺癌的反应率好,客观有效率达到42.2%。本实验考虑洛铂不会产生交叉耐药,安全性好,在保证治疗耐受性好的基础上,可能会增加疗效,故以洛铂联合伊立替康治疗晚期小细胞肺癌。国内有蒋侃、黄诚[8]对伊立替康联合洛铂二线治疗复发小细胞肺癌的临床观察结果已公布,其SCLC患者接受洛铂联合伊立替康方案的疗效与本研究的疗效相近,再次证实了伊立替康联合洛铂方案对于晚期小细胞肺癌治疗失败的患者是值得采用的方案。
在临床工作中,轻度毒副反应容易耐受,而重度毒副作用不宜耐受或致死。故本研究中我们更关注重度毒副反应发生率。而且试验中未出现危及生命的严重不良事件,包括患者严重感染、腹泻、出血甚至死亡。两组化疗方案主要的毒副反应为骨髓抑制和胃肠道反应。本试验对象多数为老年人,由于接受过多程化放疗,其骨髓造血和储备功能已受损,在二线化疗中有毒副反应加重的趋势,成为重度反应的易感人群。其中洛铂主要的剂量限制性毒性是血小板减少,但实验组中未出现明显出血倾向,仅2例老年患者因纠正重度血小板减少而推迟化疗,无死亡病例。另外,洛铂的胃肠道及肾脏毒性较轻微,此为年老合并有体质消瘦、饮食下降和肾功能不全的患者带来了福音。此外还需注意伊立替康的迟发型腹泻与洛铂化疗后骨髓抑制时机重合的可能性。国内外临床报道中显示,一线采用顺铂方案的实体瘤,包括胃、小细胞肺癌[9]和结肠癌[10],如果二线采用含LBP方案化疗,实验患者可获得良好的依从性与耐受性,故LBP较DDP更能使患者获益[11-12]。本研究结果与此类报道类似,该方案较适用于复发及进展的小细胞肺癌二线治疗。
洛铂联合方案较顺铂联合方案延长了疾病稳定时间,在控制肿瘤进展方面有一定优势,而且胃肠道毒副反应降低对于提高治疗耐受性作用显著。但同时,洛铂的毒副反应需要在临床上得到足够的重视,而且相较于顺铂,其价位更高。我们主张在洛铂联合伊立替康方案二线治疗广泛期小细胞肺癌之前,要将患者的体质情况和经济能力综合考虑。鉴于洛铂联合方案疗效较优,且相对安全并易耐受,故值得在临床中继续推广和研究。
[参考文献]
[1]American Cancer Society.Cancer Facts&Figures 2015[R].Atlanta:American Cancer Society,2015:12-24.
[2]禚银玲,李世云,赵晨睛,等.洛铂联合依托泊昔治疗广泛期小细胞肺癌的临床疗效观察[J].山东医药,2012,52(14):61-62.
[3]高文斌,邓蓉,韩佩妍,等.洛铂对肺癌HTB-56、HTB -56/DDP细胞株生长抑制作用的研究[J].中华肺部疾病杂志:电子版,2012,5(2):33-35.
[4]Jalal S I,Bhatia S,Einhorn L H,et al.Paclitaxel plus bevacizumab in patients with chemosensitive relapsed small cell lung cancer(SCLC):a safety,feasibility and efficacy trial from Hoosier Oncology Group[J].J Clin Onco,2008,26(15):707.
[5]Chattopadhyay S,Machado-Pinilla R,Manguan-García C,et al.MKP1/CL100 controls tumor growth and sensitivity to cisplatin in non-small-cell lung cancer[J].Oncogene,2006,25(23):3335-3345.
[6]Enomoto Y,Kenmotsu H,Watanabe N,et al.Efficacy and Safety of Combined Carboplatin,Paclitaxel,and Bevacizumab for Patients with Advanced Non-squamous Nonsmall Cell Lung Cancer with Pre-existing Interstitial Lung Disease:A Retrospective Multi-institutional Study[J].Anticancer Res,2015,35(7):4259-63.
[7]Xie CY,Xu Y P,Jin W,etal.Antitumor activity of lobaplatin alone or in combination with antitubulin agents in non-small-cell lung cancer[J].Anticancer Drugs,2012,23(7):698-705.
[8]蒋侃,黄诚,吴标,等.伊立替康联合洛铂治疗复发广泛期小细胞肺癌临床观察[J].中国实用医药,2011,6 (18):1-2.
[9]林丽珠,周岱翰,郑心婷.洛铂联合氟尿嘧啶和甲酰四氢叶酸治疗晚期耐药胃癌、结直肠癌疗效观察[J].中国肿瘤临床,2007,34(5):286-288.
[10]杨柳青,施毅,秦叔逵,等.洛铂联合长春瑞滨治疗晚期非小细胞肺癌的临床研究[J].临床肿瘤学杂志,2006,11(12):890-895.
[11]Limited A I.Lobaplatin:D 19466[J].Drugs in R&D,2003,4(6):369-372.
[12]Kinehara Y,Minami T,Kijima T,etal.Favorable response to trastuzumab plus irinotecan combination therapy in two patients with HER2-positive relapsed small-cell lung cancer[J].Lung Cancer,2015,87(3):321-325.
[收稿2015-01-10;修回2015-03-10]
(编辑:王福军)
The comparative observation of irinotecan combined with lobapatin or cisplatin in the treatment of recurrent or progressive extensive stage small cell lung cancer
Shi Lei,Bai Yuju,Li Ning,Yang Weibing,Li Lie,Xing Shiyun,Yue Guojun,Luo Yi,Zhang Tingyou
(Department of Thoracic Oncology,The Affiliated Tumor Hospital of Zunyi Medical University,Zunyi Guizhou 563099,China)
Objective To compare the efficacy and toxicity of lobaplatin(LBP)or DDP joint with irinotecan (CPT-11)-based chemotherapy in the treatment of small cell lung cancer patients.M ethods41 cases of SCLC patientswere randomly divided into experimental and control group.All of 21 cases in experimental group were treated with LBP 30mg per squaremeter at day 1,CPT-11 65mg/m2at day 1,8,and 21 days of a cycle.And 20 cases in control group were treated with CPT-11 65mg per squaremeter at day 1 and day 8.DDP 25mg per squaremeter at day 1 to day 3,21 days for a cycle.Each case has completed at least two cycles of chemotherapy.Results The objective response rate,disease control,survival time between the two groups showed no difference(P>0.05);The experimental group’s average progression-free survival timewas prolonged(P=0.04). Major toxicity:in the experimental group after the treatment,Ⅲ-Ⅳdegree of thrombocytopenia was 38.1%,while control group was20%(P=0.03).In the control group after the treatment,theⅢ~Ⅳdegree of nausea and vomitingwas9.5%,while itwas35%in the experimental group(P=0.049).Conclusion CPT-11 joint LBP scheme as the second-line treatment of small cell lung cancer(SCLC)recurrence or progress has certain advantages in controlling the progress of the tumor and tolerable.
small cell cancer;irinotecan;lobaplatin;chemotherapy;recurrence
R734.2
B
1000-2715(2015)04-0408-04
柏玉举,男,教授,研究方向:肿瘤综合治疗,E-mail:SL4772@sina.com。

