水浴消解和微波消解-原子荧光法测定土壤中汞和砷的研究
刘欢欢,徐云龙,赵 杰 (苏州国环环境监测有限公司,江苏苏州 215000)
汞及其化合物属于剧毒物质,可通过呼吸道、皮肤或消化道等途径侵入人体。进入水体的无机汞离子可转变为毒性更大的有机汞,经食物链进入人体而引起全身中毒[1]。砷在自然界分布很广,存在于食物、水体、土壤和空气中[2]。土壤中砷和汞的污染来自于工业污染和农业污染,其中工业污染是由含砷和汞的废水、废气和废渣的排放而造成的,农业污染大部分是由含砷、汞农药和杀虫剂的使用所致[3]。世界卫生组织将砷、汞的污染与中毒列为重要公害。随着无公害农产品和绿色食品产业的不断发展,农业部制定了相关标准,对无公害食品和绿色食品产地环境的砷、汞作出严格的限量规定[4]。同时,国家环境质量标准也将砷、汞列为必检项目[5]。在土壤分析中,常采用比色法、原子吸收法[6]、原子荧光法[7]。前2种方法的测定结果较稳定,缺点是操作繁琐,分析时间长,灵敏度偏低,含量低的样品无法得到定量结果,不能满足环境的评价标准要求[8]。目前,消解土壤样品的前处理方法较多[9-10],主要有微波消解、水浴消解、电热板湿法消解、高压釜消解等。微波消解由于其溶样能力强、溶剂用量少和速度快等特点,已成为一种新颖的样品预处理技术,目前被广泛地应用于各种试样的前处理方法中[11-13]。而水浴消解是湿法消解的一种改进,特别适合大批量土壤样品的分析。氢化物发生和原子荧光光谱法的联用技术是近年发展较快的分析技术[14-16]。笔者采用微波消解和水浴消解2种前处理方法做对比,通过对2个土壤标准物质和2个土壤实际样品的精密度、准确度和回收率的研究来比较2种方法对测试土壤中汞和砷的影响。研究表明,2种前处理方法的检出限、精密度、准确度和回收率均能满足环境土壤检验的要求,均可广泛地应用于环境土壤的监测,而微波消解法具有更好的精密度、准确度和回收率。
1 材料与方法
1.1 仪器 氢化物原子荧光光度计,AFS-830型,北京吉天仪器有限公司;砷、汞编码空心阴极灯,北京有色金属研究总院;断续流动自动进样系统。微波消解仪,ETHOS1型,Milestone;可调恒温电热水浴锅(最大可调温度100℃)。所有玻璃器具在每次使用前于浓度20%盐酸溶液中浸泡24 h以上,自来水冲净后用蒸馏水、二次蒸馏水清洗。
1.2 试剂
1.2.1 砷标准储备液。1 000 μg/ml,国家有色金属及电子材料分析测试中心,GSB04-1714-2004,147045-2,有效期2014.7-2016.7。
1.2.2 砷标准使用液。取10 ml 1 000 μg/ml砷标准储备液,逐级稀释至10.0 mg/L,供配砷制标准系列溶液使用。
1.2.3 汞标准储备液。1 000 μg/ml,国家有色金属及电子材料分析测试中心,GSB04-1729-2004,13527-2,有效期2013.5-2015.5。
1.2.4 汞标准使用液。取10 ml 1 000 μg/ml汞标准储备液,逐级稀释至100 μg/L,供配汞制标准系列溶液使用。
1.2.5 土壤标准物质。GSBZ50012-88(ESS-2),购自中国环境监测总站;GBW07453(GSS-24),购自国家标准物质研究中心(北京)。
1.2.6 1#样品和2#样品。分别采自农田土壤和工厂附近土壤。
1.2.7 硫脲-抗坏血酸混合溶液。配制质量体积分数为5%的混合溶液。
1.2.8 汞标准系列溶液。取5只100 ml容量瓶,分别加入0.80、1.60、2.40、3.20、4.00 ml汞标准使用液,用浓度 5% 盐酸定容至刻度,摇匀,配制成浓度为 0.80、1.60、2.40、3.20、4.00 μg/L的汞标准系列溶液,同时作标准空白处理,即配即用。
1.2.9 砷标准系列溶液。取6只100 ml容量瓶,分别加入0.40、0.80、1.20、1.60、2.00、2.40 ml砷标准使用液和 10.0 ml硫脲-抗坏血酸混合溶液,用浓度5%盐酸定容至刻度,摇匀,配制成浓度为40、80、120、160、200、240 μg/L 砷标准系列溶液,同时作标准空白处理。
1.2.10 还原剂。配制质量体积分数为1.0%的硼氢化钾溶液,溶解于浓度0.5%氢氧化钾溶液中,宜用时现配(用于测试汞);配制质量体积分数为2.0%的硼氢化钾溶液,溶解于浓度0.5%的氢氧化钾溶液中,宜用时现配(用于测试砷)。
1.2.11 (1+1)王水。取1份硝酸和3份盐酸混合,用超纯水稀释1倍。
1.2.12 载流。浓度 5%HCl。
1.3 样品前处理
1.3.1 水浴消解。准确称取风干后的土壤样品(100目)0.5 g于50 ml具塞比色管中,加入少许水润湿样品,加入10 ml(1+1)王水,加塞后摇匀,于沸水浴中消解2 h,其间每隔30 min摇动一次。消解完毕后取出冷却,加入2 ml盐酸,用超纯水定容至刻度,摇匀后静置,取上清液,待测。测砷时,需向每25 ml待测液中加入2 ml硫脲-抗坏血酸混合溶液,摇匀,30 min后上机测试。同时,做样品空白处理。
1.3.2 微波消解。准确称取风干后的土壤样品(100目)0.5 g,置于溶样杯中,用少量水润湿,在通风橱中先加入6 ml盐酸,再慢慢加入2 ml硝酸,混匀,使得样品与消解液充分接触。若有剧烈化学反应,则待反应结束后再将溶样杯置于消解罐中密封。将消解罐装入消解罐支架后放入微波消解仪的炉腔中,确认主消解罐上的温度传感器、压力传感器均已与系统接好后,按表1的升温程序进行微波消解,程序结束后冷却。待罐内温度降至室温后,在通风橱中取出,缓慢泄压放气,打开消解罐盖。将消解后的溶液过滤、转移至50 ml容量瓶中,洗涤、定容后摇匀待测。测砷时,需向每25 ml的待测液中加入2 ml硫脲-抗坏血酸混合溶液,摇匀,30 min后上机测试。同时,做样品空白处理。

表1 微波消解升温程序
1.4 仪器条件
1.4.1 汞。灯电流30 mA;负高压270 V;原子化器高度8 mm;载气流量300 ml/min;屏蔽气流量800 ml/min;注入体积0.5 ml;测量方式为标准曲线法;读取方式为峰面积。
1.4.2 砷。灯电流60 mA;负高压265 V;原子化器高度8 mm;载气流量300 ml/min;屏蔽气流量800 ml/min;注入体积0.5 ml;测量方式为标准曲线法;读取方式为峰面积。
1.5 分析测定 将标准系列溶液和待测样品倒入自动进样器中,设定好仪器分析条件,分别测定标准曲线和样品,测定完成后自动计算结果。
2 结果与分析
2.1 标准曲线 汞标准系列线性方程为I=332.448 1×Conc-17.555 1,相关系数(r)为0.999 6;砷标准系列线性方程为 I=5.151 5 ×Conc+2.659 7,相关系数(r)为0.999 7。
2.2 检出限 根据仪器设定的检出限程序,连续测定空白溶液11次,用3倍空白样品荧光值的标准偏差除以标准曲线斜率为该仪器的砷、汞最低检出限,即砷为0.089 μg/L,汞为0.012 μg/L。因此,该仪器的砷、汞最低检出浓度分别为0.009、0.001 mg/kg。
2.3 精密度 取土壤标准物质、1#样品和2#样品,按照“1.3”中试验方法进行样品的前处理和测定。由表2和表3可知,采取水浴消解法测定的汞和砷的相对标准偏差分别为3.8% ~9.2%和2.3% ~5.5%,而采取微波消解法测定的汞和砷的相对标准偏差分别为1.9% ~6.8%和1.4% ~2.3%,说明这2种方法的精密度均符合要求。从相对标准偏差的数值来看,微波消解法的相对偏差较水浴消解法低,说明微波消解法具有更好的精密度。
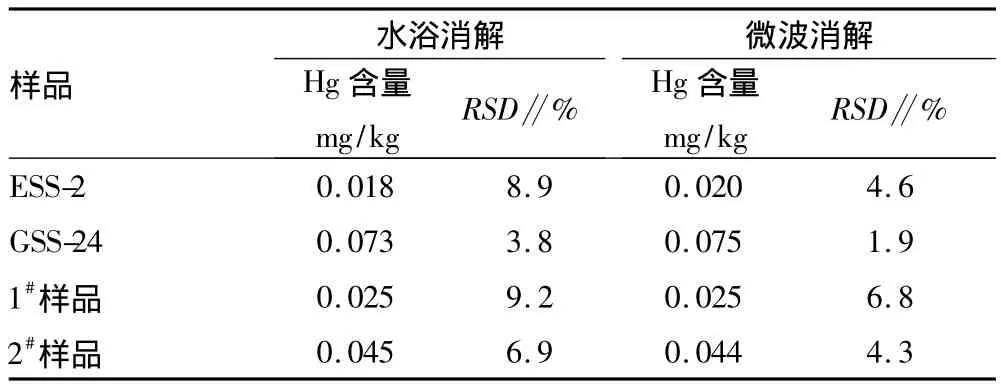
表2 方法的精密度(Hg)

表3 方法精密度(As)
2.4 回收率 在1#样品和2#样品中,加入高、低浓度的汞、砷标准溶液,采用水浴消解法和微波消解法进行前处理,测定样品的回收率。由表4和表5可知,采取水浴消解法和微波消解法汞的回收率分别为92.0% ~102%和97.5% ~99.0%,砷的回收率分别为90.0% ~110% 和92.0% ~102%。
2.5 准确度 取土壤标准物质(ESS-2和GSS-24),按照“1.3”试验方法预处理。由表6可知,采取2种消解方法测定的汞和砷的值均在土壤标准物质的保证值范围内,说明2种前处理方法的准确度均满足要求;而微波消解的值更接近于标准物质的真值,说明微波消解法对样品的测定具有更好的准确度。
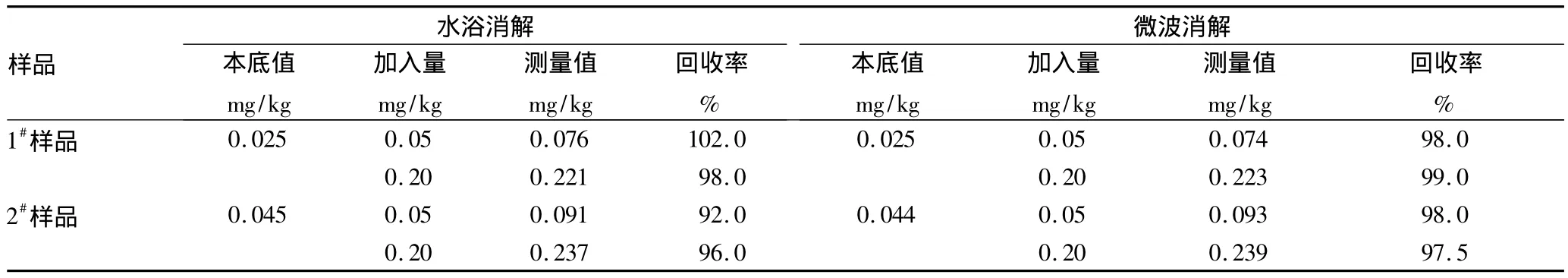
表4 Hg的回收率
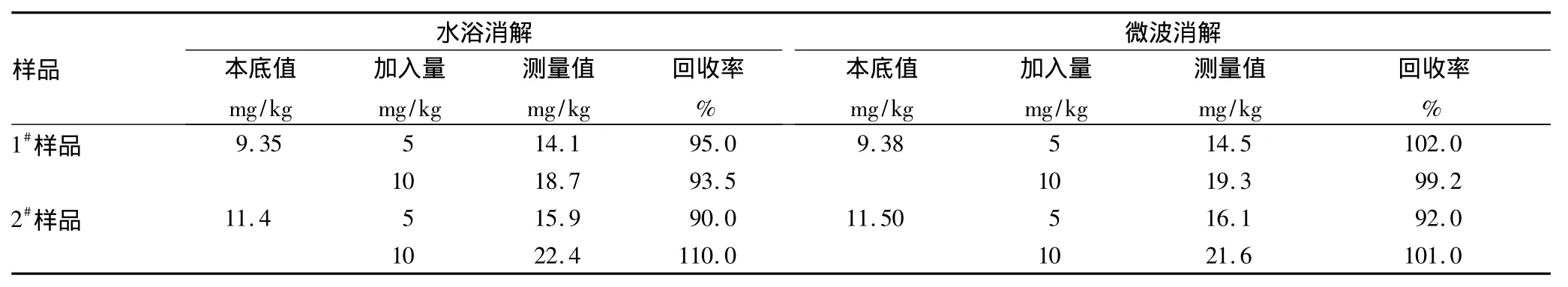
表5 As的回收率

表6 标准物质测定结果mg/kg
3 结论
采取水浴消解法和微波消解法测定土壤中汞和砷含量,在检出限、精密度、准确度和回收率上均能满足土壤检测的要求。水浴消解法操作简单,需要的仪器设备易得,但耗时长,在精密度、准确度和回收率上略逊于微波消解法。而微波消解法仪器设备较先进,耗时短,溶剂用量少,溶样效果好,具有更好的精密度与准确度,在目前的预处理方法中已得到广泛的应用。
[1]鲁丹,李海涛.微波消解-氢化物发生原子吸收光谱法测定食物中的汞[J].光谱学与光谱分析,1999,19(3):394 -396.
[2]杨海霞,汝少国,王震宇,等.原子荧光法同时测定海产品中砷、汞[J].环境科学与技术,2012,35(S1):248-251.
[3]何振立.污染及有益元素的土壤化学平衡[M].北京:中国环境科学出版社,1998:244 -275.
[4]中国标准出版社第一编辑室.无公害食品标准汇编[G].北京:中国标准出版社,2003:3 -14.
[5]中国标准出版社第一编辑室.绿色食品标准汇编[G].北京:中国标准出版社,2003:86 -91.
[6]张衍林.流动注射-氢化物原子吸收法测定轻油中的砷[J].石油化工,1995,24(12):66 -70.
[7]徐浩龙.高压消解-双道氢化物发生-原子荧光光谱法同时测定女贞属苦丁茶中砷与汞[J].分析科学学报,2012,28(5):734 -736.
[8]舒天阁,王维,许惠英.石墨消解-原子荧光法测定土壤中的汞和砷[J].化学分析计量,2014,23(2):27 -29.
[9]杨丽洲,陶大钧.土壤和底质中砷的形态及前处理技术[J].甘肃环境研究与监测,2000,13(1):17-19.
[10]齐文启,孙宗光,石金宝.环境检测实用技术[M].北京:中国环境科学出版社,2006:161 -179.
[11]王永芳,韩红伟,赵磬.微波高压消解-火焰AAS法测定食品中的钙、铁、镁、锰、锌、铜等元素[J].卫生研究,1997,26(2):133 -134.
[12]郝琳,马强.微波密闭消解-冷原子吸收法测定生物试样中的微量汞[J].中国卫生检验杂志,1998,8(4):215 -216.
[13]汤毅珊.微波消解-原子荧光法测定中药中的汞、砷[J].中药新药与临床药理,1999,11(3):177-179.
[14]谢永臻.流动注射氢化物发生原子荧光法测定中药中的微量砷、汞[J].分析科学学报,1997,13(4):296 -299.
[15]江志刚.氢化物-原子荧光法测定海产品中的微量砷[J].光谱实验室,1999,16(3):33 -36.
[16]江志刚.氢化物-原子荧光法测定粮食中的砷[J].分析实验室,1999,18(1):58-60.

