抗生素磺胺甲恶唑在模拟太阳光下的光解
闻长虹, 毛顺, 郑丽英, 李文军, 杨基峰
抗生素磺胺甲恶唑在模拟太阳光下的光解
闻长虹1, 毛顺2, 郑丽英2, 李文军2, 杨基峰2
(1. 池州职业技术学院园林系, 安徽池州, 247000; 2. 湖南文理学院化学化工学院, 湖南常德, 415000)
为了弄清磺胺类药物在水体中的环境行为, 以磺胺甲恶唑为模型化合物, 研究其在模拟太阳光下的光解特征, 考察不同因素对降解行为的影响。实验结果表明, 磺胺甲恶唑在模拟太阳光下发生光解, 光解速率随着质量浓度的升高而下降, 最高降解速率达到0.36 h-1; 同时, 在酸性条件下(尤其pH值小于5), 其降解半衰期显著低于碱性条件下(pH值为8)的降解半衰期, 最小为2.10 h; 并且在不同质量浓度NO3-下磺胺甲恶唑的降解速率会发生变化, 低质量浓度促进降解, 而高质量浓度抑制降解。
磺胺甲恶唑; 光解; 模拟太阳光
抗生素常用于治疗和预防人体和动物因微生物感染所引起的疾病。这些抗生素最终会通过生活污水、医院废水、生产过程等方式进入环境介质中, 在不同水体中被检出[1-3]。由于它们的生物活性和潜力可诱导自然种群产生耐药性, 因此水体环境中抗生素的广泛存在将可能引起生态安全问题[4-6]。
磺胺类药物是目前应用非常广泛的一类抗生素, 用药后可通过各种途径进入水体环境[7-8], 从而可能引起一些急性和慢性毒性效应。磺胺类药物通常含有5或6个杂环, 这使得它们在紫外-可见光照射下能够吸收一定波长的光, 从而发生直接光解[9]; 通过能量转移或自由基的攻击产生化学反应而引起的光化学降解也通常发生[10]。目前关于磺胺类物质的降解已有一定研究[11], 但不同磺胺类药物的结构还存在一定差异。
基于此, 本实验对磺胺甲恶唑在模拟太阳光下的光降解行为进行研究, 考察pH值、硝酸盐、药物质量浓度等因子对光解过程的影响, 最终为磺胺甲恶唑的光降解行为提供基础数据。
1 材料与方法
1.1 材料
药剂: 磺胺甲恶唑(>98%)购自阿拉丁公司(上海), 其化学结构如图1所示; 甲醇(色谱纯)购自美国天地公司; 硝酸钠(分析纯)购自天津大茂试剂有限公司; 其他有机溶剂均为分析纯; 实验所用水均为超纯水。
仪器: 多功能光化学反应器及配套500 W氙灯(上海岩征实验仪器有限公司); Agilent 1260高效液相色谱仪(美国安捷伦); BSA1 24S电子天平(德国赛多利斯)。
图1 磺胺甲恶唑的化学结构
1.2 光解实验
光解反应均在多功能光化学反应器中进行, 光源为500 W氙灯, 波长> 290 nm。移取30 mL 10 mg/L磺胺甲恶唑(均溶解于超纯水)于100 mL 石英管中, 并将其置于旋转反应器中反应。为了保证反应在恒定的温度下进行, 采用冷阱装置控制温度在25 ℃左右。实验过程中, 每隔一定时间取样, 采用高效液相色谱仪分析样品中磺胺甲恶唑的质量浓度。每一实验重复3次, 同时设置暗反应对照实验。
1.3 分析方法
磺胺甲恶唑采用高效液相色谱法进行测定, 具体操作条件如下: 色谱柱为Waters (2.1 mm × 150 mm, 5 μm); 流动相是甲醇:0.1%磷酸=30: 70的溶液; 检测器为光电二极管阵列检测器, 检测波长为270 nm, 流速为0.8 mL/min, 进样量为20 μL, 柱温为30 ℃。
1.4 光解动力学
2 结果与讨论
2.1 初始质量浓度对磺胺甲恶唑光解的影响
为考察不同初始质量浓度对磺胺甲恶唑光解作用的影响, 研究在pH值为5、质量浓度为10 mg/L条件下进行, 实验结果见图2。由图2可以看出, 质量浓度对降解速率影响非常大, 当质量浓度为5 mg/L时, 降解率达95%以上; 而高质量浓度的药物只有不到25%发生降解。通过准一级动力学模型拟合后, 得到的相关系数2均大于0.99, 说明磺胺甲恶唑的降解符合准一级动力学模型(表1)。

图2 不同质量浓度药物对光降解的影响

表1 不同条件下的磺胺甲恶唑的准一级动力学模型参数
在质量浓度为5 mg/L时, 其降解速率常数为0.36 h-1, 半衰期为1.93 h; 当质量浓度为10 mg/L和20 mg/L时, 其降解速率常数分别为0.03 h-1和0.04 h-1, 半衰期分别为23.1 h和17.3 h。以上结果说明, 在光子量不变的情况下(氙灯功率不变), 单位分子所获得的光子量在逐渐减少, 此结果和其他研究相吻合。磺胺甲恶唑吸收模拟太阳光, 引起结构的变化而降解成其他物质。图3为不同时间段样品的液相色谱图, 从图3可以看出, 在0 h时色谱图中在4.4 min出现了磺胺甲恶唑的色谱峰; 而当反应进行到4 h时, 磺胺甲恶唑的色谱峰明显下降, 同时在2.5 min和3.1min出现其他两个物质的色谱峰, 说明反应过程中至少产生2种降解产物。

图3 不同时间样品的液相色谱图
2.2 pH值对光解作用的影响
不同地区水体的pH值通常情况下会有一定差异, 为了弄清pH值对模型化合物光解作用的影响, 考察了在质量浓度为5mg/L时4种不同pH值下的光解情况, 实验结果见图4。由图4可看出, 在不同pH值条件下磺胺甲恶唑的降解率存在一定差异, 尤其当pH值为8时, 降解率仅为40%。为了更好说明问题, 采用准一级动力学模型对降解曲线进行拟合, 相关系数2均大于0.99, 表明它们均遵循准一级动力学模型。表1中在pH值为5, 6和7时, 其降解速率常数分别为0.33, 0.29和0.29 h-1, 降解半衰期分别为2.10, 2.39和2.39 h; 而在pH值为8时, 其降解速率常数显著下降(= 0.06 h-1), 降解半衰期高至11.6 h。

图4 不同pH值对光降解的影响
由于磺胺甲恶唑具有2个不同酸碱解离常数, pa分别为1.85和5.60。在不同环境条件下, 其以不同的形态存在, 具体的酸碱分布分数见图5。

图5 磺胺甲恶唑的酸碱分布分数
由图5可以看出, 在pH值为5的条件下, 磺胺甲恶唑主要以不带电荷形式存在, 少部分以带负电荷形式存在; 当pH值不断上升时(pH值为6, 7和8), 磺胺甲恶唑则以负电荷形式存在, 尤其当pH值为8时, 完全以带负电荷形式存在。与以上结果比较, 说明当磺胺甲恶唑以不同形式存在时, 其对光子的吸收存在一定差异, 中性形态对光子吸收的能力更强。
2.3 硝酸根离子对磺胺甲恶唑光解的影响
硝酸根离子广泛存在于各种水体中, 本研究采用NaNO3配制了不同质量浓度NO3-以考察其对磺胺甲恶唑光解作用的影响, 实验结果见图6。结果显示当加入不同质量浓度NO3-时, 磺胺甲恶唑的降解率出现一定程度的差异, 具体表现为低质量浓度促进光解, 高质量浓度抑制光解。在紫外光照射下, NO3-的最大吸收波长为302 nm, 发生反应:,,,光解产物。
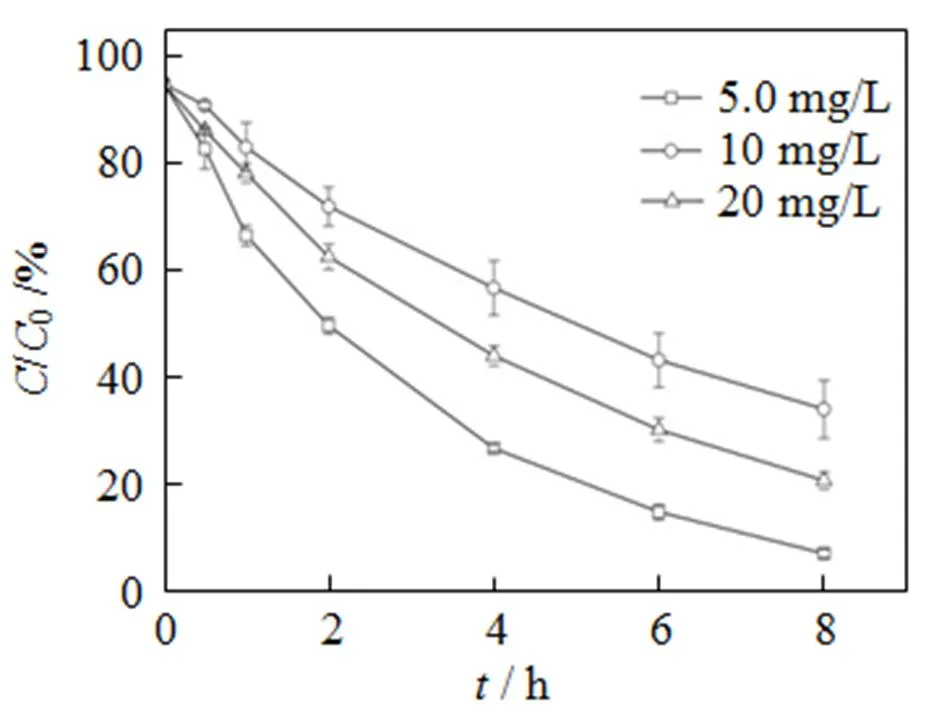
图6 不同质量浓度硝酸根离子对光降解的影响
采用准一级动力学模型拟合后, 获得的结果表明降解曲线符合该模型。当加入1 mg/L的NO3-时, 其降解速率常数为0.20 h-1, 降解半衰期为3.47 h; 当质量浓度升高至5 mg/L, 其降解速率常数为0.31 h-1, 降解半衰期为2.24, 降解速率明显提高, 说明NO3-的存在有助于自由基的产生, 从而引起磺胺甲恶唑的降解。但是当NO3-质量浓度上升到10 mg/L时降解速率反而出现下降(0.12 h-1), 降解半衰期为5.78 h, 这可能是由于过量的NO3-吸收了大量的光子, 从而减少与磺胺甲恶唑的作用。
3 结论
磺胺类药物广泛存在于各种水体中, 它们在太阳光的照射下可能会发生一定程度的降解。本实验的研究结果表明了磺胺类药物中的磺胺甲恶唑在模拟太阳光下不仅能够发生降解, 而且随着环境条件的变化其降解率会发生一定变化, 如pH值、质量浓度和NO3-等。本实验的研究结果对于磺胺甲恶唑的水环境行为及其生态风险评估提供一定的基础数据。
参考文献:
[1] Ellis J B. Pharmaceutical and personal care products (PPCPs) in urban receiving waters [J]. Environmental Pollution, 2007, 144: 184-189.
[2] Barcelo D, Petrovic M. Pharmaceuticals and personal care products (PPCPs) in the environment [J]. Analytical and Bioanalytical Chemistry, 2007, 387: 1 141-1 142.
[3] Richardson B J, Lam P K S, Martin M. Emerging chemicals of concern: Pharmaceuticals and personal care products (PPCPs) in Asia, with particular reference to Southern China [J]. Marine Pollution Bulletin, 2005, 50: 913-920.
[4] Tao R, Ying G G, Su H C. Detection of antibiotic resistance and tetracycline resistance genes in Enterobacteriaceae isolated from the Pearl rivers in South China [J]. Environmental Pollution, 2010, 158: 2 101-2 109.
[5] Su H C, Ying G G, Tao R, et al. Class 1 and 2 integrons,resistance genes and antibiotic resistance inisolated from Dongjiang River, South China [J]. Environmental Pollution, 2012, 169: 42-49.
[6] Liu F, Ying G G, Yang L H, et al. Terrestrial ecotoxicological effects of the antimicrobial agent triclosan [J]. Ecotoxicology and Environmental Safety, 2009, 72: 86-92.
[7] Yang J F, Ying G G, Zhao J L, et al. Simultaneous determination of four classes of antibiotics in sediments of the Pearl Rivers using RRLC–MS/MS [J]. Science of the Total Environment, 2010, 408: 3 424-3 432.
[8] Zhou L J, Ying G G, Zhao J L, et al. Trends in the occurrence of human and veterinary antibiotics in the sediments of the Yellow River, Hai River and Liao River in northern China [J]. Environmental Pollution, 2011, 159: 1 877-1 885.
[9] Trovó A G, Nogueira R F P, Agüera A, et al. Photodegradation of sulfamethoxazole in various aqueous media: persistence, toxicity and photoproducts assessment [J]. Chemosphere, 2009, 77: 1 292-1 298.
[10] Prados-Joya G, Sánchez-Polo M, Rivera-Utrilla, et al. Photodegradation of the antibiotics nitroimidazoles in aqueous solution by ultraviolet radiation [J]. Water Research, 2011, 45: 393-403.
[11] Nasuhoglu D, Yargeau V, Berk D. Photo-removal of sulfamethoxazole (SMX) by photolytic and photocatalytic processes in a batch reactor under UV-C radiation (lambdamax = 254 nm) [J]. Journal of Hazardous Materious, 2011, 186: 67-75.
(责任编校:刘晓霞)
Photodegradation kinetics of antibiotic sulfamethxoazole by simulated sunlight in aqueous solution
Wen Changhong1, Mao Shun2, Zheng Liying2, Li Wenjun2, Yang Jifeng2
(1. Department of Horticulture, Chizhou Vocational and Technical College, Chizhou 247000, China; 2. College of Chemistry and Chemical Engineering, Hunan University of Arts and Science, Changde 415000, China)
To understand environmental behavior of sulfa drugs in aqueous phase, the photodegradation characteristics are investigated under simulated sunlight irradiation using sulfamethxoazole as a model chemical. During the experiment, the effects of different factors on degradation are explored. The results show that sulfamethoazole could be degraded and the degradation rate constant could decline as the increase of the chemical concentration and the highest value was 0.36 h-1at the concentration of 5 mg/L; The degradation rate was higher in acidic condition than that in alkali condition and the shortest half life of degradation was 2.10 h at pH5; For nitrate ion, low level could enhance the degradation rate but inhibit for high level.
sulfamethoxazole; photodegradation; simulated sunlight
http://www.cnki.net/kcms/detail/43.1420.N.20150428.1621.001.html
10.3969/j.issn.1672–6146.2015.02.015
X 13
1672–6146(2015)02–0047–04
杨基峰, clark_yang@yeah.net。
2015-02-27
中国博士后基金(2014M562104); 湖南省自然科学基金(13JJ3155); 常德市科技计划项目(2014J188)

