壳聚糖固化菜籽多酚微球对Pb、Cd、Hg的吸附研究
安薪憬 张沙沙 魏瑞芝 王承明
(华中农业大学,武汉 430070)
壳聚糖固化菜籽多酚微球对Pb、Cd、Hg的吸附研究
安薪憬 张沙沙 魏瑞芝 王承明
(华中农业大学,武汉 430070)
通过甲醛将菜籽多酚固定在壳聚糖微球,制成壳聚糖固化菜籽多酚微球,研究其对水中Pb、Cd、Hg离子的吸附效果。该微球对Pb、Cd、Hg的最大吸附量分别为88.50、117.15、147.25 mg/g。其吸附行为符合Freundlich等温吸附方程。壳聚糖固化菜籽多酚微球对Pb、Cd、Hg的吸附动力学可以用拟二级速率方程来描述。使用4种解吸剂分别对3种离子进行解吸试验,发现硝酸对3种离子的解吸效果较好,该吸附剂可重复使用。
壳聚糖 菜籽多酚 微球 重金属离子 吸附
菜籽多酚是存在于菜籽饼粕中的一类植物次生代谢产物[1],且其含量高于其他油料粕,大约是大豆粕的30倍[2]。菜籽多酚作为抗营养因子,能与蛋白质、维生素、多糖等结合,影响菜籽粕中蛋白质、碳水化合物等在动物体内的消化吸收,甚至产生毒性作用[3],限制了其在饲料中的应用。研究表明,菜籽多酚具有很强的抗氧化和清除自由基的作用,同时具有抗肿瘤、降血糖、抑菌等生理活性[4-8]。将多酚类物质固化在纤维素、胶原纤维、壳聚糖等介质上可得到对许多金属离子有较高吸附容量的吸附材料[9-11]。酚类物质中2个相邻的酚羟基能以氧负离子的形式与金属离子螯合形成稳定的五元环生成物[12]。壳聚糖作为自然界中存在的惟一的碱性多糖,具有资源丰富,安全无毒等优良的功能。壳聚糖粉末经交联反应,制成的壳聚糖微球,提高了其稳定性和机械强度[13],且便于回收利用。
本试验研究利用壳聚糖微球固化菜籽多酚,制得壳聚糖固化菜籽多酚微球,并研究该微球对Pb、Cd、Hg的吸附特性,以期掌握其应用规律。
1 材料与方法
1.1 试剂与仪器
壳聚糖粉末、PEG、戊二醛溶液:国药集团化学试剂有限公司;液体石蜡、戊二醛、NaOH、无水乙醇、Pb(NO3)2、Cd(NO3)2、HgCl2、及其他试剂等均为分析纯;菜籽多酚:自提取。
722型分光光度计:天津市普瑞斯仪器有限公司;AA-6300原子吸收分光光度计:岛津国际贸易(上海)有限公司。
1.2 试验方法
1.2.1 壳聚糖微球的制备
称取10.0 g壳聚糖粉末,溶于200 mL 2%的醋酸水溶液中,加入1.0 g PEG,充分搅拌使之全溶,然后加入200 mL的液体石蜡和1 mL乳化剂,继续搅拌使体系均匀。加入50 mL戊二醛,反应2 h。混合物倾入大量的V(无水乙醇)∶V=10%NaOH水溶液)=1∶1中,搅拌后抽滤,反复洗涤得壳聚糖微球[9,14]。
1.2.2 壳聚糖固化菜籽多酚微球的制备
配制一定质量分数的菜籽多酚溶液100 mL,加入1.0 g壳聚糖微球,调节 pH,加入一定体积的2.5%戊二醛溶液,水浴40℃反应一段时间后,过滤,洗涤得到壳聚糖固化菜籽多酚微球。
试验得到最优固定化条件:在40℃下,取1.0 g壳聚糖微球,加入100 mL质量分数为0.22%的菜籽多酚溶液,调节pH值为4.3,加入0.9 mL 2.5%的戊二醛溶液,反应7 h后,得到壳聚糖固化菜籽多酚微球,菜籽多酚的固定量为107.18 mg/g。
1.2.3 pH值对吸附容量的影响
分别取壳聚糖微球和固化菜籽多酚微球0.10 g,放入质量分数为 200.0 mg/L的 Pb(NO3)2、Cd(NO3)2、HgCl2溶液中,调节各溶液的 pH值分别为3、4、5、6、7。在 303 K下振荡吸收 24 h,测定吸附后溶液中金属离子的质量分数,计算吸附剂对不同金属离子的吸附容量。
1.2.4 温度对吸附平衡的影响
取壳聚糖固化菜籽多酚微球0.10 g,放入质量分数为200.0 mg/L的 Pb(NO3)2、Cd(NO3)2、HgCl2溶液中,分别调节各溶液的pH值至最佳pH条件。分别在303、313、323 K下振荡吸收24 h,测定吸附后溶液中金属离子的质量分数,计算壳聚糖固化菜籽多酚微球对不同金属离子的吸附容量。
1.2.5 吸附动力学试验
在一定的时间间隔内取样分析各溶液中离子的含量,试验条件见表1。
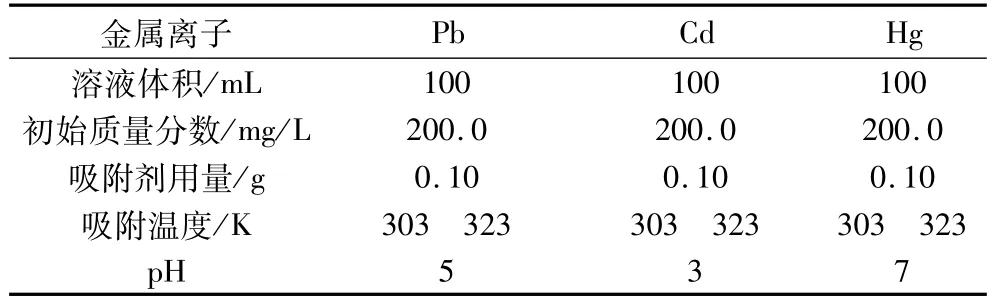
表1 吸附动力学试验条件
1.2.6 Pb、Cd、Hg的混合吸附
配制 Pb、Cd、Hg离子质量分数为 66.8 mg/L的混合液,分别调节 pH值为3、4、5、6、7,加入到 0.10 g壳聚糖固化菜籽多酚微球中,测定不同pH值时,壳聚糖固化菜籽多酚微球对混合溶液中不同金属离子的吸附容量。
1.2.7 解吸试验
分别配制 Pb2+、Cd2+、Hg2+的水溶液,加入壳聚糖固化菜籽多酚微球,在最佳吸附条件下进行吸附试验后,过滤,分别取0.10 g吸附后的壳聚糖固化菜籽多酚微球,加入到100 mL 0.02 mol/L柠檬酸、0.02 mol/L H3PO4、0.1 mol/L HNO3、0.1 mol/L氨水溶液中,在303 K下解吸24 h后,测定解吸液中各离子含量,计算解吸量。
1.2.8 壳聚糖固化菜籽多酚微球可重复利用试验
配制 Pb2+、Cd2+、Hg2+的溶液,加入壳聚糖固化菜籽多酚微球,分别在最佳条件下进行吸附试验,并用0.1 mol/L HNO3溶液进行解吸试验,反复进行4次,每次吸附和解吸后测定各离子含量。
1.2.9 金属离子含量的测定
原子吸收分光光度计测定溶液中金属离子的含量。
2 结果与讨论
2.1 壳聚糖固化菜籽多酚微球的鉴定
通过对壳聚糖微球和壳聚糖固化菜籽多酚微球的IR扫描图谱分析,确定菜籽多酚是否被固定。结果显示:在3 448 cm-1附近的宽峰变窄,这可能是由于酚类物质中的羟基参加反应导致的;而在1 718 cm-1处出现羰基特征吸收峰,1 652 cm-1处出现苯环骨架振动吸收,765 cm-1处出现苯环C—H键的面外弯曲振动吸收峰。因此,可以说明菜籽多酚已经被固定到壳聚糖微球上了。
2.2 pH值对平衡吸附容量的影响
由图1~图3可知,壳聚糖固化菜籽多酚微球对3种离子的吸附比没有固化菜籽多酚的壳聚糖微球的效果好,且pH值对3种离子的吸附有影响。
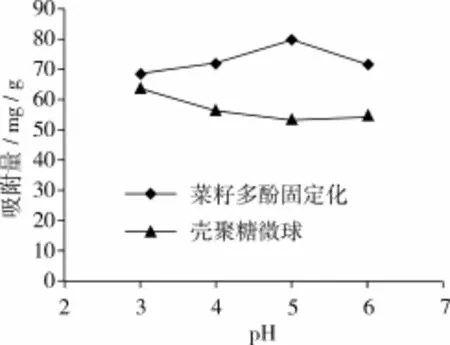
图1 pH值对Pb吸附量的影响
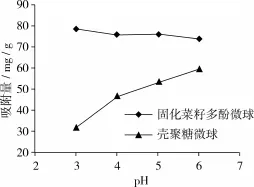
图2 pH值对Cd的吸附量的影响
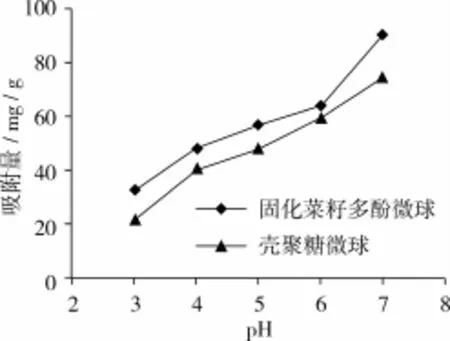
图3 pH值对Hg吸附量的影响
HgCl2在水中主要以[HgCl]+和(HgCl2)2的形式存在。随着pH升高,离解反应减弱,聚合反应增强,溶液中(HgCl2)2增加。由软硬酸碱原理可知,中性分子是比阳离子更软的酸,更容易与吸附剂结合。因此,壳聚糖固化菜籽多酚微球对Hg的吸附容量随pH值升高而增加[18]。
而Pb和Cd在水溶液中可发生溶剂化、水解和聚合等反应,形成几种不同的水解产物。当pH值升高,水解和聚合作用增强,这可能影响多酚与Pb和Cd的配位结合,导致吸附容量下降[18]。
2.3 温度对吸附容量的影响
由图4~图6可以看出,随着温度升高,壳聚糖固化菜籽多酚微球对Hg和Cd的平衡吸附量明显增加,表明该吸附反应是一个吸热过程。然而,温度升高对Pb的平衡吸附量影响并不大,表明壳聚糖固化菜籽多酚微球对Pb的吸附反应热不明显。
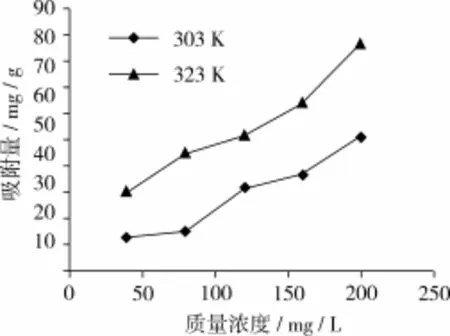
图4 温度对壳聚糖固化菜籽多酚微球吸附Hg的影响
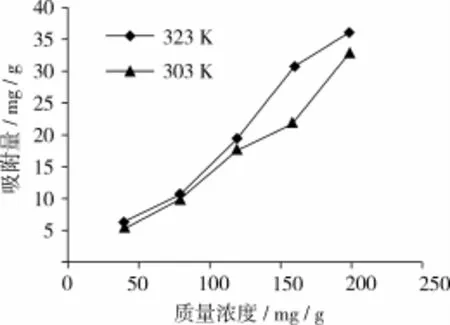
图5 温度对壳聚糖固化菜籽多酚微球吸附Pb的影响

图6 温度对壳聚糖固化菜籽多酚微球吸附Cd的影响
Freundlich方程可以用来描述金属离子在吸附剂表面的吸附行为,其方程式为:

式中:qe为平衡吸附量/mg/g;Ce为平衡质量浓度/mg/L;k及 1/n为 Freundlich参数(分别与吸附容量和吸附强度有关)。用 Freundlich方程分别对303 K和323 K时Pb、Cd、Hg的吸附过程进行拟合分析,结果见表2。Freundlich模型中,1/n为表示吸附强度的参数,n>1时,有利于吸附,n值越大,表示吸附作用力越强;k值越大,表示吸附容量越大。由表2可以看出,随着温度的升高,n值变大,k值变大,说明温度升高使得壳聚糖固化菜籽多酚微球对离子的吸附强度增加,且吸附容量增加,这与试验结果一致。

表2 壳聚糖固化菜籽多酚微球吸附Pb、Cd、Hg的Freundlich参数
2.4 吸附动力学
图7~图9是壳聚糖固化菜籽多酚微球对Pb、Cd、Hg的吸附动力学曲线。由图7~图9可知,在吸附开始一段时间内,壳聚糖固化菜籽多酚微球对3种离子的吸附量随时间变化显著,在一定时间后,吸附量增加趋于平缓,直至达到吸附平衡。微球对Pb、Cd、Hg的最大吸附量分别为88.50、117.15、147.25 mg/g。
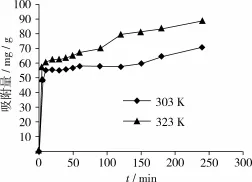
图7 壳聚糖固化菜籽多酚微球对Pb的吸附动力学曲线

图8 壳聚糖固化菜籽多酚微球对Cd的吸附动力学曲线

图9 壳聚糖固化菜籽多酚微球对Hg的吸附动力学曲线
分别用拟一级动力学方程和拟二级动力学方程对Pb、Cd、Hg的上述吸附过程进行拟合分析。拟一级动力学方程和拟二级动力学方程式为:
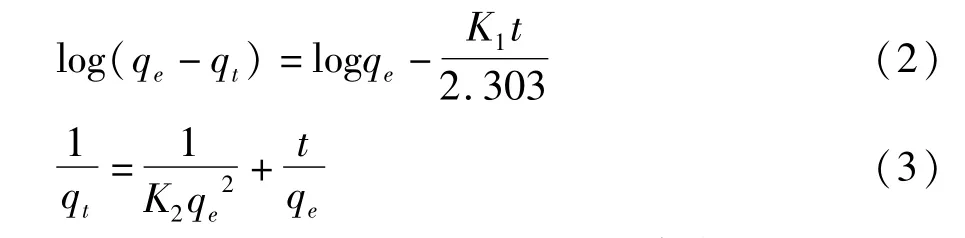
式中:K1为拟一级动力学方程的速率常数/min-1;K2为拟二级动力学方程的速率常数/g/mg·min;qe和qt分别为平衡时间和t时间的吸附量/mg/g。
由表3试验数据可得,拟一级动力学方程和拟二级动力学方程都能拟合吸附动力学的试验数据,但是拟二级的拟合效果较好(R>0.99),且计算所得的qe与实际测得数据接近。因此,拟二级动力学方程可以适用于壳聚糖固化菜籽多酚微球对3种重金属离子的吸附过程。

表3 固定菜籽多酚微球吸附金属离子的动力学参数
2.5 混合吸附试验
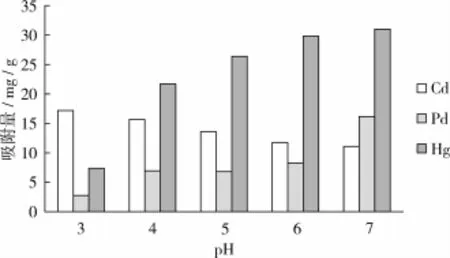
图10 pH值对混合溶液中Pb、Cd、Hg吸附量的影响
图10结果显示,在混合溶液中壳聚糖固化菜籽多酚微球对3种离子吸附时,pH值的影响与其单独吸附时相似,随pH值升高,壳聚糖固化菜籽多酚微球对Hg和Pb的吸附量增加,对Cd的吸附量减小。
2.6 解吸试验
采用不同的解吸剂分别对吸附了Pb、Cd、Hg 3种重金属离子的壳聚糖固化菜籽多酚微球进行解吸试验,结果见图11。结果显示,硝酸对Pb、Hg的解吸效果最好,柠檬酸对Cd的解吸效果最好。总体而言,硝酸对3种离子的解吸效果均较好,而氨水对3种离子的解吸效果最差,因此考虑用硝酸进行解吸。
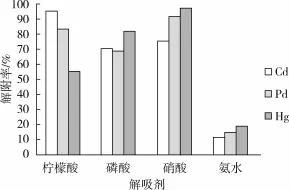
图11 不同的解吸剂对解吸效果的影响
2.7 重复利用次数
通过对Pb、Cd、Hg离子混合液进行4次吸附-解吸试验,测定每次吸附量,结果见图12。有结果可以看出,重复使用壳聚糖固化菜籽多酚微球,该微球对3种离子的吸附量逐次下降,到第4次时壳聚糖固化菜籽多酚微球对3种离子的吸附量下降到第1次的30%左右。因此考虑该微球使用2~3次后进行再生过程。
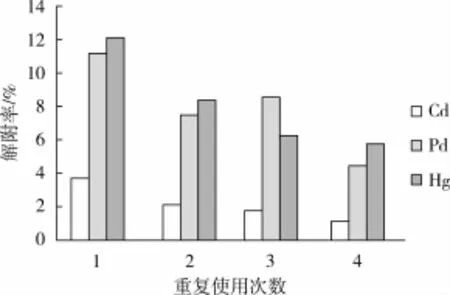
图12 重复利用壳聚糖固化菜籽多酚微球对Pb、Cd、Hg吸附量的影响
3 结论
通过甲醛将菜籽多酚固定在壳聚糖微球,制成壳聚糖固化菜籽多酚微球,研究了其对水中Pb、Cd、Hg重金属离子的吸附效果。由于离子在水溶液中的存在形式不同,因此壳聚糖固化菜籽多酚微球对3种离子的吸附过程有些微不同,该微球对Pb、Cd、Hg的最大吸附量分别为 88.50、117.15、147.25 mg/g。但是,该微球对3种重金属离子的吸附行为符合Freundlich等温吸附方程,其吸附动力学可以用拟二级速率方程来描述。
研究中分别使用4种解吸剂对3种离子进行解吸试验,发现硝酸对3种离子的解吸效果最好,且该微球可重复使用性较强。因此,壳聚糖固化菜籽多酚微球对Pb、Cd、Hg的吸附效果较好。
[1]肖頔,王承明.水酶法提取油菜籽粕中多酚的研究[J].中国粮油学报,2012,27(4):50-53,58
[2]Shahidi F,Naczk M.An overview of the phenolics of canola and rapeseed:chemical,sensory and nutritional significance[J].Journal of the American Oil Chemists’Society,1992,69(9):917-924
[3]刘世娟,李吕木.菜籽多酚的抗营养作用机理及减量措施[J].中国粮油学报,2011,26(4):112-117
[4]严奉伟,罗祖友,薛照辉,等.菜籽多酚级分-1的体外抗氧化作用及其机制[J].中国粮油学报,2005,20(5):115-119
[5]严奉伟,严赞开,王辰,等.菜籽多酚在四氧嘧啶致糖尿病小鼠体内的降血糖作用[J].食品科技,2006,31(12):198-201
[6]严奉伟,郝晶晶.菜籽多酚抑菌作用研究[J].食品工业,2011(2):1-2
[7]王承明,严奉伟,吴谋成.菜籽多酚的抗肿瘤和增强免疫作用研究[A].第十二届国际油菜大会筹备委员会.第十二届国际油菜大会论文集[C].第十二届国际油菜大会筹备委员会,2007:9
[8]严奉伟,罗祖友,薛照辉,等.菜籽多酚的抗氧化作用[J].中国油脂,2005,30(7):54-57
[9]肖玲,贲伟伟.壳聚糖固化单宁微球的制备及其吸附性能[J].精细化工,2006,23(8):733-737
[10]陈玲,寇正福,刘坐镇,等.大孔球形纤维素固定化单宁的性能表征及其在黄酒中的应用[J].离子交换与吸附,2006,22(5):446-454
[11]王茹,廖学品,侯旭,等.胶原纤维固化杨梅单宁对Pb2+、Cd2+、Hg2+的吸附[J].林产化学与工业,2005,25(1):10-14
[12]Palma Graciela,Freer Juanita,Baeza Jaime.Removal of metal ions by modified Pinusradiata bark and tannins from water solutions[J].Water research,2003,37(20)::4974-4980
[13]宋艳艳,孔维宝,宋昊,等.磁性壳聚糖微球的研究进展[J].化工进展,2012,31(2):345-354
[14]刘秀芝,肖玲,杜予民,等.邻氨基苯酚改性壳聚糖树脂的制备及吸附性能的研究[J].离子交换与吸附,2002,18(5):399-405
[15]Singleton V L,Joseph A,Rossi,Jr.Colorimetry of total phenolics with phosphomolybdic-phosphototungstic acid reagents[J].American Journal for Enology and Viticulture,1965,16(3):144-158
[16]李海燕.基于水处理的壳聚糖树脂的制备、表征及功能性研究[D].青岛:中国海洋大学,2011
[17]张力平.多酚型大孔吸附树脂的制备及吸附机理的研究[D].北京:北京林业大学,2005
[18]王茹.胶原纤维固化杨梅单宁对金属离子的吸附研究[D].成都:四川大学,2006.
Adsorption of Pb,Cd and Hg on Polyphenol Immobilized Chitosan Microspheres
An Xinjing Zhang Shasha Wei Ruizhi Wang Chengming
(Huazhong Agricultural University,Wuhan 430070)
Polyphenols have been immobilized on chitosan microspheres by formaldehyde in the paper.The adsorption effects of Pb,Cd and Hg ions on polyphenol immobilized chitosan microspheres have been studied as well.The maximum adsorption capacities of Pb,Cd and Hg on the microspheres were 88.50,117.15,147.25 mg/g respectively.The adsorption performance was corresponded with Freundlich isotherm equation.The adsorption kinetics of Pb,Cd and Hg on polyphenol immobilized chitosan microspheres could be expressed by pseudo-second-rate equation.Four categories of desorbent were successively used in ion desorption experiments,and the results showed that the nitrate was the best for desorption of three ions.Further,the adsorbent was available to be reused.
chitosan,rapeseed polyphenol,microsphere,heavy metal ions,adsorption
O636.1
A
1003-0174(2015)09-0098-05
2014-04-01
安薪憬,女,1989年出生,硕士,粮食、油脂与植物蛋白工程
王承明,男,1964年出生,教授,博士生导师,农产品加工与贮藏、食品安全、食品化学

