异喹啉骨架的化合物合成研究进展
异喹啉骨架的化合物合成研究进展
唐天
(东华理工大学化学生物与材料科学学院,江西 南昌 330013)
摘要:含有异喹啉骨架的化合物在医药、临床医学,以及构建分子结构多样化的高纯度类天然产物库等方面起着重要的作用而深受关注。文章综述了近年来异喹啉骨架化合物合成方法的研究进展。
关键词:药物中间体异喹啉合成进展
1.引言
含有异喹啉骨架的化合物是一类非常重要的药物中间体,广泛应用于很多具有生物活性的天然产物和药物分子中[1]。
自然界中约10,000种生物碱按照基本结构可分为60类左右,其中最大的一类就是含有异喹啉骨架的生物碱。再细分可主要分为苄基异喹啉类(如罂粟碱)、双苄基异喹啉类(汉防己所含生物碱,如汉防己甲素)、原小檗碱类(黄连所含生物碱,如小檗碱)和吗啡类(如吗啡、可待因)等[2]。
H-吡唑并[5,1-a]异喹啉类衍生物是异喹啉化合物中一类很好的例子,它在医学领域已经表现出了显著的生物活性,如下图(Figure 1-1)所示的化合物A,复旦大学吴劼课题组于2010年合成的,属于1-取代H-吡唑并[5,1-a]异喹啉类衍生物。该化合物在生物测试中,对细胞分裂周期蛋白25B(CDC25B)、T细胞蛋白酪氨酸磷酸酶(TC-PTP)、蛋白酪氨酸磷酸酶1B(PTP1B)表现出良好的抑制能力[3]。
而近些年来,合成此类化合物的方法也层出不穷,

Figure 1-1
各显神通[4,5]。
其中,利用邻炔基苯甲醛腙合成H-吡唑并[5,1-a]异喹啉衍生物的方法[5],在近几年来倍受关注。
2.邻炔基苯甲醛腙合成H-吡唑并[5,1-a]异喹啉衍生物
自从2009年,丁秋平博士等发现了邻炔基苯甲醛腙可以在亲电试剂(如单质碘、单质溴或氯化碘)的作用下,温和而高效地生成一系列可以稳定存在的4-卤代异喹啉氮氮偶极子(Scheme 2-1)[6],随后还可以在过渡金属催化剂的催化下进一步发生偶联反应,引入不同的官能团。

Scheme 2-1
在之后的研究中,他们又发现当用催化量的路易斯酸(如三氟甲磺酸银)代替单质碘、溴和氯化碘等亲电试剂时,可以高效地得到4-位无取代的异喹啉氮氮叶立德(Scheme 2-2)。

Scheme 2-2
不论是4-位有取代还是4-位无取代的异喹啉氮氮叶立德,均可以利用来与含有不饱和键的化合物发生[3+2]环化反应,构建H-吡唑并[5,1-a]异喹啉衍生物。
之后,陈知远博士等以邻炔基苯甲醛腙为原料,三氟甲磺酸银为路易斯酸催化剂,在生成了4-位无取代的异喹啉氮氮叶立德中间体之后,再在碱的作用下直接与端炔进行[3+2]环化反应,合成了一系列2-取代H-吡唑并[5,1-a]异喹啉衍生物(Scheme 2-3)[5a]。

Scheme 2-3
随后,又分别在单质碘和单质溴的作用下,通过生成4-卤代异喹啉氮氮偶极子中间体,再与丁炔二酸二甲酯或末端炔烃反应,合成6-卤代H-吡唑并[5,1-a]异喹啉衍生物(Scheme 2-4,2-5)[5b,5c];并可以利用6-位的卤素进一步与末端炔烃或取代硼酸发生偶联反应,从而合成6-位其他取代的H-吡唑并[5,1-a]异喹啉衍生物。
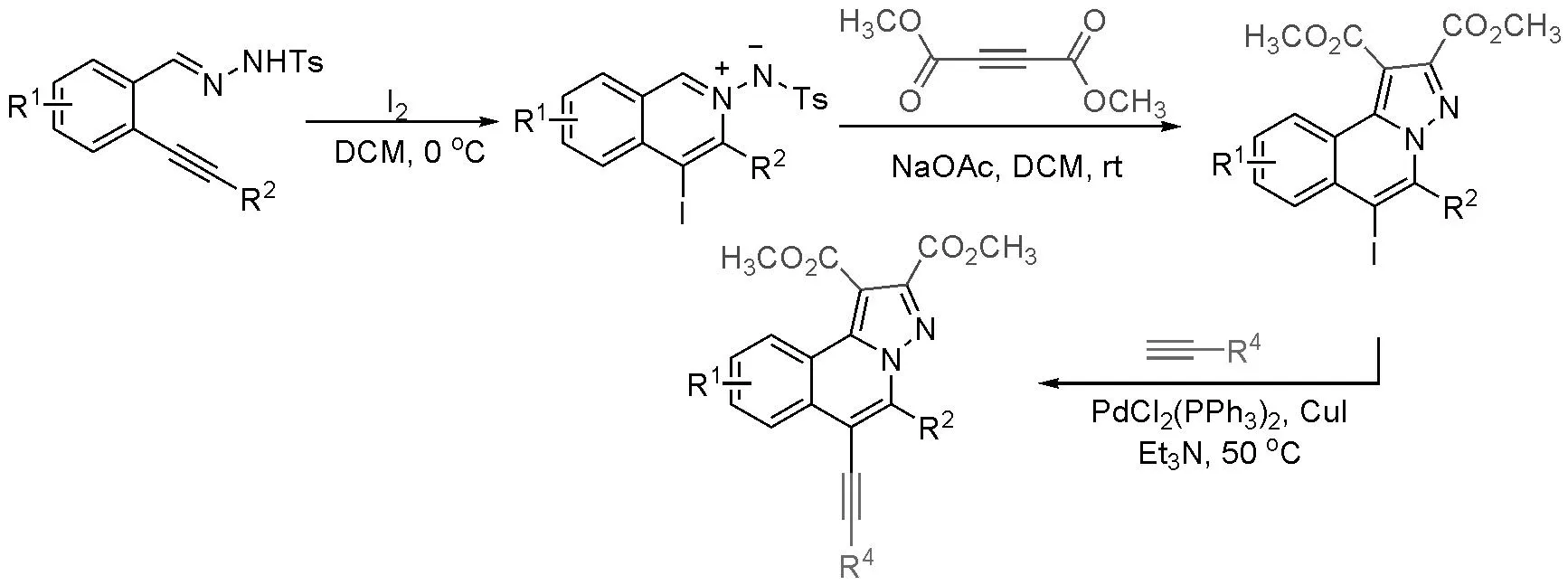
Scheme 2-4
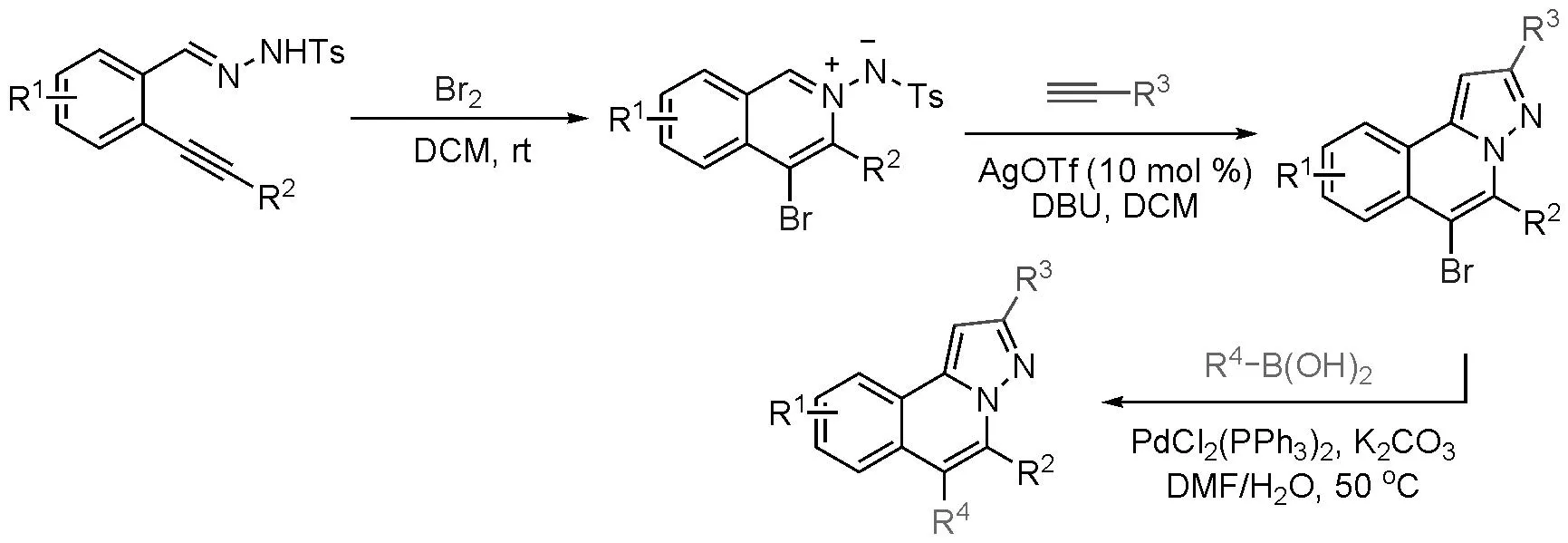
Scheme 2-5
2010年,吴劼课题组利用与以往相似的策略,又发展了一例邻炔基苯甲醛腙与烯醇硅醚的环化反应,合成了一系列1,2-二取代的H-吡唑并[5,1-a]异喹啉衍生物(Scheme 2-6)[5d]。

Scheme 2-6
同年,吴劼组利用单质溴的促进作用,使邻炔基苯甲醛腙转化为4-溴异喹啉氮氮偶极子中间体,进而在DABCO的作用下、NMP中、70℃下,与α,β-不饱和羰基化合物反应,合成了一系列1-取代的H-吡唑并[5,1-a]异喹啉衍生物(Scheme 2-7)[5e];并发现,当反应条件改为K3PO4作碱、DMA作溶剂、室温时,该反应可以给出3-对甲苯磺酰基四氢吡唑并[5,1-a]异喹啉衍生物。
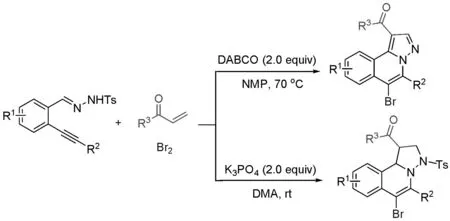
Scheme 2-7
Yao等也在吴劼组的研究工作基础上,提出了以1,1-二酯基环丙-2-烯作为进攻异喹啉氮氮偶极子的亲核试剂,在AgOTf和RhCl(PPh3)3的共催化下,同样实现了1-取代H-吡唑并[5,1-a]异喹啉衍生物的合成(Scheme 2-8)[5f]。

Scheme 2-8
2013年,刘洪亮等也利用AgOTf和RhCl(PPh3)3的共催化,以2-乙烯基环氧乙烷为亲核试剂,进攻由邻炔基苯甲醛腙原位生成的异喹啉氮氮偶极子,合成了一系列1-醛基-2-甲基的H-吡唑并[5,1-a]异喹啉衍生物(Scheme 2-9)[5g]。

Scheme 2-9
3.邻炔基苯甲醛肟合成含有异喹啉骨架的化合物
除了利用邻炔基苯甲醛腙合成含有异喹啉骨架的化合物外,利用邻炔基苯甲醛肟也能在亲电试剂(如单质碘、单质溴或氯化碘)或路易斯酸的作用下发生6-endo环化反应,从而得到含有异喹啉骨架的异喹啉氮氧偶极子,从而可以用来构建结构不同的含有异喹啉骨架的化合物。接下来,我将对近几年来利用邻炔基苯甲醛肟合成含有异喹啉骨架的化合物的方法进行概述[7,8]。
2008年,复旦大学的丁秋平博士等[7a]利用邻炔基苯甲醛肟在单质溴的作用下发生6-endo环化反应,合成了一系列可以稳定存在的异喹啉氮氧偶极子(Scheme 3-1)。

Scheme 3-1
2009年丁秋平博士等[8a]又利用串联反应将邻炔基苯甲醛肟在单质溴的作用下与丁炔二酸二甲酯反应,反应经过一个重排过程得到了一个非预期产物异喹啉甲亚胺叶立德(Scheme 3-2)。

Scheme 3-2
同年,Shin等[7b]利用三氟甲磺酸银和三氟甲磺酸的共催化实现了从邻炔基苯甲醛肟到异喹啉的转化。作者给出的机理解释是其反应过程经历了O-烷基肟类化合物的氧化还原反应(Scheme 3-3)。随后Zhang等[7c]也实现了类似的转化(Scheme 3-4)。
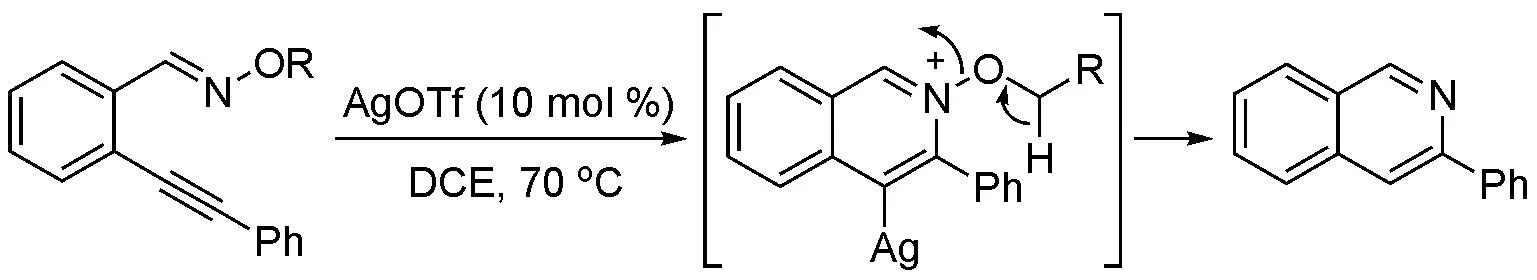
Scheme 3-3

Scheme 3-4
后来,余星昕博士等[7d]也以O-甲基邻炔基苯甲醛肟在卤化铜的作用下实现了4-卤代异喹啉衍生物的合成(Scheme 3-5)。
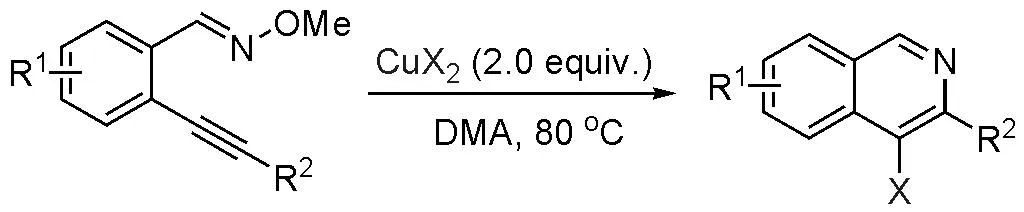
Scheme 3-5
此外,Shin等[7e]还用金催化剂通过串联环化反应实现了由邻炔基芳基酮肟到异喹啉或异吲哚的转化(Scheme 3-6)。
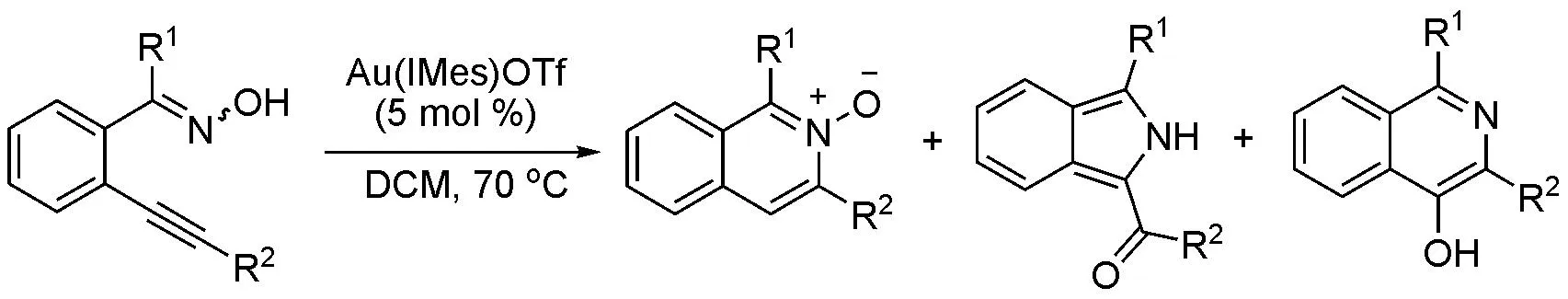
Scheme 3-6
2010年,叶盛青等[8b]在单质溴的作用下,使邻炔基苯甲醛肟转化为4-溴异喹啉氮氧偶极子中间体,进而与α,β-不饱和羰基化合物反应,合成了一系列1-取代4-溴异喹啉衍生物(Scheme 3-7)。
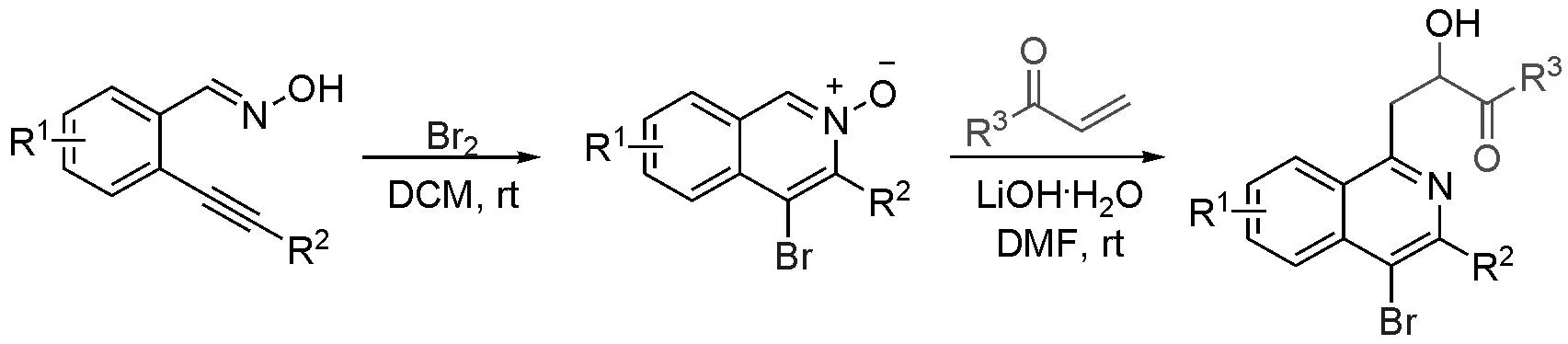
Scheme 3-7
2011年,叶盛青等[8c,8d]利用单质溴的促进作用,使邻炔基苯甲醛肟与碳二亚胺反应,在经历了4-溴异喹啉氮氧偶极子中间体后,转化了一系列1-取代-4-溴异喹啉衍生物;而后者可以进一步在钯的催化下与硼酸试剂发生偶联反应,生成1,4-二取代异喹啉衍生物(Scheme 3-8)。
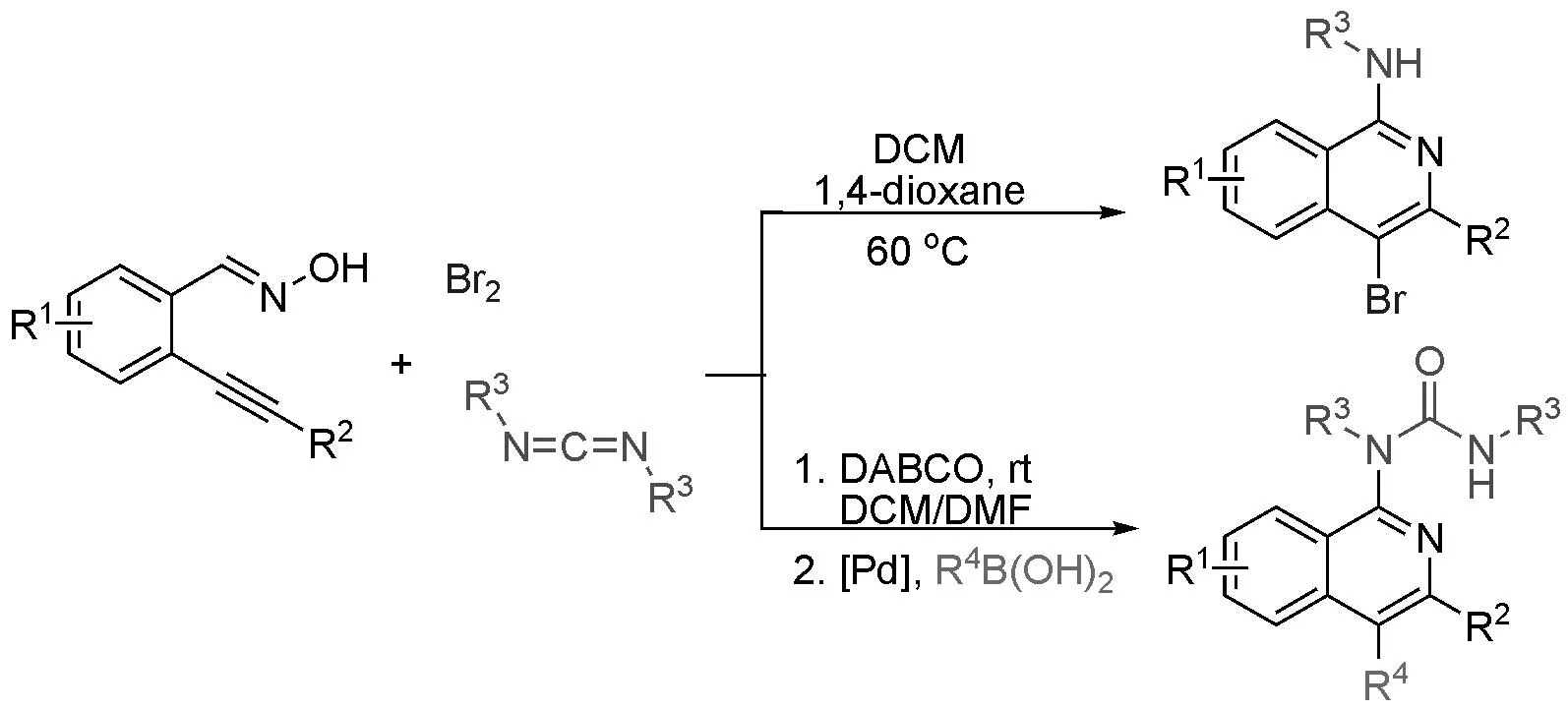
Scheme3-8
2012年,肖潜等[8e]也利用相似的策略,在三氟甲磺酸银的催化下,是邻炔基苯甲醛肟经历异喹啉氮氧偶极子中间体,再与咪唑或苯并咪唑类化合物反应,合成了一系列1-位咪唑类化合物取代的异喹啉衍生物(Scheme 3-9(1));同年,丁秋平等[8f]则是利用银和钯的共催化使邻炔基苯甲醛肟与卤代芳烃反应,合成了一系列1-芳基取代的异喹啉衍生物(Scheme 3-9(2));2013年,刘洪亮等[8g]在三氟甲磺酸银和三乙胺的共同作用下,将邻炔基苯甲醛肟与取代的乙酰氯反应,合成了一系列烷基酸异喹啉-4-酯衍生物(Scheme 3-9(3))。
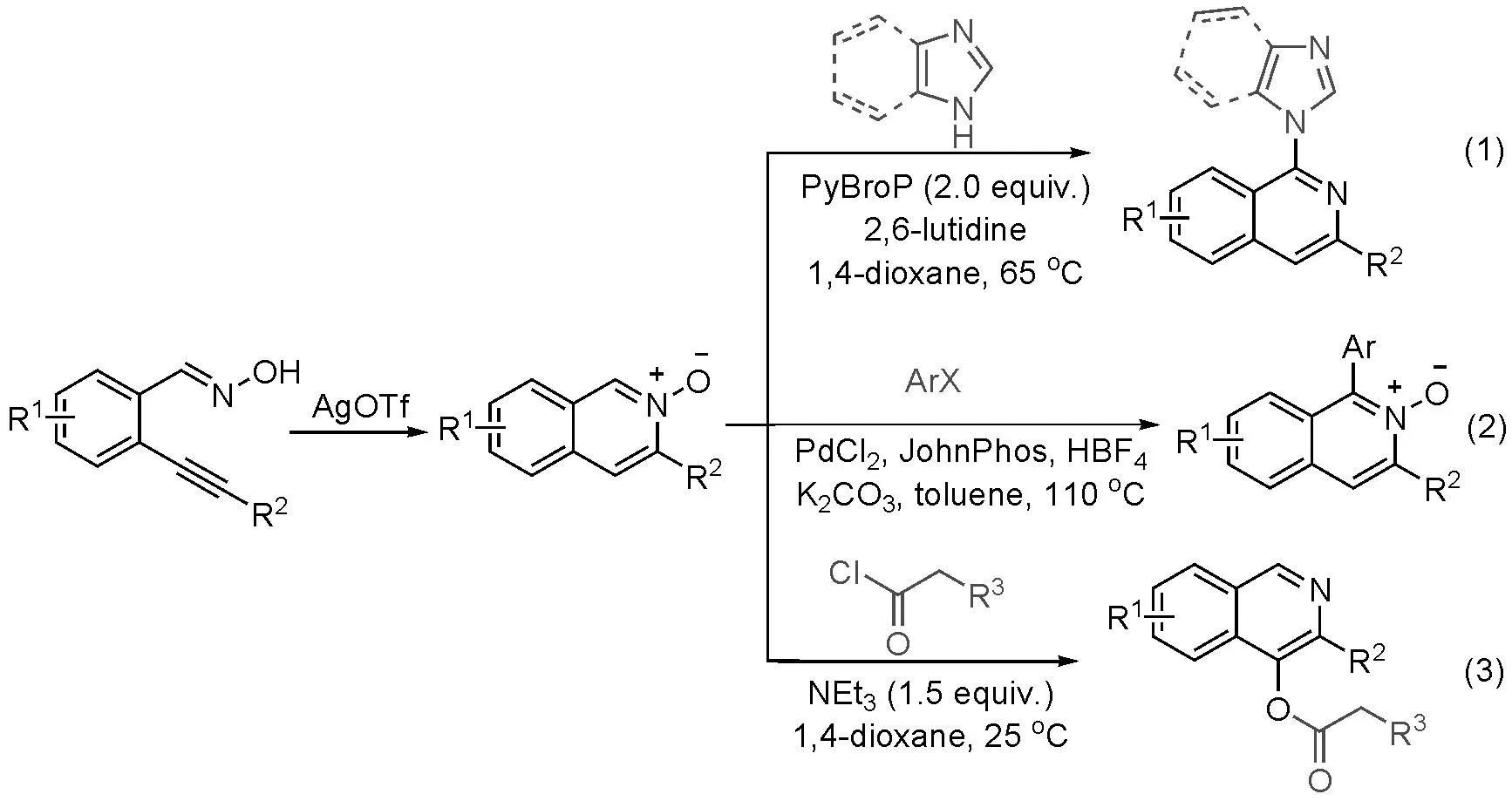
Scheme 3-9
综上所述,含有异喹啉骨架的化合物,包括H-吡唑并[5,1-a]异喹啉衍生物,是具有多种用途的小分子化合物,广泛存在于功能材料和具有显著生物活性的天然产物和候选药物分子中。因此,化学家们不断寻找新的高效方法来合成含有这类骨架化的合物。
参考文献
[1]Bentley,K.W.The Isoquinoline Alkaloids;Hardwood Academic:Amsterdam,1998;Vol.1
[2]杨秀伟,《生物碱》,化学工业出版社,2005,ISBN:7-5025-6331-8.
[3]Z.Chen,J.Wu,Org.Lett.2010,12,4856.
[4](a) Hernández,S.;SanMartin,R.;Tellitu,I.;Domínguez,E.Org.Lett.2003,5,1095.(b) Li,X.;Zhao,M.J.Org.Chem.2011,76,8530.(c) Huple,D.B.;Chen,C.-H.;Das,A.Liu,R.-S.Adv.Synth.Catal.2011,353,1877.
[5](a) Chen,Z.;Yang,X.;Wu,J.Chem.Commun.2009,45,3469.(b) Chen,Z.;Ding,Q.;Yu,X.;Wu,J.Adv.Synth.Catal.2009,351,1692.(c) Chen,Z.;Su,M.;Yu,X.;Wu,J.Org.Biomol.Chem.2009,7,4641.(d) Yu,X.;Chen,Z.;Yang,X.;Wu,J.J.Comb.Chem.2010,12,374.(e) Ren,H.;Ye,S.;Liu,F.;Wu,J.Tetrahedron,2010,66,8242.(f) Yao,L.;Yu,X.;Mo C.;Wu,J.Org.Biomol.Chem.2012,10,9447.(g) Liu,H.;Liu,G.;Qiu,G.;Pu,S.;Wu,J.Tetrahedron 2013,69,1476.
[6]Ding,Q.;Chen,Z.;Yu,X.;Peng,Y.;Wu,J.Tetrahedron Lett.2009,50,340.
[7](a) Ding Q.;Wu,J.Adv.Synth.Catal.2008,350,1850.(b) Huo,Z.;Tomeba,H.;Yamamoto,Y.Tetrahedron Lett.2008,49,5531.(c) Hwang,S.;Lee,Y.;Lee,P.H.;Shin,S.Tetrahedron Lett.2009,50,2305.(d) Zhang,J.;Gao,H.Adv.Synth.Catal.2009,351,85.(e) Yu,X.;Wu,J.J.Comb.Chem.,2009,11,895.
[8](a) Ding,Q.;Wang,Z.;Wu,J.J.Org.Chem.2009,74,921.(b) Ye,S.;Gao K.;Wu,J.Adv.Synth.Catal.2010,352,1746.(c) Ye,S.;Wang,H.;Wu,J.Tetrahedron 2011,67,4628.(d) Ye,S.;Wang,H.;Wu,J.ACS Comb.Sci.2011,13,120.(e) Xiao,Q.;Ye,S.;Zheng,D.;Zhang,L.;Wu,J.Mol.Divers.2012,16,261.(f) Ding,Q.;Wang,D.;Sang,X.;Lin,Y.;Peng,Y.Tetrahedron 2012,68,8869.(g) Liu,H.;Liu,G.;Pu,S.;Wang,Z.Org.Biomol.Chem.2013,11,2898.
Progress in synthesis of isoquinoline skeleton compounds
TANG Tian
(FacultyofChemistryBiologyandMaterialSciences,EastChinaInstituteofTechnology,JiangxiNanchang330013)
Abstract:The compounds containing isoquinoline skeleton have attracted much attention because of their widely applications in medicine,clinical medicine and generating the libraries of natural product-like compounds with structural diversity and stereo-chemical diversity.This review covers the latest results on the synthesis of isoquinoline skeleton compounds.
Key Words:drug intermediate;isoquinoline;synthesis;progress

