构建“盐类的水解”概念的教学策略
杨青山 叶 漫
(贵阳乐湾国际实验学校 贵州贵阳 550024)
构建“盐类的水解”概念的教学策略
杨青山 叶 漫
(贵阳乐湾国际实验学校 贵州贵阳 550024)
解决化学教学中的重点概念是提高教学质量的关键。以“盐类的水解”教学为例,由情景设计问题,以“概念”为主线,实现由易到难的突破,由感性上升到理性的认识高度,所有的教学都是围绕概念的建构展开的。
概念;盐类的水解;反思
盐类的水解概念的建构是化学知识在形成过程中所遵循的“从生动的直观抽象思维,并从抽象思维再到实践”的认识过程,为的是在化学教学中培养学生分析和解决问题的能力。在这个过程中,学生经历了一个由感觉、直觉和表象构成的感性认识阶段,同时也经历了一个由比较、分析、判断、推理等构成的理性思维阶段[1]。因此,笔者尝试在新课程的教学设计中变换思路,紧紧抓住某些盐电离出的离子会促进水的电离这一核心,让学生自己建构出盐类水解的概念。
一、教材和学情分析
盐类的水解是在水溶液中的离子平衡这一大背景下,对前两节所学的水的电离及溶液酸碱性知识的综合运用,有一定的思维难度。盐类水解概念的建构目的是让学生在获得基础知识与基本技能的过程中,学会学习并获得积极的情绪生活和良好的情感体验,鼓励学生在探究、讨论交流的过程中互相学习,以培养学生的应用意识和创新意识,体验科学的魅力。
笔者所教班级情况:学生基础扎实,具有较好的思考与质疑、交流与合作的学习习惯。通过教学,基本了解学生的学习现状和发展潜能,确定合适的教学起点、教学重点,使教学设计和教学实施具有针对性。
二、教学设计的基本思想
1.学习目标
知识与技能:掌握盐类水解的概念,从概念出发,理解实质,学会应用。
过程与方法:在探究盐溶液的酸碱性过程中,进一步引起对概念的重视,提高概念思维及分析问题的能力。
情感态度与价值观:通过分析盐类水解的过程,使学生亲历科学知识获取的过程,以学生的体验、感悟为依据,实现师生之间的情感交流,激发学生的学习潜能。
2.学习路径的设计

(1)体验思考 感知概念
对知识的兴趣的第一个源泉,第一颗火星,就在于教师对上课时要讲的教材和要分析的事实所抱的态度[2]。当学生完全进入到情境体悟(感知概念)中时,教师要峰回路转,提出有探究价值的问题来启发学生思考,使学生的注意力不知不觉地由实验现象转移到了本质问题——概念的建构。
(2)定向探究 形成概念
在教学中注重建构学生自主知识(形成概念),而不是将结论和答案直接灌输给学生,以学生为中心并不否认教师的指导作用,而是教师的角色发生了转变。在此阶段中,教师要有目的地提出针对性的问题,设计出有利于学生知识学习的问题。
(3)补偿矫正 理解概念
通过前面的概念建构,学生已经初步掌握了概念的基本内容,但对概念的实质、形成概念的条件,影响概念的因素等问题缺乏系统性的学习。因此,教师要加以引导,要对概念的形成教学过程中缺失进行补偿,增强学生对概念的理解,教师在补充中要充分起到主导的作用,切记不可将要补充的知识告诉学生,要让学生自己建构知识体系,这样对概念的理解、掌握、运用等会上升到一定的高度,有助于学生思维发散能力的培养。
(4)扩展迁移 深化概念
化学教学不仅要从学生的生活中提出化学问题,还必须结合现实生活中的实际问题,让学生运用化学知识和化学的思维方式去看待分析与解决现实中的问题,从而使学生体验到化学的价值,进一步感受到化学与现实生活的紧密联系,实现概念的深化。因此,教师提出与实际生活、生产有关的问题,供学生讨论,在交流的过程中对概念进行深化,扩展学生的知识,为下节课的教学埋下伏笔。
三、构建“盐类的水解”概念的教学过程
环节1:体验思考 感知概念
良好的开端是成功的一半,一个良好的导入能唤起学生的学习动机,激发学生的兴趣。在众多灵活多变的课堂引入方式中,探究实验以出现有趣现象,最能引起学生的求知欲望。
[教师]:创设情境
众所周知:酸溶液呈酸性,碱溶液呈碱性,那么对于酸和碱恰好中和生成的盐来说,其溶液是否一定呈中性?要想知道答案,各位不妨亲自动手一试。
[学生]:合作探究
4人一组,每组桌前事先提供三种盐溶液试剂。结果见表。

盐溶液 NaCl CH3COONa NH4Cl酸碱性 中性 碱性 酸性
[教师]:提出问题
由水电离产生的OH-与H+数目应该是相等的,当加入某些盐之后,溶液的酸碱性发生了明显的变化,表明c(OH-)不等于c(H+),无论盐的电离还是水的电离都不会直接导致溶液中c(OH-)和c(H+)不相等,那么,某些盐呈现不同酸碱性是什么原因呢?
[学生]:感知概念
以水的电离平衡为基础,分析盐类电离的阴、阳离子与水电离出的OH-与H+结合弱酸或弱碱的趋势,明确不同盐溶液呈现不同酸碱性的本质原因,同时深化对过去所学“离子反应发生条件”的认识。
设计意图:由于溶液的酸碱性取决于c(OH-)和c(H+)的相对大小,因此,水的电离平衡就必然地成为分析问题的关键。教师创设特定的探究实验,提出富有矛盾性的问题,为“盐类的水解”概念的学习定向做准备。
环节2:定向探究 形成概念
溶液中盐的电离都是在水分子的作用下,由此可见,在溶液中的各种离子并非独立存在,它们在运动过程中相互作用,那么,这些离子间的相互作用又是如何影响溶液酸碱性的呢?所以,对溶液呈现酸碱性原因的实质:溶液中c(OH-)和c(H+)不相等的原因进行定向探究。
[教师]:策略指导、组织讨论
教师:醋酸钠溶液中存在哪些电离?
学生:CH3COONa=Na++CH3COO
H2O⇌OH-+H+
教师:电离出的离子能相互反应吗?
学生:CH3COO-+H+⇌CH3COOH
教师:醋酸钠溶液为什么显“碱性”?
学生:CH3COONa电离出的CH3COO-与H2O电离出的H+结合,生成了弱电解质CH3COOH,促进了水的电离,最终使溶液中的 c(OH-)>c(H+)。
教师:那么,氯化铵溶液为什么显酸性呢?什么是盐类的水解?
[学生]:共同探讨、形成概念
学生概括总结,根据自己对盐类水解的认识和理解用自己的语言来表述,师生共同加以修正补充和完善,使之用词正确,表达科学。
设计意图:通过以上的合作探究,就是要使学生的思维从宏观深入到微观,从静态转到动态,并直抵问题的核心:盐类的水解。
环节3:补偿矫正 理解概念
[教师]:合理引导、促进提高
既然盐类水解存在水解平衡,能否从化学平衡的角度来探讨一下影响盐类水解平衡的因素有哪些?如何影响?
教师提供资料,辅助学生思考。
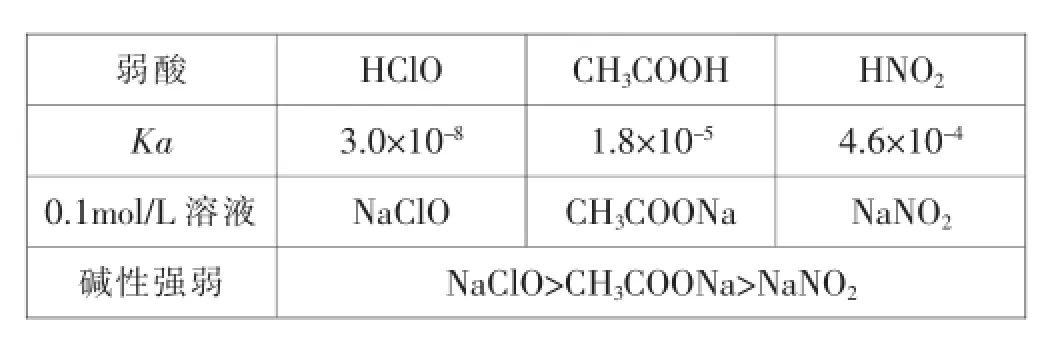
弱酸 HClO CH3COOH HNO2Ka 3.0×10-8 1.8×10-5 4.6×10-40.1mol/L溶液 NaClO CH3COONa NaNO2碱性强弱 NaClO>CH3COONa>NaNO2
除此之外,必要时教师可以提示学生注意观察水解反应的逆反应,并由此判断水解反应是放热还是吸热反应,进而推测温度对水解平衡是如何影响的。
[学生]:协作交流、理解概念
影响盐类水解的因素:
内因:生成盐的酸、碱相对强弱——越弱越水解。
外因:温度:升高温度,水解程度增大(因为水解过程吸热);浓度:浓度越小,水解程度越大。
设计意图:教师在关键、难点之处适时加以点拨,使学生进一步的观察和思考,对自己的解释进行补偿、矫正与评价。
环节4:扩展迁移 深化概念
[教师]:补偿练习、总结评价
理论是为实际服务的,结合本节课的内容,请课后思考下面几个问题:
为什么纯碱溶液可用于去油污?可以采取什么方法增强它的去污能力?
长期施用氮肥(NH4)2SO4的土壤会有什么不良后果?
将AlCl3溶液蒸干,得到的固体不是AlCl3,而是Al2O3,原因是什么?如何才能制得AlCl3固体。
……
[学生]:知识迁移、深化概念
……
设计意图:学生主动地对当前所学的知识意义的自主建构,解决知识迁移扩展有关的问题,将知识外化,提升能力。以此来对盐类水解的概念进行深化。
四、教学案例反思
化学概念的教学是要充分利用教材而不是教教材。在教学中,教师要有理性的精神,审视的态度,批判的眼光,去理解和使用教材,并敢于突破教材,针对教情、学情的实际,对教材进行科学的再加工,以合理的问题为背景,让学生以“概念形成”的方式获得概念。充分发挥学生的主观能动性,给学生提供积极、有效的化学概念思维活动的机会,创新设计教学过程。化学概念的建构更有助于学生:整理资料——整合知识——形成某化学主题的已有概念——在已有结构知识体系中嵌入新概念——在记忆体系中巩固知识内容——修正与完善;有助于学生高级思维的训练与发展。
[1]袁维新.科学概念的建构性教学模式与策略探析[J].教育科学,2007,23(1):24~28
[2]苏霍姆林斯基.给教师的建议[M].北京:教育科学出版社,1984:57
1008-0546(2015)07-0036-03
G632.41
B
10.3969/j.issn.1008-0546.2015.07.012
*中国化学会化学教育专业委员会“十二五”规划课题(课题批准号HJ2014-0023)成果。

