酚氧桥联多核铜(Ⅱ)配合物的合成、结构和磁性
谢齐威 崔爱莉 寇会忠
(清华大学化学系,北京100084)
酚氧桥联多核铜(Ⅱ)配合物的合成、结构和磁性
谢齐威崔爱莉寇会忠*
(清华大学化学系,北京100084)
利用柔性酚胺类配体N,N′-二甲基-N,N′-(2-羟基-4,5-二甲基苄基)乙二胺(H2L)与Cu(Ⅱ)反应,合成了2个新的酚氧桥联多核Cu(Ⅱ)配合物[CuII3(L)2(CH3OH)2](ClO4)2(1),[CuII3(L)2(CuICl2)2](2)。配合物1~2中,3个Cu2+之间通过2个酚氧桥连接,形成线性三核结构。两边的铜离子分别被配体L2-上的N2O2螯合配位,轴向与甲醇分子的氧(配合物1)或[CuCl2]-的氯(配合物2)配位,形成四方锥配位构型。中间铜离子与两侧L2-上的4个酚氧原子以平面四边形配位。CuII-O-CuII键角为100.14°~101.79°。对配合物1~2进行变温磁化率测量表明,铜离子之间通过酚氧桥存在强的反铁磁耦合,磁耦合常数J分别为-277(9)cm-1(配合物1)和-299(3) cm-1(配合物2)(基于自旋哈密顿算符(Ⅱ)=-2J(Ŝ1·Ŝ2+Ŝ2·Ŝ3)。J值与酚氧桥桥联键角有一定相关性,即Cu-O-Cu桥联键角越大,反铁磁耦合越强。
柔性配体;铜;多核配合物;磁性;混合价
分子磁性材料研究是配位化学的研究热点之一,已引起了化学、物理和材料等研究工作者的广泛关注。分子磁性材料在信息存储、量子计算机和分子自旋电子学等领域都有重要的研究价值[1-7]。其中,Cu(Ⅱ)特殊的电子结构和配位构型以及Jahn-Teller效应使得Cu(Ⅱ)基分子磁性材料被大量合成和研究[8-11]。例如,电子构型为3d9的Cu(Ⅱ)仅含有一个未成对电子,可以方便用来进行磁性相互作用强度的评估,有利于进行铜多核配合物磁性与结构的相关
性研究[12-14]。
近十年来,酚氧桥联的多核铜配合物已有较多报道,人们对其磁性与结构的相关性的认识也逐渐深入[14]。但迄今为止,大多数酚氧桥联铜配合物是基于不饱和希夫碱类配体的,导致结构类型的单一。本文使用了一个饱和柔性N2O2四齿配体(H2L),与Cu (Ⅱ)反应得到了2个新型三核Cu(Ⅱ)配合物,表征了其结构,研究了配合物的结构与磁性相关性。
1 实验部分
1.1试剂与仪器
3,4-二甲基苯酚、甲醛37%水溶液、N,N′-二甲基乙二胺、二水合氯化铜、六水合高氯酸铜、无水甲醇、去离子水、无水乙醇均从试剂公司直接购买得到。N, N′-二甲基-N,N′-(2-羟基-4,5-二甲基苄基)乙二胺(H2L)按文献方法合成[15]。红外光谱数据在Nicolet 7199B型Fourier变换红外光谱仪(KBr压片)上测试。磁性测量在MPMS-7 SQUID磁强计(Quantum Design公司)上进行,样品为直接收集的晶体样品。
1.2实验过程
配合物[CuII3(L)2(CH3OH)2](ClO4)2(1):将0.2 mmol (72.0 mg)H2L配体溶于20 mL无水甲醇中,加入0.4 mmol(144.0 mg)的Cu(ClO4)2·6H2O固体,混合均匀后缓慢加入0.1 mmol(14.0 μL)的三乙胺,溶液变为深红色。在空气中搅拌1 h后过滤,滤液在空气中缓慢挥发溶剂结晶。2 d后得到深红色长方块状晶体。产率35%。元素分析(C46H68Cl2Cu3N4O14)测定值(%):C, 47.8;H,6.2;N,5.0;理论值(%):C,47.5;H,5.9;N, 4.8。IR(KBr,cm-1):3 591,3 486,2 920,2 858,1 617,1 498,1 455,1 362,1 211,1 096,927,752,623。
配合物[CuII3(L)2(CuICl2)2](2):配合物2的合成与配合物1类似,只是使用CuCl2·2H2O代替了Cu (ClO4)2·6H2O。得深红色块状晶体。产率30%。元素分析(C44H60Cl4Cu5N4O4)测定值(%):C,45.5;H,5.2;N, 4.5;理论值(%):C,45.2;H,5.2;N,4.8。IR(KBr, cm-1):3 219,2 912,1 612,1 566,1 405,1 288,1 209,1 092,879,750,572。
1.3单晶X-射线结构测定
配合物1~2的单晶X射线衍射实验在Rigaku R-AXIS RAPID IP衍射仪上采用石墨单色化的Mo Kα射线(λ=0.071 073 nm)作为入射辐射在室温下进行。
配合物1~2的晶体结构模型由直接法解出,非氢原子坐标通过差值Fourier合成确定,并对非氢原子的坐标及其各向异性热参数进行限制性最小二乘法修正。氢原子采用几何加氢方法确定,各向同性修正。结构解析和精修分别采用SHELXS-97和SHELXL-97程序[16-17]。
CCDC:1057549,1;1057550,2。
2 结果与讨论
柔性配体H2L与铜盐以1∶2的物质的量之比反应,碱性条件下形成酚氧桥联三核Cu(Ⅱ)配合物阳离子单元[Cu3(L)2]2+。配合物1中2个高氯酸根作为阴离子平衡电荷,而配合物2中原位形成的2个[CuICl2]-阴离子维持电荷平衡,得到2个中性配合物。值得一提的是,反应均在空气中进行,通过缓慢挥发反应溶液得到了目标配合物的晶体。说明了在形成配合物2过程中发生了Cu2+氧化L-的反应,形成了[CuCl2]-配离子,这种形成[CuCl2]-的现象还未见文献报道。配合物1红外数据中1 096 cm-1处强宽吸收峰为高氯酸根的红外特征峰,其余对应的配体红外谱峰与文献报道的混合价Mn3-L2-配合物相似[18]。
2.1晶体结构
配合物1~2的晶体学数据如表1,配合物1~2的结构示意图如图1~2所示,部分键长和键角列于表2。
2个配合物均为中心对称的结构,都包含了2个酚氧基桥联的直线型CuII3三核单元[Cu3(L)2]2+。配体L2-采用了与刚性席夫碱配体类似的平面配位模式,配体4个配位原子N2O2处于Cu(Ⅱ)离子平面位置配位。不同的是柔性L2-配体整体与所螯合的铜离子的共面性较差,如图1侧视图所示。类似情况也见于还原希夫碱形成的三核铜配合物[19-21]。
在配合物1、2中,Cu(1)处于对称中心位置,由4个酚氧配位形成平面四方形配位构型,Cu-O键长处于0.192 3(3)~0.195 33(17)nm的范围。两端的CuII离子处于四方锥的五配位环境,配合物1中四方锥顶点由甲醇的氧原子配位,Cu-O键长为0.226 4(5) nm,比平面配位原子键长要明显长一些。配合物2中则为[CuICl2]-上的氯离子占据四方锥顶点位置,Cu-Cl键长为0.260 13(9)nm。配合物2中CuI离子处于直线二配位环境,Cu-Cl键长为0.212 15(10)~0.214 16(10)nm,为线形Cu(I)-Cl配位键的典型键长[22-23]。在配合物1和2中,分子堆积时没有出现分子间的π…π相互作用。配合物1中的2个高氯酸根阴离子上的氧原子与CuII离子有弱配位相互作用,Cu-O键长为0.283 3(7)nm。
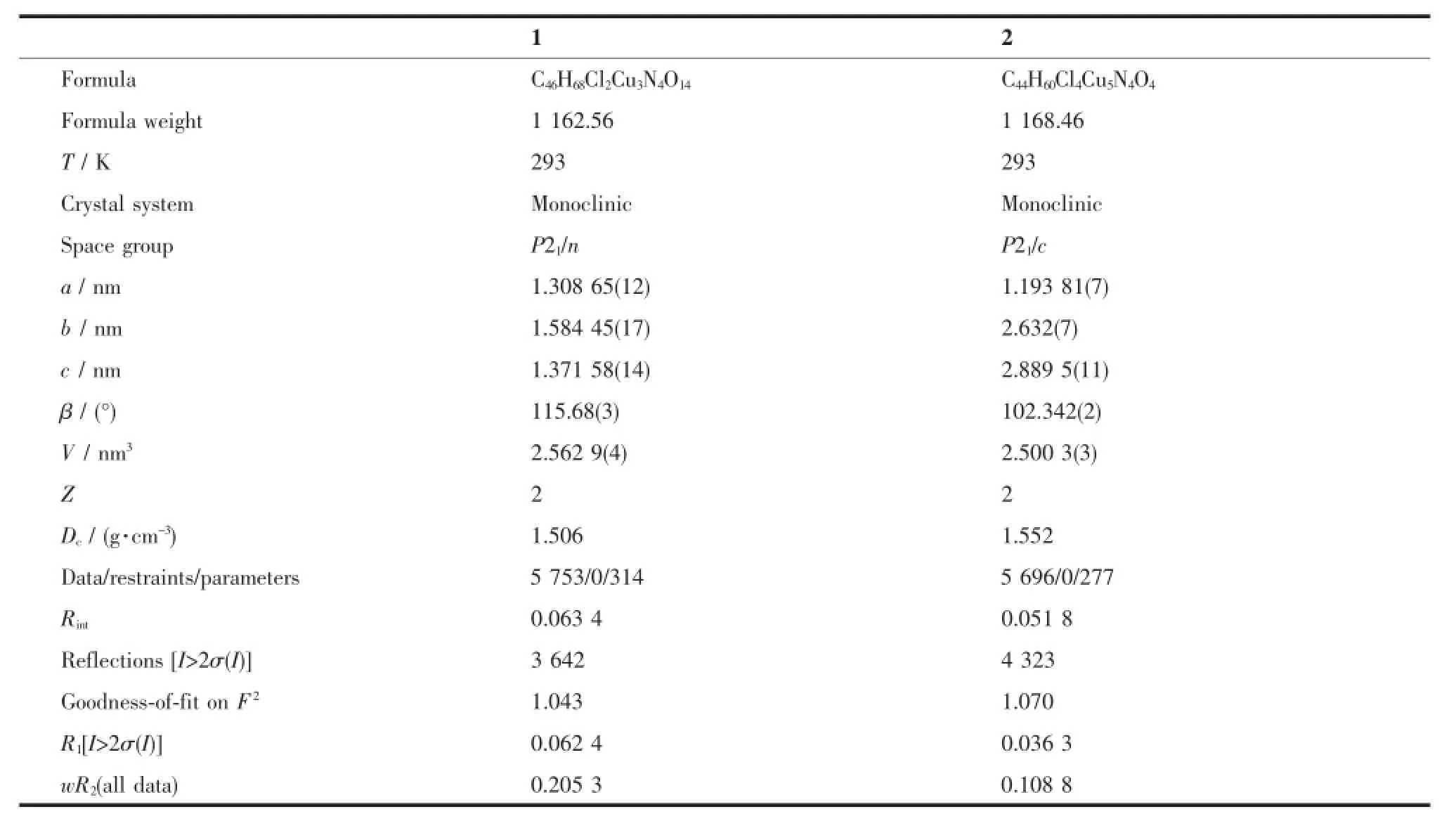
表1 配合物1和2的晶体学数据Table 1Crystallographic data for complexes 1 and 2

表2 配合物1、2的主要键长(nm)和键角(°)Table 2Selected bond distances(nm)and bond angles(°)for Complexes 1~2
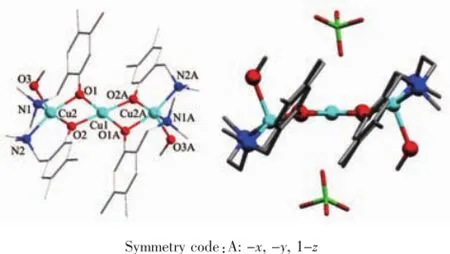
图1 左:配合物1的晶体结构;右:分子侧视图(显示了弯曲的配体L2-)Fig.1 Left:Crystal structure of complex 1;Right:side view of the molecule showing the curved ligands L2-
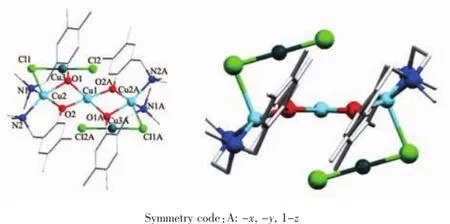
图2 左:配合物2的晶体结构;右:配合物分子侧视图Fig.2 Left:Crystal structure of complex 2;Right:side view of the molecule
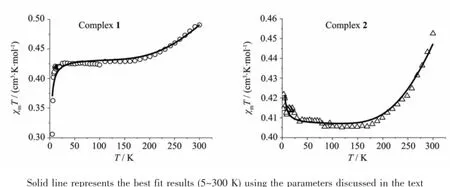
图3 配合物1、2的χmT~T图Fig.3 Temperature dependence of χmT for complexes 1 and 2
2.2磁学性质
配合物1、2的变温摩尔磁化率在外场2 000 Oe下测定,χmT对温度T作图如图3所示。随着温度的降低,χmT值随着温度的降低而减小,说明了分子内CuII离子之间为反铁磁相互作用。室温时,配合物1、2的χmT均接近0.46 cm3·K·mol-1,比CuII3三核自旋体系无相互作用时的理论值1.125 cm3·K·mol-1(取g=2.0)要小,这是由于强烈的反铁磁作用导致的。2个配合物在170 K以下χmT达到一个平台,数值为0.43 cm3·K·mol-1(配合物1)和0.405 cm3·K·mol-1(配合物2),与单个CuII离子的理论χmT值基本相当(0.375 cm3·K·mol-1,取g=2.0)。说明此时酚氧桥联的三核铜已经形成短程磁有序反平行排列。在20 K以下χmT值的降低或升高应该是源于分子间的弱磁相互作用。

图4 配合物1、2在2 K下的饱和磁化强度曲线Fig.4 Field dependence of magnetization at 2 K for complexes 1 and 2
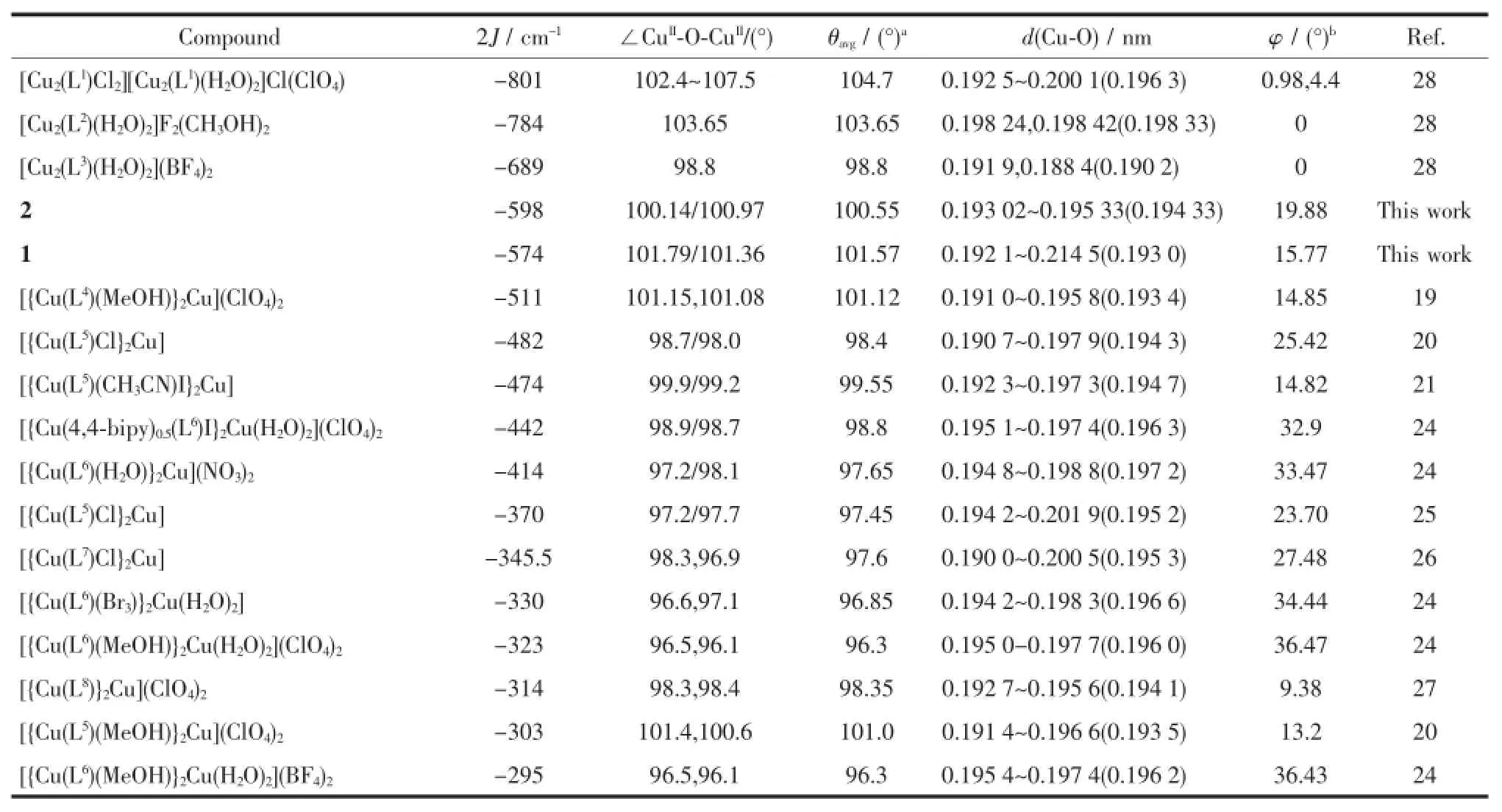
表3 双酚氧桥联铜(Ⅱ)配合物的磁性比较Table 3Comparison of the magnetic property for bis(phenoxo)-bridged Cu(Ⅱ)complexes
配合物1、2的各向同性自旋哈密顿算符为((Ⅱ)=-2J(Ŝ1·Ŝ2+Ŝ2·Ŝ3),对应Cu2+的S值为S1=S2=S3= 1/2。由于配合物1、2的Cu2+为中心对称的线性三核结构,可以忽略两端Cu2+离子之间的磁相互作用。基于该哈密顿算符推导出的磁化率公式为:
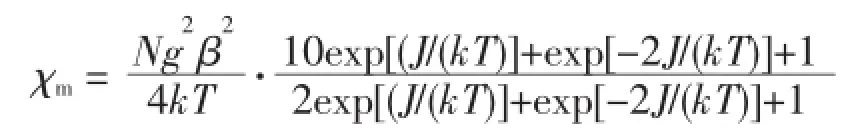
曲线拟合时使用3个变量J、g和zJ拟合,zJ为分子间磁耦合常数。在5~300 K温度范围内的数据能够得到满意的拟合,如图3中实线所示。相应的拟合参数为:J=-277(9)cm-1,g=2.15(1),zJ=-1.2(2)cm-1(配合物1),和J=-299(3)cm-1,g=2.08(1),zJ=0.25(2) cm-1(配合物2)。说明相邻Cu(Ⅱ)-Cu(Ⅱ)间存在强反铁磁相互作用,而分子间存在较弱的反铁磁或铁磁相互作用。
配合物在2 K温度下的M-H曲线在0~50 kOe场强范围内测定,结果如图4所示。配合物1、2的磁化强度随着外场场强增大缓慢增加,50 kOe时配合物1的磁化强度为0.98Nβ,配合物2的为0.96Nβ。实验值对应于反平行CuⅡ3体系残余1个CuⅡ的理论值Nβ,实验点与单核CuⅡ离子布里渊曲线吻合得比较好(图4)。
为了研究该结构下CuⅡ离子之间磁耦合作用与结构之间的关系,将配合物1、2结构、磁性数据与文献报道类似结构配合物进行了对比[19-21,24-28],这些多核CuⅡ配合物中CuⅡ离子之间均以2个酚氧桥连接,具体配合物的结构和磁性数据列于表3中。由于拟合时所用哈密顿算符不同,所有配合物的磁耦合常数统一取2J进行比较。可以看出,配合物都呈现反铁磁耦合,即通过桥联双酚氧原子相邻铜离子轨道上的单电子进行轨道重叠。因此,反铁磁耦合强度主要取决于下面几个因素[24]:(1)Cu-O-Cu桥联键角;(2)Cu-Ophenoxo键长;(3)CuO2Cu二面角,其中Cu-O-Cu键角起主要作用。
表3数据显示,2J值与Cu-O键长和二面角没有好的相关性,而与Cu-O-Cu键角密切相关。图5为根据表3中数据画出的2J与Cu-O-Cu平均键角的相关图。从图中可看出,随着CuⅡ-O-CuⅡ键角的增大,配合物反铁磁效应增强[14]。根据现有数据进行拟合得到关系式:2J=4 785.5-52.9θ,其中J的量纲为cm-1。
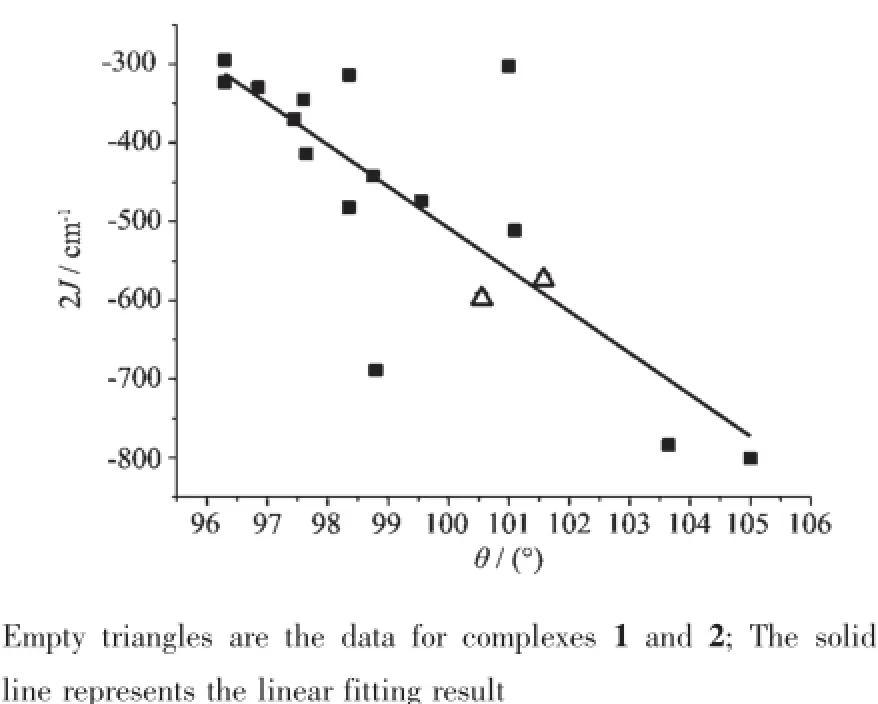
图5 双酚氧桥联铜(Ⅱ)配合物的磁耦合常数2J与Cu-O-Cu键角的相关性Fig.5 Relationship between the coupling constant 2J and the Cu-O-Cu bond angles for diphenoxo-bridged Cu(Ⅱ)complexes
3 结论
利用柔性配体H2L,合成了1个三核CuⅡ3及1个五核CuⅡ3CuⅠ2配合物,表征了配合物的结构和磁性。结果表明,2个配合物均存在强烈的反铁磁耦合。与文献报道酚氧桥联铜(Ⅱ)配合物进行对比分析,发现由双酚氧桥桥联的铜(Ⅱ)离子之间磁耦合常数与CuⅡ-O-CuⅡ桥联键角相关:CuⅡ-O-CuⅡ桥联键角越大,传递的反铁磁作用越强,而CuO2Cu二面角和Cu-O键长起到次要作用,一定程度上影响磁耦合强度的大小。
[1]Kahn O.Molecular Magnetism.New York:VCH,1993.
[2]GAO En-Qing(高恩庆),LIAO Dai-Zheng(廖代正).Chem.J. Chinese Universties(高等学校化学学报),1999,20(8):1179-1185
[3]GAO Song(高松),BAI Ou(白欧),YI Tao(易涛),et al.Acta Chim.Sinica(化学学报),2000,58(12):1666-1669
[4]FENG Xiao-Jia(冯小佳),LI Yang-Guang(李阳光),ZHANG Zhi-Ming(张志明),et al.Acta Chim.Sinica(化学学报), 2013,71(12):1575-1588
[5]LIN Shuang-Yan(林双燕),GUO Yun-Nan(郭云南),XU Gong-Feng(许公峰),et al.Chinese J.Appl.Chem.(应用化学),2010,27(12):1365-1371
[6]WANG Qing-Lun(王庆伦),LIAO Dai-Zheng(廖代正).Prog. Chem.(化学进展),2003,15(3):161-169
[7]WANG Tian-Wei(王天维),LIN Xiao-Ju(林小驹),WEI Ji-Zong(韦吉宗),et al.Chinese J.Inorg.Chem.(无机化学学报),2002,18(11):1071-1080
[8]LIANG Shu-Hui(梁淑惠),CHE Yun-Xia(车云霞),ZHENG Ji-Min(郑吉民).Chinese J.Inorg.Chem.(无机化学学报), 2005,21(7):1035-1038
[9]LU Tong-Bu(鲁统部),XIANG Hua(向华),LI Xiao-Yan (李晓燕),et al.Chem.J.Chinese Universities(高等学校化学学报),2000,21(2):187-189
[10]Fu D G,Chen J,Tan X S,et al.Inorg.Chem.,1997,36:220-225
[11]Kou H Z,Gao S,Zhang J,et al.J.Am.Chem.Soc.,2001, 123:11809-11810
[12]CHENG Peng(程鹏),LIAO Dai-Zheng(廖代正),YAN Shi-Ping(闫世平),et al.Chemistry(化学通报),1995,58(8):51 -52
[13]Bai Y L,Tangoulis V,Huang R B,et al.Chem.Eur.J., 2009,15:23772383
[14]WANG Qing-Lun(王庆伦),LIAO Dai-Zheng(廖代正).Chem. Res.(化学研究),2003,14(2):74-80
[15]Tshuva E T,Gendeziuk N,Kol M.Tetrahedron Lett.,2001, 42:6405-6407
[16]SheldrickGM.SHELXS-97,ProgramforAutomatic SolutionofCrystalStructure,UniversityofGöttingen, German,1997.
[17]Sheldrick G M.SHELXL-97,Program for Crystal Structure Refinement,University of Göttingen,German,1997.
[18]Xie Q W,Chen X,Hu K Q,et al.Polyhedron,2012,38:213 -217
[19]Song Y F,Gamez P,Roubeau O,et al.Eur.J.Inorg.Chem., 2003:2924-2928
[20]Song Y F,Gamez P,Roubeau O,et al.Inorg.Chim.Acta, 2005,358:109-115
[21]Song Y F,Albada G A,Quesada M,et al.Inorg.Chem. Commun.,2005,8:975-978
[22]Cui Y,Chen J,Chen G,et al.Acta Cryst.,2001,C57:349-351
[23]Siemeling U,Vorfeld U,Neumann B,et al.Chem.Commun., 1997:1723-1724
[24]Botana L,Ruiz J,Seco J M,et al.Dalton Trans.,2011,40: 12462-12471
[25]Song Y F,van Albada G A,Tang J,et al.Inorg.Chem., 2007,46:4944-4950
[26]Bu X H,Du M,Shang Z L,et al.Inorg.Chem.,2000,39: 4190-4199
[27]Du M,Zhao X J,Guo J H,et al.Eur.J.Inorg.Chem., 2005,294-304
[28]Thomspson L K,Mandal S K,Tandon S S,et al.Inorg. Chem.,1996,35:3117-3125
Synthesis,Structure and Magnetic Properties of Phenoxo-Bridged Polynuclear Cu(Ⅱ)Complexes
XIE Qi-WeiCUI Ai-LiKOU Hui-Zhong*
(Department of Chemistry,Tsinghua University,Beijing 100084,China)
Two polynuclear copper complexes containing the flexible ligand N,N′-dimethyl-N,N′-(2-hydroxy-4,5-dimethylbenzyl)ethylenediamine(H2L)have been prepared and characterized structurally and magnetically.The complexes have the formula[CuII3(L)2(CH3OH)2](ClO4)2(1)and[CuII3(L)2(CuICl2)2](2).X-ray single-crystal structure analyses show that both complexes contain linear CuII-CuII-CuIIcores where adjacent Cu(Ⅱ)ions are doubly bridged by phenolate groups of L2-.The coordination sphere of the terminal Cu(Ⅱ)ions is square pyramidal with the methanol oxygen(complex 1)or the chloride ion of[CuCl2]-(complex 2)situated at the apical position, whereas the central Cu(Ⅱ)has a square coordination environment.The CuII-O-CuIIbridging bond angles are in the range of 100.14°~101.79°.Magnetic studies show that both complexes exhibit strong antiferromagnetic interaction with the spin exchange coupling constants(J)of-277(9)cm-1(1)and-299(3)cm-1(2)((Ⅱ)=-2J(Ŝ1·Ŝ2+Ŝ2·Ŝ3).The antiferromagnetic interactions have been found to be mainly related to the CuII-O-CuIIbond angles.Larger Cu-OCu bond angles correspond to stronger antiferromagnetic interaction(more negative J values).CCDC 1057549,1; 1057550,2.
flexible ligand;copper;polynuclear;magnetism;mixed-valent
O614.121
A
1001-4861(2015)09-1798-07
10.11862/CJIC.2015.219
2014-05-07。收修改稿日期:2015-06-02。
国家重点基础研究发展计划(No.2013CB933403)和国家自然科学基金(No.91222104,21771103,20121318518)资助项目。
*通讯联系人。E-mail:kouhz@mail.tsinghua.edu.cn

