利用电石渣和碳酸钠制备轻质碳酸钙的研究
郭俊文,王俊中,孙炜岩
(内蒙古工业大学化工学院,内蒙古呼和浩特 010051)
电石渣是电石与水反应放出乙炔气体后的残渣,其颜色呈灰色,结构疏松。目前大多企业对电石渣的处置均采用露天堆置,导致土地严重碱化,空气污染,水源污染,同时含占用大量的土地资源,与目前提倡的环境友好型企业的要求格格不入。因而对电石渣的资源化利用就显得尤为重要。随着目前各行各业对作为工业上应用非常厂泛的一种填充剂轻质碳酸钙的需求量日益增加,而轻质碳酸钙又具有生产附加值高、用途广、性能优等特点[1-5]。轻质碳酸钙在各行各业都有有着非常巨大的开发潜能和广阔的应用前景[6-13]。所以利用电石渣为原料经过一定工艺加工以后,可以生产附加值比较高的轻质碳酸钙。
本研究以碳酸钠为碳源,聚乙二醇为保护剂,利用碳化法制备了面心立方结构的纳米轻质碳酸钙,并通过IR、粒径分布、X-RD、SEM 等手段进行了表征。
1 实验部分
1.1 原料及仪器
原料:聚乙二醇(分析纯,上海化学试剂厂);碳酸钠(分析纯,天津市化学试剂三厂);电石渣。
仪器:德国布鲁克AXS 有限公司 D8 Adwance 型X 射线衍射仪;日本日立公司S-3400N 型扫描电子显微镜;美国Nicolet 公司Nexus 670 傅里叶变换红外光谱仪。
1.2 轻质碳酸钙制备
利用电石渣制备轻质碳酸钙的主要步骤可分为以下几个步骤:电石渣的溶解制取氢氧化钙溶液,确定氢氧化钙的浓度,碳化,离心过滤,干燥。
(1)制取氢氧化钙溶液
称取电石渣2.5kg,均匀地分成十份。依次将每一份电石渣搅拌溶解,每次溶解时加入1200mL的蒸馏水,半小时将其抽滤,回收滤液将其装入瓶中。
(2)确定氢氧化钙的浓度
配制0.5mol/L 的盐酸用于滴定氢氧化钙溶液,用甲基橙溶液作指示剂。取待测液25.00mL,加入2~3 滴的指示剂滴定。计算出氢氧化钙的浓度为0.021mol/L。
(3)碳化
取氢氧化钙溶液1000mL,根据已知溶液中的Ca2+的量,加入相应的表面活性剂的量,并搅拌120分钟,使Ca2+的与表面活性剂充分结合。向溶液中滴入0.02mol/L 的Na2CO3溶液边搅拌边通入。直至溶液pH 值为7 时停止。
(4)离心过滤
用离心机过滤碳化后的溶液,转速控制在3000r/min。
(5)干燥
将离心后的产品放在干燥箱中干燥,干燥温度为100℃。
1.3 测试与表征
X 射线衍射测试用德国布鲁克AXS 有限公司生产的D8 Adwance 型X 射线衍射仪,用以分析合成出的轻质碳酸钙的物相,电压为40 kV,电流为20 mA。扫描电镜测试用日本日立公司的S-3400N 型扫描电子显微镜观察样品的形貌,电压为15kV~20 kV。红外光谱测试用美国Nicolet 公司Nexus 670 傅里叶变换红外光谱仪上测定,波数范围为:50cm-1~120 000cm-1,信噪比33400∶1,分辨率0.1 cm-1,线性度0.07 %,检测目的为定性分析,测定条件为KBr 压片法。
2 结果与讨论
2.1 FT-IR 表征
图1、图2 分别为聚乙二醇的单体与氢氧化钙的浓度比为1:1 和2:1 时的红外吸收光谱图。
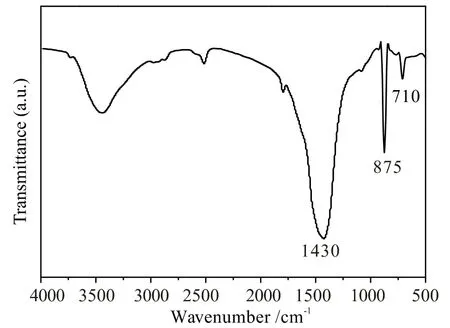
图1 轻质碳酸钙FT-IR 图 (聚乙二醇的单体与氢氧化钙的浓度比为1∶1) Fig.1 The FT-IR spectrum of light calcium carbonate (The concentration ratio of polyethylene glycol monomers and calcium hydroxide was 1:1)
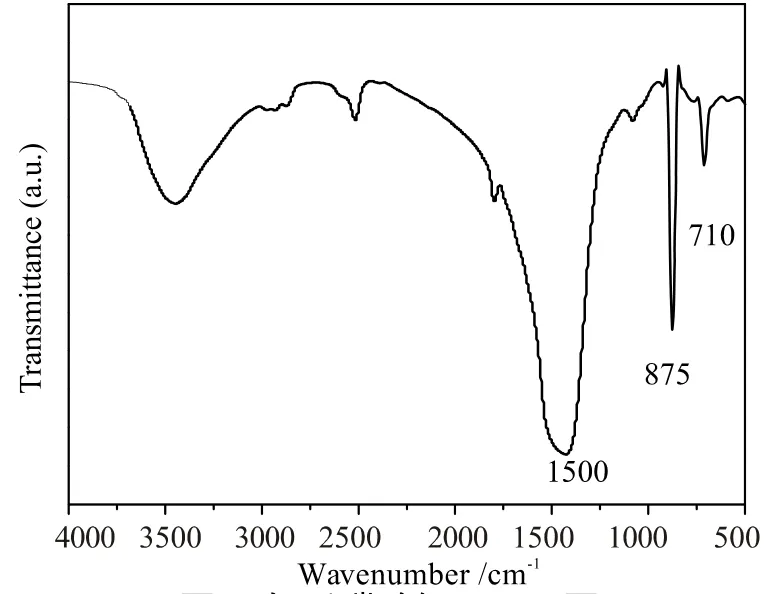
图2 轻质碳酸钙FT-IR 图 (聚乙二醇的单体与氢氧化钙的浓度比为2∶1) Fig.2 The FT-IR spectrum of light calcium carbonate (The concentration ratio of polyethylene glycol monomers and calcium hydroxide was 2:1)
2.2 XRD 表征

图3 轻质碳酸钙XRD 图 (聚乙二醇的单体与氢氧化钙的浓度比为1∶1) Fig.3 The XRD parttern of light calcium carbonate (The concentration ratio of polyethylene glycol monomers and calcium hydroxide was 1:1)
从图3 可以发现,在2θ 角为23.18o、29.52°、36.08°、39.48°、43.2°、47.64°、48.6°和57.34°处出现了衍射峰,这些衍射峰与立方面心结构纳米碳酸钙标准谱图一致,说明制备的产品为立方面心结构纳米碳酸钙。
从图4 可以发现,在2θ 角为23.2°、29.58°、36.1°、39.6°、43.24°、47.68°、48.6°和57.46°处出现了衍射峰,这些衍射峰与立方面心结构纳米碳酸钙标准谱图一致,说明制备的产品为立方面心结构纳米碳酸钙。
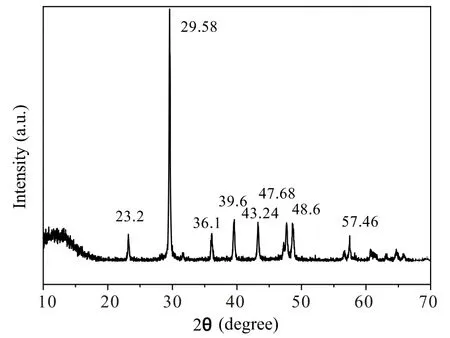
图4 轻质碳酸钙XRD 图 (聚乙二醇的单体与氢氧化钙的浓度比为2∶1) Fig.4 The XRD parttern of light calcium carbonate (The concentration ratio of polyethylene glycol monomers and calcium hydroxide was 2:1)
2.3 SEM 表征

图5 轻质碳酸钙SEM 图 (聚乙二醇的单体与氢氧化钙的浓度比为1∶1) Fig.5 The SEM image of light calcium carbonate (The concentration ratio of polyethylene glycol monomers and calcium hydroxide was 1:1)
通过图5 可以看出,产品的粒度分布相对均匀,有晶体团聚堆砌状呈现,是一种以立方面心结构为主晶型的碳酸钙。 通过图6 可以看出,产品的粒度分布更不均匀,晶体分散性更差,晶体抱团现象更加明显,但仍是一种以立方面心结构为主晶型的碳酸钙。

图6 轻质碳酸钙SEM 图 (聚乙二醇的单体与氢氧化钙的浓度比为2∶1) Fig.6 The SEM image of light calcium carbonate (The concentration ratio of polyethylene glycol monomers and calcium hydroxide was 2:1)
3 结论
(1)以碳酸钠为碳源,利用碳化法成功制备了一种面心立方结构的轻质碳酸钙,制备过程中使用聚乙二醇为分散剂。
(2)当聚乙二醇的单体与氢氧化钙的浓度比为1:1 时,碳酸钙的分散度比2:1 时的分散效果好。
[1]胡晓波,刘宝树,胡庆福.重质碳酸钙生产现状及其发展[J].中国粉碎技术,2001(1):65-67.
[2]胡庆福,胡晓湘,宋丽英.中国碳酸钙工业生产现状及其发展对策[J].中国非金属矿工业,2004(4):53-56.
[3]吴绍吟,练恩生.纳米碳酸钙的特点与应用[J].橡胶工业,1999,46:146-151.
[4]Suzuki, K, Harada, M, Shioi A, Growth mechanism of CdS ultrafine particles inwater in oil microemulsion[J]. J Chem Eng Japan, 1996, 29: 264–276.
[5]韩维屏. 国外超细碳酸钙制备工艺概况[J].化学与粘合,1984(3):183-186.
[6]汤秀花.纳米碳酸钙的制备及应用评述[J].四川化工,2006:(4):20-30.
[7]王文堂.纳米碳酸钙的应用与生产技术[J].化工科技市场,2001(9):12-15.
[8]禹坤. 纳米碳酸钙的合成理论与应用进展[J]. 无机盐化工,2008,8(8):4-7.
[9]Hiroji Shibazaki, Setsuji Edagawa, Hisashi Hasegawa, et al. Process for preparing cubic crystals of calcium carbonate. US, 4124688[P]. 1978 - 11 – 07.
[10]Yong Sheng Han, Hadiko,Masayoshi Fuji, et al. Effect of flow rate and CO2content on the phase and morphology of CaCO3prepared by bubbling method [J]. Journal of Crystal Growth, 2005 (276): 541–543.
[11]Gernot Krammer, Günter. Garnot staudinger formation of calcium carbonate sub-micron particles in a high shear stress three -phase reactor [J]. Particle & Particle Systems Characterization, 2002 (19): 348–351.
[12]Donald Richard Deutsch, Kenneth James wise. Process for the preparation of discrete particles of calcium carbonate:US, 5741471 [P]. 1998-04–21.
[13]John H. Advances in Fine Particle’s Processing[J]. Elsevier Sci. Publishing Co. Inc, 1990:181-186.

