纯液体饱和蒸汽压测定实验的教学体会
刘振华 鲁伟 邵则淮
【摘 要】纯液体饱和蒸气压的测定实验中,有多年教学经验的教师采用通俗易懂的公式兼图解的方式进行讲解原理,强调实验的关键点和注意事项,把难获得的实验点数据用启发式及思考题方式来教授,达到了明显的师生互动教学效果。文章对实验装置中改进部分作了分析,既可保证实验精度, 降低实验消耗费用, 又能避免环境污染。
【关键词】纯液体饱和蒸汽压测定实验 改进 静态法则
纯液体饱和蒸汽压测定实验是物理化学的经典实验,由于它实用性强,理论和操作要求高,至今是许多高校必做的实验之一。
笔者在多年从事物理化学实验准备及教学工作中 ,在原有实验装置的基础上,对不适合及使用起来不方便的实验装置进行更新,经过多届学生的使用,取得了较好的教学效果。十多年来,笔者对在实验教学中出现的新问题积极研究,在实验课的讲解和指导实验过程中积累了一些经验与同行们共享。
一、改进方面
(一)传统自制的水银压力计虽然读数正确,但体积太大,所需水银量也大,组装时易产生不安全因素,学生使用不小心折断或敲破玻璃管时,就会引起很大的回收及处理洒落在桌上和地上水银的麻烦,整个安装实验装置很复杂。现已改为DPCY-2C型饱和蒸汽压压力仪,经多年使用效果很好,量程选择灵活,系统连接方便,既安全又正确快速。
(二)改传统的固定压力温降法为固定温度升压法,前者如减压系统稍有漏气就较难测准数据。
(三)改自制简易的水俗温度搅拌装置为HK-1D型恒温水槽,前者热得快加热不稳定且水俗温度场分布不均,自然冷却速度慢,后者搅拌装置和数显温度既美观又方便调节和正确读数。
二、实验原理
在一定温度下, 与纯液体处于平衡状态时的蒸气压力, 称为该温度下的饱和蒸气压。 纯液体的蒸气压是随温度变化的, 其关系可用 Clausius- Clapeyron方程式表示: dlnP/dT=△Hm/RT2。
式中P为液体在温度T时的饱和蒸汽压(Pa),T为热力学温度(K),△Hm为液体摩尔气化热(J·mol-1),R为气体常数。温度变化不大时,△Hm可视为常数,将上式积分可得:lnp=-△Hm/RT+A=-B/T+A。
式中A为积分常数,此数与压力P的单位有关。由上式可见,若在一定温度范围内,测不同温度下的饱和蒸汽压,以lnp对1/T作图,可得一直线,直线的斜率为-△Hm/R, 而由斜率可求出实验温度范围内液体的平均摩尔气化热△Hm。
当外压不同,液体的沸点也不同,液体的蒸汽压等于101.325KPa时的沸腾温度称为液体的正常沸点。从图中也可求得该液体的正常沸点。
本次实验采用静态法测定环己烷的饱和蒸汽压,通常是用平衡管进行测定的。平衡管由 A 球和 U 形管 B、C 连接而成(如图1所示),待测物质置于球管内,U形管中放置被测液体,将平衡管和抽气系统、压力计连接,在一定温度下,当U形管中的B、C液面在同一水平时,表明U形管两臂液面上方的压力相等,记下此时的温度和压力,则压力计的示值就是该温度下液体的饱和蒸汽压,或者说,所测温度就是该压力下的沸点。可见,利用平衡管可以获得并保持体系中为纯试样的饱和蒸汽,U形管中的液体起液封和平衡指示作用。
图1 平衡管示意图
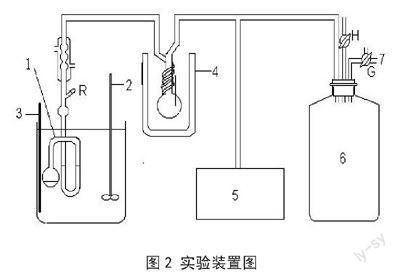
本实验的具体实验装置见图2。
图2 实验装置图
1.连冷凝管的平衡管;2.搅拌器;3.温度计;4冷阱;5.DPCY-2C型饱和蒸汽压压力仪;6.缓冲储气罐;7.接真空泵(G为抽气活塞;H为放空活塞)
三、静态法测定原理讲解
(一)讲解时一定要特别强调液封有两个作用:
1.阻止C管上部的空气进入A球内;
2.读数时起平衡指示作用,因此实验时无论何时都要保持液封的存在。
(二)实验时有三种情况
1.C管液面高于B管液面:
C面>B面,此时液体充分沸腾,C管液面高于B管h高度,B、C二管取一个水平等压面,则PC=P外+ρgh=PB=PA= P饱。式中P外对应的是真空泵抽空到缓冲储气罐中的压力,ρ是待测液体的密度,P饱是某一温度下纯液体达到气液相平衡时的饱和蒸汽压。
2.C管液面等于B管液面:则PC=P外=PB=PA = P饱
根据静态法原理要使B、C二管相平才能读数,而PA在一定温度下是个定值。因此要使h=0成立,必须改变P外,在这里应增大P外,由于是减压系统,增大P外意味着减压的程度小一点,具体操作时稍微转动H放空活塞漏入小量空气就会观察到B、C二管相平,快速读出此时的T和P表,而真实的P饱=P外=P大气压-P表,此时应快速调高恒温槽温度,等到达到设定温度时液体再次沸腾,再次稍微转动H放空活塞漏入小量空气就会观察到B、C二管相平,这样就能获得第二组数据,依次获得40℃,45℃,50℃,55℃,60℃,65℃,70℃,75℃对应下的T和P表。
3.C管液面低于B管液面:
C面
(三)大气压下的沸点测定
几乎所有的实验教材都没有说明具体怎么操作,只是指明当体系完全与大气相通时(压力计读数为0KPa),记录B、C液面相平时的水俗温度。对此学生们很有困难,不知如何下手,因前面的数据都是通过漏入小量空气使B、C相平后读数的,可现在减压装置的去除已无法漏入空气,但必须使B、C相平才能读数。
我们把这样的测定作为实验思考题来讲解的,首先提示环己烷大气压下的沸点通常在80℃~81℃,一切想增加或减少外压的方法是无效的;其次提醒大家设计的方法必须符合原理且可操作性,然后要求学生在前面做数据的同时要设计出实验方案,尤其是在等待升温的过程中同组同学可相互讨论。就这样,学生们的实验积极性就调动起来了,他们开始动脑筋积极思考并相互讨论,达到了本次实验的教学效果。
经过归纳与汇总,学生们设计了以下几种方案来测定大气压下环己烷的沸点:
1.在做完了70℃下气液相平衡时的T和P表后,实验者要迅速重新设定水的温度为81℃,并在仔细观察升温过程中要缓慢转动H放空活塞漏入小量空气,在接近79℃时必须使压力测量仪读数为零,此时再观察到B、C相平后就可读数。
2.在做完了70℃下气液相平衡时的T和P表后,实验者要一次性地转动H放空活塞与大气相通并迅速重新设定水的温度为81℃,待水的温度达到81℃时样品液体是充分沸腾的,此时C管液面高于B管液面,必须重新设定水的温度为79℃,这样加热器就不会再工作了,只要慢慢等待自然冷却,待观察到B、C相平后就可读数。
3.在做完了70℃下气液相平衡时的T和P表后,实验者要一次性地转动H放空活塞与大气相通并迅速重新设定水的温度为81℃,待水的温度达到81℃时样品液体是充分沸腾的,此时C管液面高于B管液面,你必须把[控温]按键切换到[设定]按键,这样加热器就不会再工作了,你只要慢慢等待自然冷却,待观察到B、C相平后就可读数。
4.在做完了70℃下气液相平衡时的T和P表后,实验者要一次性地转动H放空活塞与大气相通并迅速重新设定水俗温度为81℃,待水俗温度达到81℃时样品液体是充分沸腾的,此时C管液面高于B管液面,必须重新设定水俗温度为79℃,这样加热器就不会再工作了,只要慢慢加入冷水冷卻,待观察到B、C相平后就可读数。
通过比较,学生们测定的大气压下的环己烷沸点数据在80℃~81℃,符合实际数据。为何要用冷却的方法才能有效呢?这是因为水的温度达到81℃时C管液面高于B管液面,要使B、C管相平,这不正好是前面40℃,45℃,50℃,55℃,60℃,65℃,70℃实验后升温的逆过程吗?
四、数据记录和处理
(一)大气压力:平均值:102.56KPa
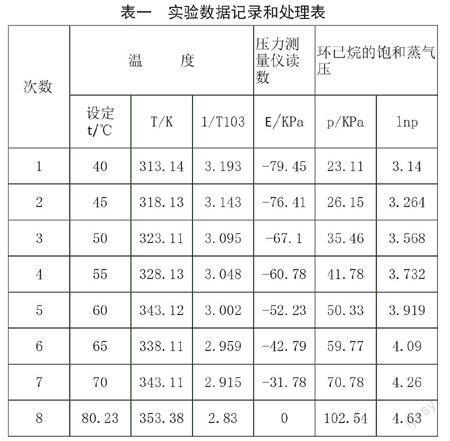
表一 实验数据记录和处理表
次数 温 度 压力测
量仪读
数 环已烷的饱和蒸气压
设定
t/℃ T/K 1/T103 E/KPa p/KPa lnp
1 40 313.14 3.193 -79.45 23.11 3.14
2 45 318.13 3.143 -76.41 26.15 3.264
3 50 323.11 3.095 -67.1 35.46 3.568
4 55 328.13 3.048 -60.78 41.78 3.732
5 60 343.12 3.002 -52.23 50.33 3.919
6 65 338.11 2.959 -42.79 59.77 4.09
7 70 343.11 2.915 -31.78 70.78 4.26
8 80.23 353.38 2.83 0 102.54 4.63
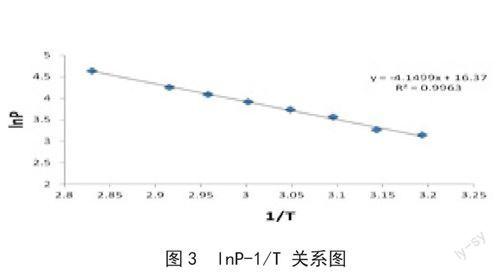
图3 lnP-1/T 关系图
(二)在坐标纸上绘制lnP-1/T关系图,从图3中可求出A和B,从而求出实验温度范围内的平均汽化热△Hm及t正常
A=16.37,B=4.150
△Hm=4.150×8.314=34.50KJ/mol, 正常沸点时,P=101.325KPa,所以t正常=1/2.832×103-273.15=79.98℃,通过查文选T正常=80.75℃,实验相对误差=0.95%。
【参考文献】
[1]北京大学化学学院物理化学实验教学组.物理化学实验[M].北京:北京大学出版社,2003: 44-46.
[2]孙尔康,徐维清, 邱金恒.物理化学实验[M].南京:南 京大学出版社,2001 : 19-22 .
[3]尹波,黄桂萍,曹利民,等.液体饱和蒸气压的测定实验的讨论[J].江西化工,2008(02).
[4]李爱昌,吴昊,等.对“纯液体饱和蒸气压的测量” 实验的几点思考[J].廊坊师范学院学校(自然科学版),2012(04).

