他克莫司治疗狼疮性肾炎40例及护理分析
籍子英,边 亚,赵丽明,智丽彩
(河北省石家庄市第二医院重症医学科,河北 石家庄 050000)
系统性红斑狼疮(SLE)是累及多器官、多系统的自身免疫性疾病,狼疮性肾炎(LN)则是SLE常见的临床表现之一,也是导致SLE患者死亡的主要原因[1]。诱导治疗阶段疗效较好的患者远期预后较好,诱导治疗效果较差的患者则容易复发并容易出现各种合并症[2]。他克莫司是新型钙调蛋白抑制剂。笔者观察了他克莫司治疗LN患者的疗效和安全性,并对其护理方法进行总结,现报道如下。
1 资料与方法
1.1 一般资料
选取2011年1月至2012年12月我院收治的80例LN患者,纳入标准:按照第7版《内科学》[3]诊断标准并经肾活检确诊为Ⅲ型、Ⅳ型LN;初发LN,病程≤24个月;系统性红斑狼疮疾病活动度评分(SLEDAI)≥9分;合并应用他克莫司和环磷酰胺治疗的适应证。排除标准:合并严重原发性高血压、糖尿病、脑血管疾病、呼吸系统疾病、肝肾功能不全、凝血功能障碍、恶性肿瘤等可能对治疗造成影响的疾病;合并精神异常;孕妇、哺乳期妇女及近期有妊娠意向的妇女;合并他克莫司或环磷酰胺应用禁忌证。剔除标准:中途退出;未严格按照医嘱进行治疗;失访。本研究已报我院伦理学委员会讨论通过并批准备案,所有入选患者对本研究可能带来的风险及收益均已知悉,并签署知情同意书。80例患者中,男 7 例,女 73 例;年龄 23~47 岁,平均(35.12±7.32)岁;病程 2~24个月,平均(12.47±6.68)个月;SLEDAI评分 9~16分,平均(12.51 ±2.12)分;Ⅲ型 LN 12 例,Ⅳ型 LN 68 例。随机分为观察组和对照组,各40例。两组患者一般资料比较,差异无统计学意义(P >0.05),具有可比性,详见表 1。
1.2 方法
观察组诱导治疗时空腹口服他克莫司胶囊(杭州中美华东制药有限公司,国药准字H20094027,规格为每粒1 mg),初始剂量为0.05 mg/kg,2次/日;服药3 d后检测全血药物浓度并调整用量,使他克莫司血药浓度维持在5~15 μg/L,诱导治疗期共3个月;之后缓慢减量至 0.04 ~0.06 mg/(kg·d),维持 6 个月;再换用来氟米特片(河北万岁药业有限公司,国药准字H20080054,规格为每片 10 mg)口服治疗,20 mg/d,维持 12个月。对照组患者诱导治疗时,予注射用环磷酰胺(江苏盛迪医药有限公司,国药准字 H32020856,规格为每支 0.1 g)静脉冲击,剂量为 0.8 mg /kg,诱导治疗期共6个月,视患者病情每2~4周进行1次冲击治疗;维持期每3~6个月进行1次冲击治疗,共18个月,冲击治疗总剂量≤150 mg/kg。两组患者同时口服醋酸泼尼松片(浙江仙琚制药股份有限公司,国药准字H33021207,规格为每片5 mg),初始剂量为 1 mg/kg,1次 /日,8周后开始减量,每 1~2周减量5 mg,至 30 mg/d后每 1~2周减量 2.5 mg,至 10 mg/d后维持治疗。治疗期间控制患者血压,对症处理患者其他症状和并发症,如患者出现严重不良反应可暂时中止或终止治疗。对两组患者均采用以下LN患者专项护理。
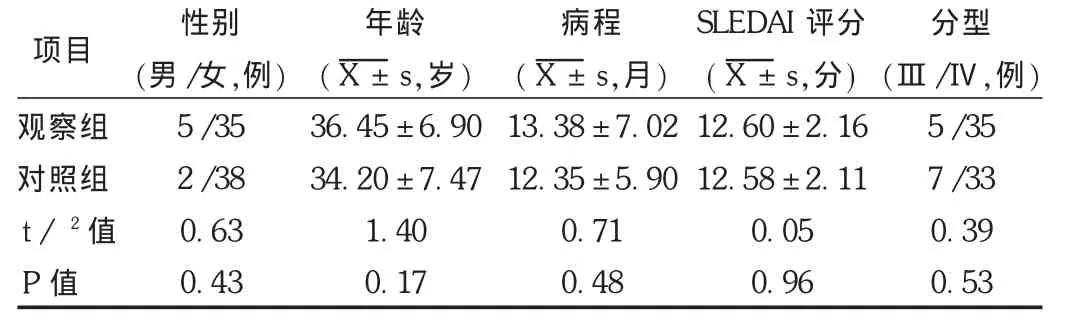
表1 两组患者一般资料比较
健康教育:患者入院后护士协助医师对患者进行SLE和LN相关健康教育,内容包括SLE和LN的病因诱因、发病机制、病理改变、治疗方法、预后和日常生活注意事项等,使患者对自己的病情有所了解,以便配合治疗。
用药护理:用药前要向患者交代清楚泼尼松冲击、环磷酰胺冲击和他克莫司治疗的不良反应情况,使患者做好心理准备,避免出现医疗纠纷;用药时要准确查对患者的用药量,环磷酰胺见光易分解,故应避光保存现配现用,同时应防范药物外渗;要密切关注患者服药情况,防止患者自行减量。
预防感染:患者用药后免疫功能受到抑制,故应密切防范感染,每日对病房设施、床单和空气进行消毒,同时密切关注患者感染情况,发现问题及时协助医师对症处理。
不良反应护理:密切关注出血性膀胱炎、胃肠道反应、肝功能损害和闭经等常见不良反应情况,发现问题后及时协助医师对症处理。
心理护理:患者在治疗期间经常出现紧张、焦虑等情绪,有的甚至可发展为精神障碍,因此在治疗过程中应密切关注患者的心理状态,经常与患者交谈以消除患者顾虑,使患者心情放松地接受治疗。
1.3 疗效评价标准
观察患者诱导治疗结束后主要实验室检查指标、治疗结束后LN缓解情况和药品不良反应情况。主要实验室检查指标为治疗6个月时的24 h尿蛋白、尿红细胞、血肌酐、补体C3和血沉指标。LN缓解评价标准:24 h尿蛋白≤0.5 g,肾功能和尿沉渣检查结果无异常,血清白蛋白≥35 g/L,无活动性狼疮症状为完全缓解;24 h尿蛋白定量在0.5~1.5 g且较治疗前下降 >50%,尿沉渣检查红细胞≤10个 /HP,血清白蛋白≥30 g/L为部分缓解;患者24 h尿蛋白定量≥1.5 g或较治疗前下降≤50%,尿沉渣检查红细胞 >10个 /HP,血清白蛋白 <30 g/L,或因严重不良反应终止治疗为无效。完全缓解和部分缓解之和为总有效。不良反应观察内容包括他克莫司、环磷酰胺及泼尼松的常见不良反应,如骨髓抑制、膀胱损害、心肺损害、高血压、过敏反应、精神症状等。
1.4 统计学处理
2 结果
观察组共36例完成研究,2例因未按医嘱治疗、2例因失访被剔除;对照组共38例完成研究,1例因中途退出、1例因失访被剔除。详见表2。结果见表3至表5。
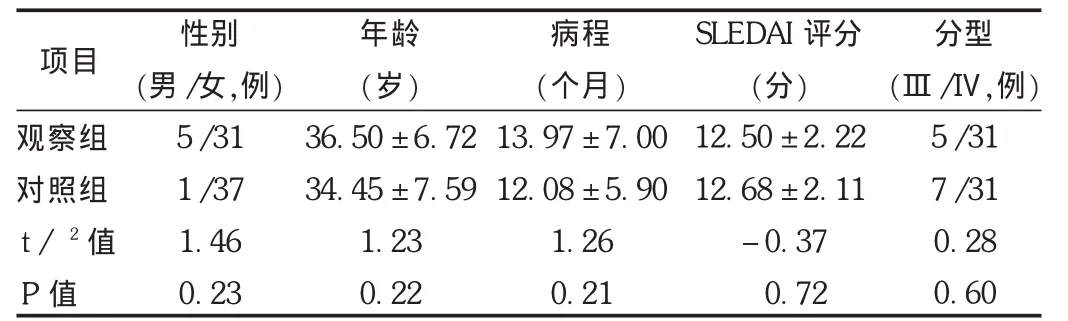
表2 两组中完成研究的患者基线资料比较
表3 两组患者诱导治疗后主要实验室指标比较()

表3 两组患者诱导治疗后主要实验室指标比较()
尿红细胞( × 1012/L)0.18 ± 0.10 0.72 ± 0.18 15.83尿蛋白(g /d)1.10 ± 0.77 1.89 ± 1.02 3.91血肌酐( mol/L)154.88 ± 52.60 120.37 ± 45.88 3.01 C3组别观察组对照组t值(g /L)0.77 ± 0.21 0.93 ± 0.17 3.61血沉(mm /h 21.68 ± 12 18.57 ± 15 0.95 0.00 0.000.00 P值0.00).45.30 0.31
3 讨论
约50%的SLE患者可出现LN,而SLE患者肾活检的LN检出率高达100%[4]。LN的发病机制是血液循环中的dsDNA等抗体与抗原结合后形成的循环免疫复合物沉积于肾小球,或dsDNA抗体与dsDNA结合后通过电荷吸附种植于肾小球,或dsDNA抗体直接与肾小球结合引发炎症反应,导致肾小球损伤。因此,免疫抑制剂治疗是目前治疗LN的主要方法。

表4 两组患者疗效比较[例(%)]

表5 两组不良反应发生情况比较[例(%)]
环磷酰胺是目前治疗增殖型LN的最常用药物,其机制为抑制免疫细胞内DNA合成,从而抑制免疫细胞的功能。但环磷酰胺治疗LN的临床缓解率并不十分满意。吴晓婵等[5]采用环磷酰胺治疗LN的临床完全缓解和部分缓解率仅为55%。同时,环磷酰胺的不良反应较严重,且发生率高,部分患者因难以耐受不得不终止治疗,从而影响了治疗效果[6]。
他克莫司是新型免疫抑制剂,可与细胞蛋白FKBP12结合,从而抑制钙依赖磷酸酶活性,阻断T细胞钙离子依赖信息通路,阻断淋巴细胞因子基因转录,从而全面抑制淋巴细胞功能。与环磷酰胺相比,他克莫司的作用靶点更专一,因此对造血干细胞、胃肠道细胞等不稳定细胞的影响较小,因而不良反应较少,抑制免疫功能的效果也更好[7-8]。
本试验结果表明,应用他克莫司联合泼尼松治疗LN,在诱导期治疗效果、治疗缓解率和药品不良反应情况方面,均明显优于对照组。但本研究病例数较少,且为单中心研究,未应用盲法,故应进一步研究。
[1]张 帆,王建文,张宝国,等.回顾性分析狼疮肾炎终末期肾病危险因素[J].中国现代医学杂志,2013,23(10):65-68.
[2]Houssiaufa, Vasconcelosc, D’Cruzd, et al.Earlyresponse to immunosuppressive therapy predicts good renal outcome in lupus nephritis:lessons from long-term follow up of patients in the Euro-Lupus Nephritis Trial[J].Arthritis Rheum,2004,50(12):3 934-3 940.
[3]陆再英,钟南山 .内科学[M].第 7版 .北京:人民卫生出版社,2008:863-865.
[4]葛均波,徐永健 .内科学[M].第 8版 .北京:人民卫生出版社,2013:488-490.
[5]吴晓婵,罗福漳.他克莫司与环磷酰胺治疗弥漫增殖性狼疮肾炎的疗效比较[J].吉林医学,2012(15):3 208-3 209.
[6]蔡 寸,胡勤晴,刘旭生,等.中西医结合预防环磷酰胺不良反应的观察[J].医学综述,2014,20(11):2 076-2 077.
[7]Nacif LS, David AI, Pinheiro RS, et al.An analysis of tacrolimus-related complications in the first 30 days after liver transplantation[J].Clinics(Sao Paulo),2014,69(11):745-749.
[8]常淑平,王 勇,王韫芳.糖皮质激素联合环磷酰胺治疗肾病综合征49 例[J].中国药业,2014,23(1):73-74.

